文档内容
2025~2026学年高三4月质量检测卷·化学
参考答案、提示及评分细则
1.B 青花瓷的主要成分属于硅酸盐,A项不符合题意;青铜是铜锡合金,属于金属材料,B项符合题意;丝绸主
要成分为蛋白质,不属于金属材料,C项不符合题意;竹简主要成分为纤维素,不属于金属材料,D项不符合
题意。
2.A NO是由N、O原子构成的双原子分子,是极性分子,A项正确;H?O的电子式为H:O:H,B项错误;
中子数为7的N:N,C项错误;NH?中N的杂化方式为sp3杂化,D项错误。
3.C SO?应用向上排空气法收集且需处理尾气,A项不能达到实验目的;乙酸乙酯和乙醇互溶,不能用分液漏
斗分离,B项不能达到实验目的;氨气易溶于水,用滴管挤入水打开止水夹后形成喷泉,氨水呈碱性,酚酞变
红,C项能达到实验目的;缺少100 mL容量瓶、胶头滴管等仪器,D项不能达到实验目的。
4.A 液氨汽化吸热,可用作制冷剂,A项正确;聚氯乙烯受热释放出有毒气体,不能用于制作食品保鲜膜,B项
错误;铝合金硬度较大,可用于制造门窗,C项错误;SO?用于葡萄酒保鲜是因其具有杀菌和抗氧化作用,D项
错误。
5.C 化合物a的分子式为C?H??O,A项错误;化合物b可发生取代、氧化等反应,但不能发生消去反应,B项
错误;苯环、酮羰基、碳碳双键均能与H?反应,1mol化合物c最多与8mol H?反应,C项正确;化合物d分子
中存在一个手性碳原子,D项错误。
6.A HF存在分子间氢键,其沸点高于HCI,A项正确;NH?存在孤电子对,键角较小,B项错误;12和CCl?均
为非极性分子,C项错误;金属Cu能导电是因为Cu中有自由电子,D项错误。
7.C a的空间结构为平面正三角形,A项错误;化合物b中含有氧元素,不属于烃,B项错误;1个c分子中含
有18个σ键,C项正确;a、c中B的价层电子对数分别为3、4,D项错误。
8.A D中子数为1,0中子数为8,D?O分子所含中子数为1×2+8=10,A项正确;标准状况下乙醇为液体,B
项错误;S-会水解,数目小于0.1NA,C项错误;22.4 L由N2和O?组成的混合气体总物质的量为1 mol,含
有原子的数目为2NA,D项错误。
9.D Fe与稀硫酸反应生成硫酸亚铁和氢气,该反应的离子方程式为Fe+2H+—Fe2++H?个,A项错误;向
H?S溶液中加入CuSO?溶液,产生黑色沉淀CuS,H?S为弱电解质不能拆分,故该反应的离子方程式为Cu2+
+H?S——CuS↓+2H,B项错误;Mg"会与OH-反应生成沉淀,正确的离子方程式为2H?O+2CI-+
Mg+通电Mg(OH)?↓+H?↑+Cl?↑,C项错误;饱和食盐水中通入氨气和CO?会析出碳酸氢钠固体,D项
正确。
10.B 由题干可知,X为H,Y为C,Z为Si,W为S。同周期元素从左到右原子半径逐渐减小,同主族元素自上
而下原子半径依次增大,原子半径:Si>S>C>H,A项错误;简单氢化物的热稳定性:CH?>SiH,B项正
【高三4月质量检测卷·化学参考答案 第1页(共4页)】确;CH?—CH?等烃中含有C—C非极性键,C项错误;Si的最高价氧化物对应的水化物H?SiO?为弱酸,W
的最高价氧化物对应的水化物为H?SO?,酸性比H?SiO?强,D项错误。
11.B 晶胞中:Cu原子数为4,Al原子数为4,S原子数为8,因此化学式为CuAIS?,A项错误;CuAIS?的摩尔
4×155B=2
质量M=(64+27+64)g·mol?1=155g·mol?1,晶胞质量为 g,晶胞体积为b×10-1?×
a62×10= g·cm?3=620X08·cm3,B项正确;基态
(a×10-10)2 cm3=a2b×10-30 cm3,晶体密度为
S、Al原子所含未成对电子数分别为2、1,个数比为2:1,C项错误;基态S原子核外电子空间运动状态有9
种,D项错误。
12.D 稀硝酸具有强氧化性,若溶液中存在SO-或HSO?,会被HNO?氧化成SO-,与Ba2+生成BaSO?白
色沉淀,A项错误;常温下,Fe在浓硝酸中发生钝化,B项错误;向苯酚溶液中加浓溴水发生取代反应,与酸
性无关,C项错误;SO?能与某些有色物质生成无色的不稳定化合物,D项正确。
13.D Zn是活泼金属,在放电时作为负极被氧化,A项正确;OH-为阴离子,在原电池放电时向负极移动,B项
正确;催化电极为正极,电极反应式为O?+2H?O+4e?=4OH-,C项正确;正极的电极反应式为O?+
2H?O+4e?—4OH-,转移1mol e时,正极反应消耗0.25 mol O?,进入电解质溶液1,电解质溶液1质
量增加8g,同时1 mol OH-移向负极区,电解质溶液1质量减少17g,故电解质溶液1质量减少17g-8g
=9g,D项错误。
14.B 根据d点、e点坐标计算,两种碱的电离常数分别为10??、10-3.4,常温下,K,(NH?OH)=10-?,A项错
误;b点时,c(H)>c(OH-),根据电荷守恒:c(CH?NH)+c(NH?OH+)+c(H+)=2c(SO-)+
c(OH-),则c(CH?NH?)+c(NH?OH+)<2c(SO?-),B项正确;H?SO;优先与碱性更强的CH?NH?反应,
则第一个滴定突变点为CH?NH?的滴定终点,由a点可知,c(CH?NH?)=0.0500 m10.00×10.00mL×2=
0.100 0 mol·L-1;第二个滴定突变点为NH?OH的滴定终点,由c点可知,c(NH?OH)=
0.0500 mol ·L-1.030.00-10.00mLX2=0.200 0 mol·L-1,C项错误;NH?OH-与NH?OH浓度相
等时溶液pH=6.0,D项错误。
15.(14分)
(1)cfgbade(2分)
(2)分液漏斗(1分);Mn(?+4H?+2c1-—Mn2++2H?O+Cl?↑(2分)
(3)除去氯气中的氯化氢气体(1分)
(4)Fe?(SO?)?+3NaClO+10NaOH—2Na?FeO?+3NaCl+3Na?SO?+5H?O(2分);高铁酸钠在碱性环境
中稳定(2分)
(5)3:2(2分)
【高三4月质量检测卷·化学参考答案 第2页(共4页)】0.4215
(6) 或其他合理形式(2分)
部分答案解析:
2×-×66 s: mo
(6)由得失电子守恒可得关系式4Na2FeO;~3O?,则样品纯度为
100?.4215Y×100??
16.(14分)
(1)3d4s2(1分);第四周期VⅢ族(1分)
(2)增大接触面积,提高反应速率和原料转化率(2分)
(3)2CoS+302蜡烧2Co+2SO?(2分)
(4)3.2≤pH<7.0(2分);CO?(2分,或其他合理答案)
(5) 1.0×10?×100?分,或其他合理答案)
(6)CoO(2分)
部分答案解析:
(6)CaCO·2H?O的质量为18.3g,nC&2)=1838.3mgr-=0.1 ml,
,根据图中的数据可知c点对应固体
的质量为7.5g,c点为Co的氧化物,c点对应固体所含氧元素的质量为7.5g-0.1 mol×59g·mol-
=1.6g,n(O°-)=16g.·6mo-=0.1 mol,
,故c点对应固体的成分是Co(。
17.(15分)
(1)+267(2分);>(1分)
(2)AC(2分)
(3)①c(2分) ②14.0(2分)
(4)①
(2分)②平衡之前,升高温度,反应速率增大,反应向正方向进行(2分) ③平衡常数减小,反应
逆向进行或放热反应达平衡后,升高温度,平衡逆向移动(2分)
部分答案解析:
(3)②由图可知,573 K时乙醇的转化率为60消耗乙醇的物质的量为△n(C?H?OH)=1mol×60%=
0.6 mol,平衡时乙醇的物质的量n(C?H?OH)=0.4 mol;CO?的选择性为85平衡时CO?的选择性+
CO的选择性=1,则CO的选择性为15根据C原子守恒可知,生成n(CO?)=0.6mol×2×85%=
1.02 mol,n(CO)=0.6 mol×2×15?.18 mol;消耗水△(H?O)=1.02 mol+×(1.02+0.18)mol=
【高三4月质量检测卷·化学参考答案 第3页(共4页)】1.62 mol,剩余水n(H?O)=3 mol—1.62 mol=1.38 mol,反应生成氢气的物质的量为n(H?)=4×
0.6 mol+1.02 mol=3.42 mol,平衡时混合气体总物质的量为n(总)=n(CO)+n(CO?)+n(H?O)+
n(H?)+n(C?H?OH)=0.18 mol+1.02 mol+1.38 mol+3.42 mol+0.4 mol=6.4 mol,则反应Ⅱ的压
-)×)~
强平衡常数1
18.(15分)
2
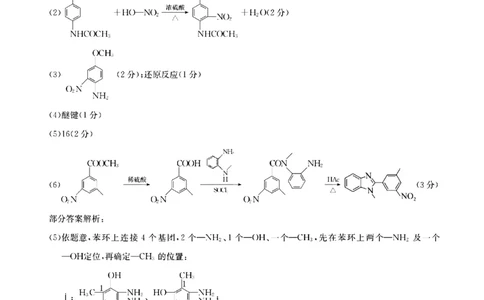
(1)C?H?NO(2分);sp3(2分)
(2分);还原反应(1分)
(3)
(4)醚键(1分)
(5)16(2分)
一成白共0O
(6)
部分答案解析:
(5)依题意,苯环上连接4个基团,2个—NH?、1个—OH、一个—CH?,先在苯环上两个—NH?及一个
一OH定位,再确定—CH?的位置:
1.(
.r
上二
;共3+3+2+3+2+3=16种。
【高三4月质量检测卷·化学参考答案 第4页(共4页)】