文档内容
2025-2026 学年度下期高三年级开学测试
化学试卷
考试时间:75分钟 总分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Bi-209 Ni-59
一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求。
1. 人类社会的发展离不开化学,化学的发展离不开科学家的不断探索。下列科学家与主要成就不相符的是
A. 伏打发明了伏打电堆,并用它通过电解法发现了钾、钠等金属元素
B. 侯德榜将氨碱法制取碳酸钠和合成氨联合起来,提高了食盐的转化率
C. 伍德沃德与多位化学家合作,成功合成了奎宁、胆固醇、维生素B 等一系列结构复杂的天然产物
12
D. 巴斯德从实验室合成的酒石酸盐中分离出两种不同光学活性的晶体
2. 下列性质或用途错误的是
A. 钠钾合金—原子反应堆的导热剂 B. 聚甲基丙烯酸甲酯—可制成电器开关、插座
C. 冠醚—有机反应的催化剂 D. 金刚砂—砂纸和砂轮的磨料
3. 下列离子反应表示正确的是
A. 向硫代硫酸钠溶液中滴加硝酸溶液:S O 2- + 2H+ = SO ↑+ S↓+ H O
2 3 2 2
B. 用铁电极作阳极,电解饱和食盐水:2Cl- + 2H O = Cl ↑+ H ↑+ 2OH-
2 2 2
C. IBr与水反应:IBr + H O ⇌ HBr + HIO
2
D. 用食醋和淀粉-KI溶液检验食盐中的IO -:IO - + 5I- + 6H+ = 3I + 3H O
3 3 2 2
4. 一种对称的阴离子[X Y ZM W ]-(结构如图)由原子半径依次增大的X、Y、Z、M、W五种短周期的p区
6 4 2 2
元素组成,基态原子中未成对电子数目Z>Y=M>X,Y与W为同主族元素。下列说法错误的是
A. 该阴离子呈现锯齿状 B. 该阴离子与季铵离子(R N+)能形成离子液体
4
C.M的氢化物的沸点不一定比Y的氢化物低 D. 第一电离能大小:Y>Z>M>X
5.用下列装置进行实验,能达到实验目的的是
A B C D
实验装置
实验目的 分离氢氧化铁胶 瓶中先通NH 再通 验证Na O 与水的反
制取网状酚醛树脂 3 2 2
体和氯化铁溶液 CO ,制备NaHCO 应放热
2 3
试卷第1页,共8页A.α-Li N的晶体类型为共价晶体 B.相邻Li与N间的作用力:层间>层内
3
C.N周围最近且等核间距的Li数目为6 D.每生成1 mol α-Li N,转移1 mol电子
3
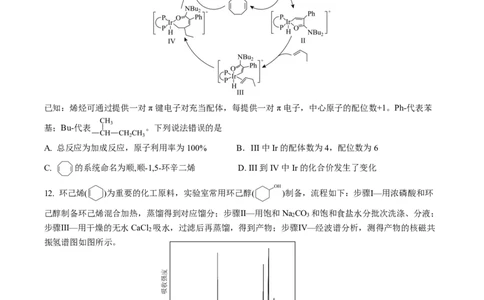
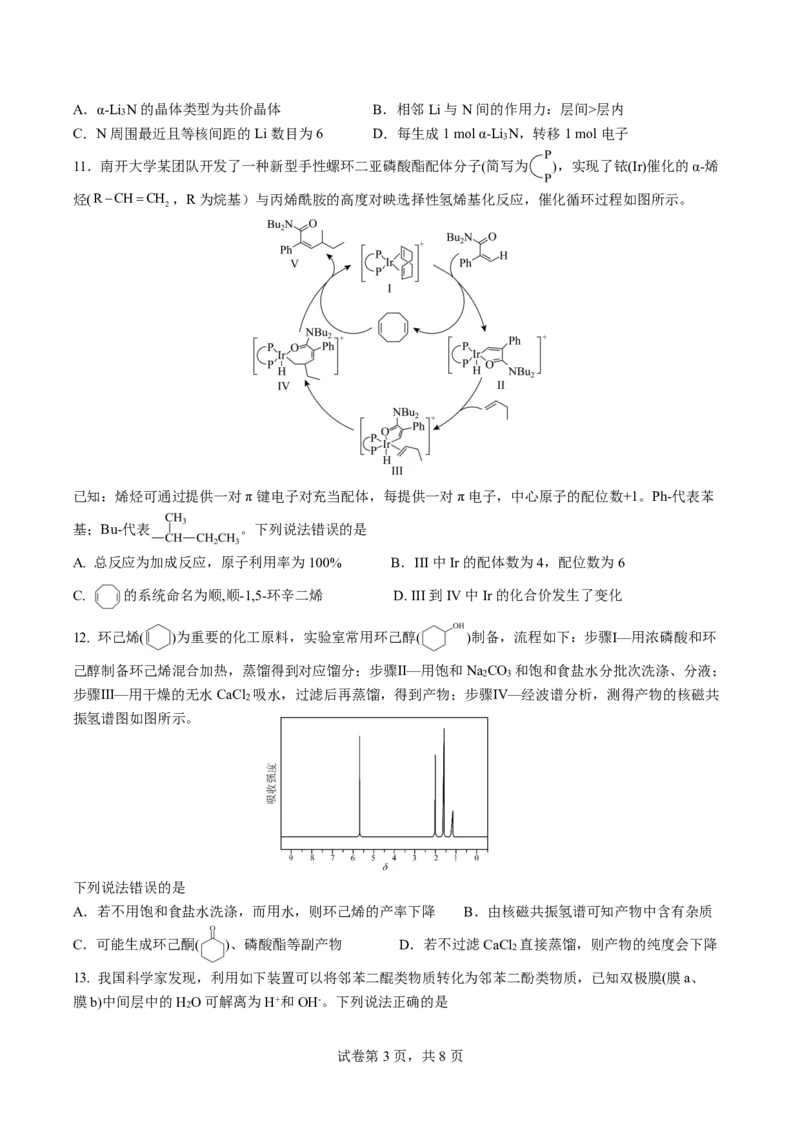
11.南开大学某团队开发了一种新型手性螺环二亚磷酸酯配体分子(简写为 ),实现了铱(Ir)催化的α-烯
烃(R-CH=CH ,R为烷基)与丙烯酰胺的高度对映选择性氢烯基化反应,催化循环过程如图所示。
2
已知:烯烃可通过提供一对π键电子对充当配体,每提供一对π电子,中心原子的配位数+1。Ph-代表苯
基;Bu-代表 。下列说法错误的是
A. 总反应为加成反应,原子利用率为100% B.III中Ir的配体数为4,配位数为6
C. 的系统命名为顺,顺-1,5-环辛二烯 D. III到IV中Ir的化合价发生了变化
12. 环己烯( )为重要的化工原料,实验室常用环己醇( )制备,流程如下:步骤Ⅰ—用浓磷酸和环
己醇制备环己烯混合加热,蒸馏得到对应馏分;步骤Ⅱ—用饱和Na CO 和饱和食盐水分批次洗涤、分液;
2 3
步骤Ⅲ—用干燥的无水CaCl 吸水,过滤后再蒸馏,得到产物;步骤Ⅳ—经波谱分析,测得产物的核磁共
2
振氢谱图如图所示。
下列说法错误的是
A.若不用饱和食盐水洗涤,而用水,则环己烯的产率下降 B.由核磁共振氢谱可知产物中含有杂质
C.可能生成环己酮( )、磷酸酯等副产物 D.若不过滤CaCl 直接蒸馏,则产物的纯度会下降
2
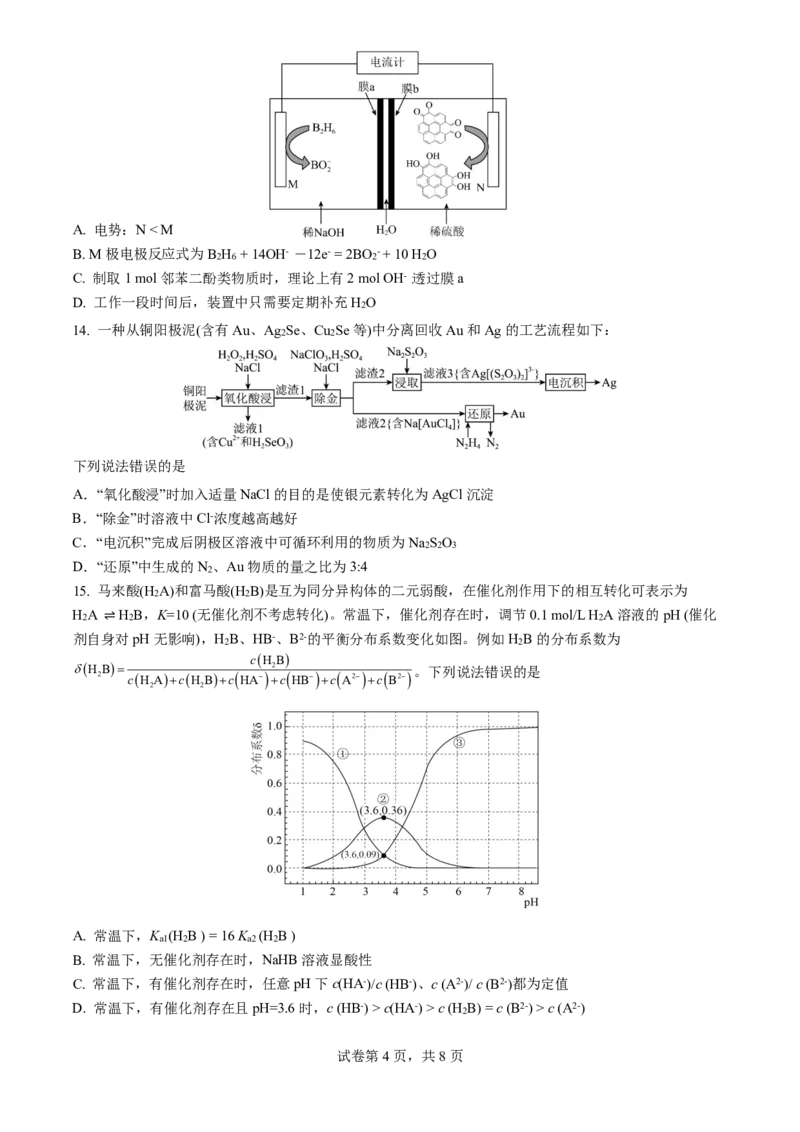
13. 我国科学家发现,利用如下装置可以将邻苯二醌类物质转化为邻苯二酚类物质,已知双极膜(膜a、
膜b)中间层中的H O可解离为H+和OH-。下列说法正确的是
2
试卷第3页,共8页A. 电势:N < M
B.M极电极反应式为B H + 14OH- -12e- = 2BO - + 10 H O
2 6 2 2
C. 制取1 mol邻苯二酚类物质时,理论上有2 mol OH- 透过膜a
D. 工作一段时间后,装置中只需要定期补充H O
2
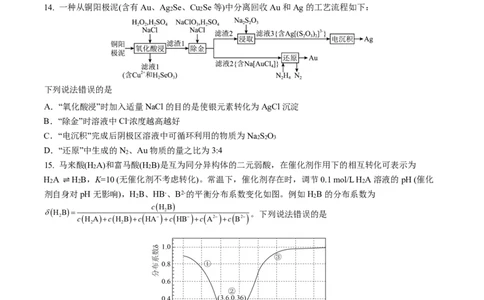
14. 一种从铜阳极泥(含有Au、Ag Se、Cu Se等)中分离回收Au和Ag的工艺流程如下:
2 2
下列说法错误的是
A.“氧化酸浸”时加入适量NaCl的目的是使银元素转化为AgCl沉淀
B.“除金”时溶液中Cl-浓度越高越好
C.“电沉积”完成后阴极区溶液中可循环利用的物质为Na S O
2 2 3
D.“还原”中生成的N 、Au物质的量之比为3:4
2
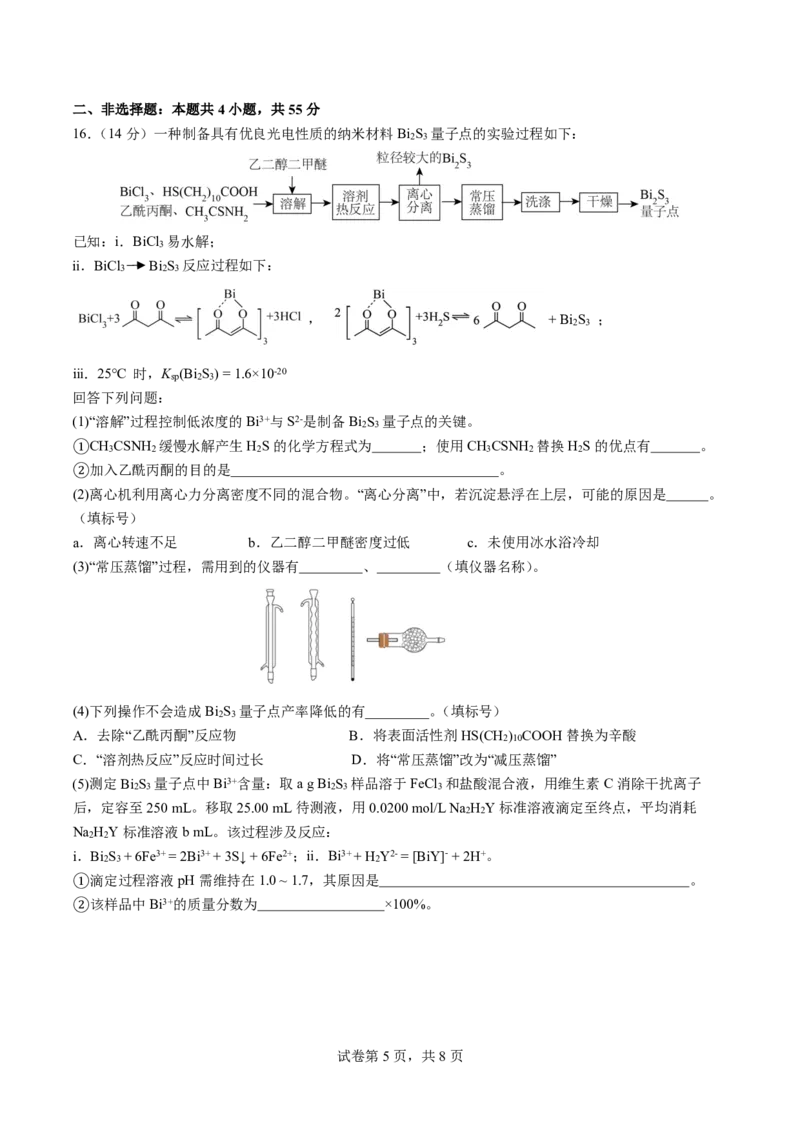
15. 马来酸(H A)和富马酸(H B)是互为同分异构体的二元弱酸,在催化剂作用下的相互转化可表示为
2 2
H A ⇌ H B,K=10 (无催化剂不考虑转化)。常温下,催化剂存在时,调节0.1 mol/L H A溶液的pH (催化
2 2 2
剂自身对pH无影响),H B、HB-、B2-的平衡分布系数变化如图。例如H B的分布系数为
2 2
c(H B)
d(H B)= 2 。下列说法错误的是
2 c(H A)+c(H B)+c ( HA-) +c ( HB-) +c ( A2-) +c ( B2-)
2 2
A. 常温下,K (H B ) = 16 K (H B )
a1 2 a2 2
B. 常温下,无催化剂存在时,NaHB溶液显酸性
C. 常温下,有催化剂存在时,任意pH下c(HA-)/c (HB-)、c (A2-)/ c (B2-)都为定值
D. 常温下,有催化剂存在且pH=3.6时,c (HB-) > c(HA-) > c (H B) = c (B2-) > c (A2-)
2
试卷第4页,共8页二、非选择题:本题共4小题,共55分
16.(14分)一种制备具有优良光电性质的纳米材料Bi S 量子点的实验过程如下:
2 3
已知:i.BiCl 易水解;
3
ⅱ.BiCl Bi S 反应过程如下:
3 2 3
, +Bi S ;
2 3
ⅲ.25℃ 时,K (Bi S ) = 1.6×10-20
sp 2 3
回答下列问题:
(1)“溶解”过程控制低浓度的Bi3+与S2-是制备Bi S 量子点的关键。
2 3
①CH CSNH 缓慢水解产生H S的化学方程式为 ;使用CH CSNH 替换H S的优点有 。
3 2 2 3 2 2
②加入乙酰丙酮的目的是 。
(2)离心机利用离心力分离密度不同的混合物。“离心分离”中,若沉淀悬浮在上层,可能的原因是 。
(填标号)
a.离心转速不足 b.乙二醇二甲醚密度过低 c.未使用冰水浴冷却
(3)“常压蒸馏”过程,需用到的仪器有 、 (填仪器名称)。
(4)下列操作不会造成Bi S 量子点产率降低的有_________。(填标号)
2 3
A.去除“乙酰丙酮”反应物 B.将表面活性剂HS(CH ) COOH替换为辛酸
2 10
C.“溶剂热反应”反应时间过长 D.将“常压蒸馏”改为“减压蒸馏”
(5)测定Bi S 量子点中Bi3+含量:取a g Bi S 样品溶于FeCl 和盐酸混合液,用维生素C消除干扰离子
2 3 2 3 3
后,定容至250 mL。移取25.00 mL待测液,用0.0200 mol/L Na H Y标准溶液滴定至终点,平均消耗
2 2
Na H Y标准溶液b mL。该过程涉及反应:
2 2
i.Bi S + 6Fe3+ = 2Bi3+ + 3S↓ + 6Fe2+;ⅱ.Bi3++ H Y2- = [BiY]- + 2H+。
2 3 2
①滴定过程溶液pH需维持在1.0 ~ 1.7,其原因是 。
②该样品中Bi3+的质量分数为 ×100%。
试卷第5页,共8页17. (14分)草酸镍NiC O 是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废
2 4
料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图:
已知:①pH增大,Fe2+被氧化的速率加快;
②草酸的K = 6.0 ×10-2 , K = 5.0 ×10-5
a1 a2
回答下列问题:
(1)生产时为提高合金废料浸出率,常采取的措施有 (填字母)。
a.适当延长浸出时间 b.高温浸出 c.分批加入混酸浸取并搅拌
(2)“萃取”步骤中萃取除去的主要金属阳离子是 。
(3)“氧化”过程中,控制70 ℃、pH小于3的条件下进行。
①“氧化”过程的离子方程式为 。
②pH为3~4时,镍的回收率降低的原因是 。
(4)“过滤”后的滤液中加入(NH ) C O 溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶
4 2 2 4
体是否洗涤干净的方法是 。
已知常温下K (NiC O ) = 1.70×10-17,当溶液pH=2时,Ni2+沉淀完全(c ( Ni2+) £1´10-5mol×L-1时认为完全
sp 2 4
沉淀),则此时溶液中草酸的浓度为 。(结果保留3位有效数字)
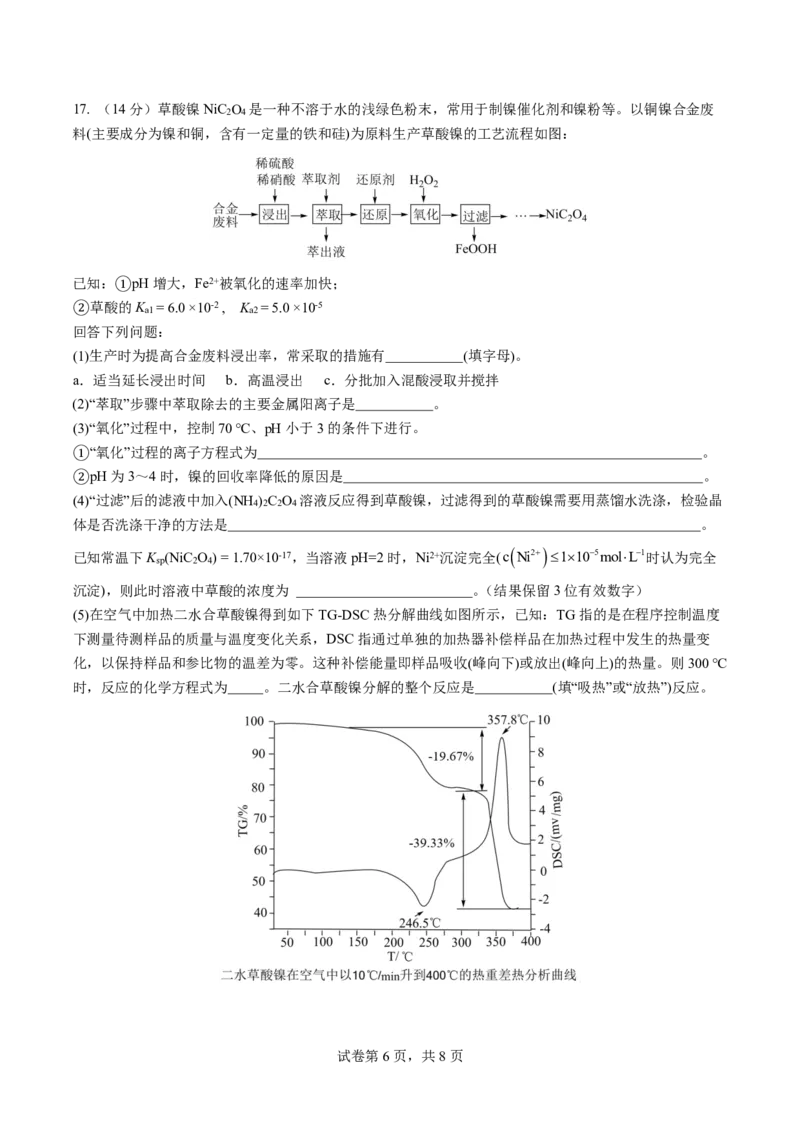
(5)在空气中加热二水合草酸镍得到如下TG-DSC热分解曲线如图所示,已知:TG指的是在程序控制温度
下测量待测样品的质量与温度变化关系,DSC指通过单独的加热器补偿样品在加热过程中发生的热量变
化,以保持样品和参比物的温差为零。这种补偿能量即样品吸收(峰向下)或放出(峰向上)的热量。则300 ℃
时,反应的化学方程式为 。二水合草酸镍分解的整个反应是 (填“吸热”或“放热”)反应。
试卷第6页,共8页18.(13分)氢气是理想的清洁和高能燃料。乙醇和水重整制氢主要发生的反应如下:
反应1:C H OH(g) + H O(g) ⇌ 2CO(g)+4H (g) ΔH = +258.1 kJ/mol ;
2 5 2 2 1
反应2:CO(g) + H O(g) ⇌ CO (g) + H (g) ΔH = -41.6 kJ/mol
2 2 2 2
回答下列问题:
(1)基态O2-的轨道表示式为 。
(2)反应C H OH(g) + 3H O(g) ⇌ 2CO (g) + 6H (g) ΔH = kJ/mol,该反应在
2 5 2 2 2
(填“较高温度”“较低温度”或“任意温度”)能自发进行。
é n(H O) ù
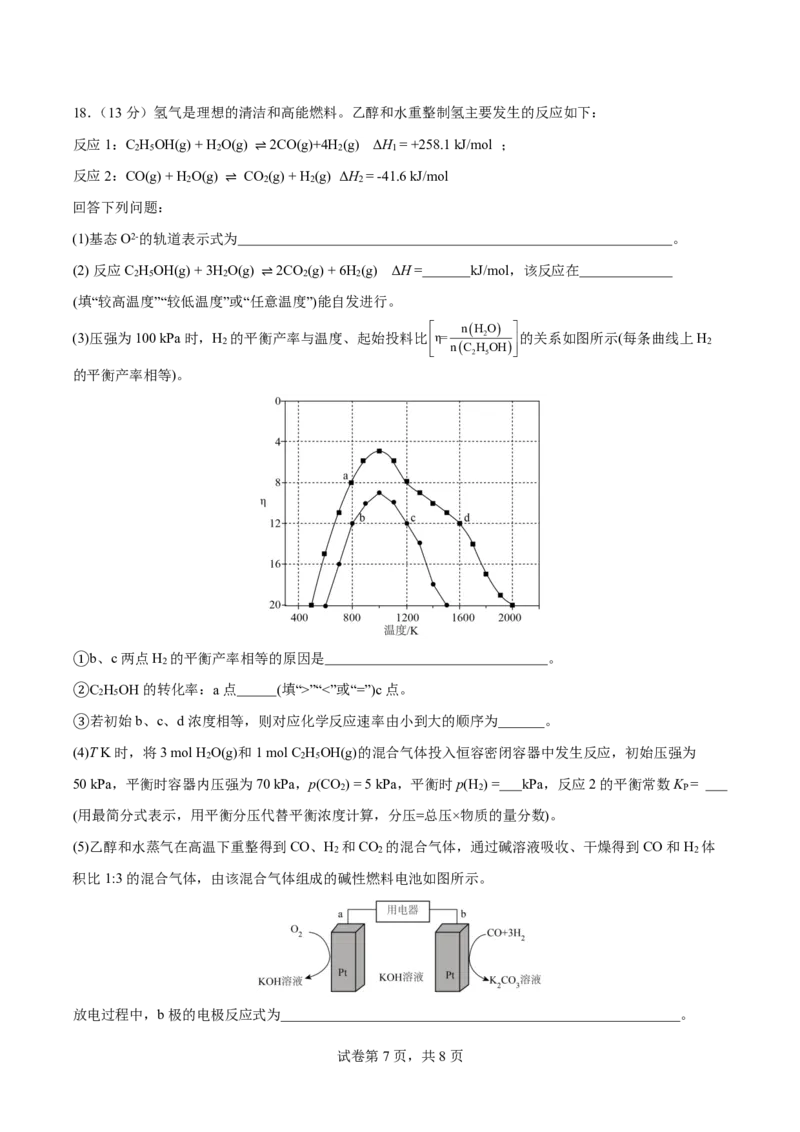
(3)压强为100 kPa时,H 2 的平衡产率与温度、起始投料比ê êë η= n(C
2
H 2
5
OH) ú úû 的关系如图所示(每条曲线上H 2
的平衡产率相等)。
①b、c两点H 的平衡产率相等的原因是 。
2
②C H OH的转化率:a点 (填“>”“<”或“=”)c点。
2 5
③若初始b、c、d浓度相等,则对应化学反应速率由小到大的顺序为 。
(4)T K时,将3 mol H O(g)和1 mol C H OH(g)的混合气体投入恒容密闭容器中发生反应,初始压强为
2 2 5
50 kPa,平衡时容器内压强为70 kPa,p(CO ) = 5 kPa,平衡时p(H ) = kPa,反应2的平衡常数K =
2 2 P
(用最简分式表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)乙醇和水蒸气在高温下重整得到CO、H 和CO 的混合气体,通过碱溶液吸收、干燥得到CO和H 体
2 2 2
积比1:3的混合气体,由该混合气体组成的碱性燃料电池如图所示。
放电过程中,b极的电极反应式为 。
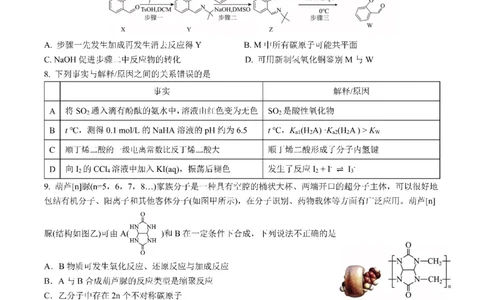
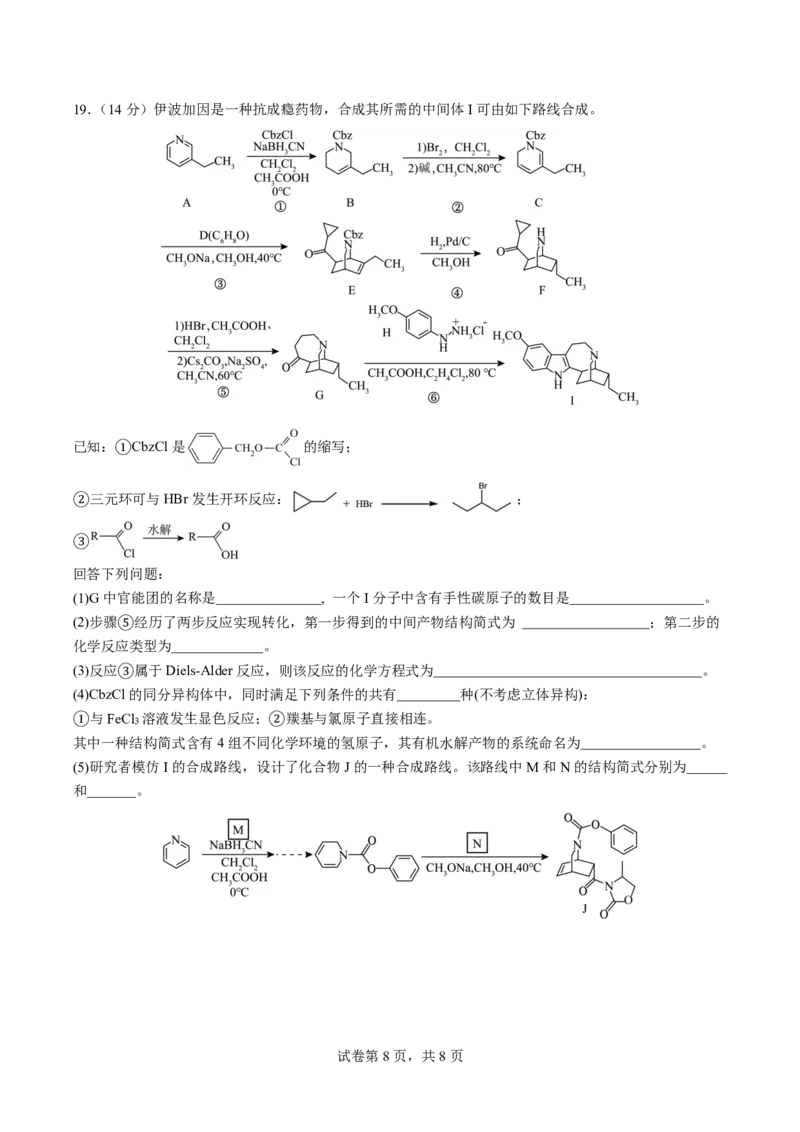
试卷第7页,共8页19.(14分)伊波加因是一种抗成瘾药物,合成其所需的中间体I可由如下路线合成。
已知:①CbzCl是 的缩写;
②三元环可与HBr发生开环反应: ;
③
回答下列问题:
(1)G中官能团的名称是 , 一个I分子中含有手性碳原子的数目是 。
(2)步骤⑤经历了两步反应实现转化,第一步得到的中间产物结构简式为 ;第二步的
化学反应类型为 。
(3)反应③属于Diels-Alder反应,则该反应的化学方程式为 。
(4)CbzCl的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构):
①与FeCl 溶液发生显色反应;②羰基与氯原子直接相连。
3
其中一种结构简式含有4组不同化学环境的氢原子,其有机水解产物的系统命名为 。
(5)研究者模仿I的合成路线,设计了化合物J的一种合成路线。该路线中M和N的结构简式分别为
和 。
试卷第8页,共8页