文档内容
成都石室中学2025-2026学年度下期高2026届二诊模拟测试
化学参考答案
一.选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A A C D C D B C A D B D C B D
1.【答案】A
【命题立意】材料的分类
【考点分析】金属材料、无机非金属材料、有机高分子材料
【详解】A 正确:碳纤维是以聚丙烯腈等为前驱体经高温碳化制得,含碳量 >90%,具有高强度、高模量、
耐高温等特性,属于新型无机非金属材料(区别于传统陶瓷、水泥)。
B 错误:橡胶跑道的主要成分是合成橡胶(如聚氨酯、三元乙丙橡胶 EPDM),属于弹性体,具有高弹性
和能量吸收能力。
C 错误:特种钢是在碳钢中加入 Cr、Ni、Mo、V 等元素形成的铁基合金,具有高强度、耐腐蚀、耐冲击
等特性,广泛用于舰船、航空等领域。
D 错误:聚碳酸酯(PC)是由双酚A与光气等缩聚而成的线型有机高分子聚合物,透明、抗冲击,是典型
的有机高分子材料,常用于眼镜片、防弹玻璃、水瓶等。
2.【答案】A
【命题立意】《物质结构与性质》(极性、配位键)、《化学反应原理》(溶解平衡、能量变化)、《有
机化学基础》(离子液体)
【考点分析】分子极性,物质相变与应用,离子液体特性,配位化学与溶解平衡
【详解】A 错误:CH 为正四面体结构,非极性分子;其燃烧热约为 890kJ/mol,在烃类中单位质量热值
4
较高(因氢含量高),故称“具有较大的燃烧热”合理,但前后句并无直接逻辑关系。
B 正确:液氨汽化热大(23.4kJ/mol),汽化时大量吸热,曾广泛用于工业制冷系统,符合物理性质与应用
的对应关系。
C 正确:硝酸乙基铵([C₂H₅NH₃][NO₃])由有机阳离子和无机阴离子构成,熔点较低(类似甲胺硝酸盐),
在广义上可视为离子液体;离子液体因含自由移动离子,具有导电性。
D 正确:配位作用确实可增加某些难溶物的溶解度(如 AgCl 在 NH₃ 中),因此“配位能力 → 可能增溶”。
3.【答案】C
【命题立意】化学用语与图示
【考点分析】物质结构基本原理和化学表达
【详解】A.苯酚与甲醛在催化剂作用下缩聚形成酚醛树脂,结构简式为 ,A
1错误;
B.邻羟基苯甲醛形成分子内氢键为: ,B错误;
D.由基态Fe原子到基态Fe2+,首先失去的是4s轨道上的电子,选项所示的价电子排布为3d54s1,4s轨道
不应该有电子,故基态Fe2+的价层电子轨道表示式为 ,D错误;
4.【答案】D
【命题立意】有机分子结构与性质
【考点分析】官能团性质、分子空间构型、反应类型及鉴别方法
【详解】A.N中碳原子有sp3和sp2(醛基)两种杂化形式,A错误;
B.Q中sp3杂化的碳原子均未连接4个不同基团,B错误;
C.N不能水解,C错误;
D.N含醛基和羟基,Q含碳碳双键和酯基,溴的四氯化碳溶液与N不反应,与Q中碳碳双键发生加成反
应而褪色,可鉴别,D正确。
5.【答案】C
【命题立意】化学实验综合
【考点分析】实验操作规范、化学反应原理、装置合理性、物质性质应用
【详解】A.NaOH具有腐蚀性,不能放在滤纸上称量,应放在小烧杯中;A错误;
B.电源正极连接了铁棒,为活性电极,则铁棒在阳极放电,不能制得氯气,B错误;
C.球形冷凝管可冷凝回流提高产率,分水器分出生成的水可提高反应转化率,C正确;
D.氯气在饱和食盐水中的溶解度很小,不会产生压强差,不能用来做喷泉实验,D错误;
6.【答案】D
【命题立意】物质结构
【考点分析】分子空间构型、元素周期律
【详解】A.Li+和H-具有相同的电子层结构,Li+核电荷数更大,离子半径更小,故r(Li+)N>C,A错误;
B. 第二电离能 O>N,O+ 的 2p 轨道是半满状态(2p³):三个电子分别占据三个 p 轨道,自旋平行(洪
特规则),能量低、结构稳定。N+的 2p 轨道是 2p²:只有两个电子在三个 p 轨道中,未达到半满,稳定
性不如半满结构。B错误;
C. N原子sp³杂化,所以∠XZQ约为109°28’,而∠YQY 中C为sp² 杂化,键角约为 120°,C正确;
D. C元素氢化物种类繁多,沸点高低难以判断,D错误。
9.【答案】A
【命题立意】有机物的结构和性质
【考点分析】本题考查聚乙烯胺化修饰中的高分子结构特征(如原子共面性)、核磁共振氢谱的解析、化
学反应类型的判断以及亲水性与极性基团的关系。
【详解】
A.聚乙烯中碳原子为饱和碳原子,以四面体结构与其他原子连接,不可能所有原子都在同一个面内,A错
误;
B.a分子的核磁共振氢谱图中有2组峰,B正确;
C.生成b的反应中有氮氮双键的断裂,是加成反应,C正确;
D.高分子c是b水解后得到,其中含羟基,可以与水形成氢键,故水溶性比聚乙烯的水溶性好,D正确;
10.【答案】D
【命题立意】化学实验基础
【考点分析】氯气与水的反应、强弱酸的判断、还原性糖的性质、键的极性对物质性质的影响。
3【详解】
A. 新制氯水中的氯气和次氯酸都能与碘化钾溶液反应生成使淀粉变蓝色的碘,则溶液变蓝色不能说明溶液
中存在氯气分子,无法证明氯气与水的反应存在限度,故A错误。
B. 若该酸为一元酸,0.01mol/L某酸溶液的pH=2,可判断为强酸,但某些二元弱酸,在浓度0.01mol/L也
可能达到pH=2,故无法判断该酸是否为强酸,B错误。
C. 麦芽糖本身就是一种还原性糖,在碱性条件下能与氢氧化铜反应产生砖红色沉淀,所以该现象不能说明
麦芽糖水解,C错误;
D.相同温度下用pH计测定0.1mol/LCF COONa溶液和CCl COONa溶液的pH,CF COONa溶液的pH更小,
3 3 3
说明酸性CF COOH>CCl COOH,这是由于F的电负性强于Cl,导致极性:C-F>C-Cl,CF COOH中羟基的
3 3 3
O-H键极性更大,更易断裂,酸性更强。D正确(人教版教材选必二P54);
故选D。
11.【答案】B
【命题立意】反应机理
【考点分析】本题考查电催化反应机理的分析,包括盐类水解与溶液酸碱性判断、氧化还原过程中元素化
合价变化、催化机理中电子与质子的作用,以及电极反应方程式的正确书写与配平。
【详解】
A.NH OHCl水溶液中的水解反应为:NH OH++H O NH OH.H O+H+,溶液呈酸性,A错误;
3 3 2 2 2
B.过程②③④均得电子,N的化合价均发生变化,B正确;
C.由历程图可知,过程⑤为:NH OH+H+=NH OH+,故M为H+,C错误;
2 3
通电
D.电催化NO与盐酸生成NH OH+的反应方程式:NO+3e-+4H+ NH OH+,D错误;
3 3
Fe
故选B。
12.【答案】D
【命题立意】简易工艺流程
【考点分析】本题考查化学工艺流程,涉及锶的电子排布(IIA族,价电子5s²)、结晶水合物脱水防水解
(HCl气流中加热)、酸浸试剂选择以及结晶控制(晶种与结晶速率对晶体颗粒的影响)。
【详解】
A.锶是第38号元素,位于元素周期表第五周期第ⅡA族,基态原子价电子排布式为5s2,A错误;
B.SrCl 为强酸强碱盐,其结晶水合物SrCl ⋅ 6H O加热时不会发生水解,直接加热脱水即可得到无水SrCl ,
2 2 2 2
B错误;
C.若用稀硫酸替代盐酸,硫酸中的SO2-会与溶液中的Ca2+结合生成微溶于水的CaSO 进入“浸出渣1”,后
4 4
续Ca2+难以除去,C错误;
D.过饱和溶液中加入晶种可提供结晶核心,促进晶体析出;结晶速度越慢,晶体生长时间越长,越易形成
大颗粒晶体,D正确;
13.【答案】C
4【命题立意】晶体结构与性质
【考点分析】本题考查化学键类型(离子键与共价键)对物质熔沸点的影响,沸点与分子间作用力、相对
分子质量的关系,二聚体(Al₂Br₆)的晶胞结构分析(分子位置、配位数)以及晶体密度计算。
【详解】A.根据题目给出的沸点数据,AlF 的沸点高达1500℃,这与离子晶体的高熔点、高沸点特征一
3
致,而AlCl 和AlBr 的沸点较低(370℃和430℃),符合分子晶体的特点,AlF 为离子晶体,熔化时破坏
3 3 3
离子键,A正确;
B.AlCl 和AlBr 均为分子晶体,相对分子质量越大,分子间作用力越大,沸点越高,AlCl 相对分子质量小
3 3 3
于AlBr ,AlCl 沸点低于AlBr ,B正确;
3 3 3
C.选取晶胞中宽上的棱心分子,由于各棱长不相等,与该棱心分子距离最近的分子为该晶胞中相邻两条高
中的棱心分子以及相邻晶胞中两条高中的棱心分子,共有4个,C错误;
D.根据均摊法,一个晶胞中Al Br 的个数为8× 1 =2,则一个晶胞的质量为m= 2×534 g,一个晶胞的体积为Vcm3,
2 6
4 NA
则Al Br 的晶胞密度为2×534 g⋅ cm−3,D正确;
2 6
NAV
故答案选C。
14.【答案】B
【命题立意】电化学基础
【考点分析】本题考查电化学基础原理在钠离子电池充电过程中的应用,包括离子迁移方向判断、电极(阴
极/阳极)识别与质量变化分析、电极反应式的书写,以及基于电子转移数与摩尔质量计算的电极质量差。
【详解】
题目图示信息表明:充电时,电极A连接电源的正极,是阳极;放电时该极被还原,作原电池正极,电极
B连接电源的负极,是阴极。放电时该极被氧化,作原电池负极。电极A的导电聚合物中掺杂了磺酸基,
充电时Na+从电极A脱嵌,进入电解质;放电时Na+嵌入电极A。电极B为Na C ,充电时Na+嵌入电极B,
x y
放电时Na+脱嵌。
A.放电时,电极B为负极,Na+脱嵌,质量减少,选项正确。
B.放电时,电极A作原电池正极,电极反应为: +ne-+nNa+
B错误。
C.充电一段时间后,嵌入电极B的Na+与通过隔膜迁移的Na+数目相同,电解质溶液中的Na+浓度基本
保持不变,C正确。
D.充电过程中,每转移1 mol e−,电极A有1 mol Na+脱嵌移至电极B,因此电极A减重23g,同时有
1 mol Na+嵌入电极B使其增重23g,则两电极质量变化相差23g-(-23g)=46g,D项正确;
故选B。
15.【答案】D
【命题立意】溶液中的离子平衡的图像综合
【考点分析】本题考查弱酸在两相中的分配平衡(K )与电离平衡(K )的综合应用,分析pH对物种分布、
d a
萃取率及平衡移动的影响,涉及平衡常数计算、浓度比较和图像分析。
5【详解】由环己烷中H A的浓度c (H A)与水相萃取率α=1−
c
环己烷
H2A
的关系可知,0.1α+c (H A)=0.1,
2 环己烷 2 0.1 mol/L 环己烷 2
则曲线①表示c (H A)随pH的变化关系,曲线②为水相萃取率的变化关系,水溶液中的c(HA−)会随着
环己烷 2
pH的增大呈现先增大后减小的变化趋势,因此曲线④为水溶液中的c(HA−)随pH的变化曲线,而A2−来源
于HA−的电离,由图可知,pH=2时,c(HA−)为0,即此时c(A2−)为0,因此曲线⑤表示c(A2−)随pH的变化
关系,故③为c(H A)随pH的变化曲线,综上:①代表c (H A)、②代表水相萃取率、③为水溶液中c(H A)
2 环己烷 2 2
的变化、④代表水溶液中的c(HA−)、⑤表示水溶液中的c(A2−),③、④交点的pH为4,交点处c(HA−)=c(H A),
2
即H A的K (H A)= c H+ ·c HA− =10−4,④、⑤交点的pH为7,即K (H A)= c H+ ·c A2− =10−7。
2 a1 2 c H2A a2 2 c HA−
A.由分析可知,曲线①代表c环己烷(H2A)的变化关系,A正确;
B.当pH=2时,代入数据得K = caq H2A = 0.02 =0.25,B正确;
d
c
环己烷
H2A 0.08
C.当pH=5时,根据图像以及上述分析可知,体系中c(HA−)>c (H A)>c(A2−),C正确;
环己烷 2
D.温度不变,K 不变,K =0.25,c (H A)=0.25c (H A),K =
c(HA−)
×c(H+)=
c(HA−)×c(H+)
=10−4,N点
d d 水 2 环己烷 2 a1 c(H2A) 0.25c
环己烷
(H2A)
c(HA−)=c (H A),c(H+)=2.5×10−5mol/L,pH=5−lg2.5=4.6。若加水体积为2VmL,K 和K 只与温度有关,
环己烷 2 d a1
不受体积影响,对交点N的横坐标无影响,即交点N的pH保持不变,D错误;
故选D。
16.(14分)【参考答案】
(1)三颈烧瓶(1分)
(2)盐酸、BaCl 溶液(1分)(只答BaCl 溶液也正确)
2 2
(3)b(1分)
(4)使蛋氨酸与碘单质充分反应、防止光照时碘单质挥发。(2分);fbecg (2分)
(5)AC(2分)
( 6 ) ①2 ( 2 分 ) ; ② (1分)
③pH过低,蛋氨酸质子化(或蛋氨酸中-NH 与H+反应),难以与Cu2+配位;pH过高,Cu2+易形成沉淀。
2
(2分)
【命题立意】物质制备与组成测定实验
【考点分析】本题考查实验仪器名称、滴定实验操作规范、离子检验试剂的选择、滴定实验误差分析、滴
定实验定量计算、配合物的结构推测与书写
【解析】(1)仪器A的名称是三颈烧瓶。
(2)验证产品是否洗涤干净可以使用盐酸、BaCl 溶液检验SO 2-。
2 4
(3)测定蛋氨酸合铜的组成时,称取试样为0.5212g,托盘天平的精度可达 0.1g、分析天平精度可达0.0001
g、台秤精度可达 0.1g,故选用b.分析天平。
6(4)蛋氨酸含量的测定时,加入过量标准碘液,置于冷、暗处放置15min既可使碘单质与蛋氨酸充分反应,
又能防止溶液光照、受热后碘单质挥发,减小实验误差;滴定管的正确操作顺序为:查漏、洗涤、润洗、
装液、排气泡、调液面、记录读数,洗涤后无需烘干也不能烘干,润洗后无需吹出润洗液。
(5)A.若测定铜含量时滴定管水洗后未用标准溶液润洗,读出标准溶液体积偏大,测得Cu2+含量偏高,则
[Cu(Met) ]中x偏小
x
B.若测定蛋氨酸含量时,滴定终点时俯视读数,读出标准溶液体积偏小,则蛋氨酸消耗I₂偏高,测得[Cu(Met) ]
x
中x偏大
C.若测定蛋氨酸含量时,滴定前滴定管尖嘴处有气泡,滴定后气泡消失,读出标准溶液体积偏大,则蛋氨
酸消耗碘单质的量偏低,测得[Cu(Met) ]中x偏小
x
(6)①测定蛋氨酸含量时,消耗 Na₂S₂O₃标准溶液 29.98mL,则与 0.5212g试样蛋氨酸反应后剩下 I₂:
29.98×0.2000×0.5×10−3 , 由 此 算 出 与 蛋 氨 酸 反 应 的 I₂= 蛋 氨 酸 的 物 质 的 量 :
20×0.2500×10−3−29.98×0.2000×0.5×10−3≈0.002
计算Cu2+含量,0.5212g试样消耗标准溶液19.98mL,由此算出Cu2+的物质的量:19.98×0.0500×10−3≈0.000999
故x近似等于2。
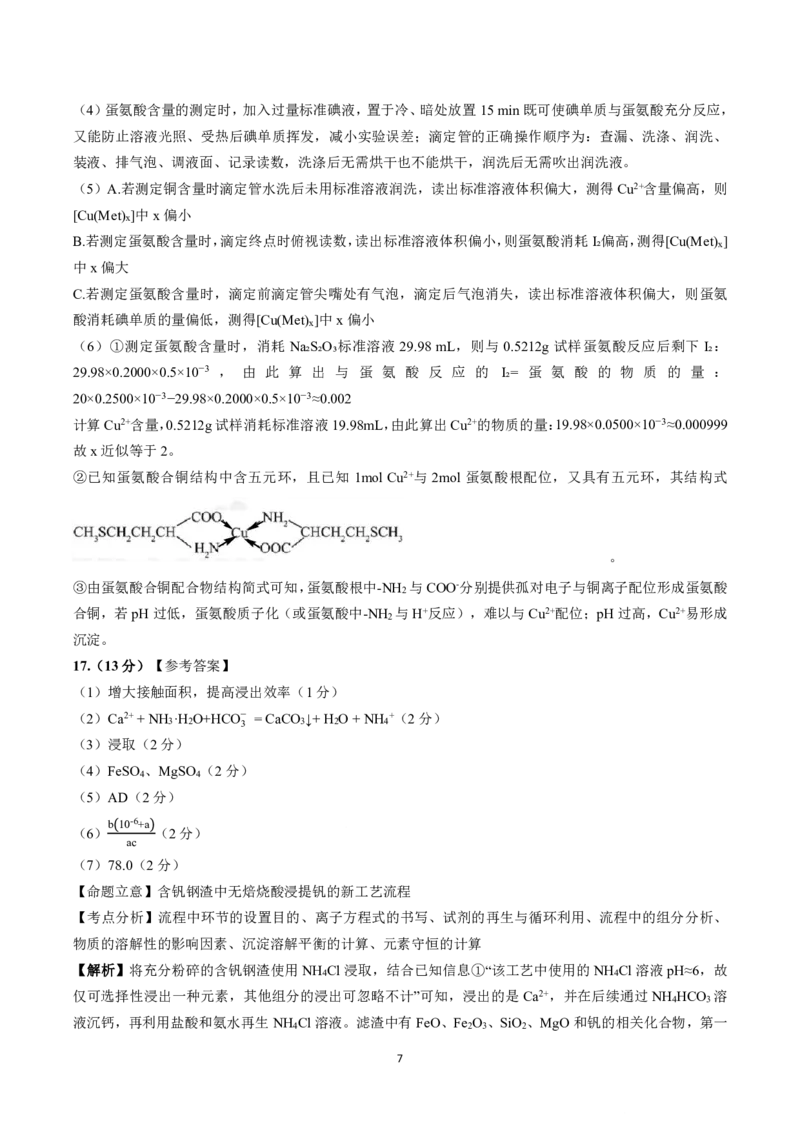
②已知蛋氨酸合铜结构中含五元环,且已知 1mol Cu2+与2mol 蛋氨酸根配位,又具有五元环,其结构式
。
③由蛋氨酸合铜配合物结构简式可知,蛋氨酸根中-NH 与COO-分别提供孤对电子与铜离子配位形成蛋氨酸
2
合铜,若pH过低,蛋氨酸质子化(或蛋氨酸中-NH 与H+反应),难以与Cu2+配位;pH过高,Cu2+易形成
2
沉淀。
17.(13分)【参考答案】
(1)增大接触面积,提高浸出效率(1分)
(2)Ca2++NH ·H O+HCO− =CaCO ↓+H O+NH +(2分)
3 2 3 3 2 4
(3)浸取(2分)
(4)FeSO 、MgSO (2分)
4 4
(5)AD(2分)
b 10-6+a
(6) (2分)
ac
(7)78.0(2分)
【命题立意】含钒钢渣中无焙烧酸浸提钒的新工艺流程
【考点分析】流程中环节的设置目的、离子方程式的书写、试剂的再生与循环利用、流程中的组分分析、
物质的溶解性的影响因素、沉淀溶解平衡的计算、元素守恒的计算
【解析】将充分粉碎的含钒钢渣使用NH Cl浸取,结合已知信息①“该工艺中使用的NH Cl溶液pH≈6,故
4 4
仅可选择性浸出一种元素,其他组分的浸出可忽略不计”可知,浸出的是Ca2+,并在后续通过NH HCO 溶
4 3
液沉钙,再利用盐酸和氨水再生NH Cl溶液。滤渣中有FeO、Fe O 、SiO 、MgO和钒的相关化合物,第一
4 2 3 2
7次酸浸浸取Fe2+和Mg2+,取滤渣进行第二次酸浸,Fe3+和钒相关离子被浸出,滤渣为SiO ,再对滤液通过
2
萃取、反萃取分离钒和铁两种元素,据此回答,
(1)粉碎的目的是增大接触面积,提高浸出效率。
(2)“浸取”时氯化铵与氢氧化钙反应生成氯化钙和氨水进入滤液,氨水与HCO -反应提供CO2−,故反应为
3 3
Ca2++NH ·H O+HCO− =CaCO ↓+H O+NH +。
3 2 3 3 2 4
(3)“沉钙”后,滤液的主要成分是NH Cl和过量的NH HCO ,先加盐酸酸化除去HCO−和CO2−,再加氨水
4 4 3 3 3
调pH值至6.4,此时混合液的主要成分是NH Cl,结合已知“该工艺中使用的NH Cl溶液pH≈6”,故混合液
4 4
可以返回至“浸取”步骤。
(4)结合已知信息②和后续才进行沉钒的步骤可知,pH=4时,三价铁和钒元素并没有被浸出,被浸出的
是Fe2+和Mg2+,此时阴离子为SO2−,故答案为FeSO 、MgSO 。
4 4 4
(5)A、钒与O形成配位键,可以使钒进入有机相,A正确;
B、配体P204中提供孤对电子的O原子带一个单位负电,可以视作是得到一个电子的阴离子,其余配体不
带电,整个配合物不显电性,形成配合物后,中心离子还是VO2+,钒元素化合价不变,B错误;
C、配合物与水形成氢键,不能解释钒进入有机相,C错误;
D、烷基具有疏水性,可以使其进入有机相,D正确;
(6)c NH4 + c OH− =a, c NH4 + ×10−6 =a, c NH4 + ×10−6 =a,c NH+ = 106ac,“沉钒”后溶液中
c NH3 ⋅ H2O c NH3 ⋅ H2O cmol/L−c NH4 + 4 1+106a
c VO− = b = b = b 10-6+a mol⋅ L−1。
3 c NH4 + 106ac ac
1+106a
(7)含钒钢渣中Ca的质量为 m(Ca)=20.0kg×56.0%× 40 =8.0kg。产出的15.60kgCaCO 中Ca的质量为
3
56
m′(Ca)=15.60kg× 40 =6.24kg。则Ca的回收率为 6.24kg ×100%=78.0%。
100 8.00kg
18.(14分)【参考答案】
(1)+205.9(2分);高温(1分)
(2)①0.4(2分);② 降低决速步的活化能,从而加快反应速率(2分)
(3)大于(1分)
(4)①H O (1分) CH (1分)
2 4
②反应I、III吸热,反应II放热;高温利于反应I、III正移,利于反应II逆向移动,使CO成为主产物(2分)
(5) (
4
2
.
.
6
6 P )3 × (
4
0
.
.
6
6 P ) 或 0.6×2.6 ×2.62p2/4.62(2分)
0.2×1
0.2 1
( P )×( P )
4.6
4.6
【命题立意】化学反应原理综合
【考点分析】盖斯定律、反应自发性分析、催化机理、反应条件对化学反应速率和平衡的影响、平衡常数
的计算。
【解析】
(1)热力学分析:解析: 反应III = 反应I - 反应II。ΔH =(+41.2)−(−164.7)=+205.9kJ⋅ mol−1。反应III
3
8为吸热反应 (ΔH>0),ΔS>0 。根据 ΔG=ΔH−TΔS<0 的判据,在高温下 TΔS 更能抵消 ΔH 的正值,使 ΔG<0,
该反应吸热且熵增,需高温自发。
(2)机理研究:观察能垒图,①TS 对应的峰值从 1.2eV 降至 0.8eV;②降低决速步的活化能,从而加
1
快反应速率。
(3)动力学规律:因为该反应 ΔH>0(吸热),升温平衡正移,平衡常数 K =k /k 增大,说明 k 增大
p 正 逆 正
的倍数更高,故 k 增大倍数大于 k 。
正 逆
(4)图像分析:已知χ(H )>χ(CH ),且温度升高χ(CH )减小,d为CH ,a为H ,又已知χ(H O)>χ
2 4 4 4 2 2
(CO),所以b为CO,c为H O;② 反应I、III吸热,反应II放热;高温利于反应I、III正移,利于反
2
应II逆向移动,使 CO 成为主产物。
(5)计算部分:
消耗CO 总量为0.8mol。生成CH 和CO的比值为1:3。列总反应方程式根据三段式计算;平衡时:
2 4
7H (g)+4CO (g)⇌ CH (g)+3CO(g)+5H O(g) n(g)总
2 2 4 2
n(始) 4 1 0 0 0 5
△n -1.4 -0.8 +0.2 +0.6 +1 -0.4
n(平) 2.6 0.2 0.2 0.6 1 4.6
( 2 . 6 P )3 × ( 0 . 6 P )
4.6 4.6
Kp=
0.2 1
( P )×( P )
4.6
4.6
19.(14分)【参考答案】
O
O
S
O
O
(1) HO (1分)(2)苯胺(1分) (3)还原反应(1分)(4)醛基(1分)
(5)
O H O
S S COONH4
HN O O HN O (2分)
+ 2[Ag(NH3)2]OH + 2Ag↓ + 3NH3 +H2O
H2
N
(6)9(2分) (1分)、 (1分)
NH2
9O
S Br
(7)13(2分) HN O (2分)
【命题立意】有机推断
【考点分析】反应类型、结构简式、有机方程式书写、有机推断与合成、同分异构体书写和判断
【解析】(1)根据有机物 E 的结构简式逆推 A 到 C 发生了与甲醇的酯化反应(取代反应),得到
O
C(O );(2)氨基直接连在苯环上,其化学名称为苯胺;(3)E→F过程中还原剂
S
O
O
HO
LiAH 将酯基还原为醇羟基,反应类型为还原反应。(4)E→F中伯醇的羟基氧化为醛基;(5)醛基被银
4
氨 溶 液 氧 化 为 羧 基 , 在 碱 性 环 境 下 得 到 羧 酸 铵 , 其 反 应 的 化 学 方 程 式 为 :
O O
H
S S COONH4
HN O O HN O ;(6)苯胺的同系物要求含有苯环
+ 2[Ag(NH 3 ) 2 ]OH + 2Ag↓ + 3NH 3 +H 2 O
1 1 1
2 2 1 1
且-NH 直接连在苯环上,故先固定碳干结构,其氨基可能位置有: 、 、 、 ,
2 3 1 2 2 2 1 1
2 1 3
H2
N
合计9种,其中核磁共振氢谱显示四组峰(峰面积之比为1:6:2:2)的结构简式为 或
NH2
(7)A到I整体的转化率为19%,I到贝利司他的产率为68.3%,故整个流程中贝利司他的产率为二者乘积
O
S Br
19%×68.3%≈13%,简化后的流程先发生苯氨基取代-Cl,得到 HN O ,再与丙烯酸甲酯发生取代加成
反应得到I。
10