文档内容
成都石室中学2025-2026学年度下期高2026届二诊模拟测试
化学
本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
注意事项:
1.答题前,务必将自己的姓名、准考证号和座位号填写在答题卡规定位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦干净后,再
选涂其他答案标号。
3.答非选择题时,必须使用0.5毫米黑色签字笔,将答案书写在答题卡规定的位置上。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 Cl-35.5 Ca-40 Br-80
第I 卷(选择题,共45分)
一.选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是最符合题
目要求的。)
1.材料是人类文明发展的里程碑。下列生产或应用中所用到的主要物质属于无机非金属材料的是
A.制造跑车机舱使用的碳纤维
B.制造操场跑道使用的橡胶
C.制造“和平方舟”甲板使用的特种钢
D.制造近视眼镜镜片使用的聚碳酸酯材料
2.下列物质结构或性质与用途对应关系错误的是
A.CH 为非极性分子,CH 具有较大的燃烧热
4 4
B.液氨汽化时吸收大量热,可用作制冷剂
C.硝酸乙基铵[ C H NH NO ]是一种“离子液体”,常温下具有良好的导电性
2 5 3 3
D.Ag+与NH 能形成配位键,AgCl在氨水中溶解度可能比水中大
3
3.下列化学用语或图示正确的是
A.酚醛树脂的结构简式:
B.邻羟基苯甲醛形成分子内氢键:
C.NaBF 的电子式为:
4
D.基态Fe2+价层电子的轨道表示式
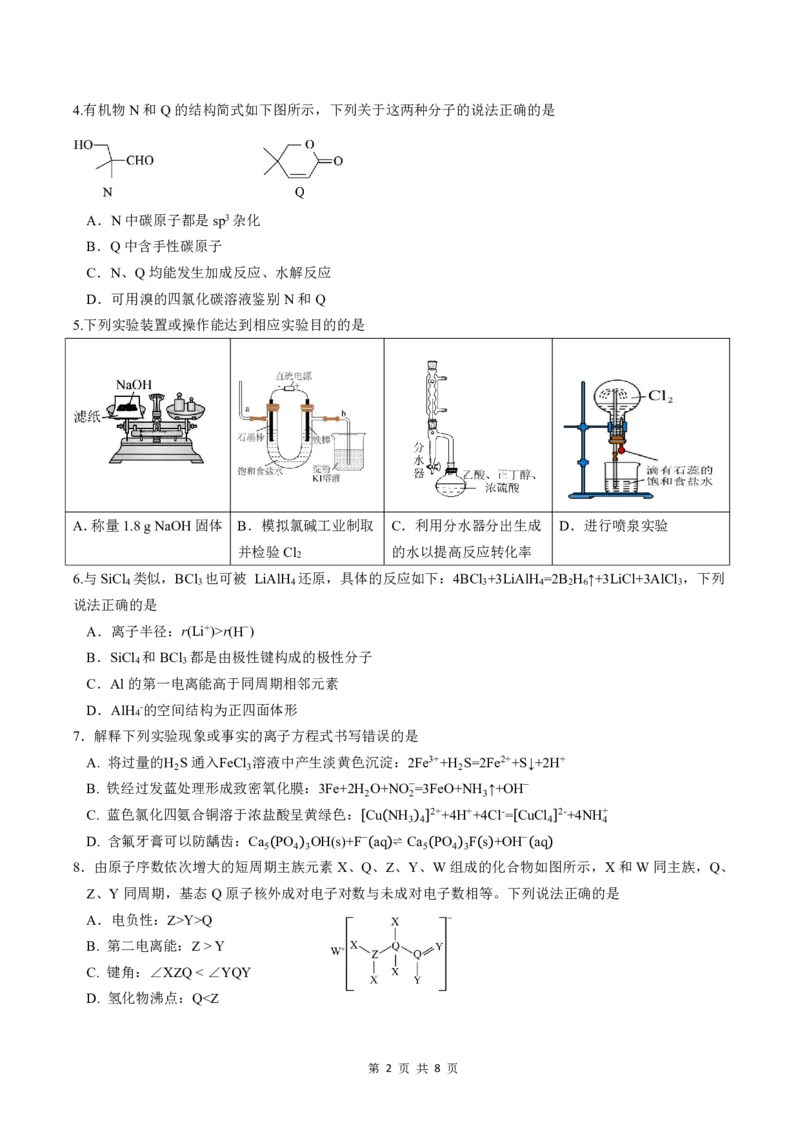
第 1 页 共 8 页4.有机物N和Q的结构简式如下图所示,下列关于这两种分子的说法正确的是
A.N中碳原子都是sp3杂化
B.Q中含手性碳原子
C.N、Q均能发生加成反应、水解反应
D.可用溴的四氯化碳溶液鉴别N和Q
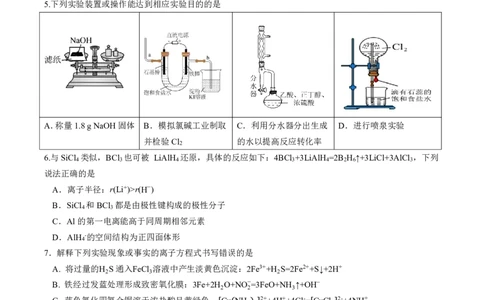
5.下列实验装置或操作能达到相应实验目的的是
A.称量1.8gNaOH固体 B.模拟氯碱工业制取 C.利用分水器分出生成 D.进行喷泉实验
并检验Cl 的水以提高反应转化率
2
6.与SiCl 类似,BCl 也可被 LiAlH 还原,具体的反应如下:4BCl +3LiAlH =2B H ↑+3LiCl+3AlCl ,下列
4 3 4 3 4 2 6 3
说法正确的是
A.离子半径:r(Li+)>r(H−)
B.SiCl 和BCl 都是由极性键构成的极性分子
4 3
C.Al的第一电离能高于同周期相邻元素
D.AlH -的空间结构为正四面体形
4
7.解释下列实验现象或事实的离子方程式书写错误的是
A. 将过量的H S通入FeCl 溶液中产生淡黄色沉淀:2Fe3++H S=2Fe2++S↓+2H+
2 3 2
B. 铁经过发蓝处理形成致密氧化膜:3Fe+2H O+NO−=3FeO+NH ↑+OH−
2 2 3
C. 蓝色氯化四氨合铜溶于浓盐酸呈黄绿色: Cu NH 2++4H++4Cl-= CuCl 2-+4NH+
3 4 4 4
D. 含氟牙膏可以防龋齿:Ca PO OH(s)+F− aq ⇌ Ca PO F s +OH− aq
5 4 3 5 4 3
8.由原子序数依次增大的短周期主族元素X、Q、Z、Y、W组成的化合物如图所示,X和W同主族,Q、
Z、Y同周期,基态Q原子核外成对电子对数与未成对电子数相等。下列说法正确的是
A.电负性:Z>Y>Q
B. 第二电离能:Z>Y
C. 键角:∠XZQ<∠YQY
D. 氢化物沸点:QC-Cl
3
D
CF COONa溶液和CCl COONa溶液的pH 更小
3 3
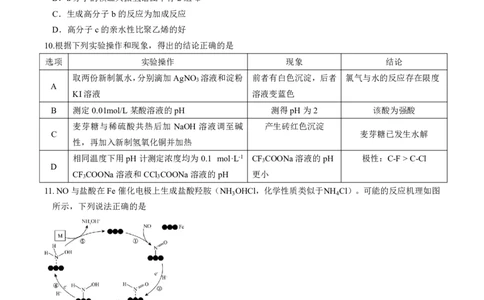
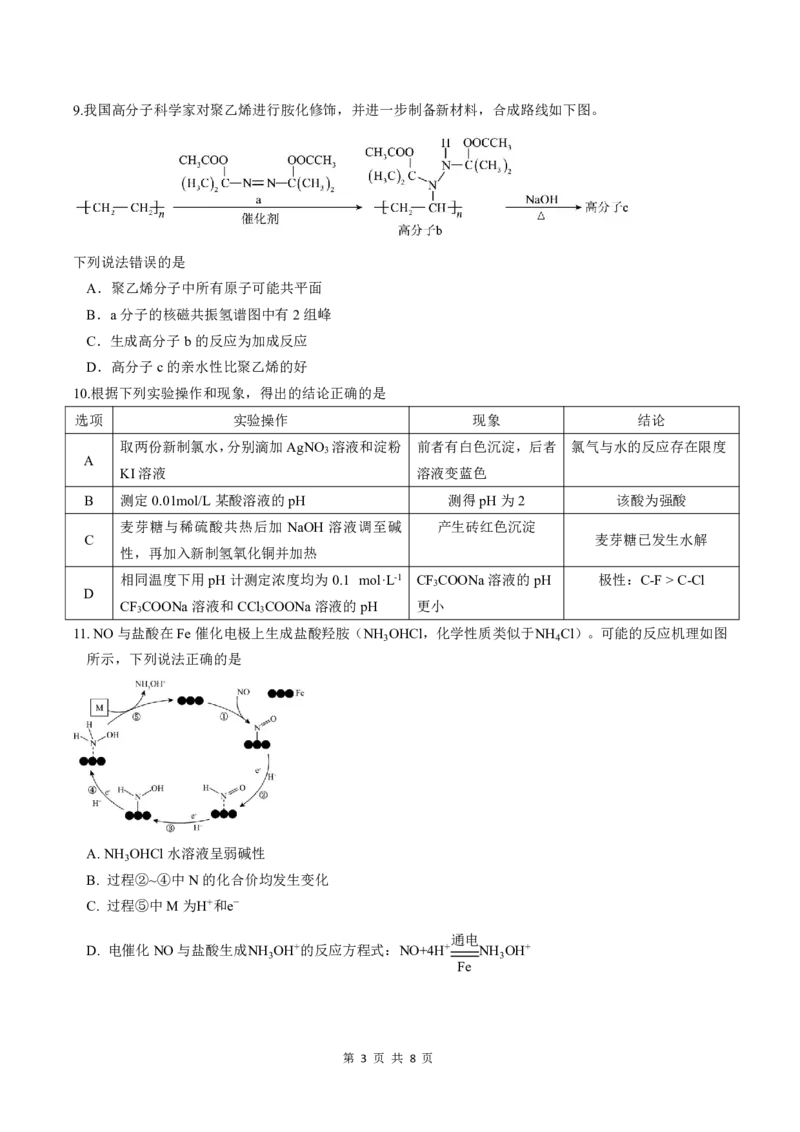
11.NO与盐酸在Fe催化电极上生成盐酸羟胺(NH OHCl,化学性质类似于NH Cl)。可能的反应机理如图
3 4
所示,下列说法正确的是
A.NH OHCl水溶液呈弱碱性
3
B. 过程②~④中N的化合价均发生变化
C. 过程⑤中M为H+和e−
通电
D. 电催化NO与盐酸生成NH OH+的反应方程式:NO+4H+ NH OH+
3 3
Fe
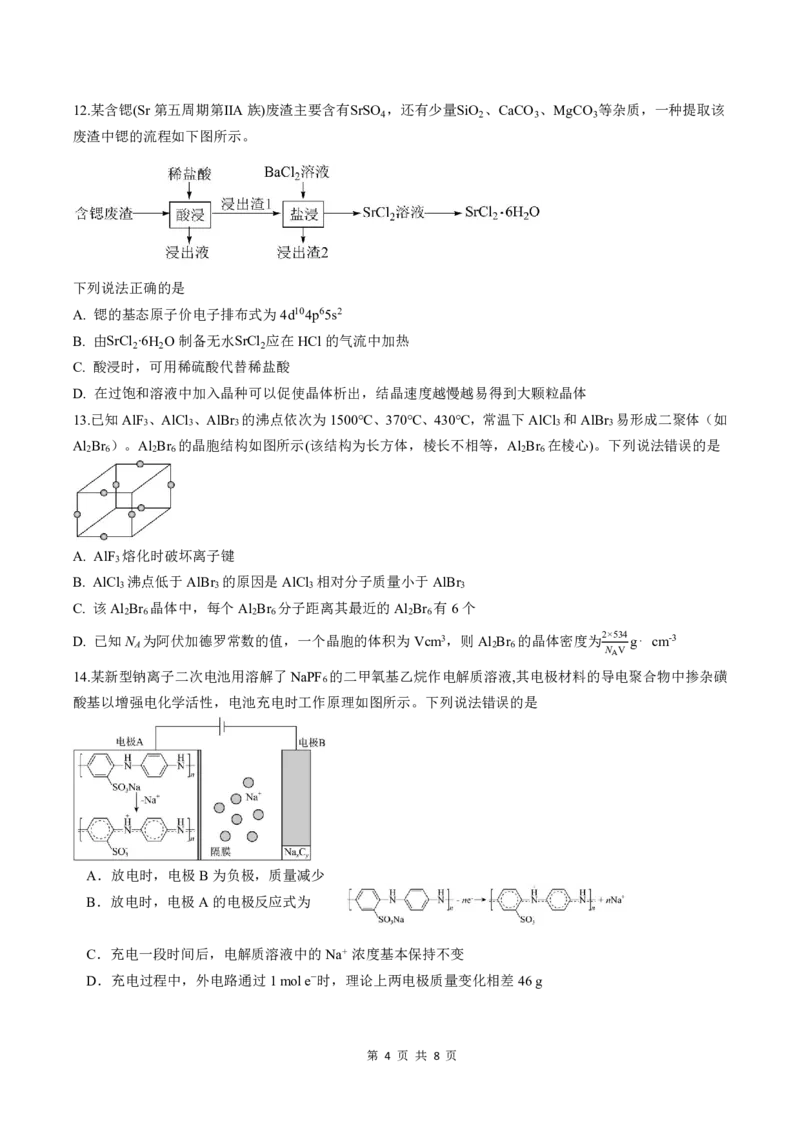
第 3 页 共 8 页12.某含锶(Sr第五周期第ⅡA族)废渣主要含有SrSO ,还有少量SiO 、CaCO 、MgCO 等杂质,一种提取该
4 2 3 3
废渣中锶的流程如下图所示。
下列说法正确的是
A. 锶的基态原子价电子排布式为4d104p65s2
B. 由SrCl ∙6H O制备无水SrCl 应在HCl的气流中加热
2 2 2
C. 酸浸时,可用稀硫酸代替稀盐酸
D. 在过饱和溶液中加入晶种可以促使晶体析出,结晶速度越慢越易得到大颗粒晶体
13.已知AlF 、AlCl 、AlBr 的沸点依次为1500℃、370℃、430℃,常温下AlCl 和AlBr 易形成二聚体(如
3 3 3 3 3
Al Br )。Al Br 的晶胞结构如图所示(该结构为长方体,棱长不相等,Al Br 在棱心)。下列说法错误的是
2 6 2 6 2 6
A. AlF 熔化时破坏离子键
3
B. AlCl 沸点低于AlBr 的原因是AlCl 相对分子质量小于AlBr
3 3 3 3
C. 该Al Br 晶体中,每个Al Br 分子距离其最近的Al Br 有6个
2 6 2 6 2 6
D. 已知N 为阿伏加德罗常数的值,一个晶胞的体积为Vcm3,则Al Br 的晶体密度为2×534 g⋅ cm-3
A 2 6
NAV
14.某新型钠离子二次电池用溶解了NaPF 的二甲氧基乙烷作电解质溶液,其电极材料的导电聚合物中掺杂磺
6
酸基以增强电化学活性,电池充电时工作原理如图所示。下列说法错误的是
A.放电时,电极B为负极,质量减少
B.放电时,电极A的电极反应式为
C.充电一段时间后,电解质溶液中的Na+ 浓度基本保持不变
D.充电过程中,外电路通过1 mol e−时,理论上两电极质量变化相差46g
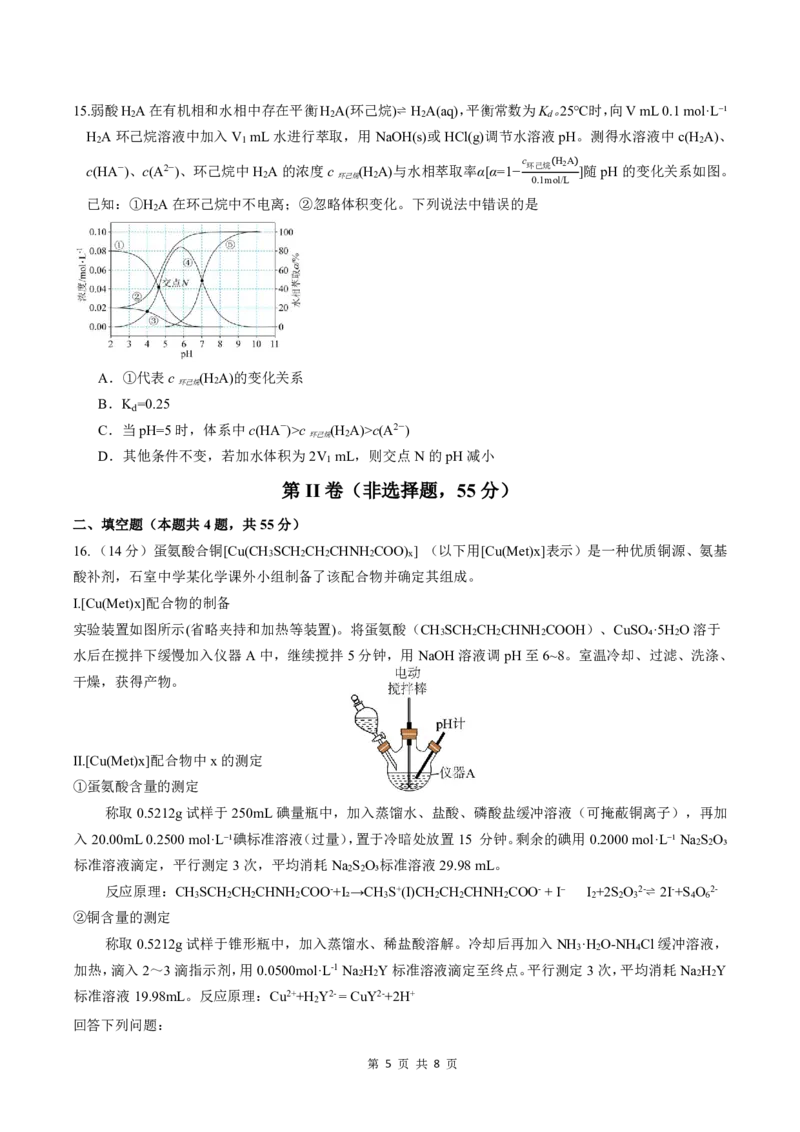
第 4 页 共 8 页15.弱酸H A在有机相和水相中存在平衡H A(环己烷)⇌ H A(aq),平衡常数为K。25℃时,向VmL0.1mol·L⁻¹
2 2 2 d
H A环己烷溶液中加入V mL水进行萃取,用NaOH(s)或HCl(g)调节水溶液pH。测得水溶液中c(H A)、
2 1 2
c(HA−)、c(A2−)、环己烷中H A的浓度c (H A)与水相萃取率α[α=1−
c
环己烷
H2A
]随pH的变化关系如图。
2 环己烷 2
0.1 mol/L
已知:①H A在环己烷中不电离;②忽略体积变化。下列说法中错误的是
2
A.①代表c (H A)的变化关系
环己烷 2
B.K =0.25
d
C.当pH=5时,体系中c(HA−)>c (H A)>c(A2−)
环己烷 2
D.其他条件不变,若加水体积为2V mL,则交点N的pH减小
1
第 II 卷(非选择题,55 分)
二、填空题(本题共4题,共55分)
16.(14分)蛋氨酸合铜[Cu(CH SCH CH CHNH COO) ] (以下用[Cu(Met)x]表示)是一种优质铜源、氨基
3 2 2 2 x
酸补剂,石室中学某化学课外小组制备了该配合物并确定其组成。
Ⅰ.[Cu(Met)x]配合物的制备
实验装置如图所示(省略夹持和加热等装置)。将蛋氨酸(CH SCH CH CHNH COOH)、CuSO₄·5H O溶于
3 2 2 2 2
水后在搅拌下缓慢加入仪器A中,继续搅拌5分钟,用NaOH溶液调pH至6~8。室温冷却、过滤、洗涤、
干燥,获得产物。
Ⅱ.[Cu(Met)x]配合物中x的测定
①蛋氨酸含量的测定
称取0.5212g试样于250mL碘量瓶中,加入蒸馏水、盐酸、磷酸盐缓冲溶液(可掩蔽铜离子),再加
入20.00mL0.2500mol·L⁻¹碘标准溶液(过量),置于冷暗处放置15 分钟。剩余的碘用0.2000mol·L⁻¹Na S O₃
2 2
标准溶液滴定,平行测定3次,平均消耗Na S O₃标准溶液29.98mL。
2 2
反应原理:CH SCH CH CHNH COO-+I₂→CH S+(I)CH CH CHNH COO-+I⁻ I +2S O 2-⇌ 2I-+S O 2-
3 2 2 2 3 2 2 2 2 2 3 4 6
②铜含量的测定
称取0.5212g试样于锥形瓶中,加入蒸馏水、稀盐酸溶解。冷却后再加入NH ·H O-NH Cl缓冲溶液,
3 2 4
加热,滴入2~3滴指示剂,用0.0500mol·L-1Na H Y标准溶液滴定至终点。平行测定3次,平均消耗Na H Y
2 2 2 2
标准溶液19.98mL。反应原理:Cu2++H Y2-=CuY2-+2H+
2
回答下列问题:
第 5 页 共 8 页(1)仪器A的名称是 。
(2)实验Ⅰ中验证产品是否洗涤干净的试剂是 。
(3)测定蛋氨酸合铜的组成时,称取试样应选用 (填标号)。
a.托盘天平 b.分析天平 c.台秤
(4)步骤①置于冷暗处放置15 分钟的目的是 ;
步骤①、②滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→ →开始滴定。
a.烘干 b.装入滴定液至零刻度以上 c.调整滴定液液面至零刻度或零刻度以下
d.用洗耳球吹出残余润洗液 e.排除气泡 f. 用滴定液润洗2至3次 g.记录起始读数
(5)下列说法正确的是 (填标号)
A.若测定铜含量时滴定管水洗后未用标准溶液润洗,测得[Cu(Met) ]中x偏小
x
B.若测定蛋氨酸含量时,滴定终点时俯视读数,测得[Cu(Met) ]中x偏小
x
C.若测定蛋氨酸含量时,滴定前滴定管尖嘴处有气泡,滴定后气泡消失,测得[Cu(Met) ]中x偏小
x
(6)①根据实验数据,[Cu(Met) ]中x= (保留1位有效数字)。
x
②已知蛋氨酸合铜结构中含五元环,请写出其结构简式(标出配位键) 。
③实验Ⅰ制备[Cu(Met)x]时用NaOH溶液调pH至6~8的原因是: 。
17.(13分)某含钒钢渣含FeO、Fe O 、SiO 、CaO、MgO和钒的相关化合物,一种从该废渣中无焙烧酸
2 3 2
浸提钒的新工艺流程如图所示。
已知:①该工艺中使用的NH Cl溶液pH≈6,故仅可选择性浸出一种元素,其他组分的浸出可忽略不计。
4
②溶液中相关离子开始沉淀和沉淀完全(c≤1.0×10−5mol⋅ L−1)时的pH:
Fe3+ Fe2+ Mg2+
开始沉淀的pH 2.2 7.5 8.1
沉淀完全的pH 3.8 9.5 9.4
回答下列问题:
(1)“粉碎”的目的是 。
(2)“沉钙”中发生反应的离子方程式为 。
(3)“酸化”和“调pH”后生成的混合液可返回 步骤(填步骤名称),实现试剂再生利用。
第 6 页 共 8 页(4)“第一次酸浸”后浸取液的主要成分有 (填化学式)。
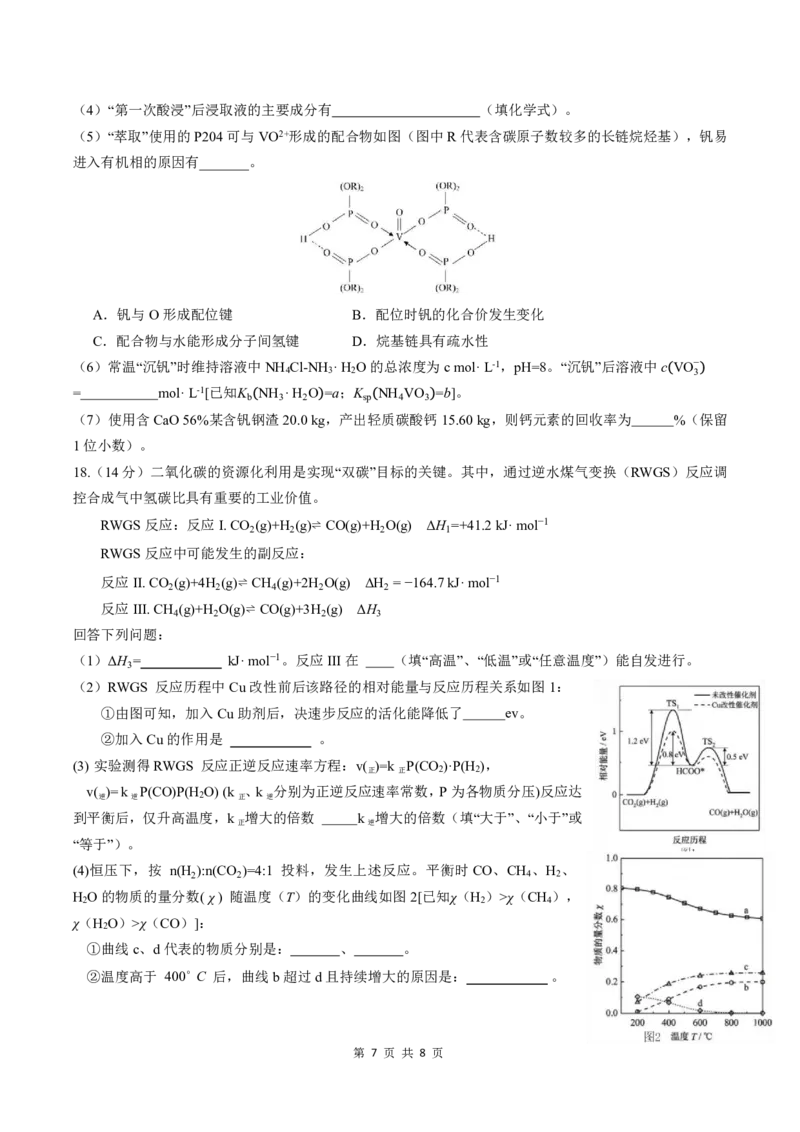
(5)“萃取”使用的P204可与VO2+形成的配合物如图(图中R代表含碳原子数较多的长链烷烃基),钒易
进入有机相的原因有_______。
A.钒与O形成配位键 B.配位时钒的化合价发生变化
C.配合物与水能形成分子间氢键 D.烷基链具有疏水性
(6)常温“沉钒”时维持溶液中NH Cl-NH ·H O的总浓度为cmol·L-1,pH=8。“沉钒”后溶液中c VO−
4 3 2 3
= mol·L-1[已知K NH ·H O =a;K NH VO =b]。
b 3 2 sp 4 3
(7)使用含CaO56%某含钒钢渣20.0kg,产出轻质碳酸钙15.60kg,则钙元素的回收率为 %(保留
1位小数)。
18.(14分)二氧化碳的资源化利用是实现“双碳”目标的关键。其中,通过逆水煤气变换(RWGS)反应调
控合成气中氢碳比具有重要的工业价值。
RWGS反应:反应I.CO (g)+H (g)⇌ CO(g)+H O(g) ΔH =+41.2kJ·mol−1
2 2 2 1
RWGS反应中可能发生的副反应:
反应II.CO (g)+4H (g)⇌ CH (g)+2H O(g) ΔH =−164.7 kJ·mol−1
2 2 4 2 2
反应III.CH (g)+H O(g)⇌ CO(g)+3H (g) ΔH
4 2 2 3
回答下列问题:
(1)ΔH = kJ·mol−1。反应III在 (填“高温”、“低温”或“任意温度”)能自发进行。
3
(2)RWGS 反应历程中Cu改性前后该路径的相对能量与反应历程关系如图1:
①由图可知,加入Cu助剂后,决速步反应的活化能降低了 ev。
②加入Cu的作用是 。
(3) 实验测得RWGS 反应正逆反应速率方程:v( )=k P(CO )·P(H ),
正 正 2 2
v( )=k P(CO)P(H O)(k 、k 分别为正逆反应速率常数,P为各物质分压)反应达
逆 逆 2 正 逆
到平衡后,仅升高温度,k 增大的倍数 k 增大的倍数(填“大于”、“小于”或
正 逆
“等于”)。
(4)恒压下,按 n(H ):n(CO )=4:1 投料,发生上述反应。平衡时CO、CH 、H 、
2 2 4 2
H O的物质的量分数(χ) 随温度(T)的变化曲线如图2[已知χ(H )>χ(CH ),
2 2 4
χ(H O)>χ(CO)]:
2
①曲线c、d代表的物质分别是: 、 。
②温度高于 400∘ C 后,曲线b超过d且持续增大的原因是: 。
第 7 页 共 8 页(5)控制反应体系总压为PkPa,按 n(H ):n(CO )=4:1 投料,发生上述反应。600∘ C,达到平衡时,CO 的转
2 2 2
化率为 80%,CH 的选择性为 25%(已知 CH 选择性 =
n(CH4)
生成 ×100%)。该温度下反应III的平衡常数
4 4
n(CO2)
消耗
K = kPa2(用分压表示,列出计算式即可)。
p
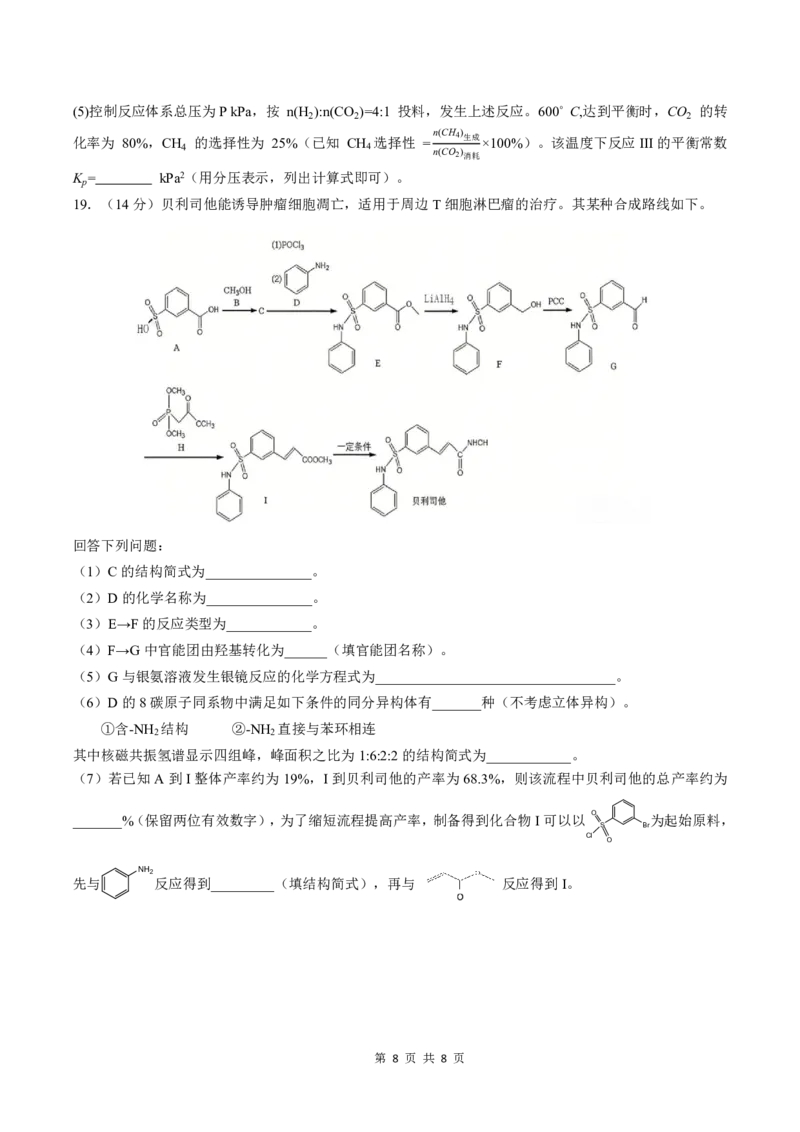
19.(14分)贝利司他能诱导肿瘤细胞凋亡,适用于周边T细胞淋巴瘤的治疗。其某种合成路线如下。
回答下列问题:
(1)C的结构简式为_______________。
(2)D的化学名称为_______________。
(3)E→F的反应类型为____________。
(4)F→G中官能团由羟基转化为______(填官能团名称)。
(5)G与银氨溶液发生银镜反应的化学方程式为__________________________________。
(6)D的8碳原子同系物中满足如下条件的同分异构体有_______种(不考虑立体异构)。
①含-NH 结构 ②-NH 直接与苯环相连
2 2
其中核磁共振氢谱显示四组峰,峰面积之比为1:6:2:2的结构简式为____________。
(7)若已知A到I整体产率约为19%,I到贝利司他的产率为68.3%,则该流程中贝利司他的总产率约为
_______%(保留两位有效数字),为了缩短流程提高产率,制备得到化合物I可以以 O 为起始原料,
S Br
Cl
O
NH2
先与 反应得到_________(填结构简式),再与 反应得到I。
第 8 页 共 8 页