文档内容
(在此卷上答题无效)
福州市 2026 届高中毕业班 4 月适应性练习
化 学
(完卷时间:75分钟;满分:100分)
友情提示:请将所有答案填写到答题卡上! 请不要错位、越界答题!
可能用到的相对原子质量:H 1 C 12 N 14 O 16 K 39
一、选择题:本题共 10 小题,每小题4分,共 40分。在每小题给出的四个选项
中,只有一项是符合题目要求的。
1.新一代人形机器人的“骨骼”“关节”“心脏”与“皮肤”等部件的制作都离
不开新型材料。下列说法正确的是
A.“骨骼”采用的高强度碳纤维增强环氧树脂属于无机非金属材料
B.“关节”框架金属钝化处理的过程,只发生物理变化
C.“心脏”所使用的固态和液态电池的能量转化方式不同
D.“皮肤”以石墨烯作感知材料,利用了石墨烯易导电等性质
2.藜芦醛是一种食用香料,可由如下反应制得。下列说法错误的是
A.该反应为取代反应
B.原儿茶醛分子中所有原子可能共平面
C.可以用FeCl 溶液鉴别原儿茶醛和藜芦醛
3
D.原儿茶醛的芳香族同分异构体均不能发生水解反应
3.X、Y、Z、W、M 为原子序数依次增大的短周期主族元素,M 的质子数是X的
3倍。由以上5种元素组成的某种盐的结构如图所示。下列说法正确的是
A.第一电离能:Z>W
B.简单离子的半径:W>M
C.键角:∠2 >∠1
D.最高价氧化物对应水化物的酸性:Y>Z
高三化学 — 1 — (共 8 页)4.以天然气、水和氮气等为原料,可合成氨和尿素[CO(NH ) ]。设 N 为阿伏加德
2 2 A
罗常数的值,下列说法正确的是
A.1 mol CO(NH ) 分子中含σ 键的数目为 7 N
2 2 A
B.2.8 g N 和1.6 g CH 所含电子数均为 N
2 4 A
C.1 mol NH 分子中氮原子的价电子对数为 3N
3 A
D.标准状况下,2.24 L H O的原子数为 0.3N
2 A
5.下列实验方法或操作能达到实验目的的是
选项 实验目的 实验方法(或操作)
将铁制镀件与铜片分别连接直流电源的
A 在铁制镀件表面镀铜
正、负极,浸入 CuSO 溶液中
4
探究温度对化学平衡的 加热0.1 mol·L⁻1 Fe(NO ) 溶液,观察溶
3 3
B
影响 液颜色变化
以甲基橙为指示剂,用标准 NaOH溶液
C 测定某醋酸溶液的浓度
滴定
验证 CH =CHCH OH中 向CH =CHCH OH中滴加少量酸性
2 2 2 2
D
含有碳碳双键 KMnO 溶液,振荡,观察溶液颜色变化
4
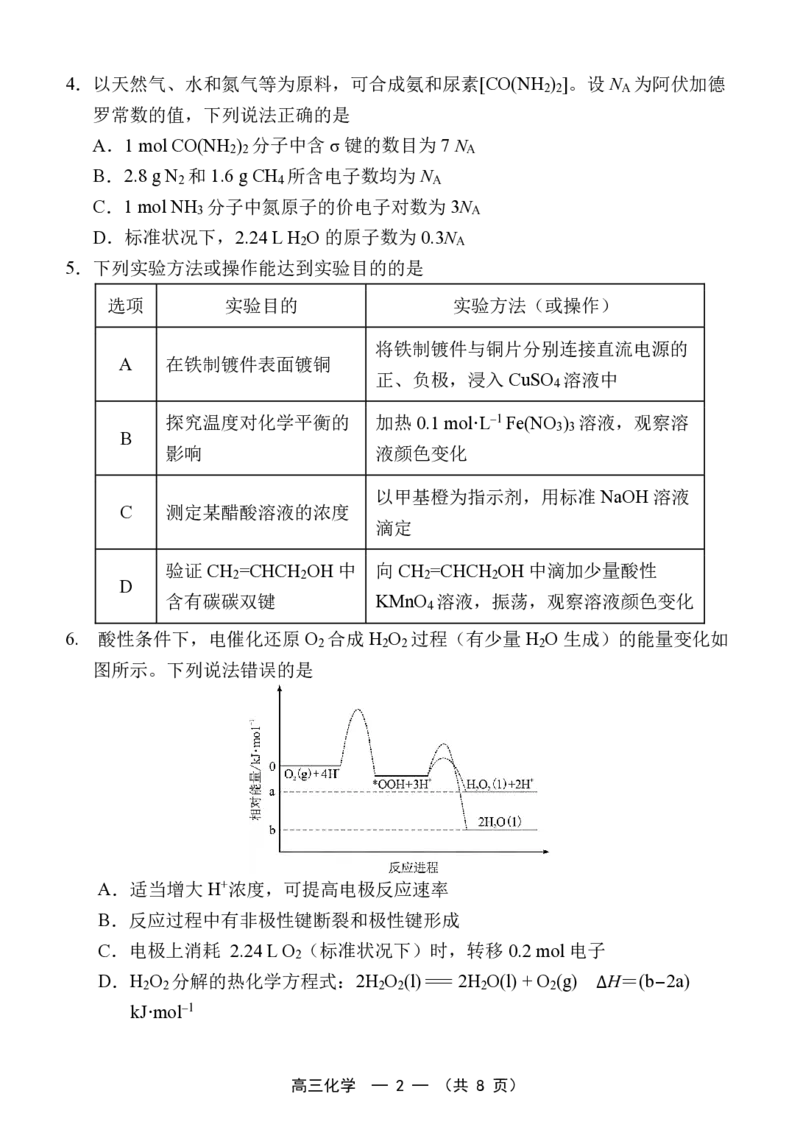
6. 酸性条件下,电催化还原 O 合成H O 过程(有少量 H O生成)的能量变化如
2 2 2 2
图所示。下列说法错误的是
A.适当增大H+浓度,可提高电极反应速率
B.反应过程中有非极性键断裂和极性键形成
C.电极上消耗 2.24 L O (标准状况下)时,转移0.2 mol 电子
2
D.H O 分解的热化学方程式:2H O (l)=2H O(l) + O (g) ∆H=(b-2a)
2 2 2 2 2 2
kJ·mol⁻1
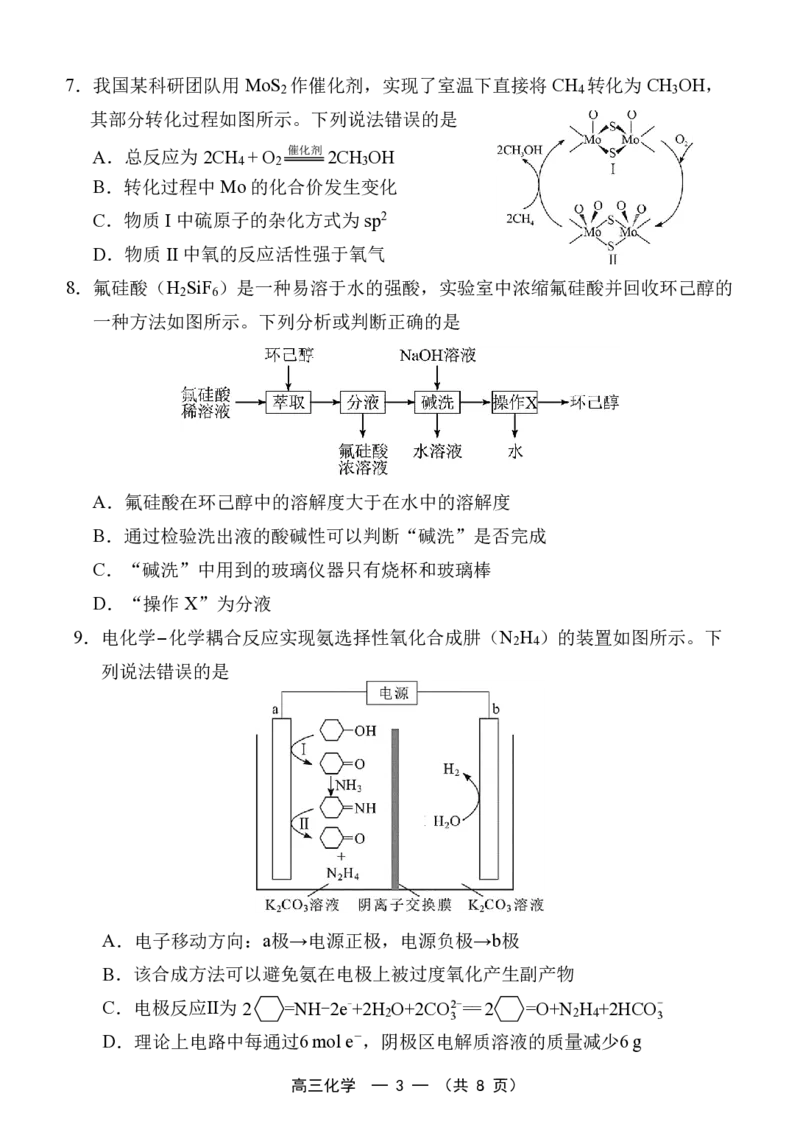
高三化学 — 2 — (共 8 页)7.我国某科研团队用 MoS 作催化剂,实现了室温下直接将 CH 转化为 CH OH,
2 4 3
其部分转化过程如图所示。下列说法错误的是
A.总反应为2CH + O
4 2
高三化学 — 3 — (共 8 页)
催 化 剂 2CH OH
3
B.转化过程中Mo 的化合价发生变化
C.物质I中硫原子的杂化方式为 sp2
D.物质II中氧的反应活性强于氧气
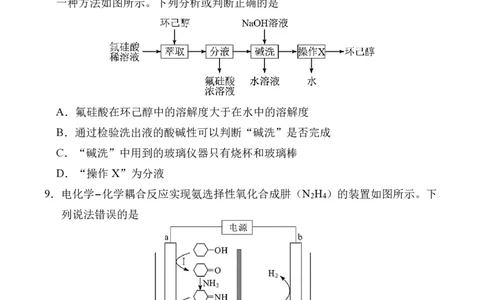
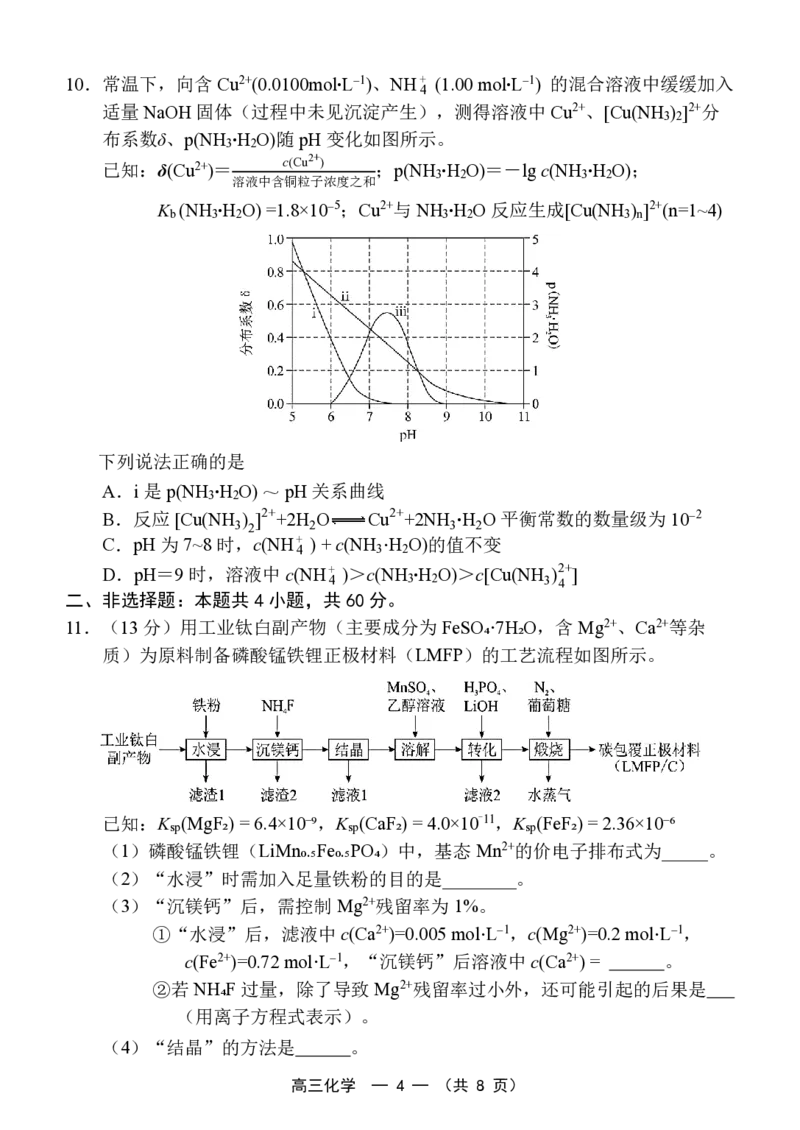
8.氟硅酸(H SiF )是一种易溶于水的强酸,实验室中浓缩氟硅酸并回收环己醇的
2 6
一种方法如图所示。下列分析或判断正确的是
A.氟硅酸在环己醇中的溶解度大于在水中的溶解度
B.通过检验洗出液的酸碱性可以判断“碱洗”是否完成
C.“碱洗”中用到的玻璃仪器只有烧杯和玻璃棒
D.“操作X”为分液
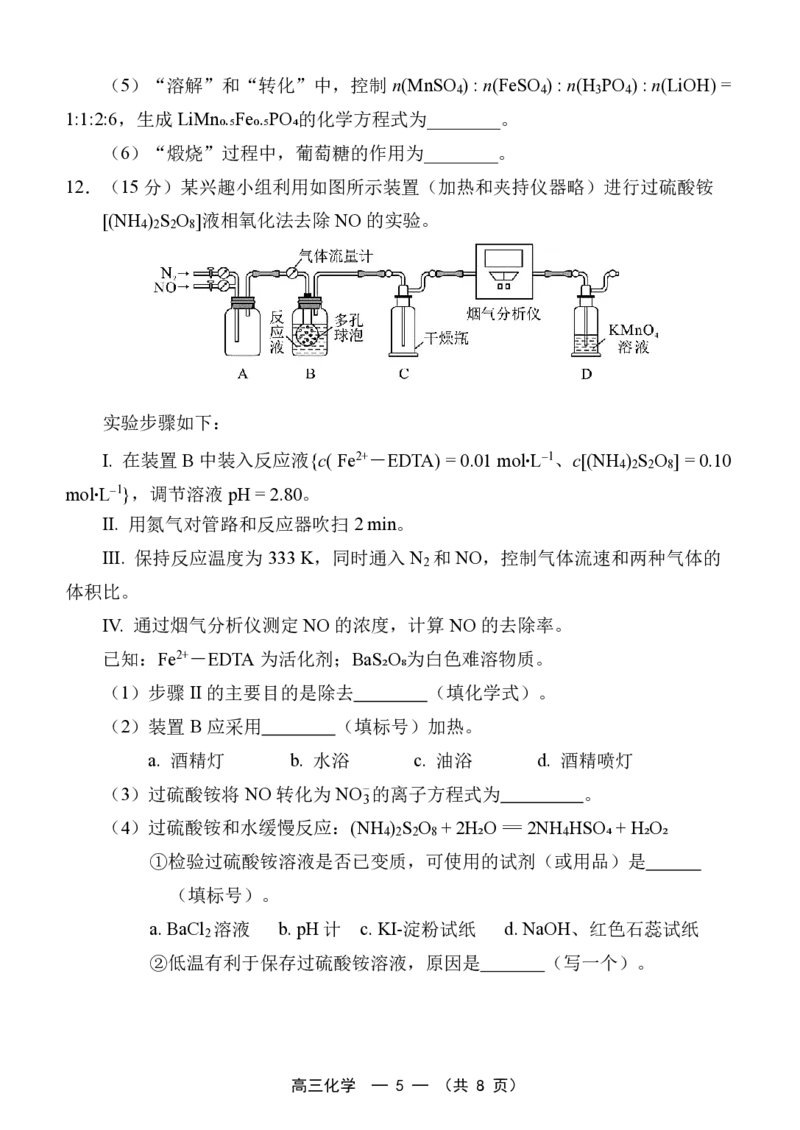
9.电化学-化学耦合反应实现氨选择性氧化合成肼(N H )的装置如图所示。下
2 4
列说法错误的是
–
A.电子移动方向:a极→电源正极,电源负极→b极
B.该合成方法可以避免氨在电极上被过度氧化产生副产物
C.电极反应Ⅱ为 2 =NH-2e-+2H
2
O+2CO 2
3
- == 2 =O+N
2
H
4
+2HCO -
3
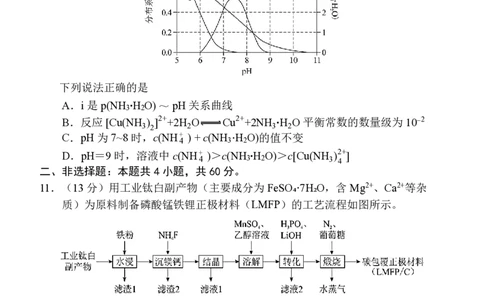
D.理论上电路中每通过6mol e-,阴极区电解质溶液的质量减少6g10.常温下,向含Cu2+(0.0100mol∙L⁻1)、NH + (1.00 mol∙L⁻1) 的混合溶液中缓缓加入
4
适量NaOH固体(过程中未见沉淀产生),测得溶液中 Cu2+、[Cu(NH ) ]2+分
3 2
布系数δ、p(NH ∙H O)随pH变化如图所示。
3 2
已知:δ(Cu2+)=
c(Cu2+)
;p(NH ∙H O)=-lg c(NH ∙H O);
3 2 3 2
溶液中含铜粒子浓度之和
K (NH ∙H O) =1.8×10⁻5;Cu2+与NH ∙H O反应生成[Cu(NH ) ]2+(n=1~4)
b 3 2 3 2 3 n
下列说法正确的是
A.i 是p(NH ∙H O) ~ pH关系曲线
3 2
B.反应 [Cu(NH ) ]2++2H O Cu2++2NH ∙H O 平衡常数的数量级为 10⁻2
3 2 2 3 2
C.pH为7~8时,c(NH + ) + c(NH ·H O)的值不变
4 3 2
D.pH=9时,溶液中 c(NH +
4
)>c(NH
3
∙H
2
O)>c[Cu(NH
3
)
4
2+]
二、非选择题:本题共 4小题,共60分。
11.(13分)用工业钛白副产物(主要成分为 FeSO₄·7H₂O,含Mg2+、Ca2+等杂
质)为原料制备磷酸锰铁锂正极材料(LMFP)的工艺流程如图所示。
已知:K (MgF₂) = 6.4×10⁻⁹,K (CaF₂) = 4.0×10⁻11,K (FeF₂) = 2.36×10⁻⁶
sp sp sp
(1)磷酸锰铁锂(LiMn₀.₅Fe₀.₅PO₄)中,基态 Mn2+的价电子排布式为_____。
(2)“水浸”时需加入足量铁粉的目的是________。
(3)“沉镁钙”后,需控制 Mg2+残留率为 1%。
①“水浸”后,滤液中 c(Ca2+)=0.005 mol·L⁻1,c(Mg2+)=0.2 mol·L⁻1,
c(Fe2+)=0.72 mol·L⁻1,“沉镁钙”后溶液中c(Ca2+) = 。
②若NH₄F 过量,除了导致 Mg2+残留率过小外,还可能引起的后果是
(用离子方程式表示)。
(4)“结晶”的方法是 。
高三化学 — 4 — (共 8 页)(5)“溶解”和“转化”中,控制n(MnSO ) : n(FeSO ) : n(H PO ) : n(LiOH) =
4 4 3 4
1:1:2:6,生成LiMn₀.₅Fe₀.₅PO₄的化学方程式为________。
(6)“煅烧”过程中,葡萄糖的作用为________。
12.(15分)某兴趣小组利用如图所示装置(加热和夹持仪器略)进行过硫酸铵
[(NH ) S O ]液相氧化法去除 NO的实验。
4 2 2 8
实验步骤如下:
I. 在装置B 中装入反应液{c( Fe2+-EDTA) = 0.01 mol∙L⁻1、c[(NH ) S O ] = 0.10
4 2 2 8
mol∙L⁻1},调节溶液pH = 2.80。
II. 用氮气对管路和反应器吹扫 2 min。
III. 保持反应温度为 333 K,同时通入 N 和NO,控制气体流速和两种气体的
2
体积比。
IV. 通过烟气分析仪测定 NO的浓度,计算 NO的去除率。
已知:Fe2+-EDTA 为活化剂;BaS₂O₈为白色难溶物质。
(1)步骤II的主要目的是除去 (填化学式)。
(2)装置B 应采用 (填标号)加热。
a. 酒精灯 b. 水浴 c. 油浴 d. 酒精喷灯
(3)过硫酸铵将NO 转化为NO - 的离子方程式为 。
3
(4)过硫酸铵和水缓慢反应:(NH ) S O + 2H₂O = 2NH HSO₄ + H₂O₂
4 2 2 8 4
①检验过硫酸铵溶液是否已变质,可使用的试剂(或用品)是
(填标号)。
a. BaCl 溶液 b. pH计 c. KI-淀粉试纸 d. NaOH、红色石蕊试纸
2
②低温有利于保存过硫酸铵溶液,原因是 (写一个)。
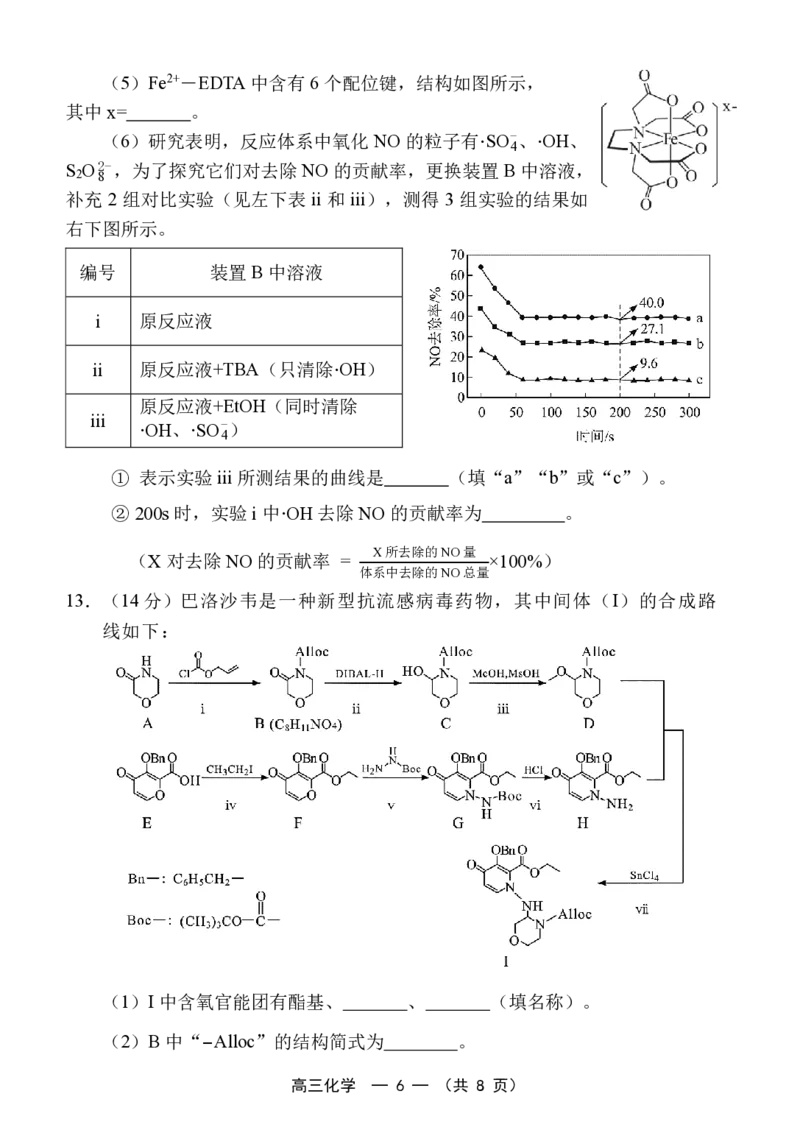
高三化学 — 5 — (共 8 页)(5)Fe2+-EDTA 中含有6个配位键,结构如图所示,
其中 x= 。
(6)研究表明,反应体系中氧化 NO 的粒子有·SO - 、·OH、
4
S O 2 - ,为了探究它们对去除 NO的贡献率,更换装置 B 中溶液,
2 8
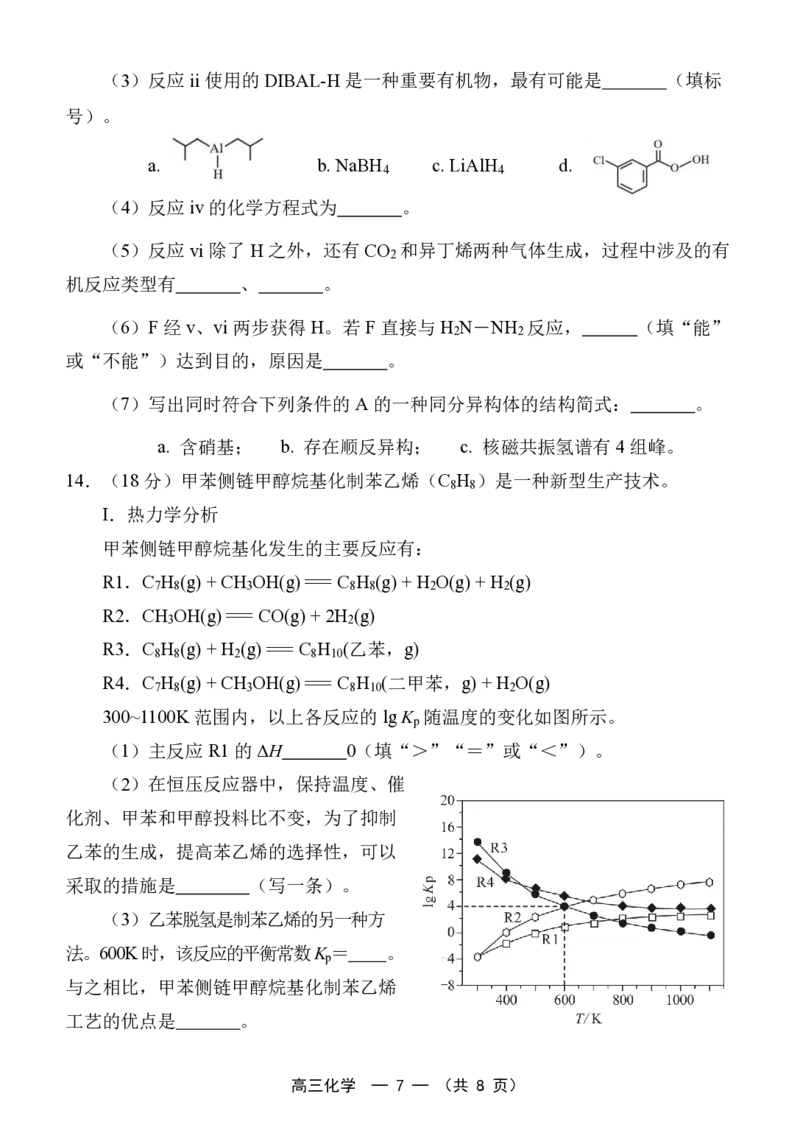
补充 2 组对比实验(见左下表 ii 和 iii),测得 3 组实验的结果如
右下图所示。
编号 装置 B 中溶液
i 原反应液
ii 原反应液+TBA(只清除·OH)
原反应液+EtOH(同时清除
iii
·OH、·SO - )
4
① 表示实验iii 所测结果的曲线是 (填“a”“b”或“c”)。
② 200s 时,实验 i 中·OH去除NO的贡献率为 。
X所去除的NO量
(X对去除NO 的贡献率 = ×100%)
体系中去除的NO总量
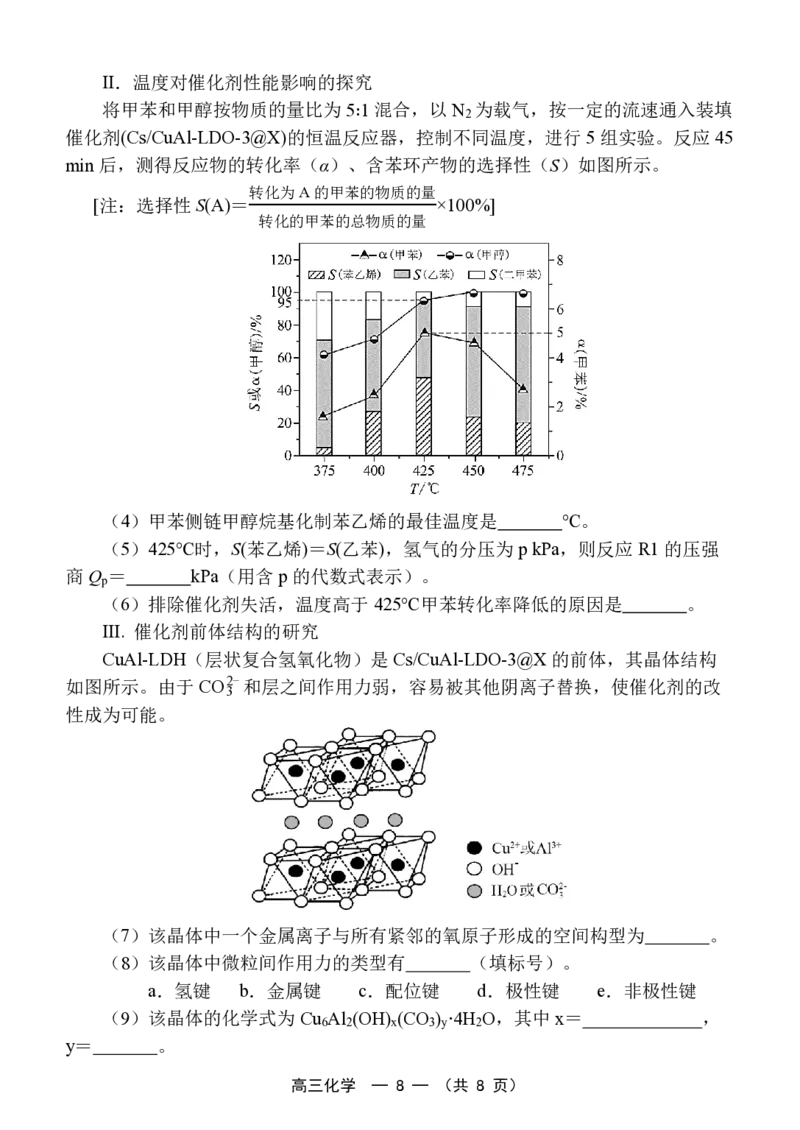
13.(14分)巴洛沙韦是一种新型抗流感病毒药物,其中间体(I)的合成路
线如下:
(1)I中含氧官能团有酯基、 、 (填名称)。
(2)B 中“-Alloc”的结构简式为 。
高三化学 — 6 — (共 8 页)(3)反应ii 使用的 DIBAL-H是一种重要有机物,最有可能是 (填标
号)。
a. b. NaBH c. LiAlH d.
4 4
(4)反应iv的化学方程式为 。
(5)反应vi 除了 H之外,还有CO 和异丁烯两种气体生成,过程中涉及的有
2
机反应类型有 、 。
(6)F 经v、vi 两步获得 H。若F 直接与 H N-NH 反应, (填“能”
2 2
或“不能”)达到目的,原因是 。
(7)写出同时符合下列条件的 A的一种同分异构体的结构简式: 。
a. 含硝基; b. 存在顺反异构; c. 核磁共振氢谱有 4组峰。
14.(18分)甲苯侧链甲醇烷基化制苯乙烯(C H )是一种新型生产技术。
8 8
I.热力学分析
甲苯侧链甲醇烷基化发生的主要反应有:
R1.C H (g) + CH OH(g)=C H (g) + H O(g) + H (g)
7 8 3 8 8 2 2
R2.CH OH(g)=CO(g) + 2H (g)
3 2
R3.C H (g) + H (g)=C H (乙苯,g)
8 8 2 8 10
R4.C H (g) + CH OH(g)=C H (二甲苯,g) + H O(g)
7 8 3 8 10 2
300~1100K范围内,以上各反应的 lg K 随温度的变化如图所示。
p
(1)主反应R1的 ΔH 0(填“>”“=”或“<”)。
(2)在恒压反应器中,保持温度、催
化剂、甲苯和甲醇投料比不变,为了抑制
乙苯的生成,提高苯乙烯的选择性,可以
采取的措施是 (写一条)。
(3)乙苯脱氢是制苯乙烯的另一种方
法。600K时,该反应的平衡常数K = 。
p
与之相比,甲苯侧链甲醇烷基化制苯乙烯
工艺的优点是 。
高三化学 — 7 — (共 8 页)II.温度对催化剂性能影响的探究
将甲苯和甲醇按物质的量比为 5∶1混合,以 N 为载气,按一定的流速通入装填
2
催化剂(Cs/CuAl-LDO-3@X)的恒温反应器,控制不同温度,进行 5 组实验。反应45
min 后,测得反应物的转化率(α)、含苯环产物的选择性(S)如图所示。
转化为A的甲苯的物质的量
[注:选择性S(A)= ×100%]
转化的甲苯的总物质的量
(4)甲苯侧链甲醇烷基化制苯乙烯的最佳温度是 ℃。
(5)425℃时,S(苯乙烯)=S(乙苯),氢气的分压为 p kPa,则反应 R1的压强
商 Q = kPa(用含 p的代数式表示)。
p
(6)排除催化剂失活,温度高于 425℃甲苯转化率降低的原因是 。
III. 催化剂前体结构的研究
CuAl-LDH(层状复合氢氧化物)是 Cs/CuAl-LDO-3@X的前体,其晶体结构
如图所示。由于 CO 2- 和层之间作用力弱,容易被其他阴离子替换,使催化剂的改
3
性成为可能。
(7)该晶体中一个金属离子与所有紧邻的氧原子形成的空间构型为 。
(8)该晶体中微粒间作用力的类型有 (填标号)。
a.氢键 b.金属键 c.配位键 d.极性键 e.非极性键
(9)该晶体的化学式为 Cu Al (OH) (CO ) ·4H O,其中x= ,
6 2 x 3 y 2
y= 。
高三化学 — 8 — (共 8 页)