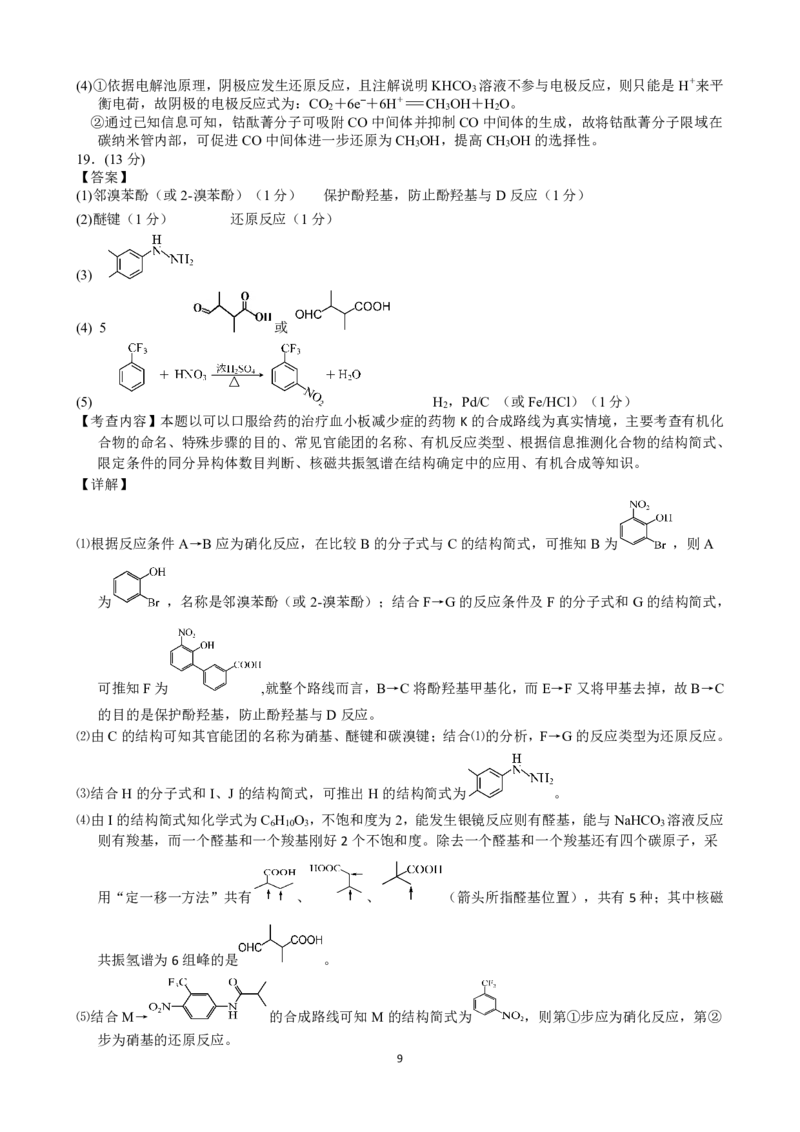文档内容
达州市普通高中 2026 届第二次诊断性测试
化学参考答案详解
第Ⅰ卷(选择题,共 45 分)
一、单项选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是最符
合题目要求的。
1.【答案】D
【考查内容】化学与STSE
【分析】本题以“达州美食文化”为情境,融合有机化学和化学与生活考点。题目围绕米粉、鸡蛋清、牛肉、
茶叶等日常食物,将淀粉、蛋白质变性、美拉德反应、茶叶抗氧化等核心知识串联,考查了学生对宏
观现象的微观解释能力及化学与生活的联系,体现了学科核心素养。
【详解】
A.包裹羊肉的米粉主要成分是淀粉,淀粉由多个葡萄糖单元组成,属于多糖,A错误;
B.加热鸡蛋清,会使鸡蛋清(蛋白质)变性,不是蛋白质的盐析,B错误;
C.高温炭火烘烤牛肉产生的香味,是牛肉中的蛋白质与糖类发生美拉德反应,同时蛋白质发生高温热分
解,并伴随脂肪的氧化裂解。这些反应生成了大量含有焦香、肉香和脂香的挥发性有机物。不是酯类
水解产生的,C错误;
D.茶多酚和维生素C均为强还原剂,具有抗氧化作用,能清除体内氧自由基、保护蛋白质及肠道膜蛋白
的结构与功能,从而减少蛋白质因氧化造成的损伤,间接促进蛋白质的吸收与利用,D正确;
2.【答案】C
【考查内容】化学用语
【分析】本题以化学用语的规范表达为背景,考查化学基础核心知识。涉及用于核素,分子间氢键,σ键
电子云轮廓图,以及VSEPR模型等考点,提升考生化学用语规范辨析能力,微观结构表征能力及逻辑
推理能力,培养宏观辨识与微观探析的核心素养。
【详解】
A.用于考古断代的碳的核素为放射性的14C,A正确;
6
B.因O的电负性大于N,O-H键极性更强,使H原子更接近“裸核”,与N的孤对电子吸引力更强,故该
氢键作用最强烈,即NH 和H O之间最强烈的氢键作用为: ,B正确;
3 2
C.HF中的σ键为s-pσ键,因此其电子云轮廓图应为 ,C错误;
D.SO2-的中心原子S周围的价层电子对数为:3+ ×(6+2-3×2)=4,有1对孤电子对,则SO2-的VSEPR
3 3
1
2
模型为: ,D正确;
3.【答案】C
【考查内容】阿伏加德罗常数N
A
【分析】本题以消除采矿业胶液中的氰化物为背景,聚焦阿伏加德罗常数N 的综合应用。试题融合了物
A
质中π键数目、溶液中原子数目、反应中电子转移数目的计算,并结合溶液守恒关系进行考查,全面检
1测了学生对化学计量关系的掌握程度及微观粒子的计算能力。
【详解】
A.1molKCN中含有1molCN-离子,CN-离子中存在碳氮三键,三键中有两个π键和一个σ键,所以1mol
CN-中含有的π键数目2N ,则0.5molCN-中含有的π键数目N ,A错误;
A A
B.常温常压下,100g质量分数为17% 的H O 溶液中,H O 的质量为100g×17%=17g,水的质量为100g
2 2 2 2
m 17g
–17g=83g。n(H O )= = =0.5mol,含有H原子数目为N ,H O中还含有H原子,因此
2 2 M 34g•mol-1 A 2
100g溶液中含有H原子数目大于N ,故B错误;
A
C.KCN+H O +H O==KHCO +NH ↑,生成1molNH 时转移2mol电子,因此生成0.3molNH 时,转
2 2 2 3 3 3 3
移电子的数目为0.6N ,故C正确;
A
D.HCO-既能水解又能电离,含碳微粒有HCO-、CO2-、H CO ,根据物料守恒HCO-、CO2-、H CO
3 3 3 2 3 3 3 2 3
数之和为0.1N ,故D错误;
A
4.【答案】B
【考查内容】化学实验基础-实验方案设计
【分析】本题聚焦化学实验现象分析、反应原理应用、物质性质与规律推导等核心知识。核心考点包括氧
化还原反应中氧化性强弱的判断、盐类水解的规律、离子的检验以及化学平衡的移动。提升考生实验
现象分析能力、逻辑推理能力、反应原理迁移应用能力及实验结论严谨性判断能力。培育证据推理与
模型认知、科学探究与创新意识、宏观辨识与微观探析的核心素养。
【详解】
A.检验NH +需要浓的强碱溶液同时加热使NH 挥发出来,加入稀氢氧化钠溶液同时未加热时试纸不变蓝
4 3
不能排除NH +存在,故A错误;
4
B.2NO (g) N O (g) ΔH<0,将充有NO 的密闭烧瓶放入热水中,平衡向逆反应方向移动,气体
2 2 4 2
颜色变深,则实验现象和结论均正确,故B正确;
C.Cl +KBrO ==Br +KClO ,只能说明BrO-的氧化性强于Cl ,而Br 作为还原产物,无法与Cl 比较
2 3 2 3 3 2 2 2
氧化性强弱,C错误;
D.CH COOH溶液中加入CH COONH 固体,溶液中CH COO-浓度增大,抑制CH COOH电离,平衡逆
3 3 4 3 3
向移动,溶液pH变大。CH COONH 溶液呈碱性结论是错的,D错误;
3 4
5.【答案】C
【考查内容】有机物的结构和性质
【分析】核心考点包括有机物共线共面判断、手性碳原子判断、同分异构体的判断、官能团性质及与Na
置换反应的定量计算,提升考生有机物结构分析能力、同分异构体推断能力、官能团性质迁移能力。
【详解】
A.具有4个手性碳原子: ,A错误;
B.含有饱和碳原子,具有甲烷的结构特点,所有碳原子不可能在同一平面上,故B错误;
C.青蒿酸不饱和度为5,其同分异构体可能有芳香族化合物,C正确;
D.题中没有说明气体是否处在标准状况下,D错误;
6.【答案】B
2【考查内容】离子方程式的书写
【分析】本题以典型离子反应为载体,重点判断物质是否拆分、反应类型(氧化还原/双水解)、反应先后
顺序与产物,同时考查守恒思想与规范书写,综合性强、易错点多,侧重对反应本质的理解。
【详解】
A.稀硝酸具有强氧化性,能将S2-氧化为硫单质,正确的离子方程式为3S2-+8H++2NO-==3S↓+2NO↑
3
+4H O,A错误;
2
B.Al3+与HS-发生完全双水解反应,生成Al(OH) 沉淀和H S气体,方程式符合反应原理,B正确;
3 2
C.在酸性条件下,IO-离子与I−离子反应生成I 单质,CH COOH是弱酸,则离子方程式为:6CH COOH
3 2 3 3
+5I−+IO-==3I +3H O+6CH COO−,C错误;
3 2 2 3
D.Ba(OH) 与NH HSO 按1:1混合反应,1molH+与1molOH-中和生成1molH O,1molBa2+与1molSO2-
2 4 4 2 4
生成1molBaSO 沉淀,还有1molOH-与1molNH +参与反应,D错误;
4 4
7.【答案】B
【考查内容】物质结构与性质
【分析】本题以干冰与冰的堆积方式、空间利用率、超分子选择性、键角大小的判断、醛基和氢氰酸加成
为载体,考查宏观辨识与微观探析、证据推理与模型认知、科学态度与社会责任化学学科核心素养,
要求学生从微观作用力、空间结构、电子效应角度分析结构与性质的关系,体现“结构决定性质、性质
决定应用”的化学思想。
【详解】
A.干冰的密度大于冰,是因为干冰中CO 是面心立方堆积,空间利用率高,而冰中水分子间存在氢键,
2
形成疏松的晶体结构,空间利用率低,A错误;
B.“杯酚”通过空腔大小选择性结合C ,实现与C 分离,故B正确;
60 70
C.BeCl 中中心Be原子为sp杂化,键角为180°,BCl 中中心B原子为sp2杂化,键角为120°,CCl 中
2 3 4
中心C原子为sp3杂化,键角为109°28′,三种物质中心原子都没有孤电子对,三者键角大小与孤电子
对无关,故C错误;
D.乙醛中醛基 C=O 极性强,电子云偏向氧,使羰基碳带部分正电荷,易被 CN-亲核进攻,乙醛与极性
分子HCN发生加成反应时,羰基氧带部分负电荷,H带正电荷,连接在氧原子上,反应生成 ,
D错误;
8.【答案】D
【考查内容】化学实验装置与操作
【分析】本题聚焦化学实验核心操作与装置设计逻辑。核心考点包括气体除杂、氧化还原滴定的操作、气
体的收集以及分子极性判断。强化考生对“实验原理-装置功能-操作规范”逻辑关系的理解与应用能力。
【详解】
A.碱石灰是碱性干燥剂,HCl是酸性气体,可被碱石灰吸收,而H 不与碱石灰反应,但气体应从干燥管
2
的粗口进入,细口排出,A错误;
B.溴水遇到KI则立刻会产生碘单质,遇淀粉立即变蓝,故不能用此方法测定KI溶液的浓度,且溴水不
能用碱式滴定管盛装,B错误;
C.NO与 CO 不反应,NO的相对分子质量为30,CO 相对分子质量为44,因此NO密度小于CO ,NO
2 2 2
应从短管通入,将密度更大的CO 从底部长管排出,才能收集NO,C错误;
2
D.水分子是极性分子,四氯化碳是非极性分子,带电的橡胶棒靠近时,极性分子会发生偏转,非极性分
子不偏转,可达到实验目的,D正确;
39.【答案】A
【考查内容】元素周期表与元素周期律
【分析】本题以元素周期律为核心依据,要求学生根据元素在周期表中的位置,判断半径、电负性、最高
价含氧酸酸性及沸点的变化规律。根据题干,W、X、Y、Z为短周期主族元素,原子序数依次增大;
基态X原子p轨道仅1个电子,电子排布式为1s22s22p1,推断X为B;Z的氢化物可用于蚀刻玻璃,Z
为F。再由Z的原子序数等于X的次外层电子数与Y的核外电子数之和,Y为N。X W 可发生剧烈水
2 6
解产生W的单质,W为H。
【详解】
A.YW 为NH ,Y W 为N H (肼),二者均存在分子间氢键,N H 比NH 形成的氢键更多,且N H
3 3 2 4 2 4 2 4 3 2 4
相对分子质量更大,沸点更高,A正确;
B.同一周期,从左到右,元素的电负性逐渐增大,则电负性Z(F)>X(B)。结合已知信息B H +6H O==
2 6 2
2H BO +6H ↑可推出B H 中H元素为﹣1价,H元素电负性比B元素大,电负性Z(F)>W(H)>X(B)。,
3 3 2 2 6
B错误;
C.根据原子半径递变规律,电子层越多,原子半径越大,同周期主族元素从左到右原子半径逐渐减小,
因此原子半径顺序为N>F>H,即Y>Z>W,C错误;
D.F元素电负性最大,非金属性最强,化合物中只有负价,没有正价,不能形成含氧酸,D错误;
10.【答案】B
【考查内容】反应历程、催化机理
【分析】核心考点包括催化剂的作用机制,化学键的断裂与生成判断,消去反应机理,碳原子的杂化方式,
总反应方程式的书写。提升考生反应历程分析能力,化学键变化辨析能力,催化反应机理理解应用能
力,培育宏观辨识与微观探析的核心素养。
【详解】
A.根据反应机理图可知产物还有H O,总反应方程式为:(CH ) CCH OH (CH ) C=CHCH +H O,
2 3 3 2 3 2 3 2
A正确;
B. 中碳正离子的杂化方式为sp2,B错误;
C.由图可知,反应中只涉及极性键的断裂和形成,C正确;
D.依据该机理可知C由羟基所连的C转移到邻碳,再由邻碳正离子与相连的碳之间形成双键推断
能发生消去反应,故D正确;
11.【答案】D
【考查内容】电化学
【分析】以我国科学家研制的可充电氢负离子全固态电池为真实情境,通过提供充放电原理和图示呈现信息,
以此考查电化学的基础知识:电解质离子的移动方向、电极的判断、电极反应式的正误判断及相关计算。根
据3NaAlH +6CeH Na AlH +2Al+6CeH 及图示信息可知,电池放电时A极为正极,电极反应
4 2 3 6 3
式为3NaAlH +6e-=Na AlH +2Al+6H-,B极为负极,电极反应式为CeH +H--e-=CeH ;充电时
4 3 6 2 3
A极为阳极,电极反应式为Na AlH +2Al+6H--6e-=3NaAlH ,B极为阴极,电极反应式为CeH +
3 6 4 3
e-=CeH +H-。
2
【详解】
A.放电时,H-移向负极,A正确。
B.充电时,阴极与外接电源的负极相接,B正确。
4C.依据上述分析,放电时B极电极反应式为CeH +H--e-=CeH ,C正确。
2 3
D.依据上述分析,充电时A极电极反应式为Na AlH +2Al+6H--6e-=3NaAlH ,A极质量增重,且每
3 6 4
转移1mole-,A极增重1g,D错误。
12.【答案】A
【考查内容】有机化学基础
【分析】有机化学中与高分子材料相关的选择题。主要考查单体分子的化学性质、聚合反应的类型判断及
聚合物重复单元的判定。
【详解】
A.由X的结构知,1molX完全水解生成3molH CO ,可消耗6molNaOH,A错误。
2 3
B.对比X、Y、Z三者的结构可知,合成Z的反应为加聚反应,原子利用率为100%,B正确。
C.1molY的结构中含2mol羟基,1mol 乙二酸的结构中含2mol羧基,满足缩聚反应的要素和特点,C
正确。
D.由C的分析可得出Z的结构如下: ,重复结构单元中含有X、Y的片段比为2∶3,
则n(N)∶n(S)∶n(O)=6∶6∶12,化为最简比n(N)∶n(S)∶n(O)=1∶1∶2,D正确。
13.【答案】C
【考查内容】晶体结构常识及简单计算
【分析】根据题中所给晶胞α=β=γ=90°,确定该晶胞为立方晶胞,Mg、
Ni、C三种原子分别位于晶胞的顶点、面心和体心,再确认1、2、
3号原子所处的位置,利用均摊法、分数坐标、密度计算公式及原
子位置关系可以解答本题。
【详解】
A.晶胞为立方晶胞,Mg、Ni、C三种原子分别位于晶胞的顶点、面心和体心,利用均摊法可知,一个晶
胞中Mg、Ni、C三种原子的个数分别为1、3、1,则晶体的化学式为MgNi C,A正确;
3
11
B.由题中所给原子1、2的分数坐标分别为(0,0,0)、( , ,1),则可确定原子3(位于晶胞右侧面心)的分数坐
22
11
标为(1, , ),B正确;
22
C.根据晶胞中Ni与Mg原子的最短距离为apm,可计算出晶胞参数为 apm= a×10−10cm, 再根据
M
密度计算公式可得晶胞密度ρ= g/cm3,C错误; 2 2
N ×( a×10−10)3
A
D.由C选项计算出晶胞参数为 apm,再根据原子1、2的位置关系,可得1和2原子间的距离为 apm,
2
D正确;
2 3
14.【答案】B
【考查内容】微型工艺流程题
【分析】根据题中所给废弃钢渣(含有FeO、Fe O 、CaO、SiO 和少量MnO等)的主要成分,可快速确定
2 3 2
设计流程的意图是去除Si、Fe、Ca元素,固定CO ,回收Mn元素并制取MnO •nH O。各除杂步骤物
2 2 2
质清楚,目的明确,再结合已知信息可做分析和计算。
【详解】
A.加入试剂A的目的是将溶液中的Fe2+氧化为Fe3+,而H O 、Cl 、MnO 等氧化剂均能在酸性条件下将
2 2 2 2
Fe2+氧化为Fe3+,A正确;
5B.“沉铁”时,加NH •H O调节溶液pH,使溶液中的Fe3+完全沉淀,而Mn2+不沉淀,则根据离子完全沉
3 2
淀时浓度c(Mn+)≤1.0×10−5mol/L,K [Fe(OH) ]=10−38.6,可得Fe3+完全沉淀时c(OH−)= =
sp 3
3Ksp[Fe(OH)3]
c(Fe3+)
mol/L=10−11.2mol/L,可得pH=2.8,所以应调节pH为2.8时Fe3+完全沉淀,B错误;
3 10−38.6
C.“沉1×锰10−
”
5前锰元素以Mn2+存在于溶液中,“沉锰”时发生反应的离子方程式为:2MnO-+3Mn2++(2+n)H
O
4 2
==5MnO •nH O↓+4H+,H+浓度增大,溶液pH变小,C正确;
2 2
D.根据题目所给钢渣中钙元素的质量分数为24%,钙的浸出率为90%,n(Ca)=n(CO ),所以m(CO )=
2 2
a×103×24%×90%
×44kg=237.6akg,D正确;
40
15.【答案】D
【考查内容】化学实验、水溶液中的离子平衡
【分析】本题以泡打粉的使用为情境,结合泡打粉主要成分NaHCO 和Na H P O (焦磷酸二氢二钠)进行考
3 2 2 2 7
查。核心考点包括离子浓度比较,电荷守恒应用,反应进行程度等,提升考生综合分析,图像解读,
数据处理及逻辑推导能力,培育宏观辨识与微观探析,证据推理与模型认知,变化观念与平衡思想的
核心素养。
【详解】
A.由图可知,随pH增大,H P O 中的H+逐渐被消耗,故①为H P O ,②为H P O-③为H P O2‾,④为HP O3-,
4 2 7 4 2 7 3 2 7 2 2 7 2 7
⑤为P O4-,故A错误;
2 7
B.根据A项分析,③代表H P O2‾的分布分数曲线,由图可知,当H P O2‾的分布分数为最大值时溶液的
2 2 7 2 2 7
pH<7,溶液显酸性,说明H P O2‾的电离大于水解,则c(HP O3-)>c(H P O-),故B错误;
2 2 7 2 7 3 2 7
C.由题干和图1信息可知,发生反应的离子方程式为:H P O2‾+HCO‾==HP O3-+CO↑+HO
2 2 7 3 2 7 2 2
D.反应OH-+H P O2‾==HP O3-+HO的平衡常数K= c(HP 2 O3 7 -) = K a3 (H 4 P 2 O 7 ) ,取③和④的交点,
2 2 7 2 7 2 c(H 2 P 2 O2 7 ‾)•c(OH-) K w
10-6.30
c(H P O2‾)=c(HP O3-),Ka (H P O )=c(H+)=1×10-6.3,则K= =107.70>105,认为反应进行完全;
2 2 7 2 7 3 4 2 7 10-14
或由图2中pH>9,H P O2‾的含量几乎为0,表明该能反应进行完全,故D正确;
2 2 7
第Ⅱ卷(非选择题,共 55 分)
二、填空题(本题4个小题,共55分)
16.(14分)
【答案】
(1) (1分)
(2)B SiO (1分)
2
(3)10‾9.2 增大反应物NH •H O的浓度,NH+消耗反应生成的OH‾,均有利于Co(OH) 溶解
3 2 4 2
2[Co(NH ) ]2++H O == 2[Co(NH ) ]3++2OH‾
3 6 2 2 3 6
(4)冷却结晶(1分) 加压酸浸(1分)
(5)C
【考查内容】工业流程题
【详解】
6(1)基态Ni2+的价电子排布图为 ;
(2)“加压酸浸”时各元素的浸出率受到
硝酸初始浓度、保温时间、浸出温度、
液固比等因素的影响,图1、2所示
为浸出温度和液固比对金属离子的
浸出率的影响,浸出温度、液固比应
选择铁的浸出率低,而其他金属浸出
率高的温度,读图1可知浸出温度应选择190℃,读图2可知液固比应选择1.6~1.7mL/g,故应应选择
B答案;矿石经硝酸加压酸浸后仅SiO 不溶,所得滤渣1的主要成分是SiO ;
2 2
(3)“氧化氨浸”时加入浓氨水与铵盐组成的缓冲溶液使Co(OH) 溶解为[Co(NH ) ]2+,溶解转化反应为
2 3 6
c{[Co(NH ) ]2+}·c2(OH‾)
Co(OH)+6NH [Co(NH)]2++2OH‾,平衡常数K= 3 6 ,[Co(NH ) ]2+ Co2+
2 3 36 3 6
c6(NH )
3
c{[Co(NH ) ]2+}
+6NH 对应K = 3 6 =1.0×105,K [Co(OH) ]=c(Co2+)•c2(OH‾)=10-14.2,则溶解转化反
3 稳 c6(NH )·c(Co2+) sp 2
3
应的平衡常数K=K ×K [Co(OH) ]=1.0×105×10-14.2=10-9.2;加入浓氨水与铵盐组成的缓冲溶液,
稳 sp 2
增大反应物NH •H O的浓度,NH+消耗反应生成的OH‾,均有利于Co(OH) 的溶解;根据已知信息
3 2 4 2
[Co(NH)]2+易被氧化为[Co(NH)]3+,所以加入H O 后反应的离子方程式为:2[Co(NH ) ]2++H O ==
36 36 2 2 3 6 2 2
2[Co(NH ) ]3++2OH‾;
3 6
(4)从浸出液中获得Mg(NO ) •6H O晶体的一系列操作为“蒸发浓缩、冷却结晶,过滤,洗涤,干燥”;
3 2 2
所得Mg(NO ) •6H O晶体经高温分解能得到NO ,再与O 和H O作用后生成HNO ,可返回到“加压
3 2 2 2 2 2 3
酸浸”工序循环利用;
(5)已知[Co(NH ) ]3+为正八面体形结构(如图3),配合物中心离子Co3+的配位数为6,
3 6
Co3+的价层电子对数为6,则杂化方式不可能为sp2、sp3、dsp3杂化,所以中心离
子Co3+的杂化方式为d2sp3;
17.(14分)
【答案】
(1)球形冷凝管(1分) 温度过低反应速率慢,温度过高浓盐酸挥发较多,均不利于金属铟溶解
(2)取滤液少量于洁净试管中,滴加2滴KSCN溶液,若溶液中未出现红色,则证明原溶液中的Fe3+已经
完全除去
(3)水(1分) 分水器中下层液体(水)的量不再增加(或回流液变得澄清)
(4)InCl •4H O InOCl+2HCl↑+3H O
3 2 2
(5)88.60 偏高
【考查内容】实验题
【详解】
(1)仪器B的名称为球形冷凝管;溶解金属铟时略微加热可加快反应速率,但浓盐酸易挥发,故加热温度不
能太高,则控温40~60℃的原因是温度过低反应速率慢,温度过高浓盐酸挥发较多,均不利于金属铟溶
解。
(2)除杂时除去溶液中的Fe3+,验证溶液中Fe3+已除尽的实验方案为:取滤液少量于洁净试管中,滴加2
滴KSCN溶液,若溶液中未出现红色,则证明原溶液中的Fe3+已经完全除去。
(3)控温回流时预先在分水器中加水,使用分水器将蒸出的环己烷与水的共沸物中的水进入下层,达到去除
7InCl •4H O中的H O的目的;当分水器中下层液体(水)的量不再增加或回流液变得澄清时,表明水
3 2 2
已经完全蒸出,可以停止加热。
(4)若直接加热InCl •4H O晶体,InCl 会发生水解反应生成InOCl,该反应的化学方程式为:InCl •
3 2 3 3
4H O InOCl+2HCl↑+3H O。
2 2
(5)根据题目所给信息,称取4.50g无水InCl 样品,配制成500mL待测液,取25.00mL待测液加入20.00
3
mL0.1000mol/LEDTA溶液(H Y2-)充分反应,再用0.05000mol/LCuCl 标准溶液滴定过量EDTA溶液,
2 2
终点时消耗标准溶液22.00mL,反应为In3++H Y2-==InY-+2H+,Cu2++H Y2-==CuY2-+2H+。这
2 2
是利用金属离子与 EDTA标准溶液进行络合滴定再返滴定的方法,则样品中InCl
3
(0.1000×20.00×10−3-0.05000×22.00×10−3)×221.5×500÷25
的质量分数列式为
4.50
×100%=88.6%;若滴定时其他操作无误,量取待测液时初始和结束读取滴定管
刻度方式如图3所示,表明所量取的待测液体积偏小,而计算时仍代入25.00mL
待测液进行计算,实际导致返滴定时所用CuCl 标准溶液体积偏小,则测定结果将
2
偏高。
18.(14分)
【答案】
(1)+41.2(1分) 高温(1分)
(2)BC
(3)①a 反应Ⅰ、Ⅲ均为放热反应,升高温度,平衡均逆向移动,CH OH的选择性降低;反应Ⅱ为吸热
3
反应,升高温度,反应Ⅱ平衡正向移动,反应Ⅲ逆向移动,均有利于升高CO的选择性
1
②0.125或
8
(4)①CO +6e‾+6H+==CH OH+H O
2 3 2
②碳纳米管内的钴酞菁分子吸附CO中间体,促进CO进一步还原为甲醇,使甲醇选择性高于管外。
【考查内容】本题以CO 催化加氢制甲醇的反应研究为真实情境,综合考查学生对反应原理的理解与应用,
2
着重考查盖斯定律、ΔG、平衡状态的标志、平衡常数的计算、电极反应式的书写等知识,以及学生对
图文内容进行综合分析与理解运用的能力。
【详解】
(1)根据盖斯定律:Ⅱ=Ⅰ-Ⅲ,ΔH =ΔH -ΔH =+41.2kJ/mol;根据ΔG=ΔH-TΔS,反应Ⅱ中ΔH>0,ΔS
2 1 3
>0,则反应II高温下能自发进行。
(2)恒温恒容的密闭体系且反应Ⅰ、Ⅲ反应前后气体分子数不等。
A.速率作为判断平衡状态的标志时,需指明两个方向,A错误。
B.由上分析可知,反应进行时体系的体积是个变量,则气体的密度是变量,根据“变量不变即平衡”得,
B正确。
C.根据反应知:CO 在消耗,n(CO )减小,CH OH在生成,n(CH OH)增多,则n(CO )∶n(CH OH)是个
2 2 3 3 2 3
变量,C正确。
K
D.恒温条件,K不变, 1恒定,D错误。
K
2
(3)①依据图1及温度对平衡移动的影响规律:反应Ⅰ、Ⅲ均为放热反应,升高温度,平衡均逆向移动,CH OH
3
的选择性降低;反应Ⅱ为吸热反应,升高温度,反应Ⅱ平衡正向移动,反应Ⅲ逆向移动,均有利于升
高CO的选择性,故表示CH OH选择性的曲线为a。
3
②由⑶①分析及图1的数据可知:M点,CO 的转化率与CH OH的选择性均为50%,再结合元素守恒,
2 3
平衡时n(CO )=0.5mol,n(CH OH)=n(CO)=0.25mol,n(H O)=0.5mol,n(H )=2mol,n(总)=4.5mol。
2 3 2 2
0.25 0.5
3 3
1
K= 4.5 4.5 =0.125或
p
0.5 2 8
3 3
4.5 4.5
8(4)①依据电解池原理,阴极应发生还原反应,且注解说明KHCO 溶液不参与电极反应,则只能是H+来平
3
衡电荷,故阴极的电极反应式为:CO +6e‾+6H+==CH OH+H O。
2 3 2
②通过已知信息可知,钴酞菁分子可吸附CO中间体并抑制CO中间体的生成,故将钴酞菁分子限域在
碳纳米管内部,可促进CO中间体进一步还原为CH OH,提高CH OH的选择性。
3 3
19.(13分)
【答案】
(1)邻溴苯酚(或2-溴苯酚)(1分) 保护酚羟基,防止酚羟基与D反应(1分)
(2)醚键(1分) 还原反应(1分)
(3)
(4) 5 或
(5) H ,Pd/C (或Fe/HCl)(1分)
2
【考查内容】本题以可以口服给药的治疗血小板减少症的药物K的合成路线为真实情境,主要考查有机化
合物的命名、特殊步骤的目的、常见官能团的名称、有机反应类型、根据信息推测化合物的结构简式、
限定条件的同分异构体数目判断、核磁共振氢谱在结构确定中的应用、有机合成等知识。
【详解】
⑴根据反应条件A→B应为硝化反应,在比较B的分子式与C的结构简式,可推知B为 ,则A
为 ,名称是邻溴苯酚(或2-溴苯酚);结合F→G的反应条件及F的分子式和G的结构简式,
可推知F为 ,就整个路线而言,B→C将酚羟基甲基化,而E→F又将甲基去掉,故B→C
的目的是保护酚羟基,防止酚羟基与D反应。
⑵由C的结构可知其官能团的名称为硝基、醚键和碳溴键;结合⑴的分析,F→G的反应类型为还原反应。
⑶结合H的分子式和I、J的结构简式,可推出H的结构简式为 。
⑷由I的结构简式知化学式为C H O ,不饱和度为2,能发生银镜反应则有醛基,能与NaHCO 溶液反应
6 10 3 3
则有羧基,而一个醛基和一个羧基刚好2个不饱和度。除去一个醛基和一个羧基还有四个碳原子,采
用“定一移一方法”共有 、 、 (箭头所指醛基位置),共有5种;其中核磁
共振氢谱为6组峰的是 。
⑸结合M→ 的合成路线可知M的结构简式为 ,则第①步应为硝化反应,第②
步为硝基的还原反应。
9