文档内容
泸县五中高2024级高一下学期第一学月考试
化学试题
化学试卷分为第一部分(选择题)和第二部分(非选择题)两部分。
满分:100分。考试时间:75分钟。
注意事项:
相对原子质量:H-1 O-16 S-32 Fe-56 Cu-64 Cl-35.5 Ag-108
第一部分 选择题(共42分)
一、选择题:本题共14小题,每小题3分,共42分。每小题给出的四个选项中,只有一项是
符合题目要求。
1.下列物质在溶于水时既需要破坏离子键也需要破坏共价键的是
A. B. C. D.
2.关于化学键和分子间作用力,下列说法中不正确的是
A.氢键是一种较强的分子间作用力 B.分子间作用力就是分子间的引力
C.含有阳离子的物质,不一定含离子键 D.某化合物中存在离子键,它一定是离子化合物
3.下列物质的转化不能一步实现的是
A. B.
C. D.
4.科学家通过测量不同碳库中 与 的比值追踪碳的来源和流动,帮助了解全球碳循环过程。下列有关
叙述正确的是
A. 与 间的转化属于化学变化 B. 与 化学性质不相同
C.等质量的 与 的质子数相同 D.每个 的质量约为
5.下列溶液的存放不能使用磨口玻璃塞的是
①氢氟酸 ②NaHSO ③KNO ④石灰水 ⑤CuSO ⑥NaOH ⑦NaSiO
4 3 4 2 3
A.④⑤⑥⑦ B.①④⑥ C.①③⑤ D.①④⑥⑦
6. 为短周期主族元素,原子序数依次增大,最外层电子数之和为19。 的最外层电子数与
其 层电子数相等, 是形成酸雨的物质之一、下列说法正确的是
A.原子半径: B.简单氢化物的沸点:
C. 与 可形成共价化合物 D. 的最高价含氧酸是弱酸
7.探究铜和浓硫酸的反应,下列装置或操作不能达到实验目的的是
A.上下移动装置甲中的铜丝可以控制反应的发生和停止
B.装置乙可用于收集SO 气体
2C.将装置甲试管中的液体经图丙操作稀释,观察稀释液颜色可确定铜与浓硫酸反应有CuSO 的生成
4
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO ·5H O
4 2
8.下列有关方程式正确的是
A. 溶液与少量 溶液反应:
B.向 溶液中滴加少量的 溶液:
C.用硫代硫酸钠溶液脱氯:
D.过量 与 (含酚酞)溶液由红色变无色:
9.已知 。设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.等物质的量的NH 和N 的分子数均为N
3 2 A
B.反应中每生成6.4gCu,NH 失去的电子数为0.2N
3 A
C.标准状况下,2.24LH O中含有的极性共价键数为0.2N
2 A
D.将0.2molNH 溶于水得到的1L氨水中,含有的NH •H O分子数为0.2N
3 3 2 A
10.如图所示的物质可用于治疗汞中毒,其中X、W、Y、M、Z是原子序数依次增大的短周期主族元素,
Y与Z位于同一主族,下列说法错误的是
A.简单离子半径:
B.M、Z和Y3种元素形成的化合物超过2种
C.简单氢化物的沸点:
D.该物质中除X外,其他原子均满足8电子稳定结构
11.将10g铜镁合金完全溶解于100mL某浓度的硝酸中,得到NO和 (不考
虑 )共0.3mol,向反应后的溶液中加入 溶液0.8L,此时溶液呈
中性,金属离子已完全沉淀,沉淀质量为18.5g。下列说法错误的是
A.该硝酸的物质的量浓度为
B.合金中铜与镁的物质的量之比为2:3
C.混合气体中NO和 的体积之比为1:2
D.铜镁合金溶解后,溶液中剩余 的物质的量为0.3mol
12.根据物质类别预测物质性质是常用的方法之一,下列预测正确的是
选项 已知性质 性质预测
A Fe能置换出 溶液中的Cu Na也能置换出 溶液中的Cu
B 氮气与氧气不容易化合 磷单质与氧气也不容易化合
C 能使澄清石灰水变浑浊 也能使澄清石灰水变浑浊
第 2 页 共 7 页D 通入氯化钡溶液,溶液不变浑浊 通入硝酸钡溶液,溶液也不变浑浊
A.A B.B C.C D.D
13.某溶液含 、 、 、 、 、 中的几种,且各离子浓度相等。为明确其组成,进行如下
实验:
①取少量溶液,加入足量稀盐酸酸化的Ba(NO ) 溶液,产生白色沉淀,过滤;
3 2
②取部分①滤液,加入足量的NaOH溶液,产生红褐色沉淀,微热,产生气体;
③取部分①滤液,加入足量硝酸酸化的AgNO 溶液,产生白色沉淀
3
关于原溶液的说法正确的是
A.需通过焰色试验确定 是否存在 B.不能确定 是否存在
C.由实验③现象可判断原溶液中含有 D.溶液中一定存在 、 、 、
14.向 稀 与稀 的混合溶液中逐渐加入铁 粉,假
设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如 图所
示,且曲线中每一段只对应一个反应。下列说法正确的是
A.A点溶液中存在 和
B.原混合溶液中 和 的浓度比为
C.
D.AB段发生的反应为置换反应
第二部分非选择题(共58分)
二、非选择题:本题共4小题,共58分。
15.(16分)A、B、D、E、X是原子序数依次增大的五种短周期元素。A是周期表中相对原子质量最小的
元素,A、B能形成两种液态化合物AB和AB 。D是短周期中原子半径最大的主族元素,E的周期序数和
2 2 2
族序数相等,D、X的原子最外层电子数之和为8。
(1)A B 的电子式为 。
2 2
(2)E在周期表中的位置是 。写出工业制备E单质原理的化学方程式 。E单质的熔点
D单质的熔点(填“高于”或“低于”)
(3)D、X两元素的最高价氧化物对应水化物相互反应的离子方程式为 。
(4)镓( Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
315G技术的发展,GaN商用进入快车道。下列相关说法中,正确的是 (填字母序号)。
A.Ga位于元素周期表的第四周期
B.GaN中Ga的化合价为+3
C.Ga3+的离子半径小于E3+的离子半径
(5)XB 是一种高效消毒剂,工业上用其处理偏中性废水中的锰,使Mn2+转化为MnO 沉淀除去,X被还原至
2 2
最低价,该反应的离子方程式为 。
(6)亚硝酸(HNO)是一种弱酸,其钠盐NaNO 具有毒性,含NaNO 的废水直接排放会引起严重的水体污染,
2 2 2
通常采用还原法将其转化为对环境无污染的气体排放,如工业上采用KI或NH Cl处理。
4
①请写出NH Cl与NaNO 反应的离子方程式: 。
4 2
②NaNO 有咸味,易被误当作食盐食用而造成中毒,请写出一种简单的方法鉴别NaCl和NaNO :
2 2
。
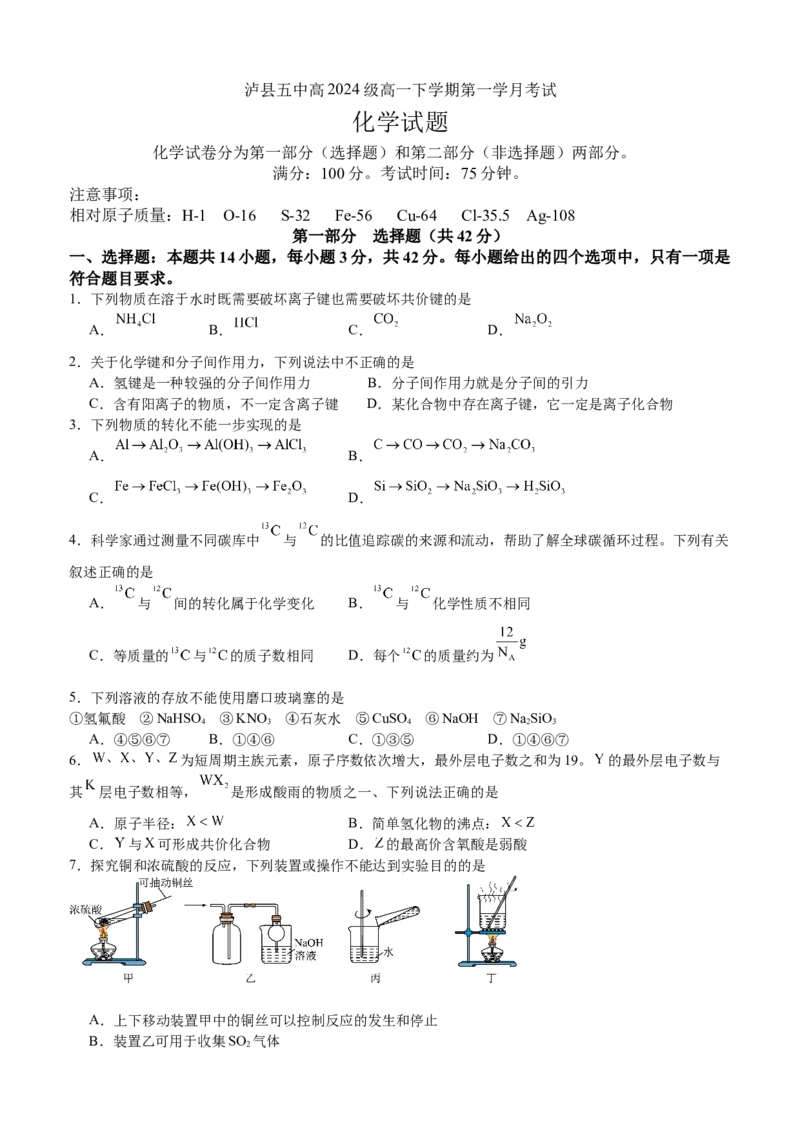
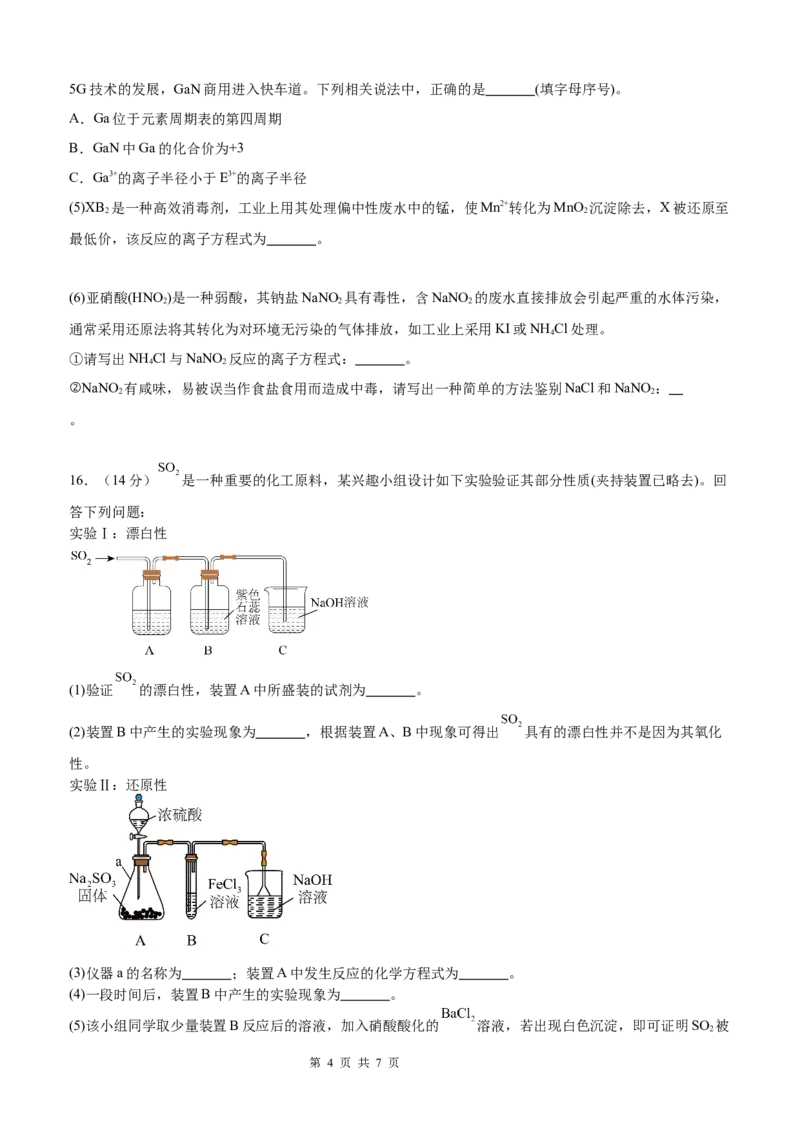
16.(14分) 是一种重要的化工原料,某兴趣小组设计如下实验验证其部分性质(夹持装置已略去)。回
答下列问题:
实验Ⅰ:漂白性
(1)验证 的漂白性,装置A中所盛装的试剂为 。
(2)装置B中产生的实验现象为 ,根据装置A、B中现象可得出 具有的漂白性并不是因为其氧化
性。
实验Ⅱ:还原性
(3)仪器a的名称为 ;装置A中发生反应的化学方程式为 。
(4)一段时间后,装置B中产生的实验现象为 。
(5)该小组同学取少量装置B反应后的溶液,加入硝酸酸化的 溶液,若出现白色沉淀,即可证明SO 被
2
第 4 页 共 7 页氧化为 。该做法 (填“合理”或“不合理”),理由是 。
(6)为了验证SO 具有还原性,实验中可以代替 溶液的试剂有_______(填字母)。
2
A.浓硫酸 B.酸性 KMnO 溶液 C.碘水 D.NaCl溶液
4
17.(14分)我国是氧化铝出产大国,一种利用铝土矿 主要成分为 、 和 制备 的工
艺流程如图所示。请回答下列问题:
已知:“滤液1”中的溶质为NaOH和 。
(1)下列说法正确的是 填标号 。
A. 属于酸性氧化物
B.Al是地壳中含量最多的金属元素
C. 可以一步转化为
(2)“悬浊液”加热至 时, 会快速与NaOH溶液反应,该反应的化学方程式为
。
(3)“操作a”的名称为 ;物质 X的化学式为 。
(4)“滤液1”中加入 溶液后,会生成 、 、 和 等,发生反应生成
的离子方程式为 ;实验室模拟 制备 ,需要使用到下列仪器中的
填仪器名称 。(5) 常被用来制造耐火材料和研磨材料,如制造耐火砖、耐火坩埚、砂纸、砂轮等,由此可知 具
有的性质为 。工业上常利用电解熔融的 来制备铝,电解 时,氧化产物与还原产物的
物质的量之比为 。
18.(14分)工业成机动车尾气中的NO会造成环境问题,可用多种方法脱除。
(1)碱液吸收:石灰乳可吸收硝酸工业的尾气(含NO、NO ),获得副产品 Ca(NO )
2 2 2。
①等物质的量NO与NO 被Ca(OH) 吸收反应的化学方程式为 。
2 2
②采用气-液逆流接触吸收(尾气从塔底进入,石灰乳从塔顶喷淋),其目的是 。
③该工艺需控制NO和NO 的物质的量之比接近1:l,若n(NO):n(NO )<1:1,
2 2
则会导致 ;若n(NO):n(NO )>1:1,则会导致 。
2
④生产中需保持弱碱性,在酸性溶液中Ca(NO ) 会发生含解,产物之一是NO,其反应的离子方程式为
2 2
。
(2)氧化法:“FeSO -H O”试剂可将NO氧化为可溶的 。
4 2 2
①Fe2+催化HO 分解产生有很强的氧化性的HO·,HO·将NO氧化为 的反应机理如图所示,Y的化学式
2 2
为 。
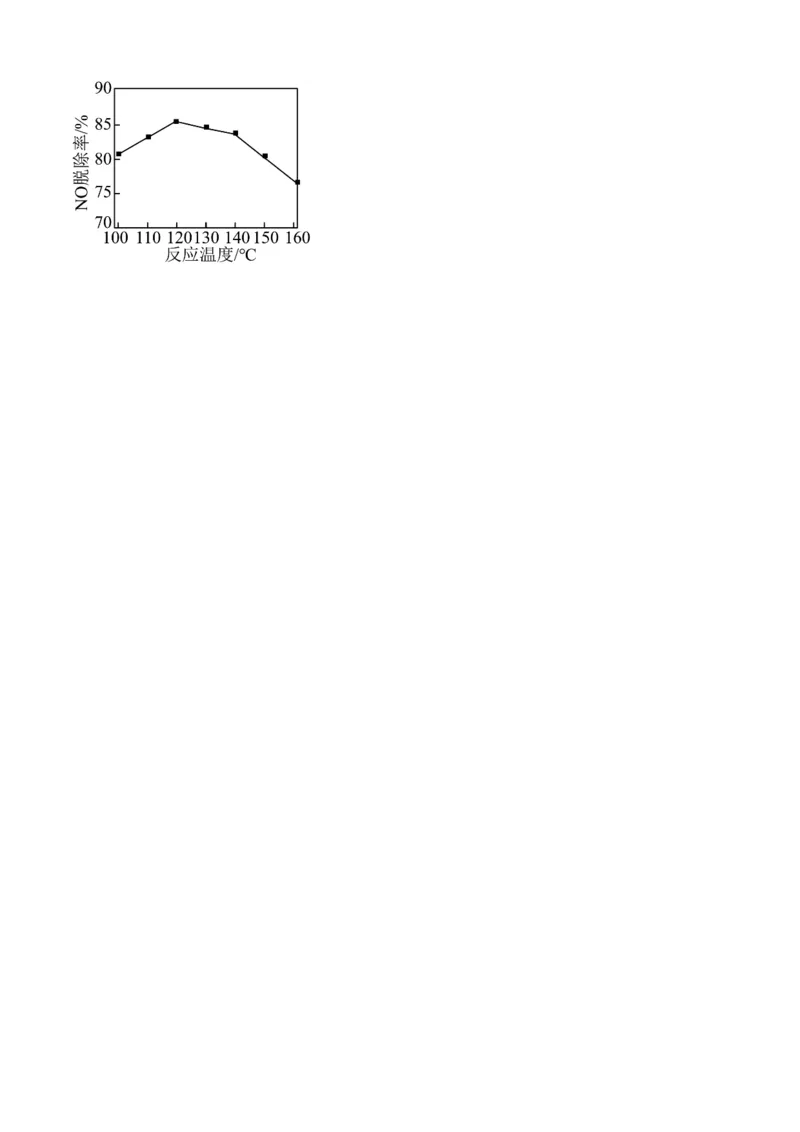
②NO脱除率随温度的变化如题图所示,温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因
是 。
第 6 页 共 7 页