文档内容
玉溪一中 2025—2026 学年上学期高一年级期中考
化学学科试卷
总分:100分,考试时间:90分钟 命题人和审题人: 余思贤 张淑 刘睿
可能用到的相对原子质量;H-1 C-12 O-16 Na-23
一、单项选择题:本题共21小题,每小题2分,共42分,在每小题给出的四个选项中,
只有一个选项是正确的。
1.下列物质属于非电解质的是( )
A. B.SO C.NaOH D.Fe
2
2.科学家最近合成一种新型的氧分子O,关于O 的下列说法,正确的是( )
4 4
A.一个O 分子由两个O 分子构成 B.O 和O 互为同素异形体
4 2 4 2
C.是一种化合物 D.是一种混合物
3.下列关于胶体的说法不正确的是( )
A.“钴钛菁”分子直径为1.3×10-9,分散在水中形成胶体,该分子直径比Na+直径
大
B.丁达尔效应是区分溶液和胶体的一种常用物理方法
C.树林中的晨曦,该现象与丁达尔效应有关
D.胶体区别于其他分散系的本质特征是丁达尔效应
4.下列物质的分类正确的是( )
酸 碱 盐 酸性氧化 碱性氧化物
物
A
B
C
D
5.化学与生活、社会发展息息相关,下列说法不正确的是( )
A.食物的腐烂是发生了氧化还原反应
B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了复分解反应
C.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中涉及氧化还原反应
D.“粉身碎骨浑不怕,要留清白在人间”诗句中涉及分解反应
6.下列离子方程式,书写正确的是( )
A.盐酸与石灰石反应:
B.硫酸铜溶液中滴加氢氧化钡溶液:
C.氢氧化镁和盐酸反应:
D.硝酸银溶液中加入盐酸:
第1页,共8页7. 实现下列物质之间的转化,需要加入氧化剂才能实现的是( )
A.Cu→Cu(NO ) B.SO →HSO C.CO→CO D.CaO→Ca(OH)
3 2 3 2 4 2 2
8.根据下列实验操作与现象得出的结论正确的是( )
选项 实验操作及现象 结论
A 向某溶液中滴加AgNO 溶液,产生白色沉淀 该溶液中一定含Cl-
3
B 向某溶液中滴加澄清石灰水,产生白色沉淀 该溶液中一定含CO
C 取少量浓硫酸,加入水中,插入温度计,温度上升 浓硫酸溶于水放热
D 向某溶液中滴加BaCl 溶液,产生白色沉淀 该溶液中一定含SO
2
9.在水溶液中,下列电离方程式不正确的是( )
A.HSO =2H++SO B.NaHCO=Na++H++CO2-
2 4 3 3
C.NaCO=2Na++CO D.Ba(OH) =Ba2++2OH-
2 3 2
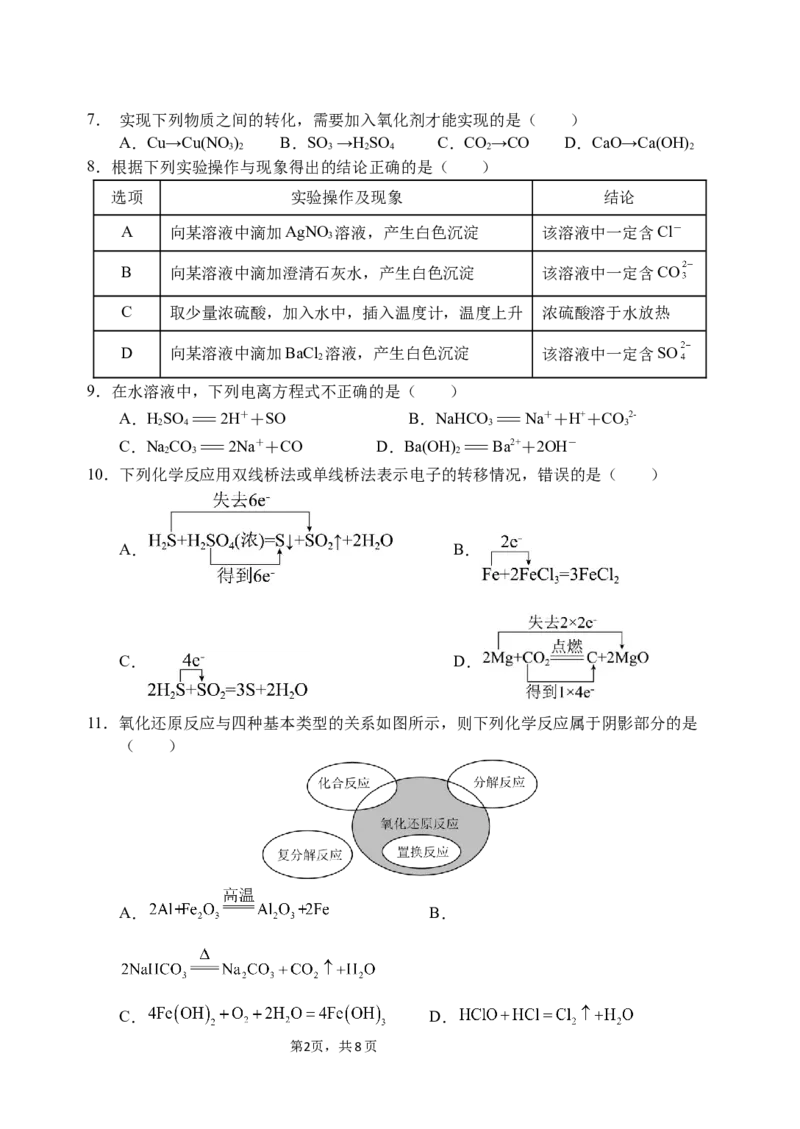
10.下列化学反应用双线桥法或单线桥法表示电子的转移情况,错误的是( )
A. B.
C. D.
11.氧化还原反应与四种基本类型的关系如图所示,则下列化学反应属于阴影部分的是
( )
A. B.
C. D.
第2页,共8页12.下列离子组在指定溶液中一定能大量共存的是( )
A.使pH试纸呈蓝色的溶液中:I−、Cl−、NO−、Cu2+
3
B.使酚酞呈深红色的溶液中:Na+、Cl−、H+、NO−
3
C.含大量Ag+的溶液中:K+、Na+、NO−、SO2−
3 4
D.透明溶液中:Na+、SO2−、NO−、Fe3+
4 3
13.下列物质转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反
应,不可能全部实现的是( )
A.
B.
C. D.
14. 下列关于电解质电离的叙述中正确的是( )
A.CaCO 在水中溶解度很小,其水溶液几乎不导电,所以CaCO 是非电解质
3 3
B.AgCl在水中溶解度很小,但溶解的AgCl全部电离,所以AgCl是电解质
C.氯气(Cl )和氨气(NH )的水溶液导电性都很好,所以它们都是电解质
2 3
D.在电流作用下,盐酸中的HCl电离成H+和Cl-
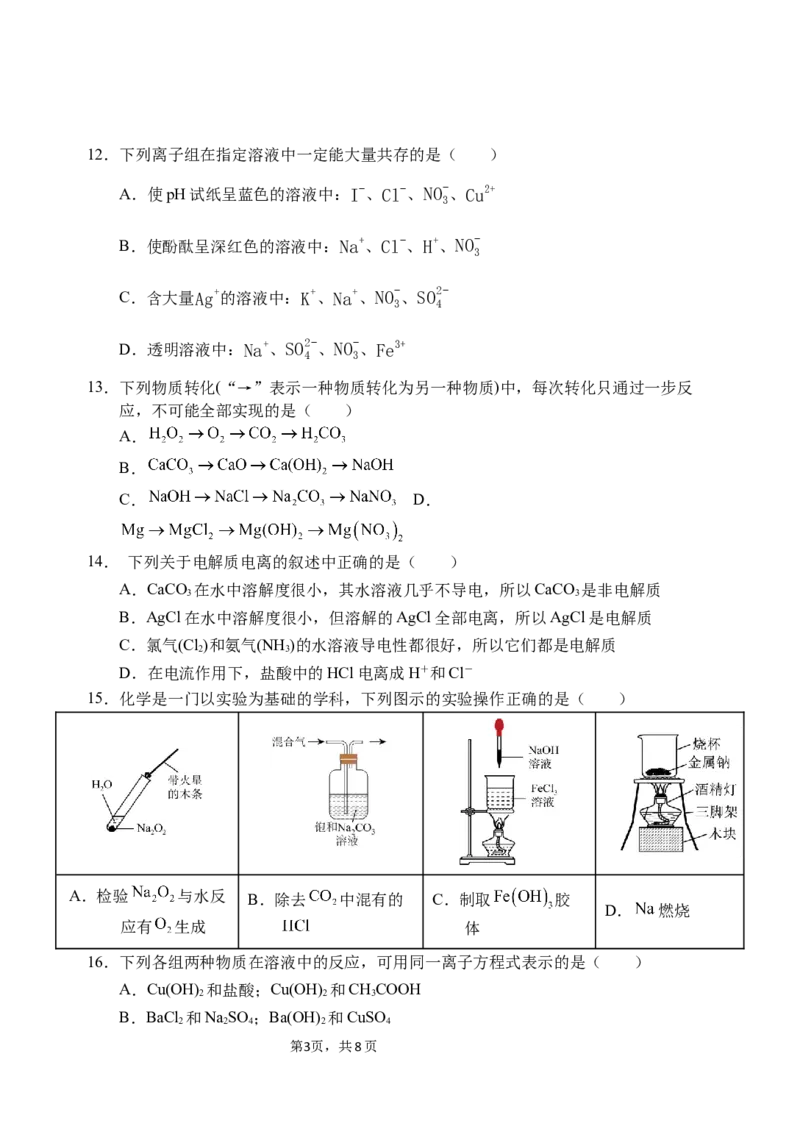
15.化学是一门以实验为基础的学科,下列图示的实验操作正确的是( )
A.检验 与水反 B.除去 中混有的 C.制取 胶
D. 燃烧
应有 生成 体
16.下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是( )
A.Cu(OH) 和盐酸;Cu(OH) 和CHCOOH
2 2 3
B.BaCl 和NaSO ;Ba(OH) 和CuSO
2 2 4 2 4
第3页,共8页C.NaHCO 和NaHSO;NaCO 和NaHSO
3 4 2 3 4
D.少量NaHCO 和Ca(OH) ;Ca(HCO ) 和少量NaOH
3 2 3 2
17.在离子反应xR++yH++O=mR3++nHO中,n和m分别是( )
2 2
A.2、2 B.2、3 C.3、3 D.2、4
18.“人生在勤,勤则不匮”,美好生活靠劳动创造。下列所述化学知识正确且劳动项
目与所述化学知识有关联的是( )
选项 劳动项目 化学知识
用铂丝蘸取少量水样进行焰色试验,火焰
A 水质检验员:某水样是钠盐溶液
呈黄色
化学实验员:检验 是否失
B
效
C 食品工程师:选择食品保鲜剂 生石灰可用作食品抗氧化剂
D 制造业工人:工业生产漂白粉 将氯气通入澄清石灰水
19.酸式盐是盐的一种, 已知HPO (亚磷酸)与足量的NaOH充分反应后只生成一种盐
3 3
NaHPO ,则下列说法正确的是( )
2 3
A.HPO 属于一元酸 B.HPO 属于三元酸
3 3 3 3
C.NaHPO 属于酸式盐 D.NaH PO 属于酸式盐
2 3 2 3
20.研究人员在金星大气中探测到了磷化氢(PH )气体。PH 常作为一种熏蒸剂,在贮粮中
3 3
用于防治害虫,一种制备PH 的流程如图所示,下列说法正确的是( )
3
A.流程中,每一步均属于氧化还原反应
B.次磷酸的分子式为HPO ,在上述反应中只表现出氧化性
3 2
C.白磷与浓NaOH溶液反应的化学方程式:P+3NaOH(浓)+3H O PH ↑+3NaHPO
4 2 3 2 2
D.理论上,1分子的白磷可生产2分子的PH
3
21.某无色溶液可能含有离子个数相同的下列某些离子中的一种或几种:K+、Fe3+、
Mg2+、H+、Cl−、CO2−、SO2−,取溶液分别进行如下实验:
3 4
①加入HNO 酸化的Ba(NO ) 溶液产生白色沉淀;
3 3 2
第4页,共8页②加入锌粉,有气泡生成; ③加入适量NaO粉末产生白色沉淀。
2
下列说法正确的是( )
A.该无色溶液中一定没有Fe3+,可能有K+
B.由①、②可知该溶液可能有CO2−
3
C.该无色溶液中一定有H+、SO2−、Mg2+和Cl−
4
D.实验③发生反应的离子方程式只有:
二、非选择题:本题共4小题,共58分,除特殊标注外,每空2分。
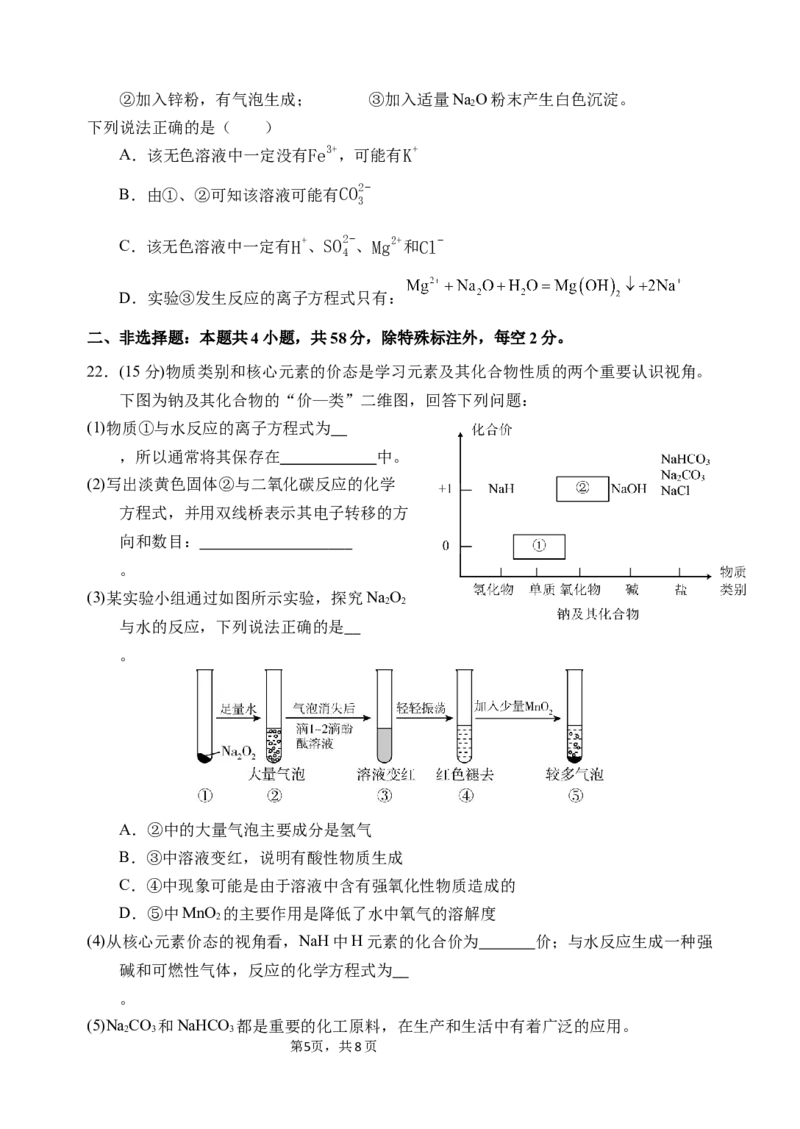
22.(15分)物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。
下图为钠及其化合物的“价—类”二维图,回答下列问题:
(1)物质①与水反应的离子方程式为
,所以通常将其保存在 中。
(2)写出淡黄色固体②与二氧化碳反应的化学
方程式,并用双线桥表示其电子转移的方
向和数目:
。
(3)某实验小组通过如图所示实验,探究NaO
2 2
与水的反应,下列说法正确的是
。
A.②中的大量气泡主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO 的主要作用是降低了水中氧气的溶解度
2
(4)从核心元素价态的视角看,NaH中H元素的化合价为 价;与水反应生成一种强
碱和可燃性气体,反应的化学方程式为
。
(5)NaCO 和NaHCO 都是重要的化工原料,在生产和生活中有着广泛的应用。
2 3 3
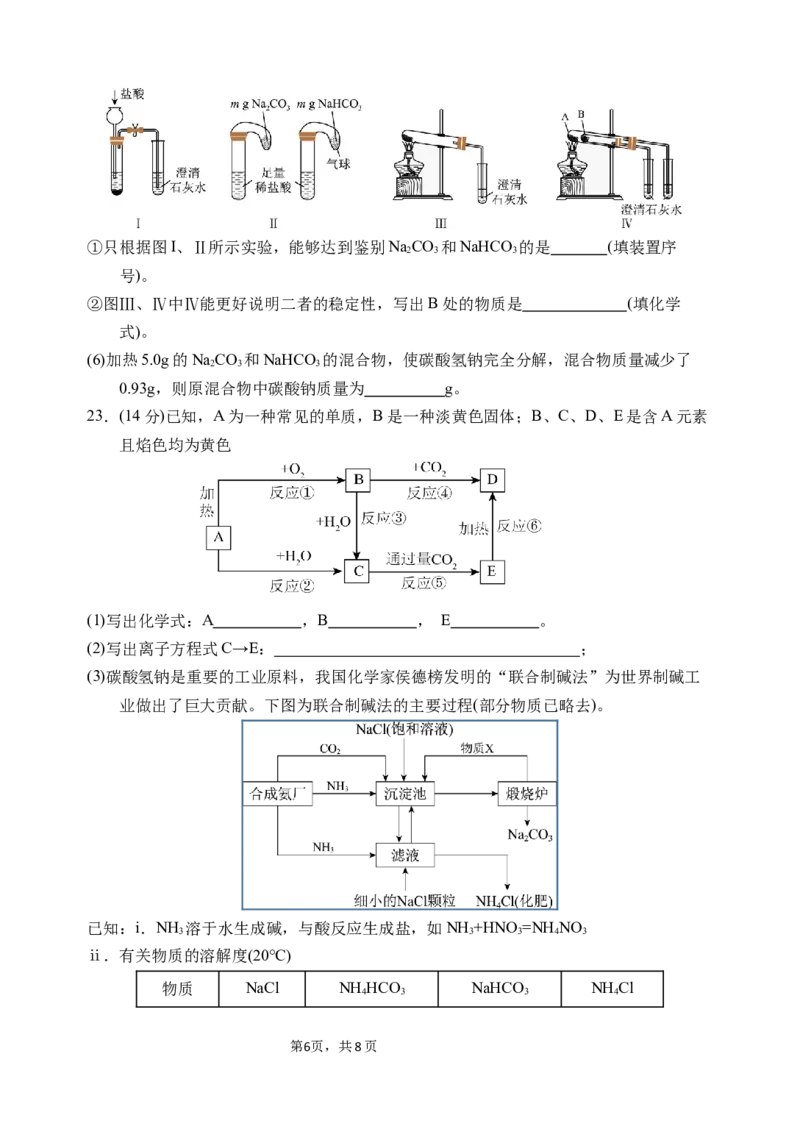
第5页,共8页①只根据图I、Ⅱ所示实验,能够达到鉴别NaCO 和NaHCO 的是 (填装置序
2 3 3
号)。
②图Ⅲ、Ⅳ中Ⅳ能更好说明二者的稳定性,写出B处的物质是 (填化学
式)。
(6)加热5.0g的NaCO 和NaHCO 的混合物,使碳酸氢钠完全分解,混合物质量减少了
2 3 3
0.93g,则原混合物中碳酸钠质量为 g。
23.(14分)已知,A为一种常见的单质,B是一种淡黄色固体;B、C、D、E是含A元素
且焰色均为黄色
(1)写出化学式:A ,B , E 。
(2)写出离子方程式C→E: ;
(3)碳酸氢钠是重要的工业原料,我国化学家侯德榜发明的“联合制碱法”为世界制碱工
业做出了巨大贡献。下图为联合制碱法的主要过程(部分物质已略去)。
已知:i.NH 溶于水生成碱,与酸反应生成盐,如NH +HNO =NH NO
3 3 3 4 3
ⅱ.有关物质的溶解度(20℃)
物质 NaCl NH HCO NaHCO NH Cl
4 3 3 4
第6页,共8页溶解度/g 36.0 21.7 9.6 37.2
ⅲ.沉淀池中析出NaHCO 晶体
3
①煅烧炉中反应的化学方程式为 ,物质X是
。
②沉淀池中发生反应的化学方程式为 。实验
室分离出沉淀的操作名称是 ;检验产品NaCO 中是否含有氯离子,需要
2 3
的试剂有 (填化学式)。
③下列说法正确的是 (填字母)。
A.沉淀池中有NaHCO 析出,是因为在该条件下NaHCO 的溶解度最小
3 3
B.滤液中主要含有NaCl、NaCO 和NH Cl
2 3 4
C.设计物质X循环的目的是提高原料的利用率
24.(15分)某校化学兴趣小组为了探究氯水中次氯酸的漂白性和稳定性,设计探究思
路并完成以下实验。请回答下列问题。
【探究思路】
【实验过程】
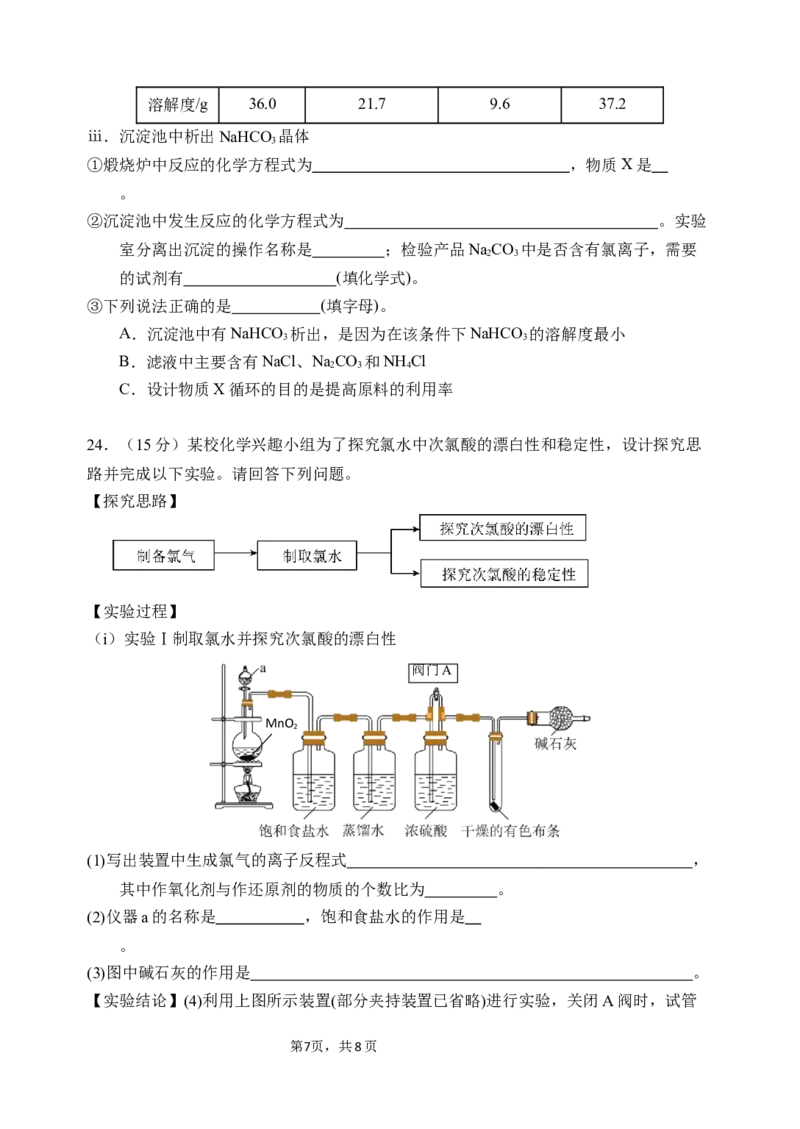
(i)实验Ⅰ制取氯水并探究次氯酸的漂白性
阀门A
MnO
2
(1)写出装置中生成氯气的离子反程式 ,
其中作氧化剂与作还原剂的物质的个数比为 。
(2)仪器a的名称是 ,饱和食盐水的作用是
。
(3)图中碱石灰的作用是 。
【实验结论】(4)利用上图所示装置(部分夹持装置已省略)进行实验,关闭A阀时,试管
第7页,共8页中的有色布条 (填“会”或“不会”)褪色;打开A阀后,有色布条褪色,
说明 。
(ii)实验Ⅱ探究氯水中次氯酸的稳定性
将传感器、氯离子传感器、氧气传感器分别与数据采集器、计算机连接,将三种传感器
分别插入盛有氯水的广口瓶,用强光照射氯水,同时采集实验数据,获得相关变化
曲线。
(5) 若能够证明氯水中HClO在光照下发生了分解反应,则图中纵坐标可以表示的物理量
是 (填字母)。(注:酸性溶液中,c(H+)越大,pH越小,溶液酸性越强。)
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的含量
25.(14分)氧化还原反应在工农业生产、日常生活中具有广泛用途。
(1)维生素C又称“抗坏血酸”,在人体内有重要功能。例如,能帮助人体将食物中不易
吸收的Fe3+转变为易吸收的Fe2+,故维生素C具有 (填“氧化性”或“还原
性”),在反应过程中维生素C发生 (填“氧化”或“还原”)反应。
(2)以NaClO 和稀盐酸为原料制备ClO ,原理如下,配平下列离子方程式:
2 2
=
ClO− + Cl− + ClO ↑ +
2 2
。
(3)反应3S+6KOH=K SO +2K S+3H O中,被氧化的物质和被还原的物质的个数之比是
2 3 2 2
。
(4) 在杀菌消毒过程中会产生少量副产物亚氯酸盐( ),需将其转化为 除去,下
ClO ClO− Cl−
2 2
列试剂中可将 转化为 的是 (填字母)。
ClO− Cl−
2
a.O b.FeSO c.KI d.KMnO
3 4 4
(5)在反应3BrF +5H O=HBrO +Br +9HF+O 中,被氧化的元素是 ,当有15
3 2 3 2 2
个水分子参加反应时,被HO还原的BrF 为 个。
2 3
第8页,共8页