文档内容
余姚中学 2025 学年 4 月质量检测高一化学试卷(选考)
命题:洪森 审题:俞琴科
可能用到的相对原子质量:
H1 C12 N14 O16 Na23 S32 Cl35.5 K39 Ca40 Fe56 Cu64
选择题部分
一、选择题(本大题共25小题,每小题2分,共50分。每个小题列出的四个备选项中只有一个是符合题目
要求的,不选、多选、错选均不得分)
1. 下列物质分类正确的是
A. 苯为电解质 B. Na O 为碱性氧化物
2 2
C. 有色玻璃为胶体 D. 水玻璃为化合物
2. 实验室配制一定物质的量浓度的溶液,需要用到的仪器是
A. B. C. D.
3.下列有关NH Cl的说法中,不正确的是
4
A.NH Cl是弱电解质 B.NH Cl易溶于水
4 4
C.实验室用于制NH D.HCl 和NH 反应可制NH Cl
3 3 4
4. 关于反应2NH OH+4Fe3+=N O↑+4Fe2++4H++H O,下列说法正确的是
2 2 2
A.生成1molN O,转移4mol 电子 B.NH OH是还原产物
2 2
C.NH OH既是氧化剂又是还原剂 D.若设计成原电池,Fe2+为负极产物
2
5. 下列化学用语表示正确的是
A.氢气的结构式为:
B.镁原子的结构示意图:
C.H C O 在水溶液中的电离方程式为:H C O =2H++C O 2-
2 2 4 2 2 4 2 4
D.用电子式表示H O的形成过程:
2
6. 下列物质互为同素异形体的是
A.1H 和2H B.CO和CO C.NH CNO和CO(NH ) D.C 和C
2 4 2 2 60 70
7. 下列说法正确的是
A. 大豆蛋白纤维属于天然纤维
B. 为了提高橡胶的强度可以用硫与橡胶作用,硫原子和高分子链之间形成分子间作用力
C. 聚甲基丙烯酸甲酯俗称有机玻璃,可用于制备光学仪器
D. 植物油含较多的饱和脂肪酸甘油酯,熔点较低
学科网(北京)股份有限公司8. 下列物质分子的所有原子,不可能处于同一平面内的是
A.二氯甲烷 B.乙炔
C.苯乙烯 D.苯
9. 物质的性质决定用途,下列两者对应关系正确的是
A.金刚石硬度大,可用于制作切削刀具 B.氧化铝具有两性,可用于制作坩埚
C.SiO 熔点高,可用于生产光导纤维 D.氨气有还原性,可用于生产铵态氮肥
2
10. 在无色透明的强酸性溶液中能大量共存的离子组是
A.K+、Na+、MnO -、NO - B.Na+、Cl-、K+、NO -
4 3 3
C.Na+、Cl-、CH COO-、NO - D.Na+、K+、CO 2-、Cl-
3 3 3
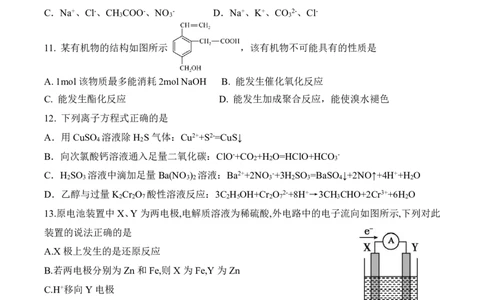
11. 某有机物的结构如图所示 ,该有机物不可能具有的性质是
A. 1mol该物质最多能消耗2mol NaOH B. 能发生催化氧化反应
C. 能发生酯化反应 D. 能发生加成聚合反应,能使溴水褪色
12. 下列离子方程式正确的是
A.用CuSO 溶液除H S气体:Cu2++S2-=CuS↓
4 2
B.向次氯酸钙溶液通入足量二氧化碳:ClO-+CO +H O=HClO+HCO -
2 2 3
C.H SO 溶液中滴加足量Ba(NO ) 溶液:Ba2++2NO -+3H SO =BaSO ↓+2NO↑+4H++H O
2 3 3 2 3 2 3 4 2
D.乙醇与过量K Cr O 酸性溶液反应:3C H OH+Cr O 2-+8H+→3CH CHO+2Cr3++6H O
2 2 7 2 5 2 7 3 2
13.原电池装置中X、Y 为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,下列对此
装置的说法正确的是
A.X极上发生的是还原反应
B.若两电极分别为Zn 和Fe,则X 为Fe,Y 为Zn
C.H+移向Y电极
D.电子流动方向为X→外电路→Y→溶液→X
14.2-丁烯(CH CH CHCH )有顺( )、反( )两种异构体。T℃,
3 3
异构体转化的能量关系如图所示,下列说法正确的是
A. 顺-2-丁烯转化为反-2-丁烯的过程属于物理变化
B. 顺-2-丁烯稳定性大于反-2-丁烯
学科网(北京)股份有限公司C. 发生加成反应时,顺-2-丁烯断键吸收的能量低于反-2-丁烯断键吸收的能量
D. T℃,1mol 顺-2-丁烯完全转化成反-2-丁烯放出热量(c-b)kJ
15. 反应XX(gg)44YY(gg)+ZZ(gg),在200℃和t℃时,X的物质的量浓度(单位:mol·L-1)随时间变
化的有关实验数据见下表:
时间/min 0 2 4 6 8 10
200℃ 1.60 1.10 0.70 0.40 0.30 0.30
t℃ 2.00 1.30 0.70 0.36 0.36 0.36
下列有关该反应的描述正确的是
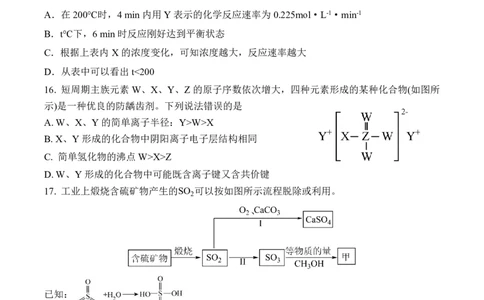
A.在200℃时,4min内用Y表示的化学反应速率为0.225mol·L-1·min-1
B.t℃下,6min时反应刚好达到平衡状态
C.根据上表内X的浓度变化,可知浓度越大,反应速率越大
D.从表中可以看出t<200
16. 短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的某种化合物(如图所
示)是一种优良的防龋齿剂。下列说法错误的是
A. W、X、Y的简单离子半径:Y>W>X
B. X、Y形成的化合物中阴阳离子电子层结构相同
C. 简单氢化物的沸点W>X>Z
D. W、Y 形成的化合物中可能既含离子键又含共价键
17. 工业上煅烧含硫矿物产生的SO 可以按如图所示流程脱除或利用。
2
已知:
下列说法正确的是
A.SO 通入品红溶液中,溶液先褪色后变红
2
B.无氧条件下,SO 通入CaCO 悬浊液中生成 CaSO
2 3 4
C.甲的结构可能为
D.硫与过量的氧气反应生成SO
3
学科网(北京)股份有限公司18. 超氧化钾(KO )可用作潜水或宇航装置中CO 吸收剂和供氧剂,反应为
2 2
4KO +2CO =2K CO +3O ,N 为阿伏加德罗常数的值。下列说法正确的是
2 2 2 3 2 A
A.22.4LCO 含有的分子数为N
2 A
B.0.1molKO 固体中含有离子的数目为0.2N
2 A
C.1L1mol·L-1 K CO 溶液中含有氧原子的数目为3N
2 3 A
D.该反应中每转移1mol电子生成O 的数目为1.5N
2 A
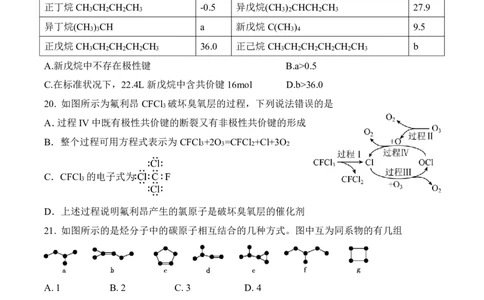
19. 在101kpa下,某些烷烃的沸点如表所示。据表分析,下列选项正确的是
烷烃 沸点 烷烃 沸点
正丁烷CH CH CH CH -0.5 异戊烷(CH ) CHCH CH 27.9
3 2 2 3 3 2 2 3
异丁烷(CH ) CH a 新戊烷C(CH ) 9.5
3 3 3 4
正戊烷CH CH CH CH CH 36.0 正己烷CH CH CH CH CH CH b
3 2 2 2 3 3 2 2 2 2 3
A.新戊烷中不存在极性键 B.a>0.5
C.在标准状况下,22.4L新戊烷中含共价键16mol D.b>36.0
20. 如图所示为氟利昂CFCl 破坏臭氧层的过程,下列说法错误的是
3
A.过程IV 中既有极性共价键的断裂又有非极性共价键的形成
B.整个过程可用方程式表示为CFCl +2O =CFCl +Cl+3O
3 3 2 2
C.CFCl 的电子式为
3
D.上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂
21. 如图所示的是烃分子中的碳原子相互结合的几种方式。图中互为同系物的有几组
A. 1 B. 2 C.3 D. 4
22. 如图所示是一种以液态肼(N H )为燃料,氧气为氧化剂,某固体氧化
2 4
物为电解质的新型燃料电池。在固体氧化物电解质的温度达700~900℃
时,O2-可在该固体氧化物电解质中自由移动,生成物均为无毒无害的物
质。下列说法正确的是
A.放电时,电子的流向为电极甲→负载→电极乙→固体氧化物→电极甲
B.放电时,电池内的O2-由电极甲移向电极乙
C.电池负极反应为:N H -4e-=4H++N ↑
2 4 2
D.当电路中通过2mole-时,电极乙上有16gO 参与反应
2
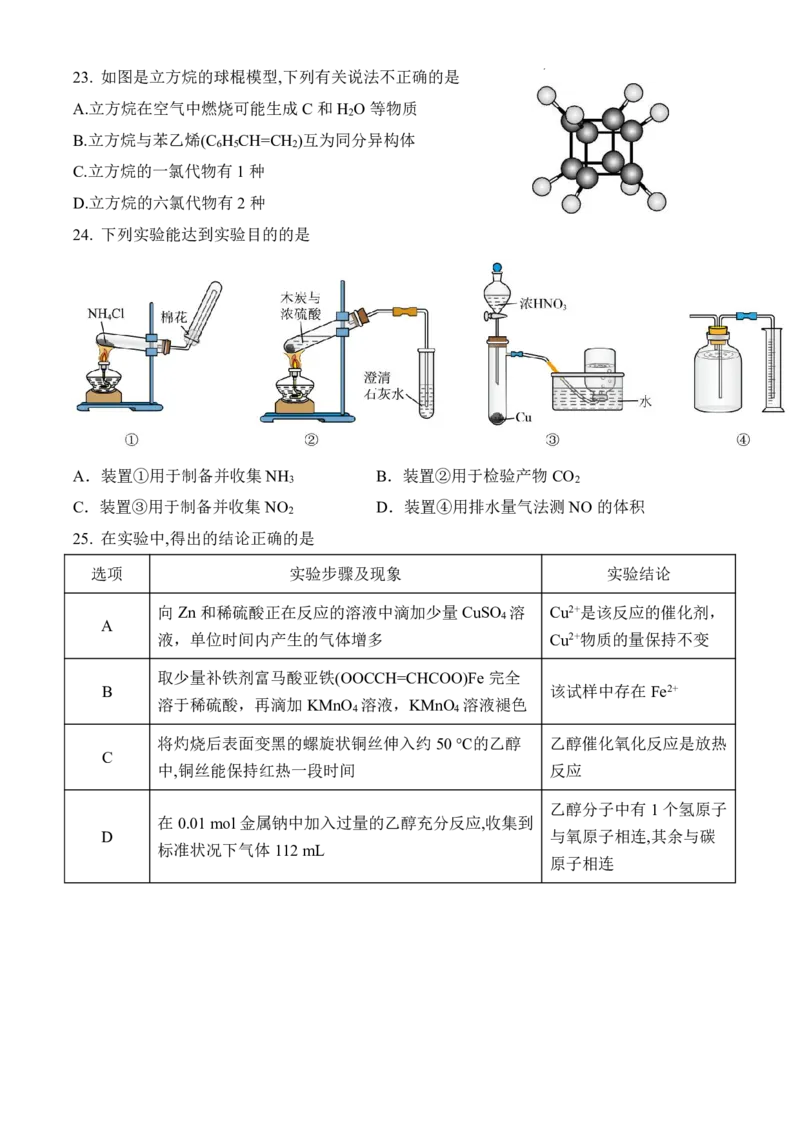
学科网(北京)股份有限公司23. 如图是立方烷的球棍模型,下列有关说法不正确的是
A.立方烷在空气中燃烧可能生成C 和H O等物质
2
B.立方烷与苯乙烯(C H CH=CH )互为同分异构体
6 5 2
C.立方烷的一氯代物有1种
D.立方烷的六氯代物有2种
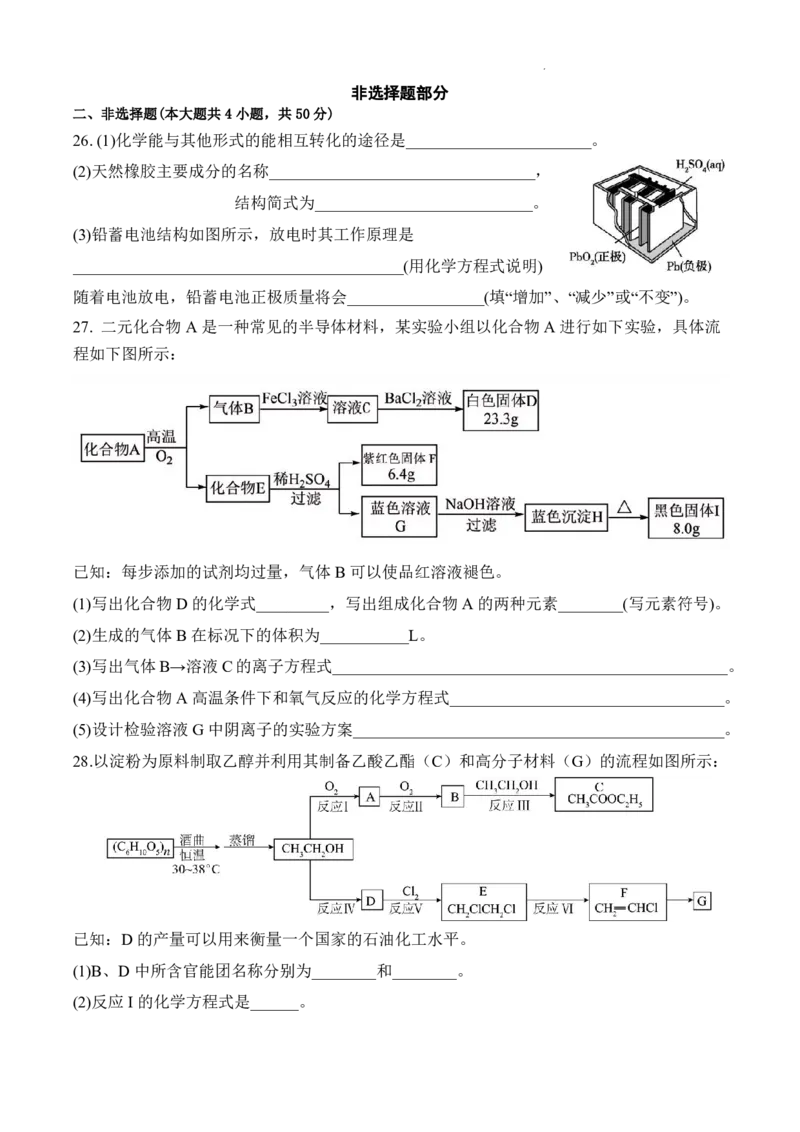
24. 下列实验能达到实验目的的是
A.装置①用于制备并收集NH B.装置②用于检验产物CO
3 2
C.装置③用于制备并收集NO D.装置④用排水量气法测NO 的体积
2
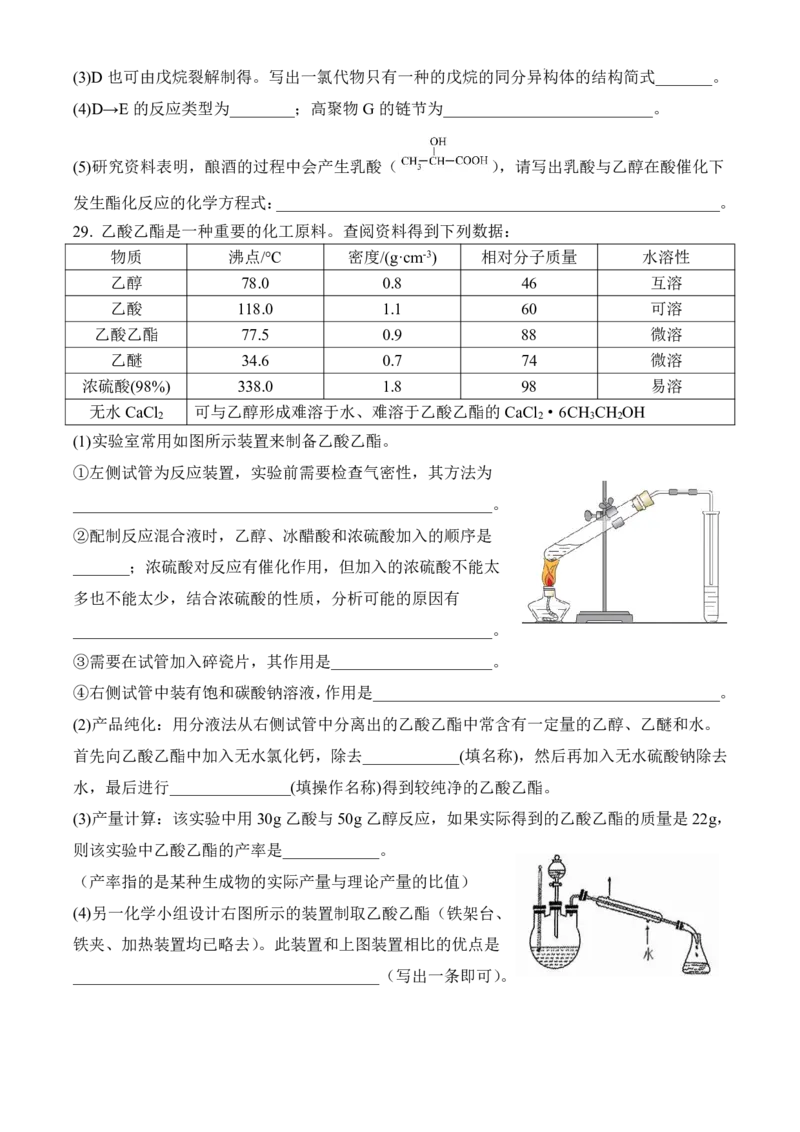
25. 在实验中,得出的结论正确的是
选项 实验步骤及现象 实验结论
向 Zn 和稀硫酸正在反应的溶液中滴加少量CuSO 溶 Cu2+是该反应的催化剂,
4
A
液,单位时间内产生的气体增多 Cu2+物质的量保持不变
取少量补铁剂富马酸亚铁(OOCCH=CHCOO)Fe 完全
B 该试样中存在Fe2+
溶于稀硫酸,再滴加 KMnO 溶液,KMnO 溶液褪色
4 4
将灼烧后表面变黑的螺旋状铜丝伸入约50℃的乙醇 乙醇催化氧化反应是放热
C
中,铜丝能保持红热一段时间 反应
乙醇分子中有1个氢原子
在 0.01mol 金属钠中加入过量的乙醇充分反应,收集到
D 与氧原子相连,其余与碳
标准状况下气体 112 mL
原子相连
学科网(北京)股份有限公司非选择题部分
二、非选择题(本大题共4小题,共50分)
26.(1)化学能与其他形式的能相互转化的途径是_______________________。
(2)天然橡胶主要成分的名称_________________________________,
结构简式为___________________________。
(3)铅蓄电池结构如图所示,放电时其工作原理是
_________________________________________(用化学方程式说明)
随着电池放电,铅蓄电池正极质量将会_________________(填“增加”、“减少”或“不变”)。
27. 二元化合物A是一种常见的半导体材料,某实验小组以化合物A进行如下实验,具体流
程如下图所示:
已知:每步添加的试剂均过量,气体B 可以使品红溶液褪色。
(1)写出化合物D 的化学式_________,写出组成化合物A的两种元素________(写元素符号)。
(2)生成的气体B 在标况下的体积为___________L。
(3)写出气体B→溶液C的离子方程式_________________________________________________。
(4)写出化合物A 高温条件下和氧气反应的化学方程式__________________________________。
(5)设计检验溶液G 中阴离子的实验方案______________________________________________。
28.以淀粉为原料制取乙醇并利用其制备乙酸乙酯(C)和高分子材料(G)的流程如图所示:
已知:D的产量可以用来衡量一个国家的石油化工水平。
(1)B、D中所含官能团名称分别为________和________。
(2)反应I 的化学方程式是______。
学科网(北京)股份有限公司(3)D 也可由戊烷裂解制得。写出一氯代物只有一种的戊烷的同分异构体的结构简式_______。
(4)D→E 的反应类型为________;高聚物G 的链节为__________________________。
(5)研究资料表明,酿酒的过程中会产生乳酸( ),请写出乳酸与乙醇在酸催化下
发生酯化反应的化学方程式:_______________________________________________________。
29. 乙酸乙酯是一种重要的化工原料。查阅资料得到下列数据:
物质 沸点/℃ 密度/(g·cm-3) 相对分子质量 水溶性
乙醇 78.0 0.8 46 互溶
乙酸 118.0 1.1 60 可溶
乙酸乙酯 77.5 0.9 88 微溶
乙醚 34.6 0.7 74 微溶
浓硫酸(98%) 338.0 1.8 98 易溶
无水CaCl 可与乙醇形成难溶于水、难溶于乙酸乙酯的CaCl ·6CH CH OH
2 2 3 2
(1)实验室常用如图所示装置来制备乙酸乙酯。
①左侧试管为反应装置,实验前需要检查气密性,其方法为
____________________________________________________。
②配制反应混合液时,乙醇、冰醋酸和浓硫酸加入的顺序是
_______;浓硫酸对反应有催化作用,但加入的浓硫酸不能太
多也不能太少,结合浓硫酸的性质,分析可能的原因有
____________________________________________________。
③需要在试管加入碎瓷片,其作用是____________________。
④右侧试管中装有饱和碳酸钠溶液,作用是___________________________________________。
(2)产品纯化:用分液法从右侧试管中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水。
首先向乙酸乙酯中加入无水氯化钙,除去____________(填名称),然后再加入无水硫酸钠除去
水,最后进行_______________(填操作名称)得到较纯净的乙酸乙酯。
(3)产量计算:该实验中用30g乙酸与50g 乙醇反应,如果实际得到的乙酸乙酯的质量是22g,
则该实验中乙酸乙酯的产率是____________。
(产率指的是某种生成物的实际产量与理论产量的比值)
(4)另一化学小组设计右图所示的装置制取乙酸乙酯(铁架台、
铁夹、加热装置均已略去)。此装置和上图装置相比的优点是
______________________________________(写出一条即可)。
学科网(北京)股份有限公司