文档内容
哈三中 2025—2026 学年度下学期高一学
年 3 月月考化学选考试卷
可能用到的相对原子质量:H 1 N 14 O 16 F 19 Na 23 Al 27 Si 28 S 32
一、选择题(共 15 小题,每题只有 1 个选项符合题意,每题 3 分,共计 45
分。)
1 .校园环境中存在着大量的化学材料, 以下不属于非金属材料的是
A .升旗广场的水泥火箭台 B .建筑外墙的红色瓷砖
C .食堂的不锈钢餐盘 D .教室里光滑透亮的玻璃
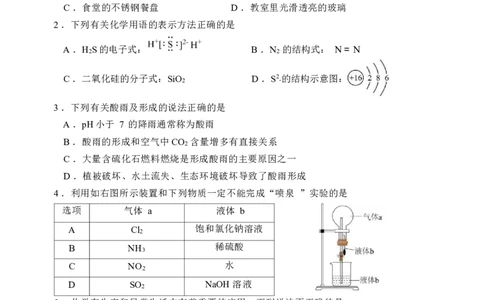
2 .下列有关化学用语的表示方法正确的是
A .H S的电子式: B .N 的结构式: N = N
2 2
C .二氧化硅的分子式:SiO 2 D .S2 - 的结构示意图:
3 .下列有关酸雨及形成的说法正确的是
A .pH小于 7 的降雨通常称为酸雨
B .酸雨的形成和空气中CO 含量增多有直接关系
2
C .大量含硫化石燃料燃烧是形成酸雨的主要原因之一
D .植被破坏、水土流失、生态环境破坏导致了酸雨形成
4 .利用如右图所示装置和下列物质一定不能完成“喷泉 ”实验的是
选项 气体 a 液体 b
A Cl 饱和氯化钠溶液
2
B NH 稀硫酸
3
C NO 水
2
D SO NaOH 溶液
2
5 .化学在生产和日常生活中有着重要的应用,下列说法不正确的是
A .二氧化硅可用于生产光导纤维,高纯硅可以制成计算机芯片
B .硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料
C .食品中可以添加适量的二氧化硫起到漂白、防腐和抗氧化的作用
D .可以利用氨气的催化氧化进行人工固氮,用于工业制硝酸
6 .下列各组离子能大量共存的是
2
A .Na+ 、K+ 、Cl- 、SiO3 - B .Fe3+ 、Cl- 、K+ 、S2-
C .NH+ 、K+ 、OH- 、MnO- D .H+ 、Cu2+ 、I- 、NO-
4 4 3
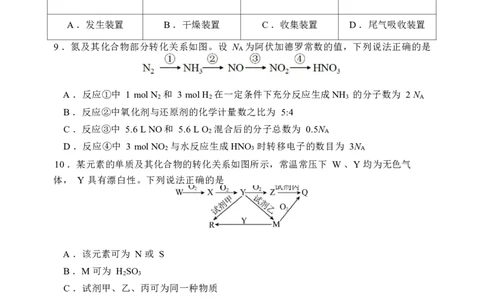
高二化学第 1页 共 6 页7 .将机动车尾气中的NO转化为N 可有效保护大气环境。从物质的性质角度考虑,下
2
列物质中不能实现该转化的是
A .CO B .NH C .KMnO D .C
3 4
8 .下列关于实验室制备氨气的各项装置正确的是
A .发生装置 B .干燥装置 C .收集装置 D .尾气吸收装置
9 .氮及其化合物部分转化关系如图。设 N 为阿伏加德罗常数的值,下列说法正确的是
A
A .反应①中 1 mol N 和 3 mol H 在一定条件下充分反应生成NH 的分子数为 2 N
2 2 3 A
B .反应②中氧化剂与还原剂的化学计量数之比为 5:4
C .反应③中 5.6 L NO和 5.6 L O 混合后的分子总数为 0.5N
2 A
D .反应④中 3 mol NO 与水反应生成HNO 时转移电子的数目为 3N
2 3 A
10 .某元素的单质及其化合物的转化关系如图所示,常温常压下 W 、Y 均为无色气
体, Y 具有漂白性。下列说法正确的是
A .该元素可为 N 或 S
B .M 可为 H SO
2 3
C .试剂甲、乙、丙可为同一种物质
D .X 与足量 O 反应可直接转化为 Z
2
11 .丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述错误
的是
A .向蔗糖中加入浓硫酸并搅拌,可观察到蔗糖逐渐变黑
B .将NO 通入淀粉碘化钾溶液中,可观察到溶液变蓝
2
C .将浓H SO 滴加在胆矾晶体上,可观察到固体由蓝色变为白色
2 4
D .将SO 通入紫色石蕊溶液中,可观察到溶液先变红后褪色
2
高二化学第 2页
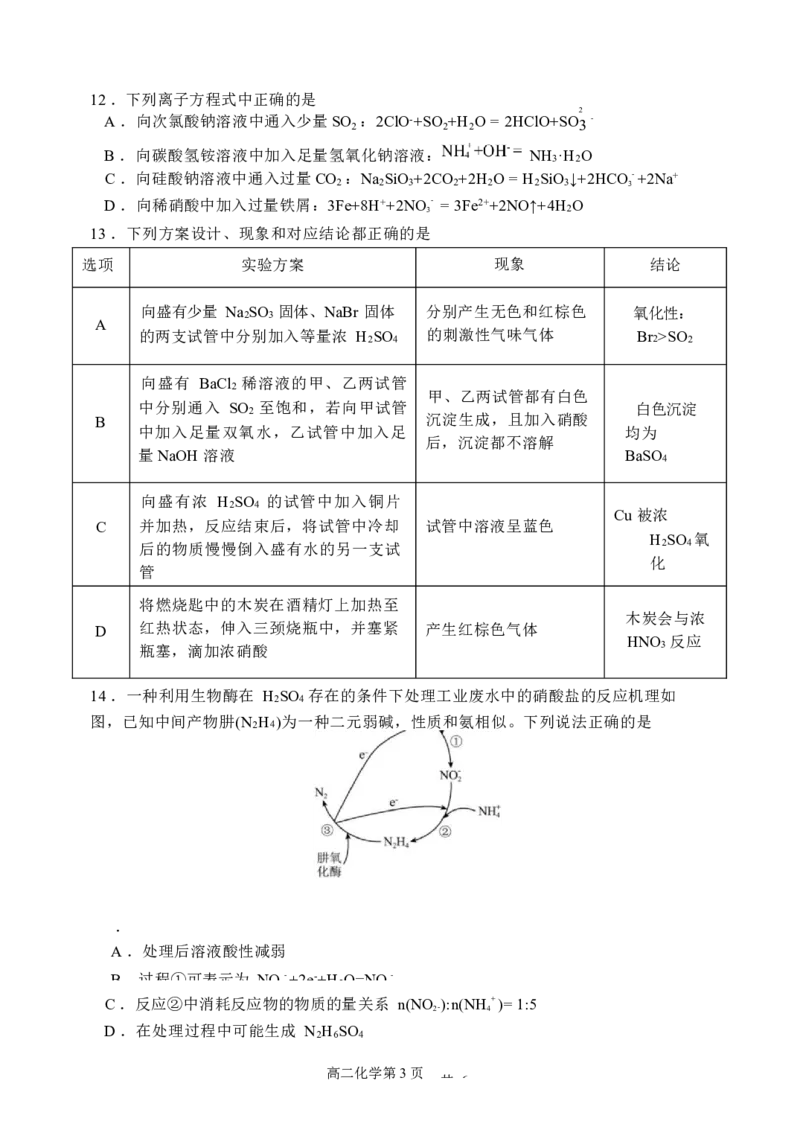
共 612 .下列离子方程式中正确的是
2
A .向次氯酸钠溶液中通入少量SO
2
:2ClO-+SO
2
+H
2
O = 2HClO+SO3 -
B .向碳酸氢铵溶液中加入足量氢氧化钠溶液: NH ·H O
3 2
C .向硅酸钠溶液中通入过量CO :Na SiO +2CO +2H O = H SiO ↓+2HCO- +2Na+
2 2 3 2 2 2 3 3
D .向稀硝酸中加入过量铁屑:3Fe+8H++2NO- = 3Fe2++2NO↑+4H O
3 2
13 .下列方案设计、现象和对应结论都正确的是
选项 实验方案 现象 结论
向盛有少量 Na SO 固体、NaBr 固体 分别产生无色和红棕色 氧化性:
2 3
A
的两支试管中分别加入等量浓 H
2
SO
4
的刺激性气味气体 Br2>SO
2
向盛有 BaCl 稀溶液的甲、乙两试管
2
甲、乙两试管都有白色
中分别通入 SO 2 至饱和,若向甲试管 白色沉淀
B 沉淀生成,且加入硝酸
中加入足量双氧水,乙试管中加入足 均为
后,沉淀都不溶解
量NaOH 溶液 BaSO
4
向盛有浓 H SO 的试管中加入铜片
2 4
Cu 被浓
C 并加热,反应结束后,将试管中冷却 试管中溶液呈蓝色
H SO 氧
后的物质慢慢倒入盛有水的另一支试 2 4
化
管
将燃烧匙中的木炭在酒精灯上加热至
木炭会与浓
D 红热状态,伸入三颈烧瓶中,并塞紧 产生红棕色气体
HNO 反应
瓶塞,滴加浓硝酸 3
14 .一种利用生物酶在 H SO 存在的条件下处理工业废水中的硝酸盐的反应机理如
2 4
图,已知中间产物肼(N
2
H4)为一种二元弱碱,性质和氨相似。下列说法正确的是
A .处理后溶液酸性减弱
B 过程①可表示为 NO- +2e-+H O=NO-
3 2 2
C .反应②中消耗反应物的物质的量关系 n(NO ):n(NH+ )= 1:5
2- 4
D .在处理过程中可能生成 N H SO
2 6 4
高二化学第3页
共 615 .某小组探究 Na S 溶液与 KMnO 溶液反应,实验过程如下:
2 4
实验序号 I II
将 6 滴(约 0.3mL) 0.01 mol/LNa S 溶 将 6 滴(约 0.3mL)0.01 mol/L 酸性
2
实验过程 液 滴加到 5 mL 0.01 mol/L 酸性 KMnO 4 溶液(H 2 SO 4 酸化至pH=0)滴
KMnO 4 溶液(H 2 SO 4 酸化至 pH=0) 加到 5 mL 0.01 mol/LNa 2 S 溶液
紫色变浅(pH<1) ,生成棕褐色沉淀 溶液呈淡黄色(pH≈8) ,生成浅粉色
实验现象
(MnO2) 沉淀(MnS)
资料:i .MnO- 在强酸性条件下被还原为 Mn2+ ,在近中性条件下被还原为 MnO 。
4 2
ii .单质硫可溶于硫化钠溶液,溶液呈淡黄色。
下列说法正确的是
2 2
A .实验 I 所得溶液中检测到有 SO4 - ,可说明 S2
-
被 MnO
4
- 氧化为 SO4 -
B .实验 I 中生成棕褐色沉淀,说明酸性条件下 S2 - 将 MnO 4 - 还原为 MnO 2
C .实验 II 中得到浅粉色沉淀,可能是 S2 - 将生成的 MnO 2 还原为 Mn2+并迅速结合所致
D .以上实验表明 Na S 溶液与 KMnO 溶液的反应只与溶液的酸碱性有关
2 4
二、非选择题(共计 55 分)
16 .(12 分)硅、硫、氮是重要的非金属元素。回答下列问题:
(1)SiO 属于 (填“酸性 ”“碱性 ”或“两性 ”)氧化物。盛装 NaOH 等碱性溶
2
液的试剂瓶不能用玻璃塞,用化学方程式解释原因:
。
(2)由 SO 制备 H SO 的过程中,一般用 98.3%的浓硫酸吸收 SO ,而不是直接用蒸馏
3 2 4 3
水吸收的原因是 。
(3)氮的固定是自然界中氮循环的重要途径,请写出一种自然固氮的途径
。人类通过控制条件可实现人工固氮,请写出最重要的人工固氮途径的化学方程式
。
(4)实验室 中浓硝酸一般保存在 中 , 并放置在 阴凉处 , 解
释原因: 。
高二化学第 4页
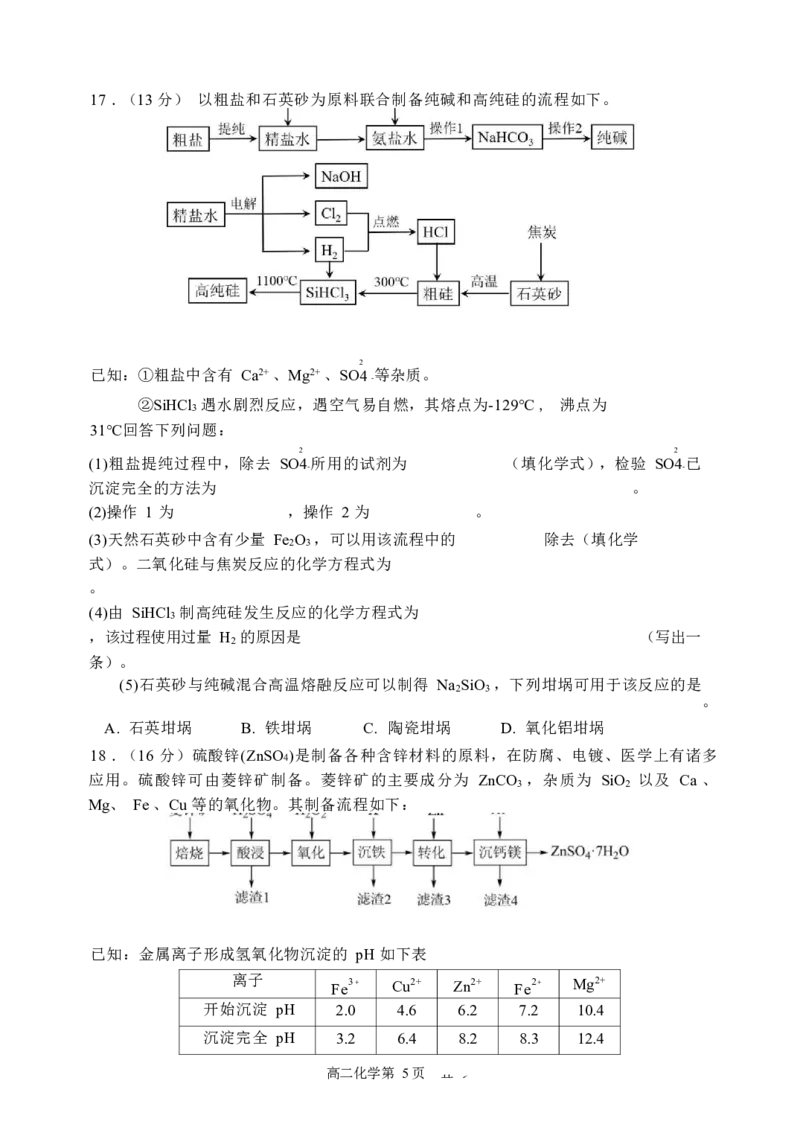
共 617 .(13分) 以粗盐和石英砂为原料联合制备纯碱和高纯硅的流程如下。
2
已知:①粗盐中含有 Ca2+ 、Mg2+ 、SO4
-
等杂质。
②SiHCl 遇水剧烈反应,遇空气易自燃,其熔点为-129℃ , 沸点为
3
31℃回答下列问题:
2 2
(1)粗盐提纯过程中,除去 SO4所用的试剂为 (填化学式),检验 SO4已
- -
沉淀完全的方法为 。
(2)操作 1 为 ,操作 2 为 。
(3)天然石英砂中含有少量 Fe O ,可以用该流程中的 除去(填化学
2 3
式)。二氧化硅与焦炭反应的化学方程式为
。
(4)由 SiHCl 制高纯硅发生反应的化学方程式为
3
,该过程使用过量 H 的原因是 (写出一
2
条)。
(5)石英砂与纯碱混合高温熔融反应可以制得 Na SiO ,下列坩埚可用于该反应的是
2 3
。
A. 石英坩埚 B. 铁坩埚 C. 陶瓷坩埚 D. 氧化铝坩埚
18 .(16 分)硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多
应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ZnCO ,杂质为 SiO 以及 Ca 、
3 2
Mg、 Fe 、Cu 等的氧化物。其制备流程如下:
已知:金属离子形成氢氧化物沉淀的 pH 如下表
离子
Fe
3+ Cu2+ Zn2+
Fe
2+ Mg2+
开始沉淀 pH 2.0 4.6 6.2 7.2 10.4
沉淀完全 pH 3.2 6.4 8.2 8.3 12.4
高二化学第 5页
共 6回答下列问题:
高二化学第 5页
共 6(1)酸浸时生成硫酸锌的化学方程式为 ,加快酸浸速率的
方法为 (写出一种)。
(2)滤渣 1 的主要成分为 (填化学式)。
(3)“氧化”过程发生反应的离子方程式为 。
(4)“沉铁” 时加入试剂 X 调节 pH,溶液 pH 的范围是 ≤pH< ,下列物
质最适合作试剂 X 的是 。
A. NaOH B. ZnO C. NH ∙H O
3 2
(5)“转化”过程发生反应的离子方程式为
。
(6)从“沉钙镁”过滤的滤液中获得 ZnSO ∙7H O 的操作为 、
4 2
、过滤、洗涤、干燥。
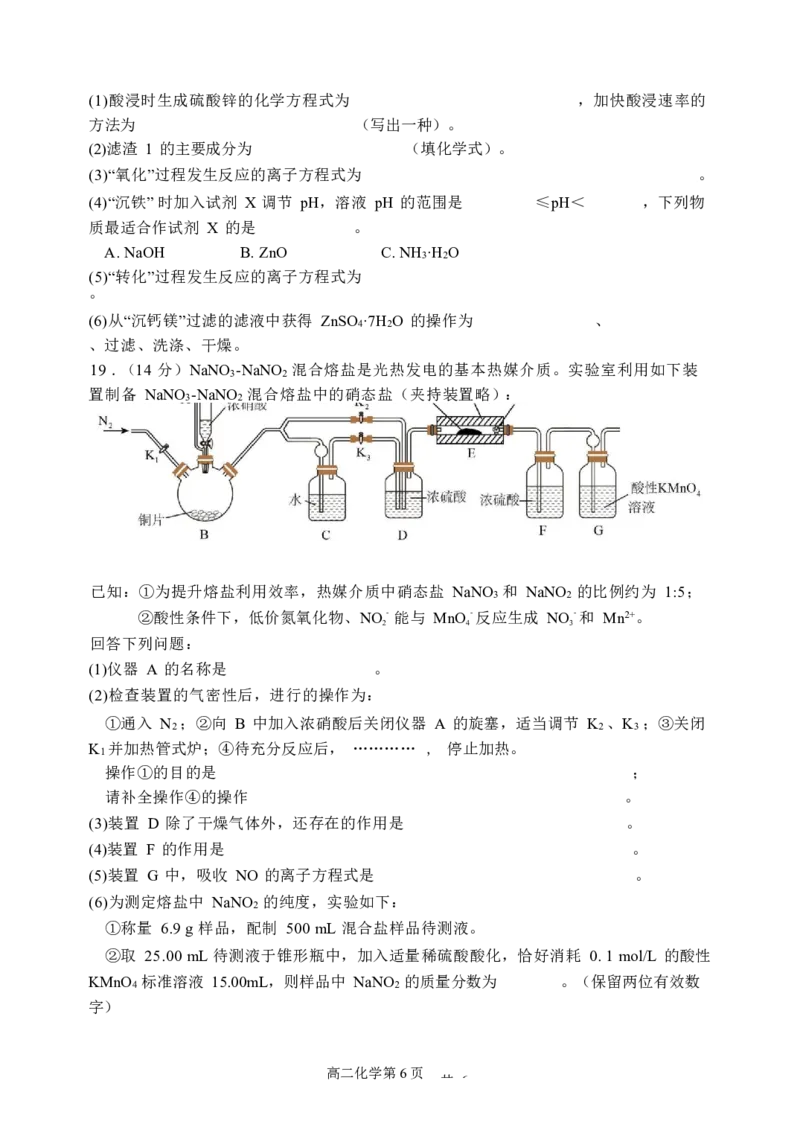
19 .(14 分)NaNO -NaNO 混合熔盐是光热发电的基本热媒介质。实验室利用如下装
3 2
置制备 NaNO -NaNO 混合熔盐中的硝态盐(夹持装置略):
3 2
已知:①为提升熔盐利用效率,热媒介质中硝态盐 NaNO 和 NaNO 的比例约为 1:5;
3 2
②酸性条件下,低价氮氧化物、NO- 能与 MnO- 反应生成 NO- 和 Mn2+。
2 4 3
回答下列问题:
(1)仪器 A 的名称是 。
(2)检查装置的气密性后,进行的操作为:
①通入 N ;②向 B 中加入浓硝酸后关闭仪器 A 的旋塞,适当调节 K 、K ;③关闭
2 2 3
K 并加热管式炉;④待充分反应后, ………… , 停止加热。
1
操作①的目的是 ;
请补全操作④的操作 。
(3)装置 D 除了干燥气体外,还存在的作用是 。
(4)装置 F 的作用是 。
(5)装置 G 中,吸收 NO 的离子方程式是 。
(6)为测定熔盐中 NaNO 的纯度,实验如下:
2
①称量 6.9 g 样品,配制 500 mL 混合盐样品待测液。
②取 25.00 mL 待测液于锥形瓶中,加入适量稀硫酸酸化,恰好消耗 0. 1 mol/L 的酸性
KMnO 标准溶液 15.00mL,则样品中 NaNO 的质量分数为 。(保留两位有效数
4 2
字)
高二化学第6页
共 6哈三中 2025—2026 学年度下学期高一学
年
3 月月考化学选考答案
一、选择题(共 15 小题,每题 3 分,共计 45 分)
1-5 CBCAD 6- 10 ACDBC 11-15 DDCDC
二、非选择题(共计 55 分)
16 .(12 分)
(1)酸性(1 分) 2NaOH + SiO = Na SiO + H O (2 分)
2 2 3 2
(2)用水作吸收剂时容易形成酸雾,吸收速度慢,不利于吸收二氧化硫(2 分)
(3)豆科植物根瘤菌或闪电释放能量 (2 分) N +3H 2NH
2 3
(4)棕色试剂瓶(1 分) 浓硝酸见光或受热易分解(2 分)
17 、(13 分)
(1)BaCl (1 分) 静置后,向上层清液中滴加 2~3 滴 BaCl 溶液,不出现浑浊,表明
2 2 2
SO4已沉淀完全(2 分)
-
(2)过滤 (1 分) 加热 (1 分)
SiHCl + H Si + 3HCl(2 分) 防止硅被氧化或防止 SiHCl 自燃(合理答案
3 2 3
均给分)(2 分)
(5)B (1 分)
18 、(16 分)
(1)ZnO + H SO = ZnSO + H O (2 分)
2 4 4 2
适当升高温度、适当增大硫酸浓度、将煅烧后的固体粉碎或搅拌(答出一种即可,合理
可以给分)(1 分)
(2)SiO 、CaSO (2 分)
2 4
(3) 2Fe2+ + H O + 2H+ = 2Fe3+ + 2H O (2 分)
2 2 2
(4)3.2(1 分) 4.6(1 分) B(1 分)
(5)Cu2+ + Zn = Cu + Zn2+ (2 分)
(6)蒸发浓缩(2 分) 冷却结晶(2 分)
19 、(14 分)
(1)恒压滴液漏斗(或恒压分液漏斗) (2 分)
(2)排尽装置中的空气,防止氧气氧化亚硝酸盐 (2 分) 打开 K ,通入 N ,排除装
1 2
置中残余气体 (2 分)
高二化学第6页
共 6(3)混合气体,便于调节 NO 和 NO 的比例(2 分)
2
(4)防止 G 中水分进入管式炉(2 分)
(5)5NO+3MnO- +4H+===5NO- +3Mn2++2H O(2 分)
4 3 2
(6)75%(2 分)
高二化学第6页
共 6