文档内容
东北育才高中 2025-2026 学年度下学期
高一年级化学科第一次月考试卷
答题时间:75 分钟 满分:100 分 命题人:郝俊刚 校对人:李想
可能用到的相对原子质量:H1O16Si28Br80Cu64Pb207
一、单选题(每小题3分,共45分)
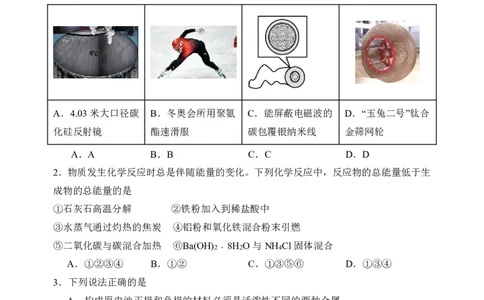
1.下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
A.4.03米大口径碳 B.冬奥会所用聚氨 C.能屏蔽电磁波的 D.“玉兔二号”钛合
化硅反射镜 酯速滑服 碳包覆银纳米线 金筛网轮
A.A B.B C.C D.D
2.物质发生化学反应时总是伴随能量的变化。下列化学反应中,反应物的总能量低于生
成物的总能量的是
①石灰石高温分解 ②铁粉加入到稀盐酸中
③水蒸气通过灼热的焦炭 ④铝粉和氧化铁混合粉末引燃
⑤二氧化碳与碳混合加热 ⑥Ba(OH) ﹒8H O与NH Cl固体混合
2 2 4
A.①②③④ B.①② C.①③⑤⑥ D.①③④
3.下列说法正确的是
A.构成原电池正极和负极的材料必须是活泼性不同的两种金属
B.原电池中负极发生还原反应,正极发生氧化反应
C.灼热的碳与二氧化碳的反应是化合反应,所以是放热反应
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
4.化学与生活、生产、科技、环境等密切相关。下列说法不
.
正
.
确
.
的是
A.食品中添加适量的SO 可以起到漂白、防腐和抗氧化等作用
2
B.“雷蟠电掣云滔滔,夜半载雨输亭皋”,雷雨天时N 转化为NO属于自然固氮
2
C.二氧化硅导光能力强,可制作光导纤维
试卷第1页,共10页D.万佛堂石窟易受酸雨腐蚀,pH<7的雨水为酸雨
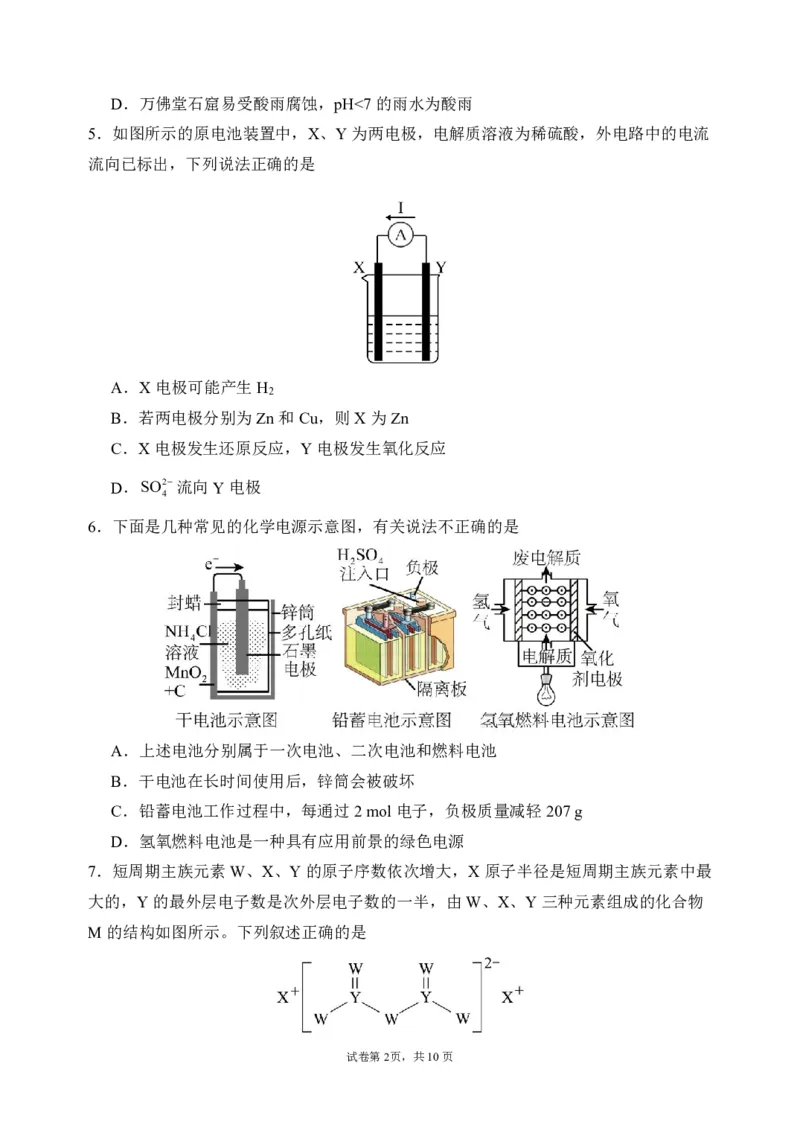
5.如图所示的原电池装置中,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电流
流向已标出,下列说法正确的是
A.X电极可能产生H
2
B.若两电极分别为Zn和Cu,则X为Zn
C.X电极发生还原反应,Y电极发生氧化反应
D.SO2流向Y电极
4
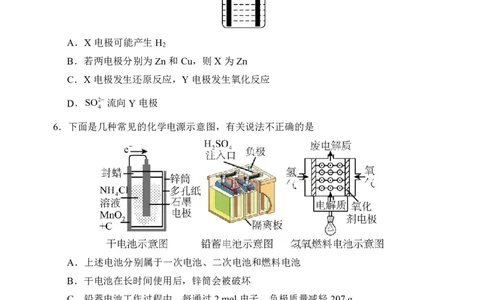
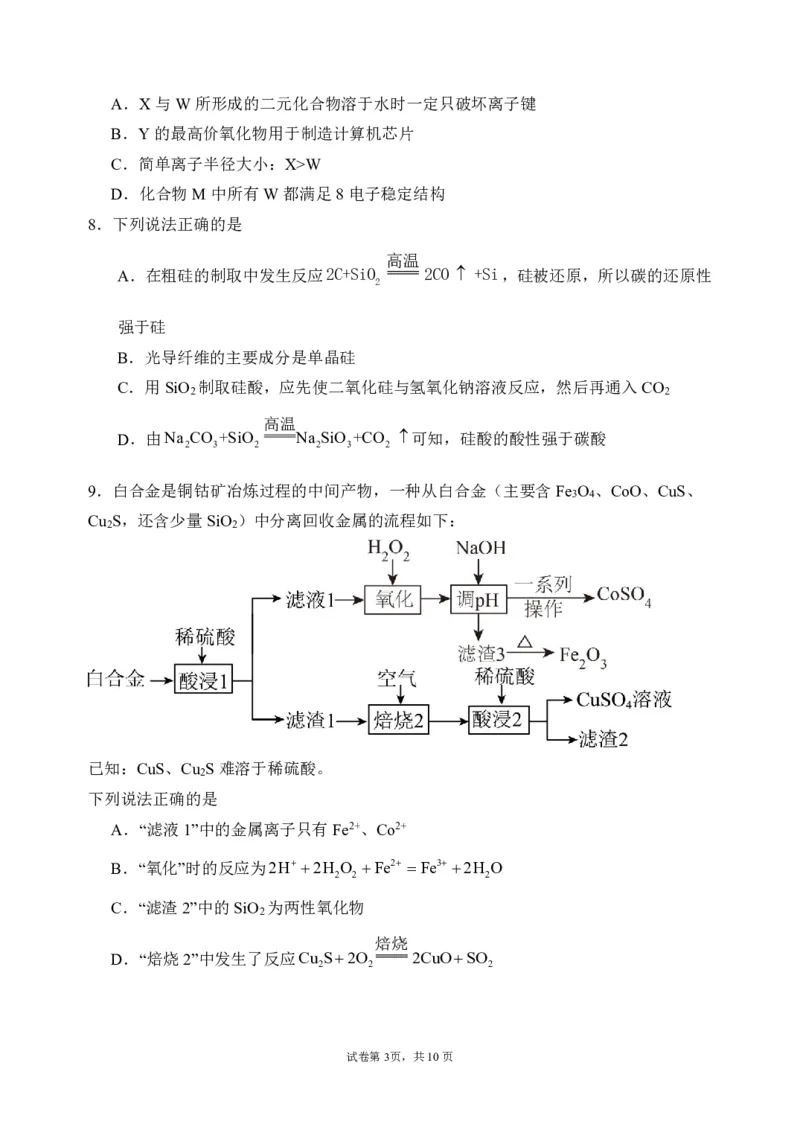
6.下面是几种常见的化学电源示意图,有关说法不正确的是
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒会被破坏
C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D.氢氧燃料电池是一种具有应用前景的绿色电源
7.短周期主族元素W、X、Y的原子序数依次增大,X原子半径是短周期主族元素中最
大的,Y的最外层电子数是次外层电子数的一半,由W、X、Y三种元素组成的化合物
M的结构如图所示。下列叙述正确的是
试卷第2页,共10页A.X与W所形成的二元化合物溶于水时一定只破坏离子键
B.Y的最高价氧化物用于制造计算机芯片
C.简单离子半径大小:X>W
D.化合物M中所有W都满足8电子稳定结构
8.下列说法正确的是
高温
A.在粗硅的制取中发生反应2C+SiO 2CO +Si,硅被还原,所以碳的还原性
2
强于硅
B.光导纤维的主要成分是单晶硅
C.用SiO 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO
2 2
高温
D.由Na CO +SiO Na SiO +CO 可知,硅酸的酸性强于碳酸
2 3 2 2 3 2
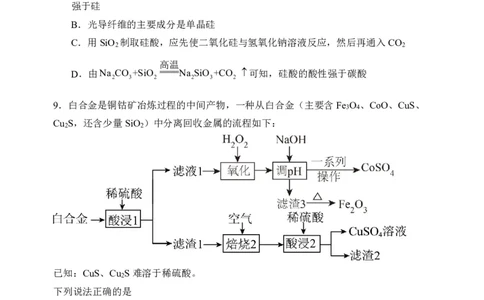
9.白合金是铜钴矿冶炼过程的中间产物,一种从白合金(主要含Fe O 、CoO、CuS、
3 4
Cu S,还含少量SiO )中分离回收金属的流程如下:
2 2
已知:CuS、Cu S难溶于稀硫酸。
2
下列说法正确的是
A.“滤液1”中的金属离子只有Fe2+、Co2+
B.“氧化”时的反应为2H 2H O Fe2 Fe3 2H O
2 2 2
C.“滤渣2”中的SiO 为两性氧化物
2
焙烧
D.“焙烧2”中发生了反应Cu S2O 2CuOSO
2 2 2
试卷第3页,共10页10.化学在生产和日常生活中有着重要的应用,下列各项的物质用途与性质或原理对应
关系正确的个数
①碳化硅的熔点高,可用作砂纸和砂轮的磨料
②二氧化硫具有抗氧化性,可用作葡萄酒的食品添加剂
③液氨汽化时吸热,可用作制冷剂
④富勒烯、碳纳米材料、石墨烯等碳纳米材料都属于新型无机非金属材料
⑤制备玻璃和水泥都用到石灰石
⑥工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
⑦二氧化硅可应用于太阳能电池
⑧陶瓷、普通玻璃、水泥、金刚砂 (SiC) 都属于硅酸盐材料
⑨NO只能用排水集气法收集,不能用排空气法收集;而NO 只能用排空气法收集,不
2
能用排水集气法
A.3 个 B.4 个 C.5 个 D.6 个
11.下列离子方程式书写正确的是
A.向Mg(HCO ) 溶液中加入过量的NaOH溶液:
3 2
Mg2++2HCO+2OH=MgCO +CO2+2H O
3 3 3 2
B.溴与冷的NaOH溶液反应:Br +2OH=Br+BrO+H O
2 2
C.向NaClO溶液中通入过量SO :SO +ClO+H O=HSO+HClO
2 2 2 3
D.FeCO 溶于稀硝酸:FeCO +2H+=Fe2++CO +H O
3 3 2 2
12.下列装置与试剂(尾气处理装置和试剂任选)能完成相应气体制备和性质验证的是
试卷第4页,共10页选项 ①中试剂 ②中试剂 性质
A Na SO +70%H SO 石蕊溶液 SO 有漂白性
2 3 2 4 2
B NaCl固体+浓H SO CH COONa溶液 酸性:HCl>CH COOH
2 4 3 3
C 小苏打+稀H SO 水玻璃 非金属性:S>C>Si
2 4
D Cu片+浓HNO KI-淀粉溶液 NO 有氧化性
3 2
A.A B.B C.C D.D
13.下列关于化学物质的用途或性质的叙述正确的说法有
①氨气极易溶于水,故可用作制冷剂
②燃煤中添加CaO可以减少SO 和温室气体的排放
2
③工业浓硝酸一般发黄是因为溶有NO
2
④二氧化硅与氢氧化钠溶液、氢氟酸均反应,属于两性氧化物
⑤足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑥浓硫酸有强吸水性,可以干燥SO
2
⑦标准状况下,O 与NO 按1:4充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓
2 2
1
度接近 mol/L
22.4
A.②⑤ B.⑤⑥ C.③⑥ D.②③⑥⑦
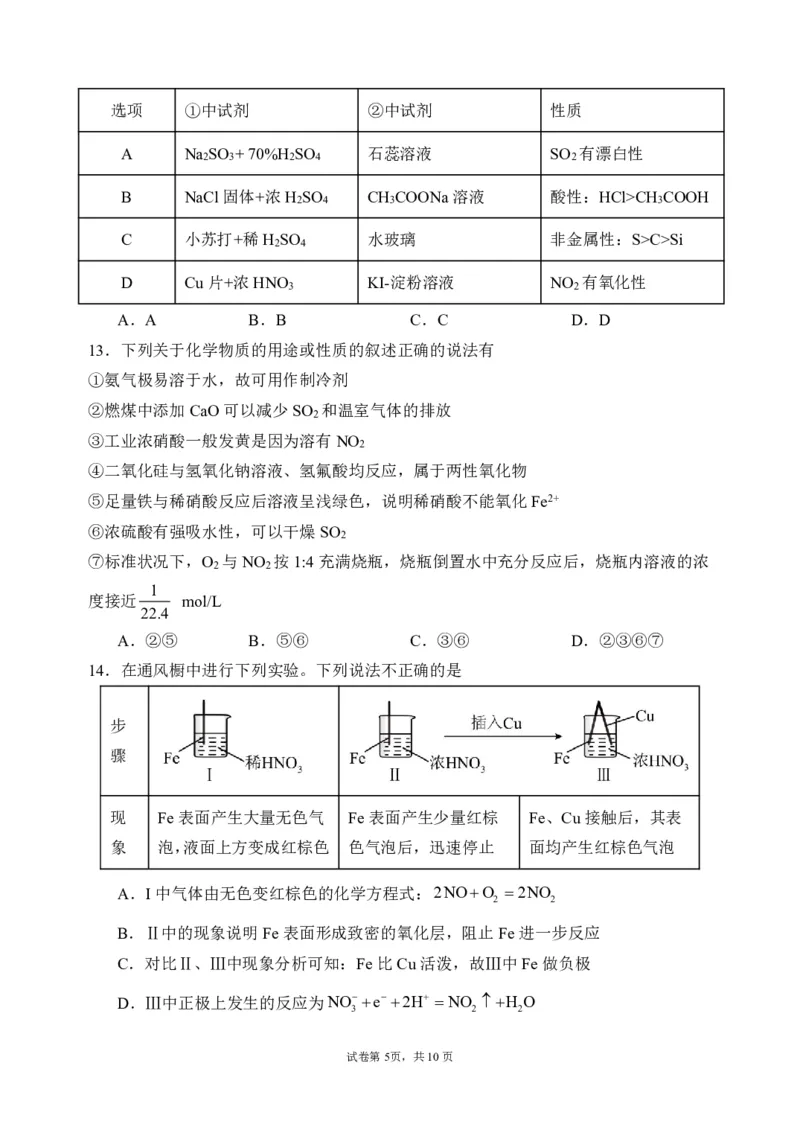
14.在通风橱中进行下列实验。下列说法不正确的是
步
骤
现 Fe表面产生大量无色气 Fe表面产生少量红棕 Fe、Cu接触后,其表
象 泡,液面上方变成红棕色 色气泡后,迅速停止 面均产生红棕色气泡
A.I中气体由无色变红棕色的化学方程式:2NOO 2NO
2 2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅱ、Ⅲ中现象分析可知:Fe比Cu活泼,故Ⅲ中Fe做负极
D.Ⅲ中正极上发生的反应为NOe2H NO H O
3 2 2
试卷第5页,共10页15.将13.6gCu和Cu O组成的混合物加入250mL一定浓度的稀硝酸中,固体完全溶解
2
生成Cu(NO ) 和NO,向所得溶液中加入1.0L0.5mol﹒L-1NaOH 溶液时,金属离子(钠离
3 2
子除外)恰好沉淀完全,生成沉淀的质量为19.6g,下列说法正确的是
A.原稀硝酸的浓度为2.4mol﹒L-1
B.原固体混合物中Cu和Cu O的物质的量之比为1:1
2
C.固体完全溶解后,剩余硝酸的物质的量为0.05mol
D.生成的NO在标准状况下的体积为1.12L
二、填空题(共55分)
16.(12分)回答下列问题:
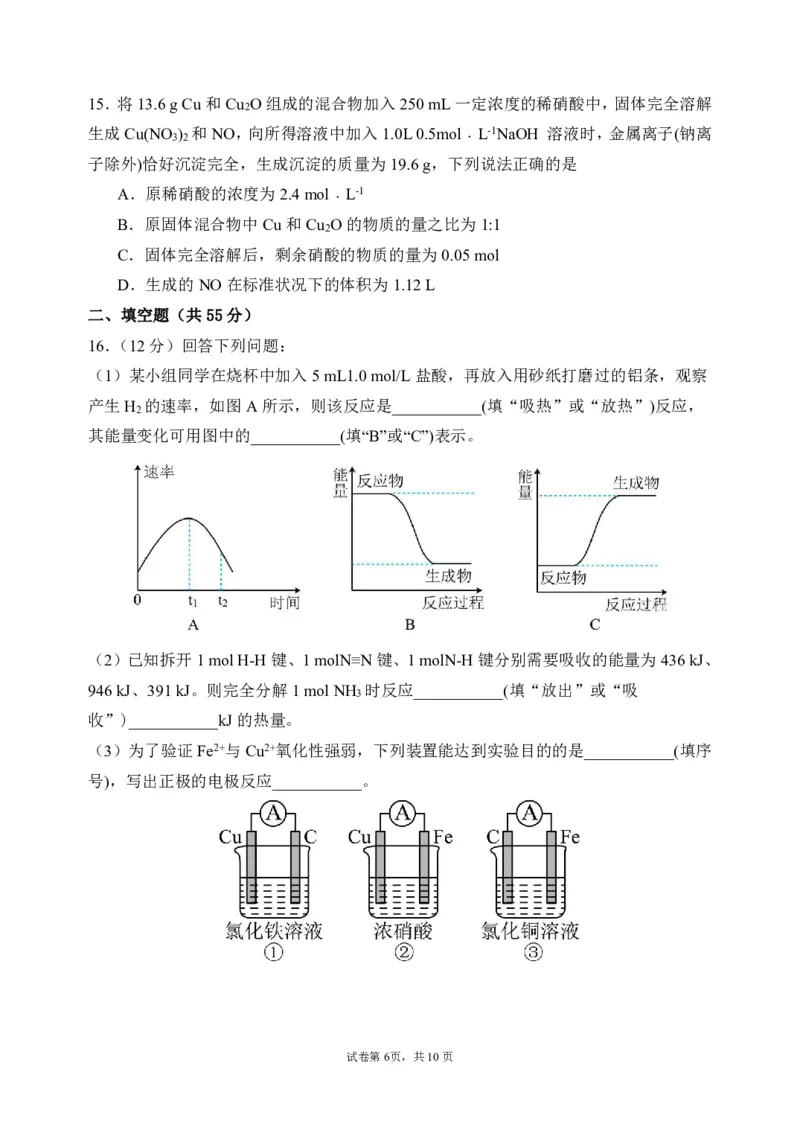
(1)某小组同学在烧杯中加入5mL1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察
产生H 的速率,如图A所示,则该反应是___________(填“吸热”或“放热”)反应,
2
其能量变化可用图中的___________(填“B”或“C”)表示。
(2)已知拆开1molH-H键、1molN≡N键、1molN-H键分别需要吸收的能量为436kJ、
946kJ、391kJ。则完全分解1molNH 时反应___________(填“放出”或“吸
3
收”)___________kJ的热量。
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是___________(填序
号),写出正极的电极反应___________。
试卷第6页,共10页17.(16分)元素周期表中第ⅤA元素组成的物质,在实际生产中有着广泛的应用。
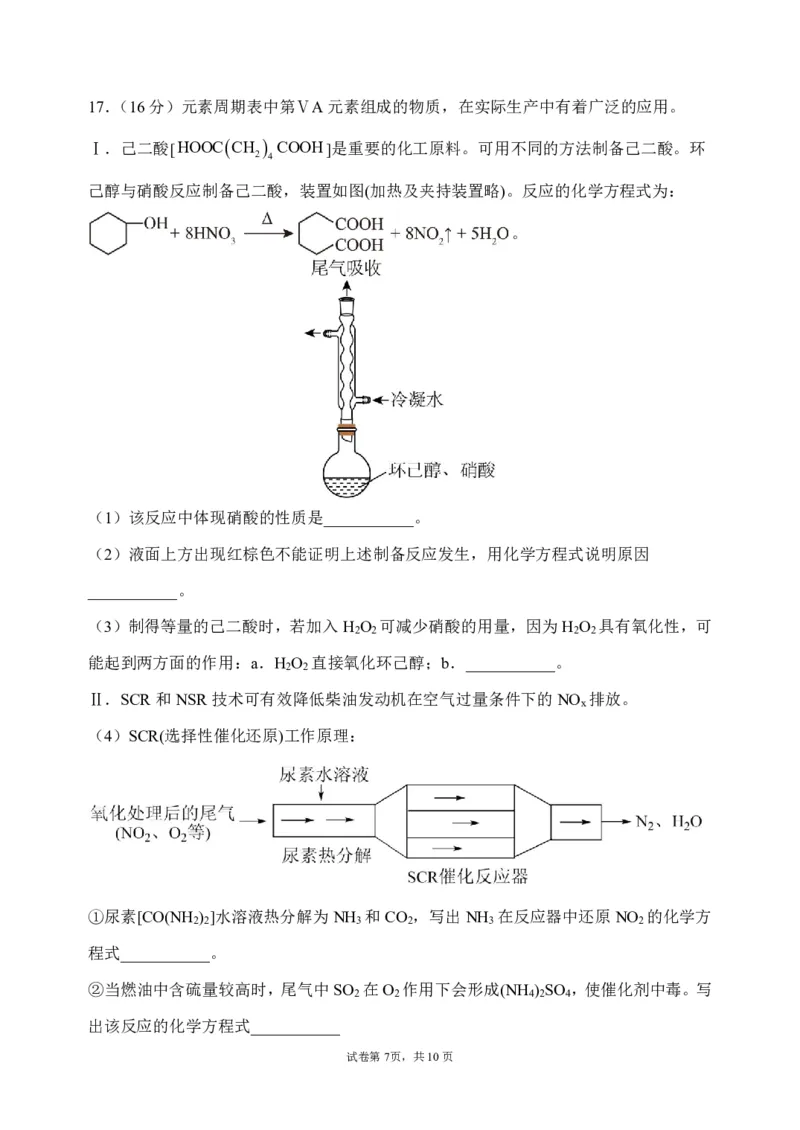
Ⅰ.己二酸[HOOCCH COOH]是重要的化工原料。可用不同的方法制备己二酸。环
2 4
己醇与硝酸反应制备己二酸,装置如图(加热及夹持装置略)。反应的化学方程式为:
。
(1)该反应中体现硝酸的性质是___________。
(2)液面上方出现红棕色不能证明上述制备反应发生,用化学方程式说明原因
___________。
(3)制得等量的己二酸时,若加入H O 可减少硝酸的用量,因为H O 具有氧化性,可
2 2 2 2
能起到两方面的作用:a.H O 直接氧化环己醇;b.___________。
2 2
Ⅱ.SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NO 排放。
x
(4)SCR(选择性催化还原)工作原理:
①尿素[CO(NH ) ]水溶液热分解为NH 和CO ,写出NH 在反应器中还原NO 的化学方
2 2 3 2 3 2
程式___________。
②当燃油中含硫量较高时,尾气中SO 在O 作用下会形成(NH ) SO ,使催化剂中毒。写
2 2 4 2 4
出该反应的化学方程式___________
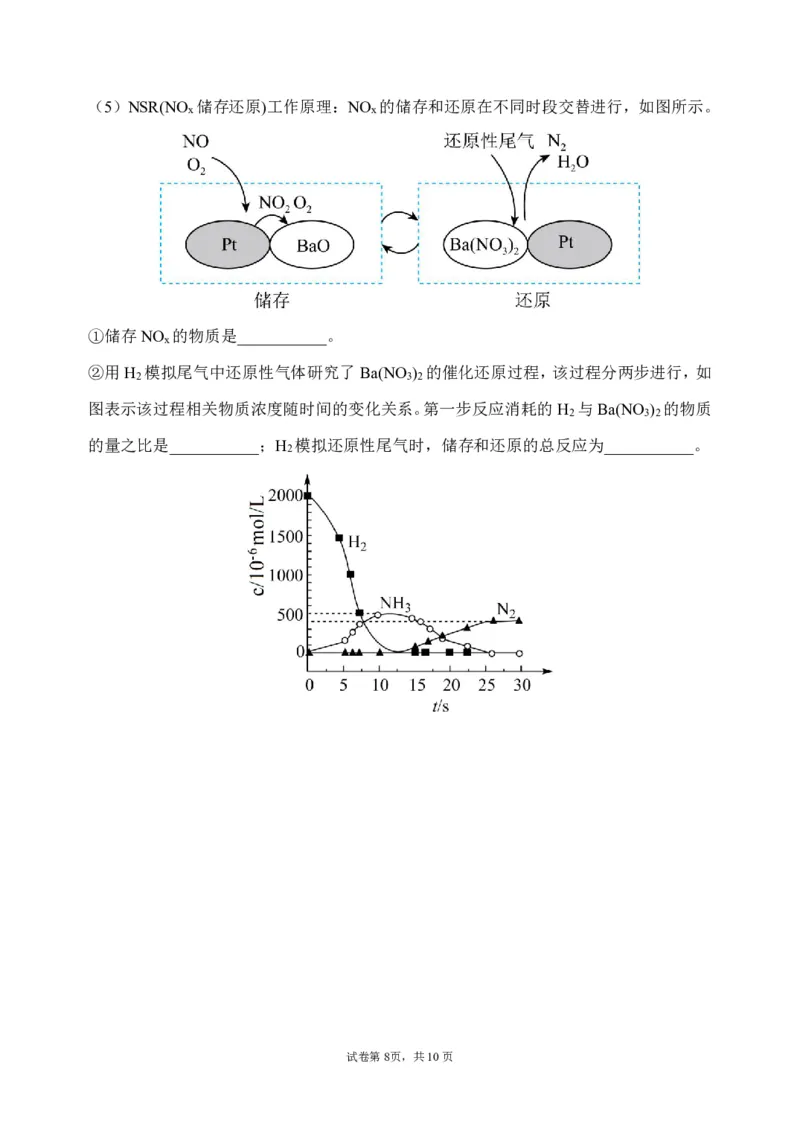
试卷第7页,共10页(5)NSR(NO 储存还原)工作原理:NO 的储存和还原在不同时段交替进行,如图所示。
x x
①储存NO 的物质是___________。
x
②用H 模拟尾气中还原性气体研究了Ba(NO ) 的催化还原过程,该过程分两步进行,如
2 3 2
图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H 与Ba(NO ) 的物质
2 3 2
的量之比是___________;H 模拟还原性尾气时,储存和还原的总反应为___________。
2
试卷第8页,共10页18.(13分)四溴化硅是制备高纯硅的关键原料。回答下列问题:
I.制备SiBr :实验室用Si和Br 制备SiBr 的装置(省略夹持仪器)如下图。实验时,
4 2 4
先通入一段时间的氮气。然后将管式炉加热至600℃,将液溴加热至50℃,同时通入冷
却水,继续通入氮气直至反应结束。反应结束后得到橙红色液体。
II.提纯SiBr :将橙红色液体加入锌粉后进一步进行提纯,得到纯度较高的SiBr 。
4 4
III.测定SiBr 纯度:取ag样品溶于适量水中,充分反应后过滤,所得沉淀经洗涤后置
4
于质量为m g的坩埚中,高温灼烧后将坩埚置于干燥器中冷却至室温,最后称量质量为
1
m g。
2
已知:①SiBr 常温下为无色透明液体,沸点为153℃,熔点为5℃,易水解,在空气中“发
4
烟”
②高温下硅酸分解生成二氧化硅
(1)A和F盛装的试剂分别是___________、___________(填名称)。
(2)实验中通入N 的作用是___________。
2
(3)仪器D的名称是___________。
(4)“提纯SiBr ”中加入锌粉的目的是___________,提纯的方法是___________。
4
(5)“测定SiBr 纯度”中将样品溶于适量水时SiBr 发生反应的化学方程式为_______。
4 4
(6)所得产品的纯度为___________(用含a、m 、m 的代数式表示)。若高温灼烧后在
1 2
空气中冷却,会导致产品纯度偏高的原因是___________。
试卷第9页,共10页19.(14分)黄金(Au)的一种化学精炼过程如下图所示。
回答下列问题:
(1)俗话说“真金不怕火炼”,从氧化还原性角度解释其原因是_______。
(2)步骤①中部分Cu与稀H SO 、O 反应,该反应的离子方程为_______。
2 4 2
(3)步骤③中银和稀硝酸反应的化学方程式为 _______ 。
(4)步骤④中的王水[V(浓硝酸):V(浓盐酸)=1:3]与Au反应生成了HAuCl 、NO和H O,
4 2
该反应的化学方程式为_______。该步骤产生的尾气中有NO,NO与足量空气混合被水
吸收过程中发生反应的化学方程式为_______。
(5)关于王水溶金的下列说法正确的是_______。
A.用到了HNO 的氧化性
3
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO 也可使Au溶解
3
(6)步骤⑥中用草酸(H C O )将溶液中的1molHAuCl 完全还原,则参加反应的草酸的
2 2 4 4
物质的量是_______mol。
试卷第10页,共10页高一年级化学科第一次月考参考答案
选择题答案(每小题3分,共45分)
1 2 3 4 5 6 7 8 9 10
A C D D B C D C D D
11 12 13 14 15
B C C C A
16.(12分)(1) 放热 2分 B 2分
(2)吸收 2分 46 2分
(3)③ 2分 Cu2++2e-=Cu 2分
17.(16分)(1)氧化性 2分
Δ
(2)4HNO 4NO +O +2H O 2分
3 2 2 2
(3)将反应生成的NO 氧化为硝酸,使硝酸循环利用,减少硝酸消耗 2分
2
催化剂
(4) 8NH +6NO 7N +12H O 2分 2SO 2 +O 2 +4NH 3 +2H 2 O=2(NH 4 ) 2 SO 4 2分
3 2 2 2
(5)BaO(作为储存剂) 2分 8:1 2分
催化剂
4NO+3O +10H 2N +10H O 2分
2 2 2 2
18.(13分)(1) 浓硫酸 1分 无水CaCl 1分
2
(2)排尽装置内空气,防止Si、Br 与空气中成分反应,同时将Br 蒸气吹入管式炉中参
2 2
加反应 2分
(3)(球形)冷凝管 1分
(4)除去未反应的Br 1分 蒸馏 1分
2
(5)SiBr 3H OH SiO 4HBr 2分
4 2 2 3
348(m m)
(6) 2 1 100% 2分 高温灼烧后在空气中冷却,SiO 会吸收空气中水蒸
2
60a
气,使m 增大,从而导致计算出的SiBr 纯度偏高 2分
2 4
试卷第11页,共10页19.(14分)【答案】(1)Au还原性弱,在高温条件下不与O 反应 2分
2
(2)2Cu+O +4H+=2Cu2++2H O 2分
2 2
(3)3Ag+4HNO =3AgNO +NO↑+2H O 2分
3 3 2
(4) Au+HNO +4HCl=HAuCl +NO↑+2H O 2分 4NO+3O +2H O=4HNO 2分
3 4 2 2 2 3
(5)AC 2分
(6)1.5 2分
试卷第12页,共10页报告查询:登录zhixue.com或扫描二维码下载App
(用户名和初始密码均为准考证号)
东北育才高中2025-2026学年度下学期高一年级化学科第一次
月考答题卡
姓名: 班级:
考场/座位号:
贴条形码区
注意事项
1.答题前,考生先将自己的姓名、班级、考场填写清楚,并认真核对
条形码上的姓名和准考证号。
2.选择题部分请按题号用2B铅笔填涂方框,修改时用橡皮擦干净,不
(正面朝上,切勿贴出虚线方框)
留痕迹。
3.非选择题部分请按题号用0.5毫米黑色墨水签字笔书写,否则作答
无效。要求字体工整、笔迹清晰。作图时,必须用2B铅笔,并描浓。 正确填涂 缺考标记
4.在草稿纸、试题卷上答题无效。
5.请勿折叠答题卡,保持字体工整、笔迹清晰、卡面清洁。
单选题
1 [A] [B] [C] [D] 6 [A] [B] [C] [D] 11 [A] [B] [C] [D]
2 [A] [B] [C] [D] 7 [A] [B] [C] [D] 12 [A] [B] [C] [D]
3 [A] [B] [C] [D] 8 [A] [B] [C] [D] 13 [A] [B] [C] [D]
4 [A] [B] [C] [D] 9 [A] [B] [C] [D] 14 [A] [B] [C] [D]
5 [A] [B] [C] [D] 10 [A] [B] [C] [D] 15 [A] [B] [C] [D]
解答题
16.(12分)
(1)___________,2分 ___________。2分
(2)___________,2分 ___________kJ的热量。 2分
(3)___________(填序号),2分
______________________________________________。2分
17.(16分)
(1)__________________。2分
(2)___________________________________________________________________。2分
(3)b._____________________________________________________。2分
(4)①_______________________________________________________________。2分
②________________________________________________________________。2分
(5)①__________。2分②___________;2分
____________________________________________________________。 2分
18.(13分)
(1)___________、___________(填名称)。2分
(2)_________________________________________________________________________。2分
(3)__________________。1分
(4)_______________________________________,1分 __________________。1分
(5)__________________________________________________________________________。2分
(6)______________________________(用含a、m 、m 的代数式表示)。2分
1 2
__________________________________________________________________________。2分
19.(14分)
(1)_______________________________________________________________。2分
(2)_______________________________________________________________。2分
(3)_______________________________________________________________ 。2分
(4)________________________________________________________。2分
________________________________________________________。2分
(5)______________。2分
(6)______________mol。2分