文档内容
辽宁省实验中学2025—2026学年度上学期第一次阶段测试
高一年级 化学试卷
考试时间:75分钟 试题满分:100分
命题人:葛秋实 校对人:高涵
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32
一、单选题(每小题3分,共15题,共45分。每题只有一个选项符合题意。)
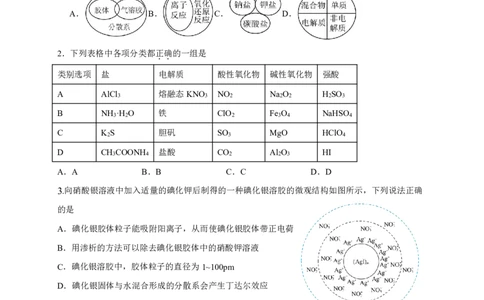
1.下列逻辑关系图示中正确的是
A. B. C. D.
2.下列表格中各项分类都正
.
确
.
的一组是
类别选项 盐 电解质 酸性氧化物 碱性氧化物 强酸
A AlCl 熔融态KNO NO Na O H SO
3 3 2 2 2 2 3
B NH ·H O 铁 ClO Fe O NaHSO
3 2 2 3 4 4
C K S 胆矾 SO MgO HClO
2 3 4
D CH COONH 盐酸 CO Al O HI
3 4 2 2 3
A.A B.B C.C D.D
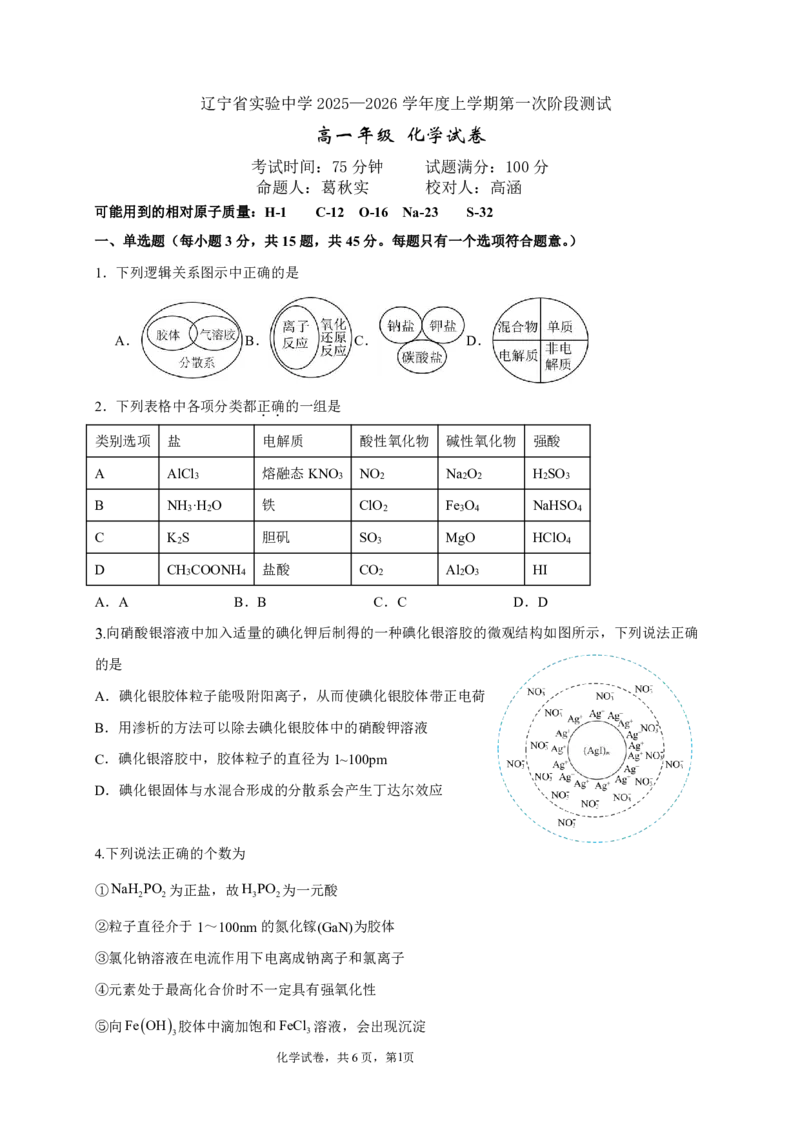
3.向硝酸银溶液中加入适量的碘化钾后制得的一种碘化银溶胶的微观结构如图所示,下列说法正确
的是
A.碘化银胶体粒子能吸附阳离子,从而使碘化银胶体带正电荷
B.用渗析的方法可以除去碘化银胶体中的硝酸钾溶液
C.碘化银溶胶中,胶体粒子的直径为1~100pm
D.碘化银固体与水混合形成的分散系会产生丁达尔效应
4.下列说法正确的个数为
①NaH PO 为正盐,故H PO 为一元酸
2 2 3 2
②粒子直径介于1~100nm的氮化镓(GaN)为胶体
③氯化钠溶液在电流作用下电离成钠离子和氯离子
④元素处于最高化合价时不一定具有强氧化性
⑤向FeOH 胶体中滴加饱和FeCl 溶液,会出现沉淀
3 3
化学试卷,共6页,第1页⑥有单质参加的反应或有单质生成的反应是氧化还原反应
⑦能电离出H的纯净物属于酸
⑧同素异形体之间转化为化学变化;核聚变和核裂变也属于化学变化
A.1个 B.2个 C.3个 D.4个
5.下列各组离子在指定溶液中一定可以大量共存的是
A.氨水中:K、Al3+、SO2、NO
4 3
B.澄清透明溶液中:NH+、K+、MnO-、SO2-
4 4 4
C.氢氧化钠溶液中:Na、Ba2、NO、HCO
3 3
D.使酚酞变红的溶液中:NH、Fe3、Cl、SO2
4 4
6.下列离子方程式正确的是
A.向MgHCO 溶液中加入过量的NaOH溶液:Mg22HCO2OH MgCO CO22H O
3 2 3 3 3 2
B.草酸与酸性KMnO 溶液反应:2MnO-+16H++5C O2-=2Mn2++10CO +8H O
4 4 2 4 2 2
C.Ba(OH) 与NaHSO 反应使溶液呈中性: Ba2++2OH-+2H++SO 2-=BaSO ↓+2H O
2 4 4 4 2
D.氯气通入冷的石灰乳中制漂白粉:Cl 2OH ClOClH O
2 2
7.某澄清透明溶液中只含HCO、Cl、CO2、SO2、Na、K、Mg2、Cu2、H、NH中的
3 3 4 4
几种,且各离子的个数相等,现进行如下实验:
①取少量该溶液,加入过量的Ba(OH) 溶液,产生白色沉淀,加热溶液无气体生成;
2
②取实验①中白色沉淀,加入足量稀盐酸,白色沉淀部分溶解;
③再取少量该溶液,逐滴加入稀盐酸,立即产生气体,振荡后静置,向上层溶液中加入AgNO 溶液,
3
产生白色沉淀,再加稀硝酸,白色沉淀不溶解。
下列关于该溶液的说法正确的是
A.一定含有Cl
B.一定不含Mg2、Cu2
C.含HCO,不含CO2
3 3
D.一定含Na和K
化学试卷,共6页,第2页8.已知硫酸亚铜易溶于水,氯化亚铜不溶于水。探究NaHSO 溶液与Cu2的反应,过程如图所示:
3
无色气体和白色沉淀经检验分别是SO 和CuCl、有关该实验说法正确的是
2
A.SO 是还原产物 B.CuCl是还原产物
2
C.无Cl时,HSO能被Cu2氧化 D.HSO被Cu2氧化时,Cl作催化剂
3 3
9.NaSbO 可用作玻璃澄清剂,可用“硝酸钠法”制备,反应方程式为
3
高温
4NaNO +4Sb+3O 4 NaSbO +2NO+2NO 。下列说法错误的是
3 2 3 2
A.NaSbO 中Sb元素的化合价为+5 B.NO、NO 均属于还原产物
3 2
C.每生成2个 NO,反应转移20个e D.反应中氧化剂和还原剂的个数之比为4∶7
10.工业上利用含铁催化剂循环处理含SO 的废气并回收碘,流程涉及以下反应
2
①2FeCl +2KI=2FeCl +2KCl+I ;②2FeCl +Cl =2FeCl ;③I +SO +2H O=H SO +2HI。根据上述反
3 2 2 2 2 3 2 2 2 2 4
应,判断下列说法正确的是
A.氧化性由强到弱的顺序为:Cl >I >Fe3+>SO2-
2 2 4
B.反应①中,当有1个FeCl 被还原时,转移的电子数为2个
3
C.该流程中FeCl 可循环利用,最终消耗了KI、SO 和Cl 等
3 2 2
D.在溶液中,Fe3+与SO 能大量共存
2
11.用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
①2NO +2NaOH=NaNO +NaNO +H O
2 3 2 2
②NO+NO +2NaOH=2NaNO +H O
2 2 2
已知:NO不能直接与NaOH溶液发生反应。下列说法错误的是
A.反应①中每消耗2个NO ,转移1个电子
2
B.反应②中氧化剂是NO ,还原剂是NO
2
C.若混合气体被完全吸收且充分反应后产物中NaNO 和NaNO 的个数比为1:2,则废气中NO
3 2 2
和NO的个数比为3:1
D.为保证废气中的氮氧化物被完全吸收,二者个数关系为:NO ≥NO
2
化学试卷,共6页,第3页12.下列关于反应的说法正确的是
A.11PH 24CuSO 12H O3H PO 24H SO 8Cu P,每24个CuSO 氧化11个PH
3 4 2 3 4 2 4 3 4 3
B.6I 11KClO 3H O6KHIO 5KCl3Cl ,产生1个Cl 时,反应转移10个e-
2 3 2 3 2 2 2
C.3Fe2++2S O 2-+O +4OH-=Fe O +S O 2-+2H O,当6个Fe2+被氧化时有2个O 被还原
2 3 2 3 4 4 6 2 2
D.K H IO 9HI 2KI4I 6H O ,还原剂与氧化剂的个数之比为7:1
2 3 6 2 2
13.将4.6g钠与1.6g硫粉迅速混合起来,并放在陶土网上加热,反应后生成的固体是
A.过氧化钠与硫 B.氧化钠与硫化钠 C.硫与硫化钠 D.过氧化钠与硫化钠
14.钠在空气中燃烧产物X和金属钠分别加入到足量水中,生成的两种气体在一定条件下恰好完全
反应,则金属钠与 X质量比为
A.1:2 B.2:1 C.23:39 D.39:23
15.某同学探究金属Na与CO 的反应,实验如下:
2
实验Ⅰ 实验Ⅱ
将点燃的金属钠伸入 将实验Ⅰ的集气瓶用水洗涤,过滤;取黑色滤渣
操作
盛有CO 的集气瓶中 灼烧;取滤液分别滴加酚酞溶液和氯化钡溶液
2
①火焰呈黄色 ①黑色滤渣可燃
现象 ②底部有黑色固体,瓶 ②滤液能使酚酞溶液变红,滴加氯化钡溶液有白
壁上附有白色固体 色沉淀生成
下列说法不正确的是
A.生成的黑色固体中含有C B.白色固体是Na O
2
C.实验说明CO 具有氧化性 D.金属Na着火不能用泡沫灭火器灭火
2
二、填空题(共4小题,共55分)
16.(13分) Ⅰ.某无色透明溶液中可能大量存在Ba2+、Mg2+、Cu2+、 Na+、Cl-、CO2-、OH-、SO2-
3 4
和NO-中的几种,且所含的各离子个数相等,请填写下列空白:
3
(1)不做任何实验就可以肯定原溶液中不存在的离子是 。
(2)取少量原溶液,加入过量的烧碱,出现白色沉淀,有关离子方程式为 。
(3)另取少量原溶液,加入过量Ba(NO ) 溶液,有白色沉淀生成,过滤,向沉淀中加入过量的稀硝酸,
3 2
沉淀不消失。取反应后的滤液,加入硝酸银溶液,有白色沉淀生成,且沉淀不溶于稀硝酸。综上所
述,原溶液中一定存在的离子有 。
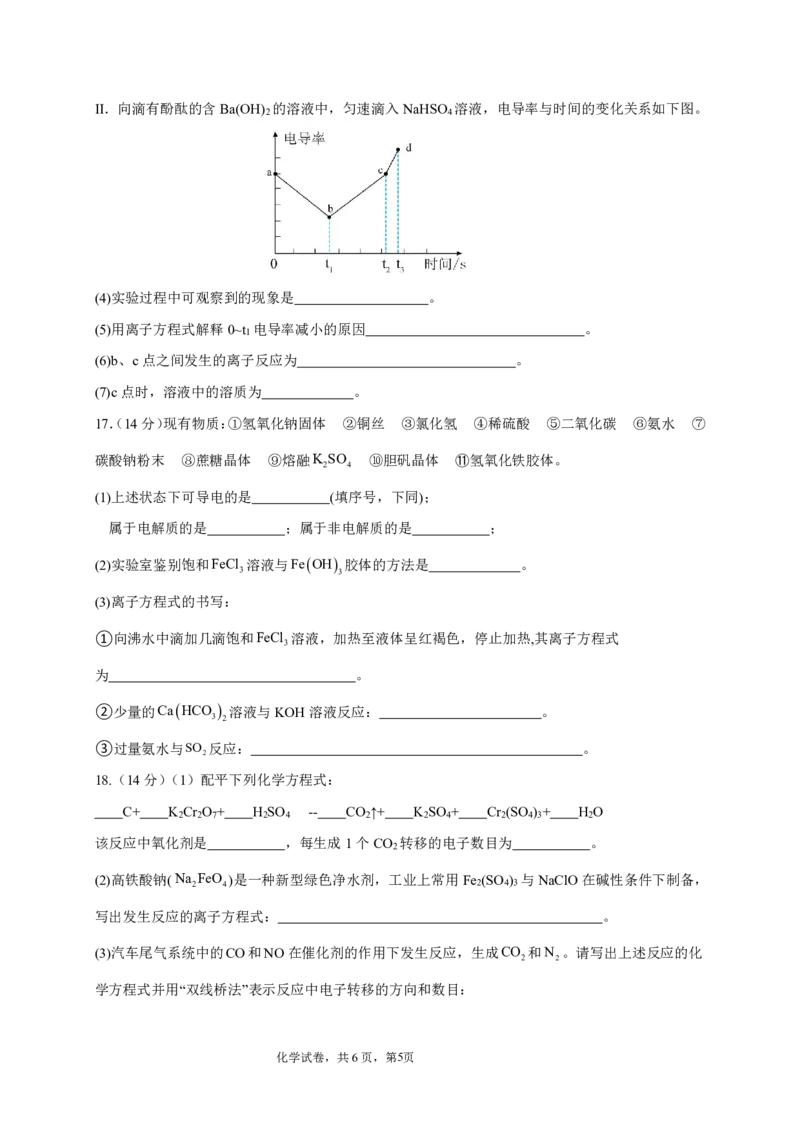
化学试卷,共6页,第4页Ⅱ.向滴有酚酞的含Ba(OH) 的溶液中,匀速滴入NaHSO 溶液,电导率与时间的变化关系如下图。
2 4
(4)实验过程中可观察到的现象是 。
(5)用离子方程式解释0~t 电导率减小的原因 。
1
(6)b、c点之间发生的离子反应为 。
(7)c点时,溶液中的溶质为 。
17.(14分)现有物质:①氢氧化钠固体 ②铜丝 ③氯化氢 ④稀硫酸 ⑤二氧化碳 ⑥氨水 ⑦
碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融K SO ⑩胆矾晶体 ⑪氢氧化铁胶体。
2 4
(1)上述状态下可导电的是 (填序号,下同);
属于电解质的是 ;属于非电解质的是 ;
(2)实验室鉴别饱和FeCl 溶液与FeOH 胶体的方法是 。
3 3
(3)离子方程式的书写:
①向沸水中滴加几滴饱和FeCl 溶液,加热至液体呈红褐色,停止加热,其离子方程式
3
为 。
②少量的CaHCO 溶液与KOH溶液反应: 。
3 2
③过量氨水与SO 反应: 。
2
18.(14分)(1)配平下列化学方程式:
C+ K Cr O + H SO -- CO ↑+ K SO + Cr (SO ) + H O
2 2 7 2 4 2 2 4 2 4 3 2
该反应中氧化剂是 ,每生成1个CO 转移的电子数目为 。
2
(2)高铁酸钠(Na FeO )是一种新型绿色净水剂,工业上常用Fe (SO ) 与NaClO在碱性条件下制备,
2 4 2 4 3
写出发生反应的离子方程式: 。
(3)汽车尾气系统中的CO和NO在催化剂的作用下发生反应,生成CO 和N 。请写出上述反应的化
2 2
学方程式并用“双线桥法”表示反应中电子转移的方向和数目:
化学试卷,共6页,第5页。
(4)下列方程式中A、B、C、D、E均为含氯元素的物质,它们之间存在如下反应:
(a)DNaOHABH O ;(b)ABNaCl;(c)BH OCH ;(d)ENaOHBCH O
2 2 2 2
试推断五种物质中氯元素的化合价由低到高的顺序为 。
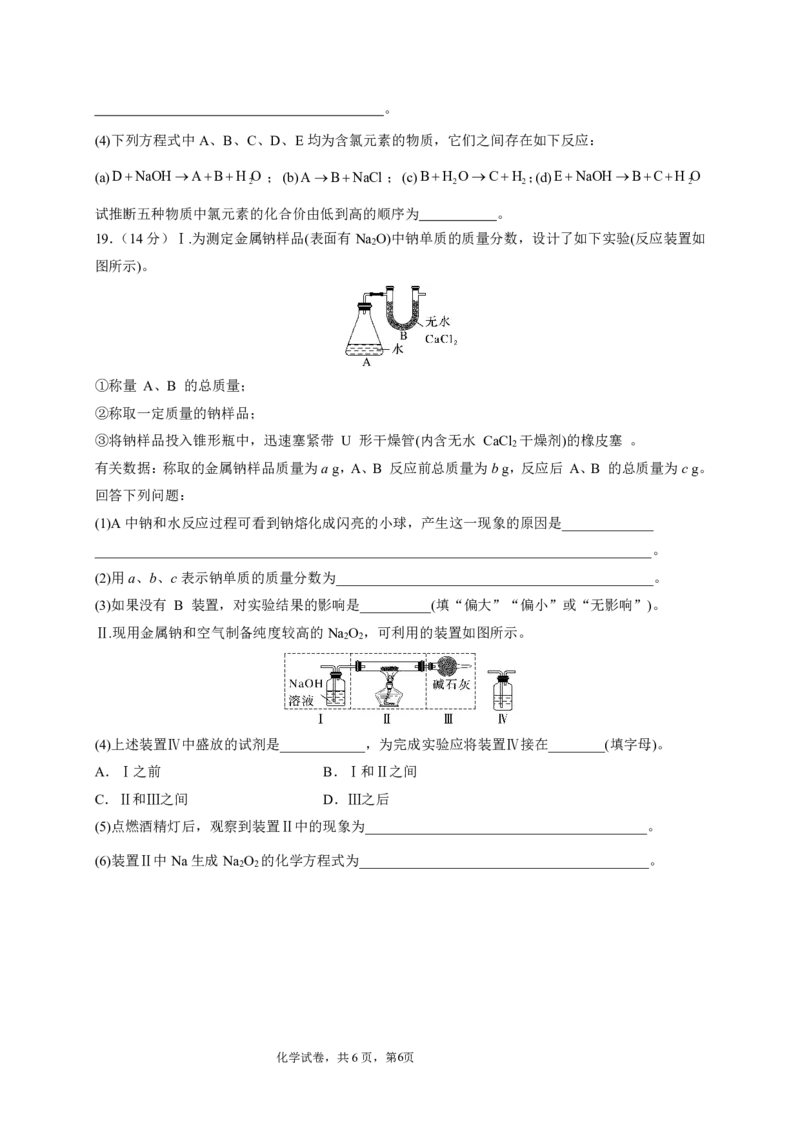
19.(14分)Ⅰ.为测定金属钠样品(表面有Na O)中钠单质的质量分数,设计了如下实验(反应装置如
2
图所示)。
①称量 A、B 的总质量;
②称取一定质量的钠样品;
③将钠样品投入锥形瓶中,迅速塞紧带 U 形干燥管(内含无水 CaCl 干燥剂)的橡皮塞 。
2
有关数据:称取的金属钠样品质量为ag,A、B 反应前总质量为bg,反应后 A、B 的总质量为cg。
回答下列问题:
(1)A中钠和水反应过程可看到钠熔化成闪亮的小球,产生这一现象的原因是_____________
_______________________________________________________________________________。
(2)用a、b、c表示钠单质的质量分数为_____________________________________________。
(3)如果没有 B 装置,对实验结果的影响是__________(填“偏大”“偏小”或“无影响”)。
Ⅱ.现用金属钠和空气制备纯度较高的Na O ,可利用的装置如图所示。
2 2
(4)上述装置Ⅳ中盛放的试剂是____________,为完成实验应将装置Ⅳ接在________(填字母)。
A.Ⅰ之前 B.Ⅰ和Ⅱ之间
C.Ⅱ和Ⅲ之间 D.Ⅲ之后
(5)点燃酒精灯后,观察到装置Ⅱ中的现象为________________________________________。
(6)装置Ⅱ中Na生成Na O 的化学方程式为_________________________________________。
2 2
化学试卷,共6页,第6页辽宁省实验中学2025—2026学年度上学期第一次阶段测试参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 D C B C B C C B D C
题号 11 12 13 14 15
答案 C D D C B
16.(13分,除特殊标注,每空2分)
(1)Cu2+ (2)Mg2++2OH-=Mg(OH) (3)Mg2+、 Na+、Cl-、SO2-
2 4
(4)有白色沉淀生成,溶液红色逐渐褪去 (5)Ba2++OH+H++SO2=BaSO +H O
4 4 2
(6)OH+H+=H O(7)Na SO (1分)
2 2 4
17.(14分,每空2分)(1)②④⑥⑨⑪ ①③⑦⑨⑩ ⑤⑧
(2)丁达尔效应
(3)①Fe3++3HO Fe(OH)(胶体)+3H+
2 3
②Ca2 2HCO2OH CaCO CO22H O
3 3 3 2
③2NH H OSO 2NH++SO2H O
3 2 2 4 3 2
18.(14分,每空2分)
(1)3C2K CrO 8H SO 3CO +2K SO 2Cr SO 8H O K CrO 4
2 2 7 2 4 2 2 4 2 4 3 2 2 2 7
(2)2Fe3 3ClO10OH 2FeO23Cl5H O
4 2
(3) (方程式和双线桥各2分)
(4)ADBEC
19.(14分,每空2分)(1)该反应为放热反应,钠的熔点低
23a+b-c
(2) ×100% (3)偏大 (4)浓硫酸 B (5)钠熔化成光亮的小球,剧烈燃烧,产生
a
△
黄色火焰,生成淡黄色固体 (6)2Na+O =====Na O
2 2 2