文档内容
运城中学 2025-2026 学年第一学期高一年级期中考试
化 学 试 题
一、单项选择题:本题共14小题,每小题3分,共42分.每题所给的答案中,只有一个是
考生请注意:
1. 本试卷共7页,满分100分,考试时间75分钟.考试结束后,交回答题纸;
2. 答题前,请务必将自己的姓名、考生号用0.5毫米黑色中性笔或碳素笔在答
题纸上进行书写;
3. 作答选择题,必须用2B铅笔将答题纸上的对应题目的答题标号涂黑涂满;
如需改动,请用橡皮擦干净后,再更正其它的答案.未在答题纸上作答的、
在答题纸规定区域以外答题的一律无效;
4. 如有作图需要,请使用2B铅笔作图,并加黑加粗,描写清楚.
正确选项.
1.化学科学和化学工业的发展,对人类文明的进步发挥了巨大的推动。下列说法错误的是
A.新药的成功研制——战胜那些危及人类生命的疾病
B.合成氨的化工技术——制造出大量能促进粮食增产的氮肥
C.功能各异的高分子材料的研制——生产出对环境无污染的聚乙烯塑料袋
D.以硅及其化合物为原料制造出的芯片和光导纤维——使人们生活丰富多彩
2.化学与生产生活联系紧密。下列说法正确的是
A.用Na CO 配制的苏打水可用于中和胃酸
2 3
B.聚氯乙烯薄膜可用于制作食品保鲜袋
C.SiO 因其导电性能优异而用于制作光纤
2
D.在钢铁部件表面进行“发蓝”处理属于化学变化
3.根据盖斯定律判断如下图所示的物质转变过程中,正确的等式是( )
A.ΔH=ΔH=ΔH=ΔH B.ΔH+ΔH=ΔH+ΔH
1 2 3 4 1 2 3 4
C.ΔH+ΔH+ΔH=ΔH D.ΔH=ΔH+ΔH+ΔH
1 2 3 4 1 2 3 4
4.下列关于化学平衡常数的叙述正确的是
A.化学平衡常数表示反应进行的程度,与温度无关
B.两种物质反应,不管怎样书写化学方程式,平衡常数均不变C.化学平衡常数等于某一时刻生成物浓度幂之积与反应物浓度幂之积的比值
D.温度一定,对于给定的化学反应,正、逆反应的平衡常数互为倒数
5.植物中山茶花、石榴可以吸收氯气,紫藤和月季对氯气的吸收净化能力也很强。在实验
室制取Cl 时,尾气一般要用NaOH溶液吸收而不用澄清石灰水吸收的理由是( )
2
A.氯气不与石灰水反应
B.澄清石灰水能吸收空气中的CO 而变浑浊
2
C.氯气与Ca(OH) 反应生成的CaCl 难溶于水
2 2
D.Ca(OH) 微溶于水,澄清石灰水中Ca(OH) 的含量少,吸收的尾气也很少
2 2
6.下列关于Na CO 、NaHCO 的叙述正确的是
2 3 3
①分别向等浓度的Na CO 和NaHCO 溶液中滴加1~2滴酚酞溶液,溶液均变红且NaHCO 溶
2 3 3 3
液颜色更深
②分别向等浓度的Na CO 和NaHCO 溶液滴加稀盐酸,NaHCO 溶液产生CO 气体较快
2 3 3 3 2
③除去NaHCO 固体中的Na CO :将固体加热至恒重
3 2 3
④能用澄清石灰水鉴别Na CO 、NaHCO 溶液
2 3 3
⑤相同温度下,溶解度:Na CO NaHCO
2 3 3
A.①③ B.②⑥ C.④⑤ D.⑥
7.下列反应的离子方程式的书写正确的是
A.氢氧化铜悬浊液中加入盐酸:
OH-+H+=H O
2
B.氯气通入NaOH溶液中制得漂白液:
Cl +2OH-=Cl-+ClO-+H O
2 2
C.碳酸钡与盐酸反应:
CO2-+2H+=H O+CO ↑
3 2 2
D.硫酸与氢氧化钡溶液混合:
H++SO2-+Ba2++OH-=BaSO ↓+H O
4 4 2
8.氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于阴影区域的是
试卷第2页,共7页△
A.Na O+H O=2NaOH B.2KMnO ¿K MnO +MnO +O ↑
2 2 4 2 4 2 2
¿
C.Zn+H SO =ZnSO +H ↑ D.2Cu O+Cu S=6Cu+SO
2 4 4 2 2 2 2
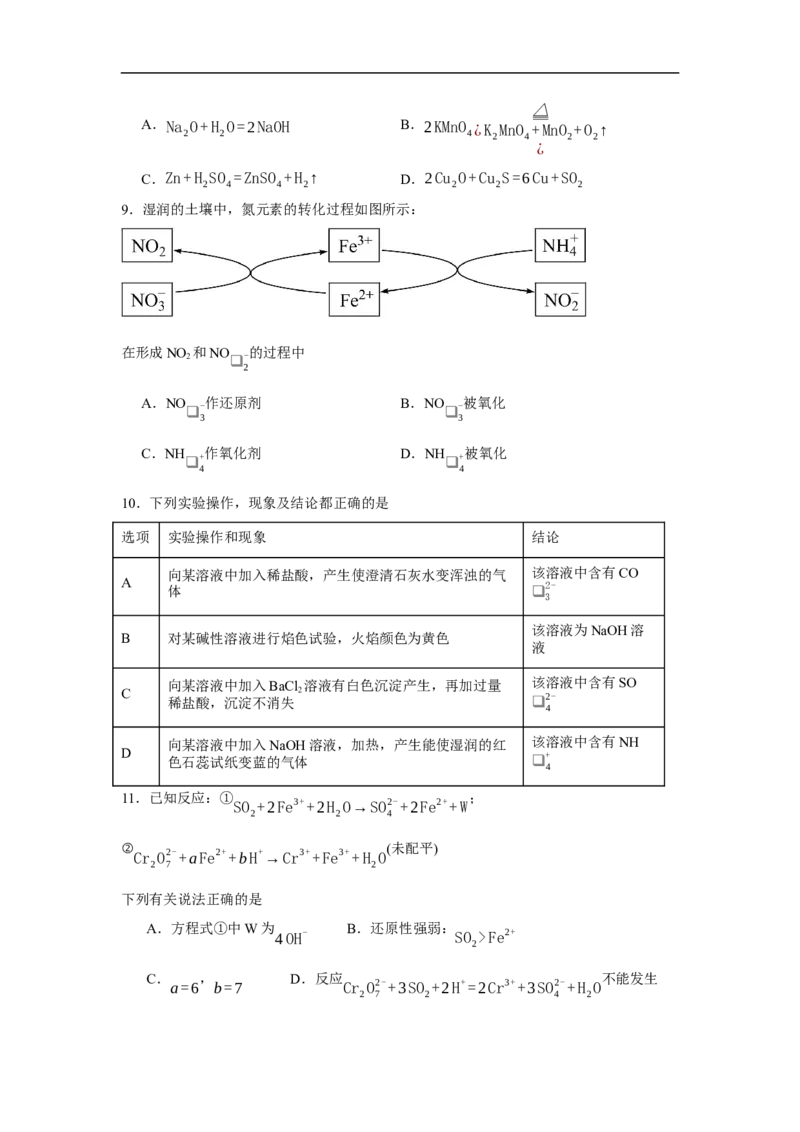
9.湿润的土壤中,氮元素的转化过程如图所示:
在形成NO 和NO 的过程中
2 ❑ -
2
A.NO 作还原剂 B.NO 被氧化
- -
❑ ❑
3 3
C.NH 作氧化剂 D.NH 被氧化
+ +
❑ ❑
4 4
10.下列实验操作,现象及结论都正确的是
选项 实验操作和现象 结论
向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气 该溶液中含有CO
A
体 ❑ 2-
3
该溶液为NaOH溶
B 对某碱性溶液进行焰色试验,火焰颜色为黄色
液
向某溶液中加入BaCl 溶液有白色沉淀产生,再加过量 该溶液中含有SO
C 2 2-
稀盐酸,沉淀不消失 ❑
4
向某溶液中加入NaOH溶液,加热,产生能使湿润的红 该溶液中含有NH
D +
色石蕊试纸变蓝的气体 ❑
4
11.已知反应:① ;
SO +2Fe3++2H O→SO2-+2Fe2++W
2 2 4
② Cr O2-+aFe2++bH+→Cr3++Fe3++H O (未配平)
2 7 2
下列有关说法正确的是
A.方程式①中W为 B.还原性强弱:
4OH- SO >Fe2+
2
C. , D.反应 不能发生
a=6 b=7 Cr O2-+3SO +2H+=2Cr3++3SO2-+H O
2 7 2 4 212.侯氏制碱法的第一步反应为CO +NH +NaCl+H O=NH Cl+NaHCO ↓。用N 表示阿
2 3 2 4 3 A
伏加德罗常数的值,下列说法正确的是
A.44gCO 含有的分子数为3N B.1molNH 中含有的氢原子数为
2 A 3
N
A
C.58.5gNaCl固体中含有的Na+数目为N
A
D.标准状况下,2.24LH O含有的分子数为0.1N
2 A
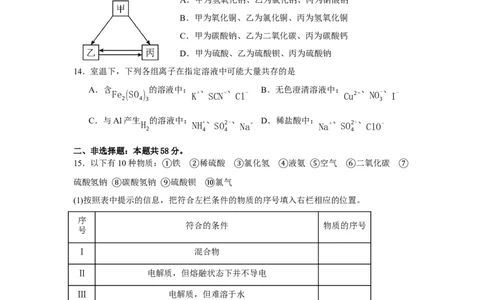
13.甲、乙、丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的
A.甲为氢氧化钠、乙为氯化钠、丙为硝酸钠
B.甲为氧化铜、乙为氯化铜、丙为氢氧化铜
C.甲为碳酸钠、乙为二氧化碳、丙为碳酸钙
D.甲为硫酸、乙为硫酸钡、丙为硫酸钠
14.室温下,下列各组离子在指定溶液中可能大量共存的是
A.含 的溶液中: 、 、 B.无色澄清溶液中: 、 、
Fe (SO ) K+ SCN- Cl- Cu2+ NO- I-
2 4 3 3
C.与Al产生 的溶液中: 、 、 D.稀盐酸中: 、 、
H NH+ SO2- Na+ Na+ SO2- ClO-
2 4 4 4
二、非选择题:本题共58分。
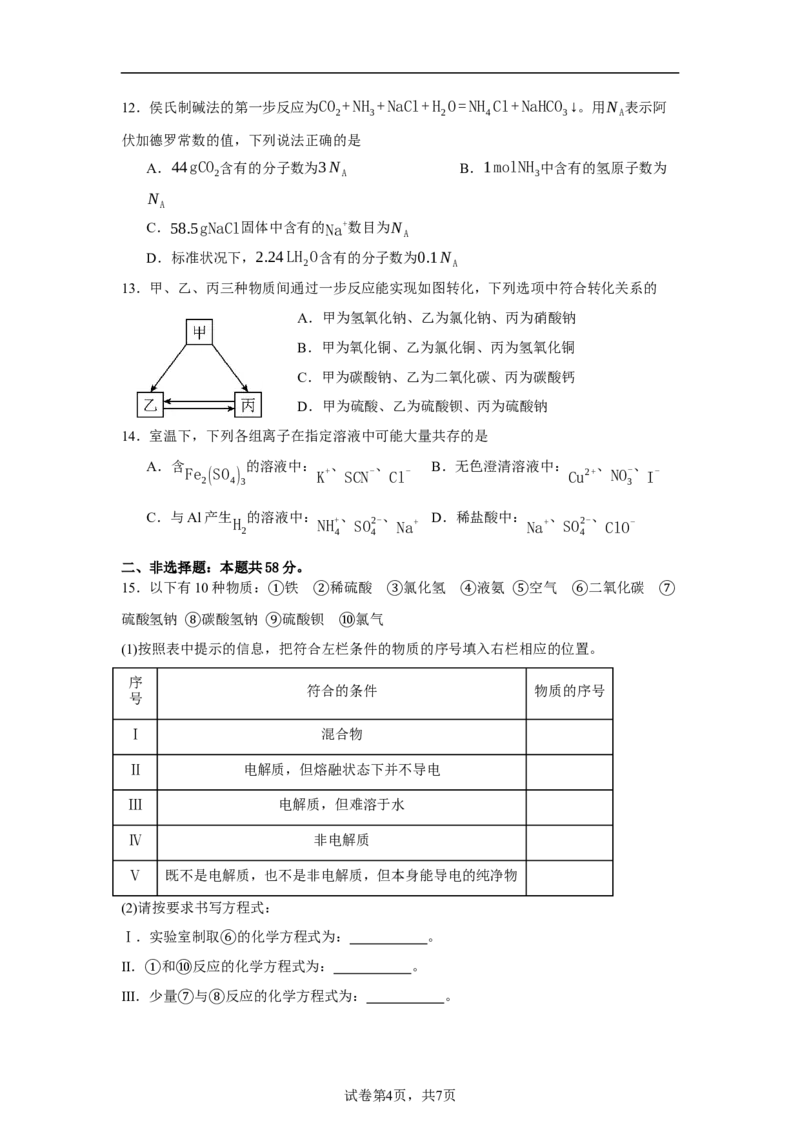
15.以下有10种物质: 铁 稀硫酸 氯化氢 液氨 空气 二氧化碳
硫酸氢钠 碳酸氢钠 ①硫酸钡② 氯气③ ④ ⑤ ⑥ ⑦
(1)按照表中⑧提示的信息,⑨把符合左栏⑩条件的物质的序号填入右栏相应的位置。
序
符合的条件 物质的序号
号
Ⅰ 混合物
Ⅱ 电解质,但熔融状态下并不导电
Ⅲ 电解质,但难溶于水
Ⅳ 非电解质
Ⅴ 既不是电解质,也不是非电解质,但本身能导电的纯净物
(2)请按要求书写方程式:
Ⅰ.实验室制取 的化学方程式为: 。
II. 和 反应⑥的化学方程式为: 。
III.①少量⑩与 反应的化学方程式为: 。
⑦ ⑧
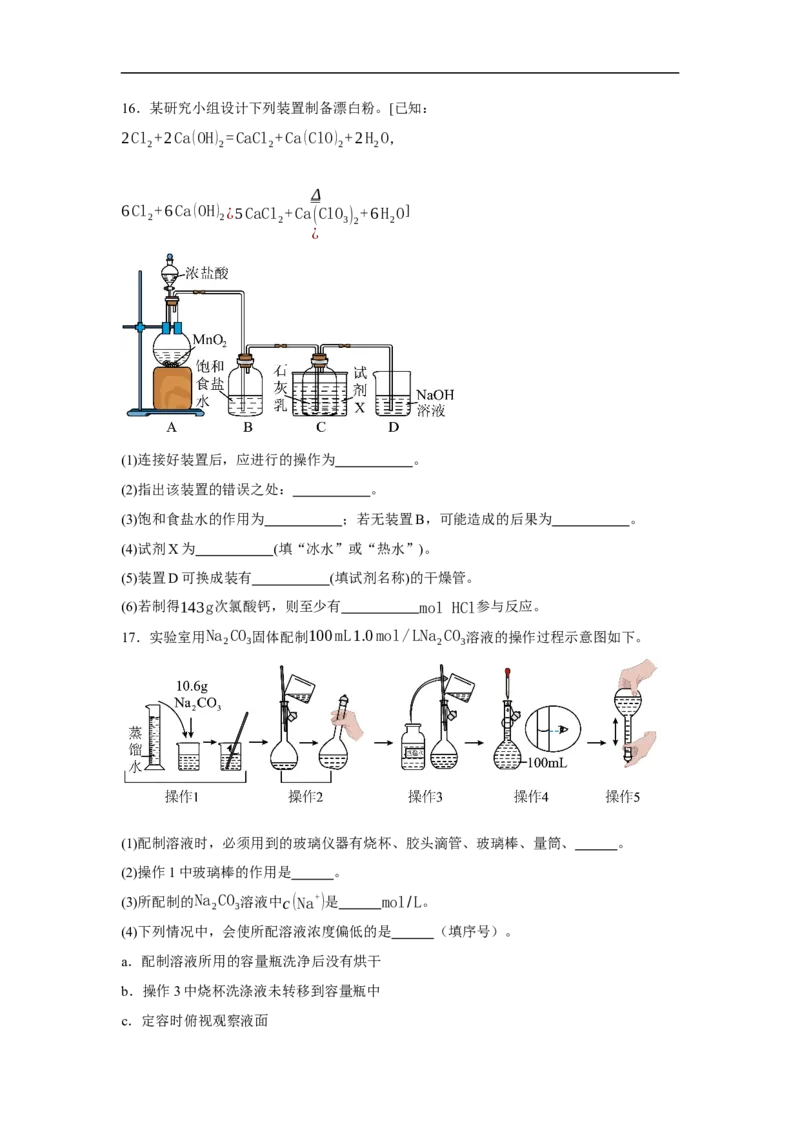
试卷第4页,共7页16.某研究小组设计下列装置制备漂白粉。[已知:
2Cl +2Ca(OH) =CaCl +Ca(ClO) +2H O,
2 2 2 2 2
Δ
6Cl +6Ca(OH) ¿5CaCl +Ca(ClO ) +6H O]
2 2 2 3 2 2
¿
(1)连接好装置后,应进行的操作为 。
(2)指出该装置的错误之处: 。
(3)饱和食盐水的作用为 ;若无装置B,可能造成的后果为 。
(4)试剂X为 (填“冰水”或“热水”)。
(5)装置D可换成装有 (填试剂名称)的干燥管。
(6)若制得143g次氯酸钙,则至少有 mol HCl参与反应。
17.实验室用Na CO 固体配制100mL1.0mol/LNa CO 溶液的操作过程示意图如下。
2 3 2 3
(1)配制溶液时,必须用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、量筒、 。
(2)操作1中玻璃棒的作用是 。
(3)所配制的Na CO 溶液中c(Na+)是 mol/L。
2 3
(4)下列情况中,会使所配溶液浓度偏低的是 (填序号)。
a.配制溶液所用的容量瓶洗净后没有烘干
b.操作3中烧杯洗涤液未转移到容量瓶中
c.定容时俯视观察液面18.现代社会中,人类的一切活动都离不开能量,研究化学能与热能、电能的转化具有重
要价值。回答下列问题:
I.化学反应与热能
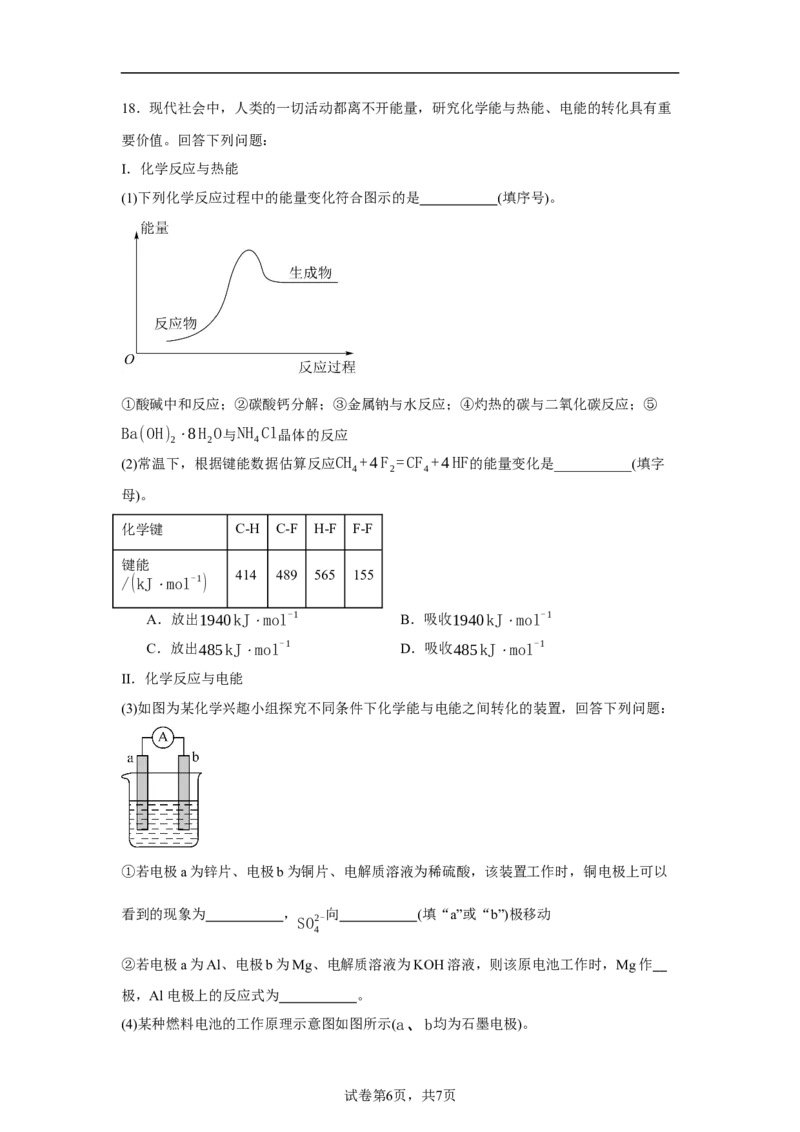
(1)下列化学反应过程中的能量变化符合图示的是 (填序号)。
①酸碱中和反应;②碳酸钙分解;③金属钠与水反应;④灼热的碳与二氧化碳反应;⑤
Ba(OH) ⋅8H O与NH Cl晶体的反应
2 2 4
(2)常温下,根据键能数据估算反应CH +4F =CF +4HF的能量变化是___________(填字
4 2 4
母)。
化学键 C-H C-F H-F F-F
键能
414 489 565 155
/(kJ⋅mol-1)
A.放出1940kJ⋅mol-1 B.吸收1940kJ⋅mol-1
C.放出485kJ⋅mol-1 D.吸收485kJ⋅mol-1
II.化学反应与电能
(3)如图为某化学兴趣小组探究不同条件下化学能与电能之间转化的装置,回答下列问题:
①若电极a为锌片、电极b为铜片、电解质溶液为稀硫酸,该装置工作时,铜电极上可以
看到的现象为 , 向 (填“a”或“b”)极移动
SO2-
4
②若电极a为Al、电极b为Mg、电解质溶液为KOH溶液,则该原电池工作时,Mg作
极,Al电极上的反应式为 。
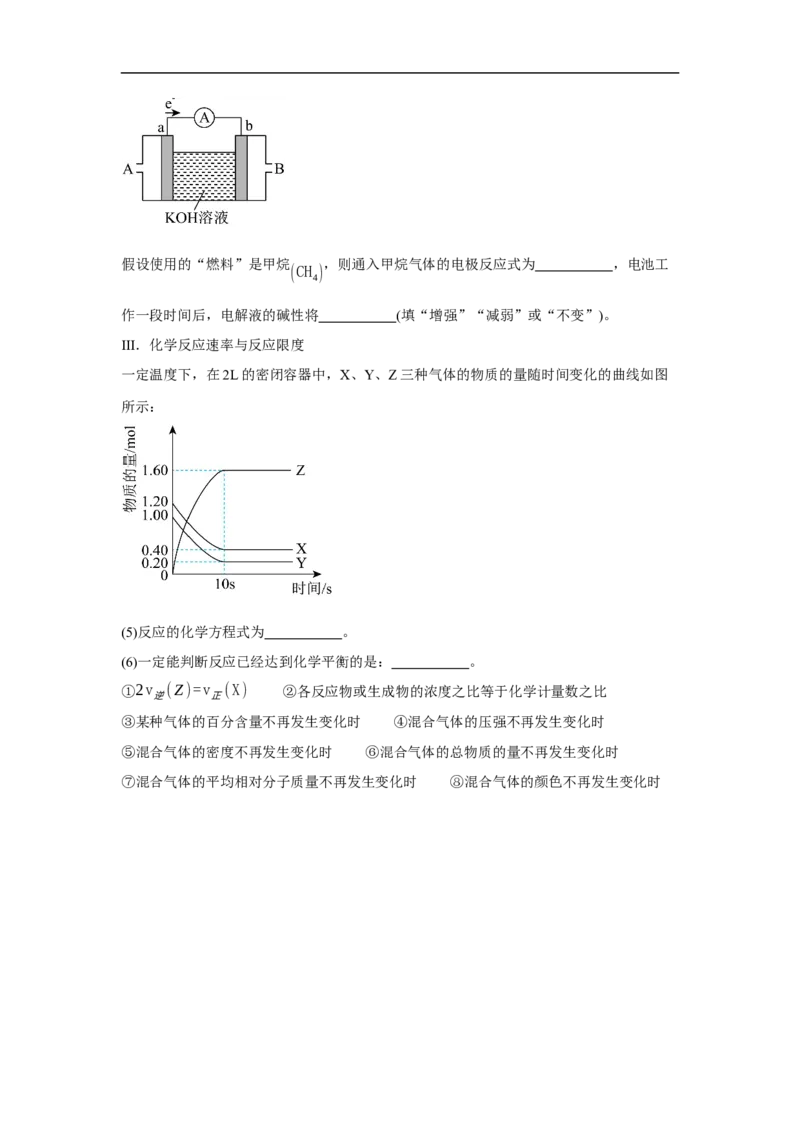
(4)某种燃料电池的工作原理示意图如图所示(a、b均为石墨电极)。
试卷第6页,共7页假设使用的“燃料”是甲烷 ,则通入甲烷气体的电极反应式为 ,电池工
(CH )
4
作一段时间后,电解液的碱性将 (填“增强”“减弱”或“不变”)。
III.化学反应速率与反应限度
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图
所示:
(5)反应的化学方程式为 。
(6)一定能判断反应已经达到化学平衡的是: 。
①2v (Z)=v (X) ②各反应物或生成物的浓度之比等于化学计量数之比
逆 正
③某种气体的百分含量不再发生变化时 ④混合气体的压强不再发生变化时
⑤混合气体的密度不再发生变化时 ⑥混合气体的总物质的量不再发生变化时
⑦混合气体的平均相对分子质量不再发生变化时 ⑧混合气体的颜色不再发生变化时