文档内容
嘉陵一中高 级第三次月考化学试题
2024
(满分:100分 考试时间:75 分钟 命题:谭剑锋)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的
姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 AI 27
第Ⅰ卷 选择题
一、选择题 共15小题,每题只有 1 个选项符合题意(每题4 分,共 60 分)
1.常温下,下列物质在空气中久置后不
.
易
.
变
.
质
.
的是
A. 金属钠 B. 硫酸钾 C. 烧碱 D. 漂白粉
2.近年来,我国航空、航天、航海事业成果显著。下列所涉及的材料不
.
属
.
于
.
金属材料的是
A.“长征五号”运载火箭使用的燃料—液氢
B.“雪龙2号”破冰船的船头材料—钢板
C.“C919”飞机机翼的壁板材料—铝合金
D.“奋斗者号”深潜器的载人球仓材料—钛合金
3.下列物质中,不
.
属
.
于
.
电解质的是
A.Cu B. H SO C. Ca(OH) D. KNO
2 4 2 3
4.下列关于物质分类的说法中,不
.
正
.
确
.
的是
A. 液氯属于纯净物 B. Na CO 属于盐
2 3
C. SO 属于氧化物 D. Fe(OH) 胶体属于碱
2 3
5.下列物质的应用中,与氧化还原反应无
.
关
.
的是
A. 用H 和Cl 制取盐酸 B. 用生石灰(CaO)作干燥剂
2 2
C. 用铝粉和NaOH作管道疏通剂 D. 用Ca(ClO) 漂白棉、麻、纸张
2
6.下列方程式与所给事实不
.
相
.
符
.
的是
1高温
A. 红热的铁与水蒸气发生反应:3Fe+4H O(g) Fe O +4H
2 3 4 2
B. 铁在氯气中燃烧:2Fe+3Cl 2FeCl
2 3
C. 钠放置在空气中表面变暗:2Na+O Na O
2 2 2
D. 用大理石和稀盐酸制取CO :CaCO +2H+ Ca2++CO +H O
2 3 2 2
7. N 为阿伏加德罗常数的值。下列说法正确的是
A
A. CO 的摩尔质量是44g
2
B. 18g H O中含有氢原子的数目为2N
2 A
C. 常温常压下,22.4L Cl 中含有氯分子的数目为N
2 A
D. 0.1 molL-1 NaOH溶液中,含有Na+的数目为0.1N
A
8.下列物质能与水反应生成碱并放出H 的是
2
A. Na O B.Fe C. Cl D.Mg
2 2 2
9.下列电离方程式书写不
.
正
.
确
.
的是
A. HNO H NO B. NaOH Na OH
3 3
C. NH Cl NH Cl D. Ca OH Ca2 OH
4 4 2
10.下列有关物质用途的说法中,不
.
正
.
确
.
的是
A. 漂白粉可用作环境的消毒剂 B. Fe O 用于制作油漆或颜料
2 3
C. 铝制餐具可用来蒸煮碱性食物 D. 碱金属的化合物可用于制烟花
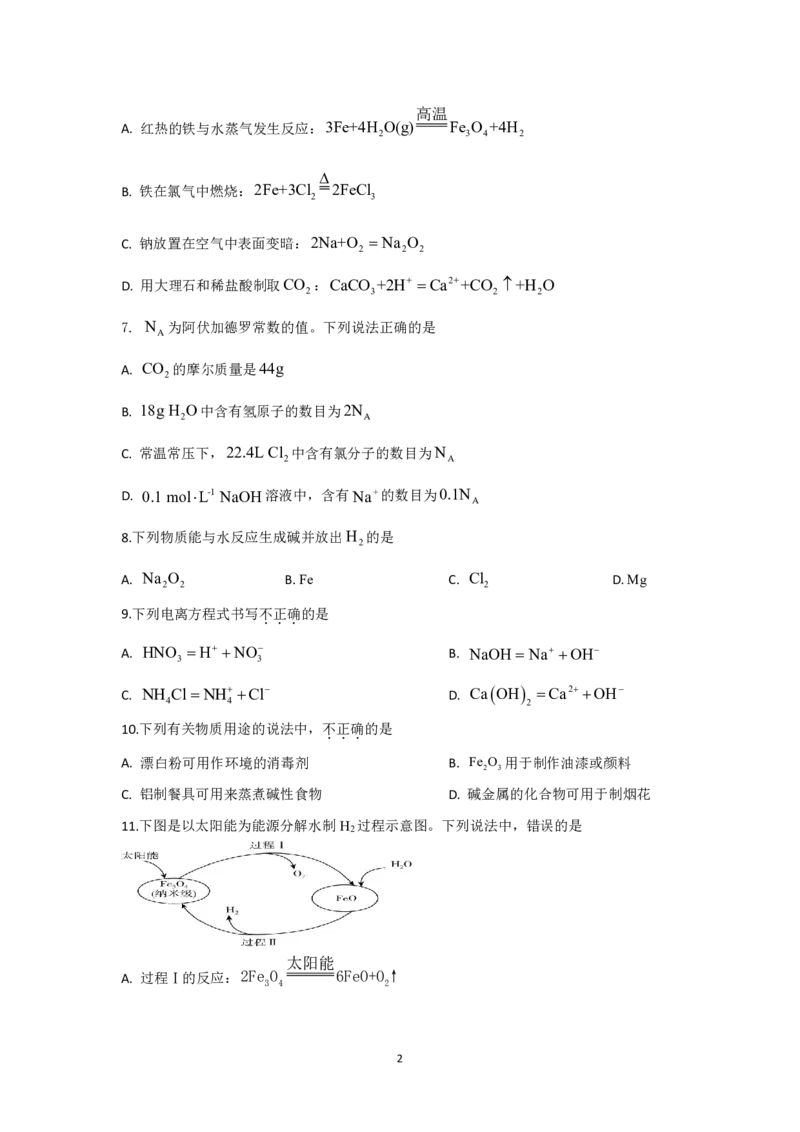
11.下图是以太阳能为能源分解水制H 过程示意图。下列说法中,错误的是
2
太阳能
A.
过程Ⅰ的反应:2Fe O 6FeO+O↑
3 4 2
2太阳能
B.
过程Ⅱ的反应:2H O 2H↑+O↑
2 2 2
C. 两个转化过程都发生了氧化还原反应
D. 纳米级Fe O 在整个过程中起催化作用
3 4
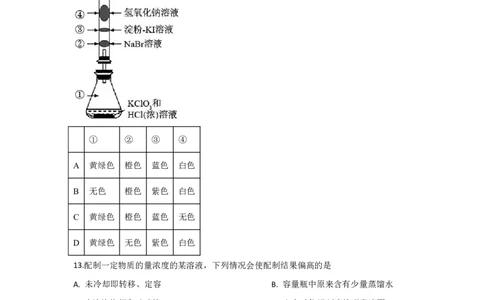
12.已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装
有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是
① ② ③ ④
A 黄绿色 橙色 蓝色 白色
B 无色 橙色 紫色 白色
C 黄绿色 橙色 蓝色 无色
D 黄绿色 无色 紫色 白色
13.配制一定物质的量浓度的某溶液,下列情况会使配制结果偏高的是
A. 未冷却即转移、定容 B. 容量瓶中原来含有少量蒸馏水
C. 未洗涤烧杯和玻璃棒 D. 定容时仰视刻度线观察液面
14.小组同学探究金属钠与KMnO 溶液的反应。
4
①向KMnO 溶液中投入一小块金属钠,溶液颜色略有变浅,继续依次投入五小块金属钠,
4
溶液变为绿色,产生气体。
②向KMnO 溶液中加入少量NaOH固体,溶液颜色无明显变化,继续加入NaOH固体,
4
溶液变为绿色,产生气体。
3已知:Mn2+无色,MnO2-绿色,对比①②,下列有关说法不
.
正
.
确
.
的是
4
A.①中溶液颜色变浅,说明KMnO 发生还原反应
4
B.①中溶液变为绿色,说明MnO- 被钠还原为MnO2-
4 4
C.②中溶液变为绿色,可能发生4MnO-+4OH- 4MnO2-+O +2H O
4 4 2 2
D.②中溶液颜色变化表明,浓度会影响物质还原性的强弱
15.向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。
向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉
淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确
的是
1000b Vc
A.c B.pm
11.2V 125
5
C.n=m+0.017Vc D.p= m
3
第Ⅱ卷 非选择题
二、 填空题(本大题有4题,共40分)
16.(每空2分,共12分)2023年杭州亚运会使用甲醇(CH OH)作为主火炬燃料。
3
点燃
(1)CH OH是一种清洁、可再生燃料,燃烧时发生反应:2CH OH+3O 2CO +4H O。
3 3 2 2 2
在该反应中每消耗1 mol CH OH,生成CO 的物质的量是_______mol,生成H O的质
3 2 2
量是_______g。
(2)CH OH燃烧时,火焰为淡蓝色。在CH OH中添加含_______(填序号)元素的化合物,
3 3
可使火炬的火焰呈黄色。
a.钠 b.钾
(3)CH 3 OH可由废弃的CO 2 制得,其原理为:CO 2 +3H 2 催 化 剂 CH 3 OH+H 2 O
在该反应中,作还原剂的物质是_____,每生成1mol CH OH,转移电子的物质的量是
3
____mol。
(4)一种富集烟气中CO 的方法示意图如下。
2
4写出“解吸”过程的化学方程式:_______。
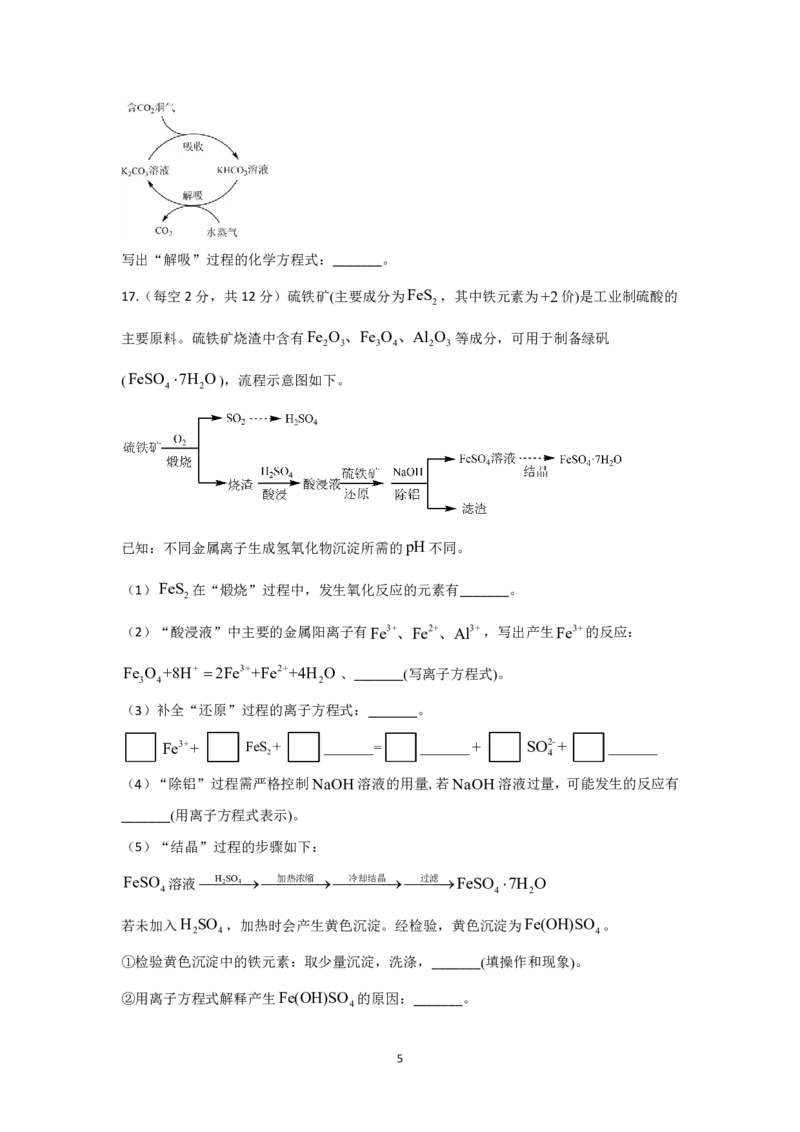
17.(每空2分,共12分)硫铁矿(主要成分为FeS ,其中铁元素为+2价)是工业制硫酸的
2
主要原料。硫铁矿烧渣中含有Fe O 、Fe O 、Al O 等成分,可用于制备绿矾
2 3 3 4 2 3
(FeSO 7H O),流程示意图如下。
4 2
已知:不同金属离子生成氢氧化物沉淀所需的pH不同。
(1)FeS 在“煅烧”过程中,发生氧化反应的元素有_______。
2
(2)“酸浸液”中主要的金属阳离子有Fe3+、Fe2+、Al3+,写出产生Fe3+的反应:
Fe O +8H+ 2Fe3++Fe2++4H O 、_______(写离子方程式)。
3 4 2
(3)补全“还原”过程的离子方程式:_______。
Fe3++ FeS + _______= _______+ SO2-+ _______
2 4
(4)“除铝”过程需严格控制NaOH溶液的用量,若NaOH溶液过量,可能发生的反应有
_______(用离子方程式表示)。
(5)“结晶”过程的步骤如下:
FeSO 溶液H2 SO4加热浓缩冷却结晶过滤FeSO 7H O
4 4 2
若未加入H SO ,加热时会产生黄色沉淀。经检验,黄色沉淀为Fe(OH)SO 。
2 4 4
①检验黄色沉淀中的铁元素:取少量沉淀,洗涤,_______(填操作和现象)。
②用离子方程式解释产生Fe(OH)SO 的原因:_______。
4
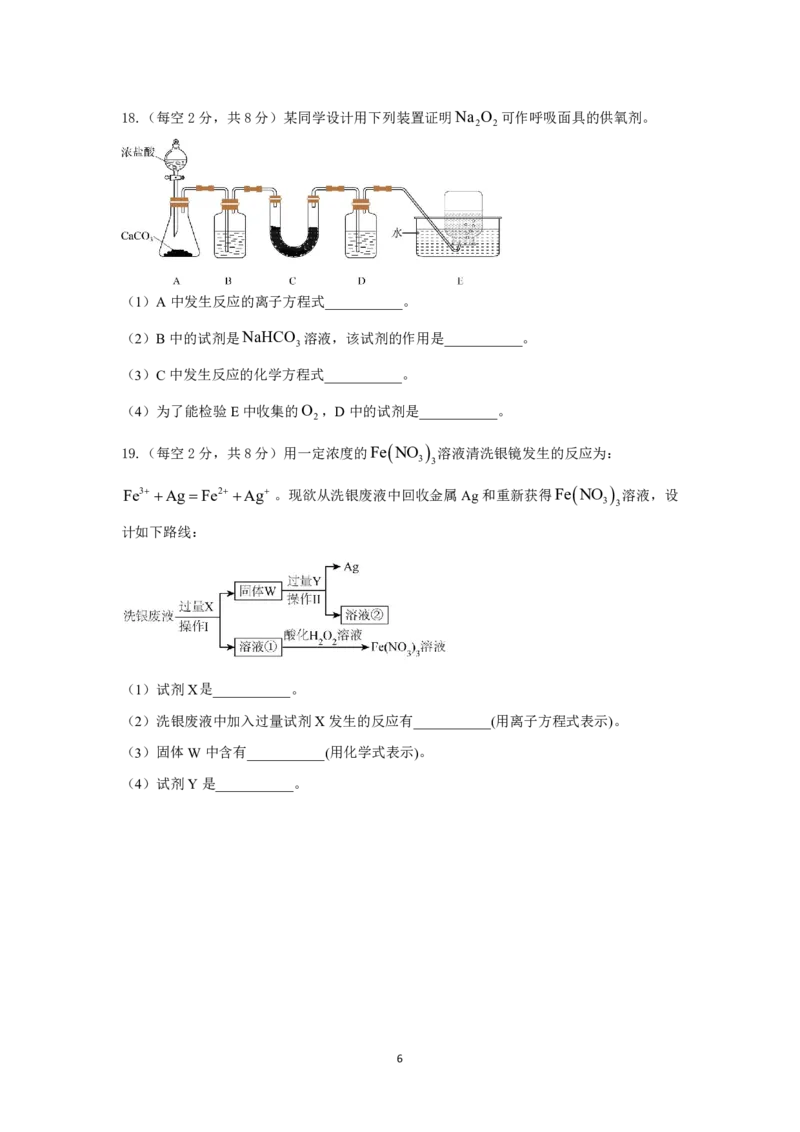
518.(每空2分,共8分)某同学设计用下列装置证明Na O 可作呼吸面具的供氧剂。
2 2
(1)A中发生反应的离子方程式___________。
(2)B中的试剂是NaHCO 溶液,该试剂的作用是___________。
3
(3)C中发生反应的化学方程式___________。
(4)为了能检验E中收集的O ,D中的试剂是___________。
2
19.(每空2分,共8分)用一定浓度的Fe NO 溶液清洗银镜发生的反应为:
3 3
Fe3 Ag Fe2 Ag 。现欲从洗银废液中回收金属Ag和重新获得Fe NO 溶液,设
3 3
计如下路线:
(1)试剂X是___________。
(2)洗银废液中加入过量试剂X发生的反应有___________(用离子方程式表示)。
(3)固体W中含有___________(用化学式表示)。
(4)试剂Y是___________。
67