文档内容
射洪中学高 2024 级高一下期半期考试
化学试题
(考试时间:75分钟 满分:100分)
注意事项:
1.答卷前,考生务必将自己的班级、姓名、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡对应题号的位置上。写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子质量:H-1 N-14
第 I 卷(选择题)
一、单选题(每题3分,共45分)
1.化学与生产、生活密切相关,下列说法不正确的是( )
A.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
B.某地区雨水的pH值为6,可以判定该雨水为酸雨
C.北斗系统组网成功,其芯片的主要成分为硅
D.葡萄酒中通常添加少量SO ,既可以杀菌,又可防止营养成分被氧化
2
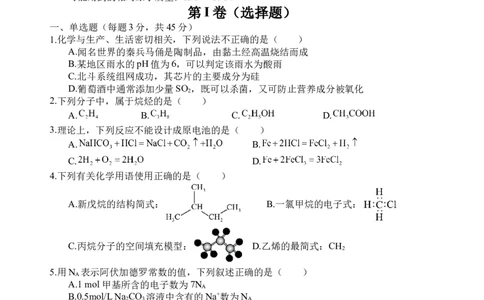
2.下列分子中,属于烷烃的是( )
A. B. C. D.
3.理论上,下列反应不能设计成原电池的是( )
A. B.
C. D.
4.下列有关化学用语使用正确的是( )
A.新戊烷的结构简式: B.一氯甲烷的电子式:
C.丙烷分子的空间填充模型: D.乙烯的最简式:CH
2
5.用N 表示阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1 mol甲基所含的电子数为7N
A
B.0.5mol/L Na CO 溶液中含有的Na+数为N
2 3 A
C.标准状况下,11.2 L CH Cl 含共价键数目为2N
2 2 A
D.3.4g NH 中含有的氢原子数为0.6 N
3 A
6.宏观辨识与微观探析是化学学科核心素养之一。下列离子方程式书写正确的是( )
A.用足量的氨水溶液吸收 尾气:
B.实验室用氯化铵和熟石灰共热制氨气:
C. 气体通入氯水中:
D.甲烷与溴蒸汽在光照条件下反应生成二溴甲烷:
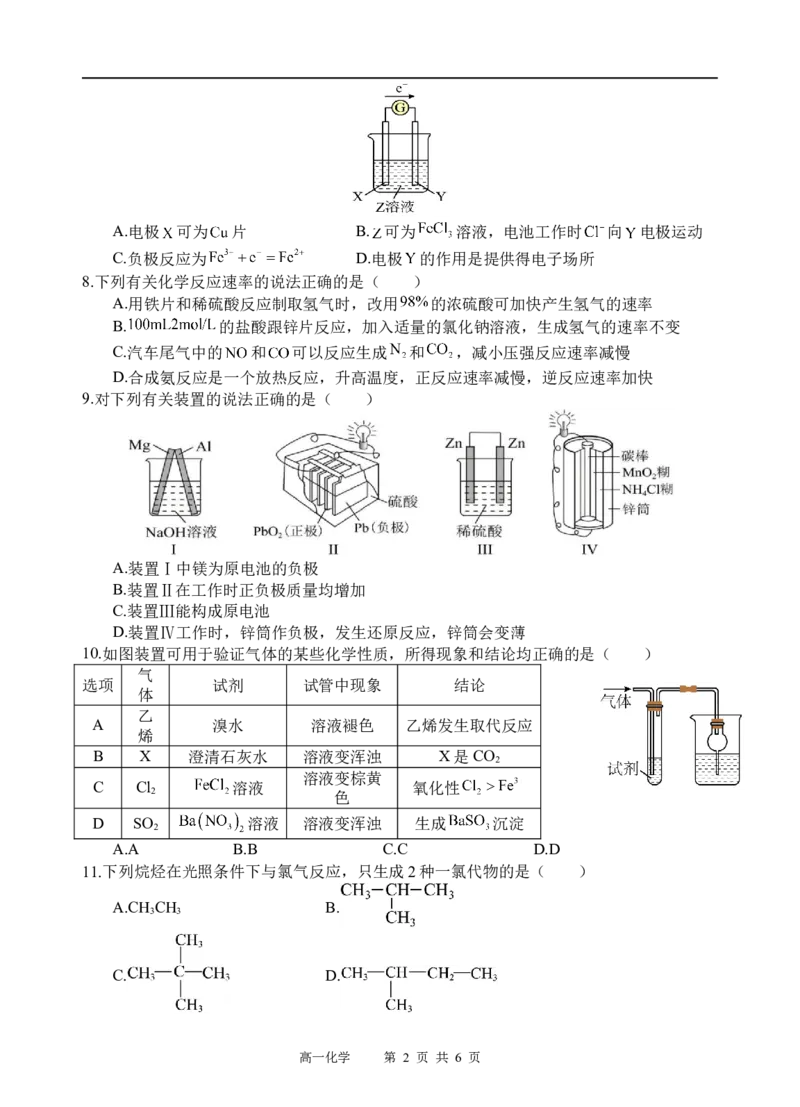
7.如图所示原电池装置的总反应为 ,电池工作时灵敏电流计的指针向右偏
转。下列说法正确的是( )
高一化学 第 1 页 共 6 页A.电极 可为 片 B. 可为 溶液,电池工作时 向 电极运动
C.负极反应为 D.电极 的作用是提供得电子场所
8.下列有关化学反应速率的说法正确的是( )
A.用铁片和稀硫酸反应制取氢气时,改用 的浓硫酸可加快产生氢气的速率
B. 的盐酸跟锌片反应,加入适量的氯化钠溶液,生成氢气的速率不变
C.汽车尾气中的 和 可以反应生成 和 ,减小压强反应速率减慢
D.合成氨反应是一个放热反应,升高温度,正反应速率减慢,逆反应速率加快
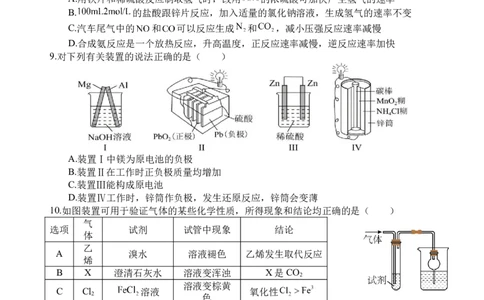
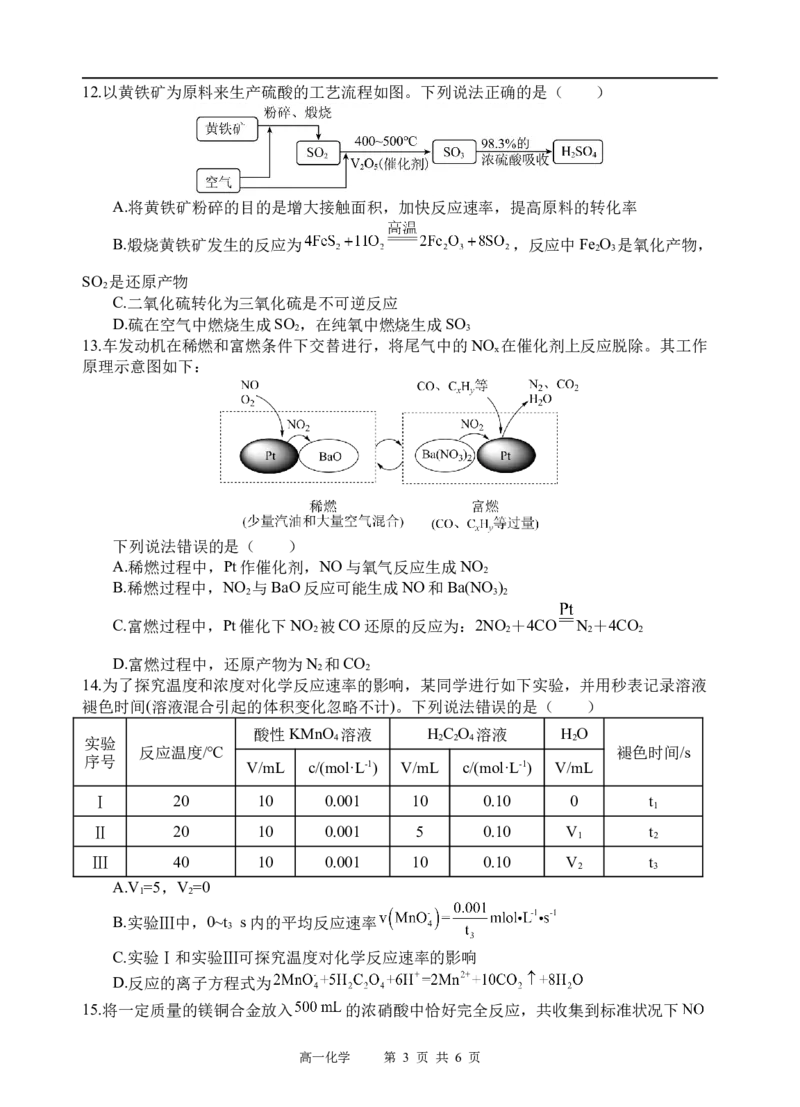
9.对下列有关装置的说法正确的是( )
A.装置Ⅰ中镁为原电池的负极
B.装置Ⅱ在工作时正负极质量均增加
C.装置Ⅲ能构成原电池
D.装置Ⅳ工作时,锌筒作负极,发生还原反应,锌筒会变薄
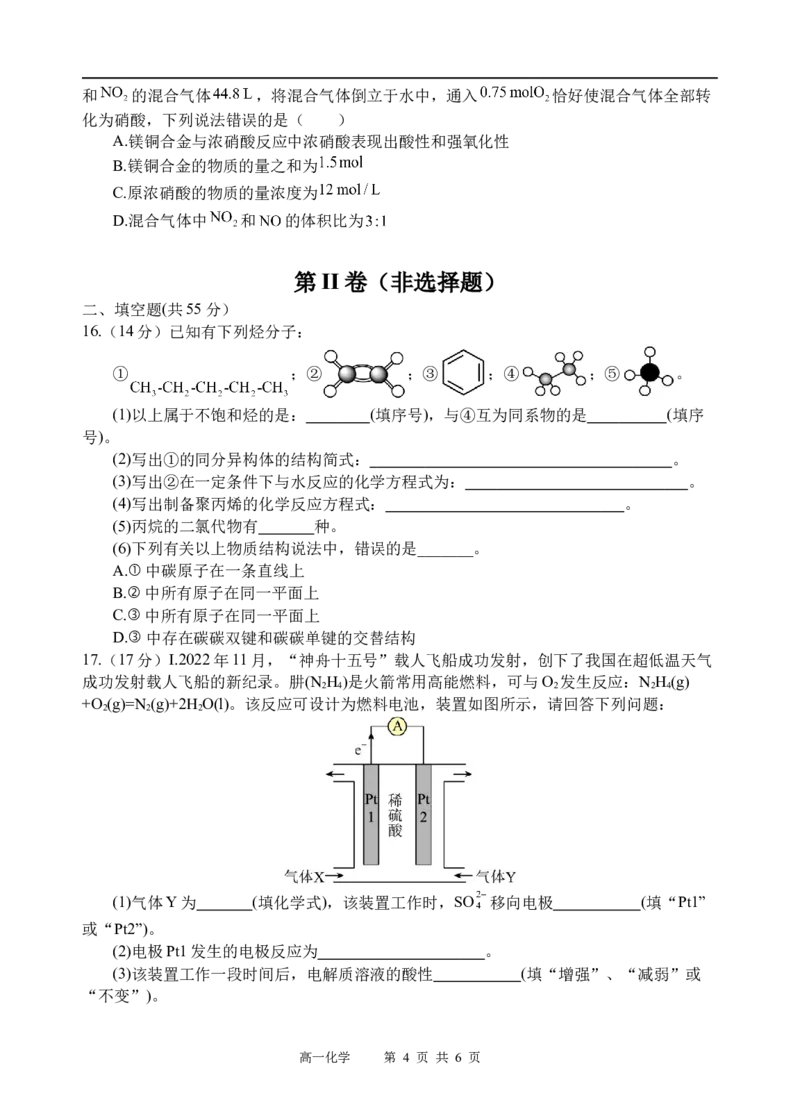
10.如图装置可用于验证气体的某些化学性质,所得现象和结论均正确的是( )
气
选项 试剂 试管中现象 结论
体
乙
A 溴水 溶液褪色 乙烯发生取代反应
烯
B X 澄清石灰水 溶液变浑浊 X是CO
2
溶液变棕黄
C Cl 溶液 氧化性
2 色
D SO 溶液 溶液变浑浊 生成 沉淀
2
A.A B.B C.C D.D
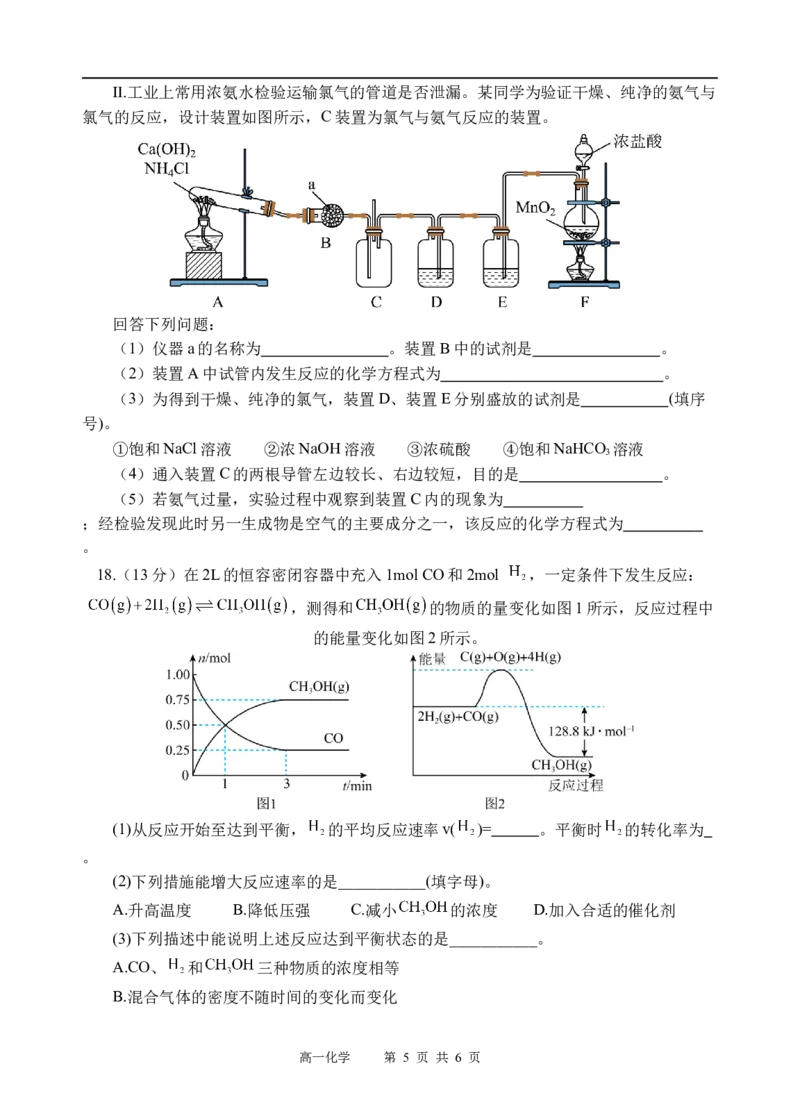
11.下列烷烃在光照条件下与氯气反应,只生成2种一氯代物的是( )
A.CH CH B.
3 3
C. D.
高一化学 第 2 页 共 6 页12.以黄铁矿为原料来生产硫酸的工艺流程如图。下列说法正确的是( )
A.将黄铁矿粉碎的目的是增大接触面积,加快反应速率,提高原料的转化率
B.煅烧黄铁矿发生的反应为 ,反应中Fe O 是氧化产物,
2 3
SO 是还原产物
2
C.二氧化硫转化为三氧化硫是不可逆反应
D.硫在空气中燃烧生成SO ,在纯氧中燃烧生成SO
2 3
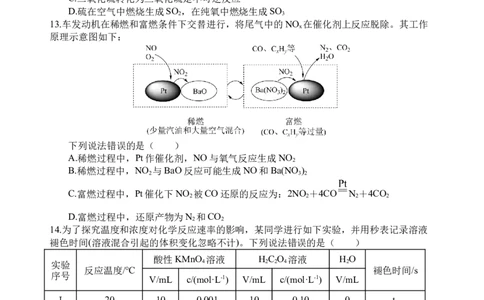
13.车发动机在稀燃和富燃条件下交替进行,将尾气中的NO 在催化剂上反应脱除。其工作
x
原理示意图如下:
下列说法错误的是( )
A.稀燃过程中,Pt作催化剂,NO与氧气反应生成NO
2
B.稀燃过程中,NO 与BaO反应可能生成NO和Ba(NO )
2 3 2
C.富燃过程中,Pt催化下NO 被CO还原的反应为:2NO +4CO N +4CO
2 2 2 2
D.富燃过程中,还原产物为N 和CO
2 2
14.为了探究温度和浓度对化学反应速率的影响,某同学进行如下实验,并用秒表记录溶液
褪色时间(溶液混合引起的体积变化忽略不计)。下列说法错误的是( )
酸性KMnO 溶液 H C O 溶液 H O
实验 4 2 2 4 2
反应温度/℃ 褪色时间/s
序号
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
Ⅰ 20 10 0.001 10 0.10 0 t
1
Ⅱ 20 10 0.001 5 0.10 V t
1 2
Ⅲ 40 10 0.001 10 0.10 V t
2 3
A.V =5,V =0
1 2
B.实验Ⅲ中,0~t s内的平均反应速率
3
C.实验Ⅰ和实验Ⅲ可探究温度对化学反应速率的影响
D.反应的离子方程式为
15.将一定质量的镁铜合金放入 的浓硝酸中恰好完全反应,共收集到标准状况下
高一化学 第 3 页 共 6 页和 的混合气体 ,将混合气体倒立于水中,通入 恰好使混合气体全部转
化为硝酸,下列说法错误的是( )
A.镁铜合金与浓硝酸反应中浓硝酸表现出酸性和强氧化性
B.镁铜合金的物质的量之和为
C.原浓硝酸的物质的量浓度为
D.混合气体中 和 的体积比为
第 II 卷(非选择题)
二、填空题(共55分)
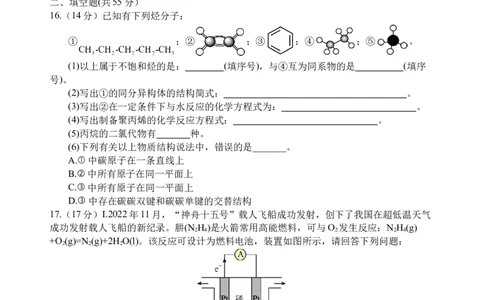
16.(14分)已知有下列烃分子:
① ;② ;③ ;④ ;⑤ 。
(1)以上属于不饱和烃的是: (填序号),与④互为同系物的是 (填序
号)。
(2)写出①的同分异构体的结构简式: 。
(3)写出②在一定条件下与水反应的化学方程式为: 。
(4)写出制备聚丙烯的化学反应方程式: 。
(5)丙烷的二氯代物有 种。
(6)下列有关以上物质结构说法中,错误的是_______。
A.①中碳原子在一条直线上
B.②中所有原子在同一平面上
C.③中所有原子在同一平面上
D.③中存在碳碳双键和碳碳单键的交替结构
17.(17分)I.2022年11月,“神舟十五号”载人飞船成功发射,创下了我国在超低温天气
成功发射载人飞船的新纪录。肼(N H )是火箭常用高能燃料,可与O 发生反应:N H (g)
2 4 2 2 4
+O (g)=N (g)+2H O(l)。该反应可设计为燃料电池,装置如图所示,请回答下列问题:
2 2 2
(1)气体Y为 (填化学式),该装置工作时,SO 移向电极 (填“Pt1”
或“Pt2”)。
(2)电极Pt1发生的电极反应为 。
(3)该装置工作一段时间后,电解质溶液的酸性 (填“增强”、“减弱”或
“不变”)。
高一化学 第 4 页 共 6 页Ⅱ.工业上常用浓氨水检验运输氯气的管道是否泄漏。某同学为验证干燥、纯净的氨气与
氯气的反应,设计装置如图所示,C装置为氯气与氨气反应的装置。
回答下列问题:
(1)仪器a的名称为 。装置B中的试剂是 。
(2)装置A中试管内发生反应的化学方程式为 。
(3)为得到干燥、纯净的氯气,装置D、装置E分别盛放的试剂是 (填序
号)。
①饱和NaCl溶液 ②浓NaOH溶液 ③浓硫酸 ④饱和NaHCO 溶液
3
(4)通入装置C的两根导管左边较长、右边较短,目的是 。
(5)若氨气过量,实验过程中观察到装置C内的现象为
;经检验发现此时另一生成物是空气的主要成分之一,该反应的化学方程式为
。
18.(13分)在2L的恒容密闭容器中充入1mol CO和2mol ,一定条件下发生反应:
,测得和 的物质的量变化如图1所示,反应过程中
的能量变化如图2所示。
(1)从反应开始至达到平衡, 的平均反应速率v( )= 。平衡时 的转化率为
。
(2)下列措施能增大反应速率的是___________(填字母)。
A.升高温度 B.降低压强 C.减小 的浓度 D.加入合适的催化剂
(3)下列描述中能说明上述反应达到平衡状态的是___________。
A.CO、 和 三种物质的浓度相等
B.混合气体的密度不随时间的变化而变化
高一化学 第 5 页 共 6 页C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2mol 的同时生成1mol
(4)该反应是 反应(填“吸热”或“放热”),已知断开1mol CO(g)和2mol
中的化学键需要吸收的能量为1924kJ,则断开1mol 中的化学键所需要吸
收 kJ的能量。
(5)汽车尾气(含有烃类、CO、 、NO等物质)治理的方法之一是在汽车的排气管上装
一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为
。
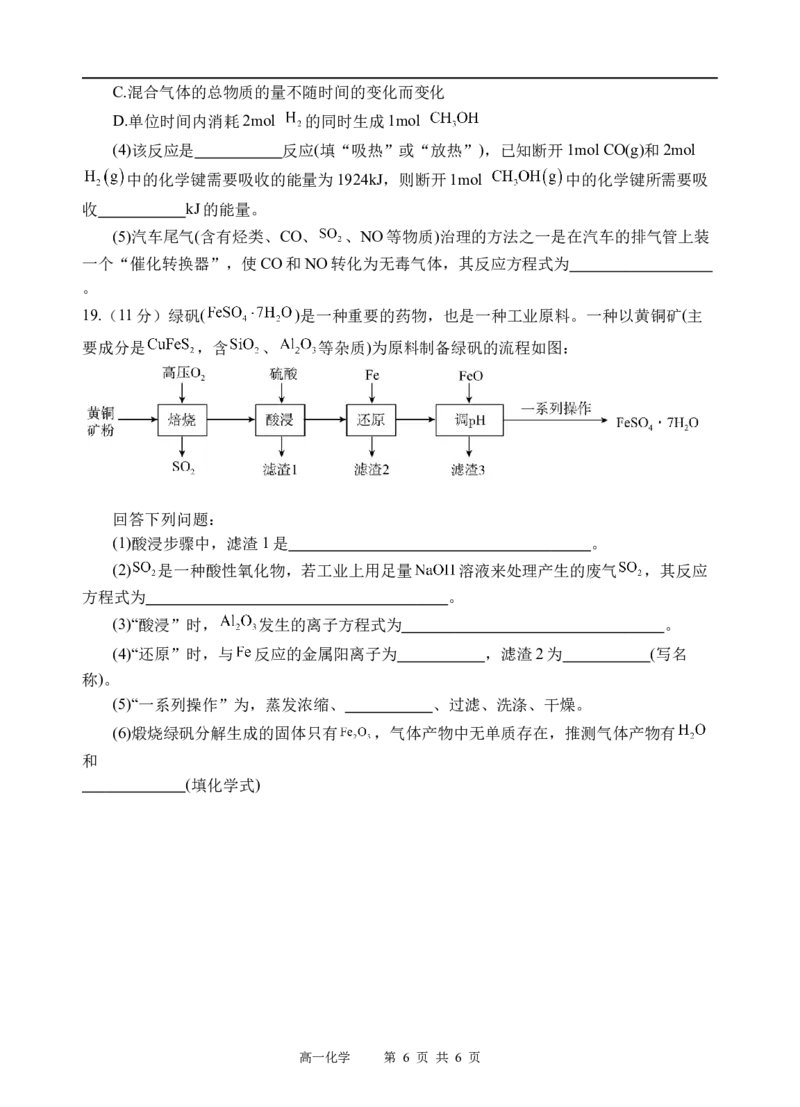
19.(11分)绿矾( )是一种重要的药物,也是一种工业原料。一种以黄铜矿(主
要成分是 ,含 、 等杂质)为原料制备绿矾的流程如图:
回答下列问题:
(1)酸浸步骤中,滤渣1是 。
(2) 是一种酸性氧化物,若工业上用足量 溶液来处理产生的废气 ,其反应
方程式为 。
(3)“酸浸”时, 发生的离子方程式为 。
(4)“还原”时,与 反应的金属阳离子为 ,滤渣2为 (写名
称)。
(5)“一系列操作”为,蒸发浓缩、 、过滤、洗涤、干燥。
(6)煅烧绿矾分解生成的固体只有 ,气体产物中无单质存在,推测气体产物有
和
(填化学式)
高一化学 第 6 页 共 6 页