文档内容
6.下列有关实验操作、现象和结论都正确的是
南充高中高 2024 级第二学期第二次月考
选项 操作和现象 结论
化 学 试 题
过量的Fe粉中加入稀HNO ,充分反应后,再滴入KSCN溶液,溶 稀HNO 将Fe氧化
3 3
A
液呈红色 为Fe3+
(时间:75分钟 总分:100 分)
命、审题人:江万涛、胡雪玫、李建忠 B 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色 浓氨水呈碱性
可能用到的相对原子质量: H1 C12 N14 O16 Mg24 Cu64 C 向Ba(NO ) 溶液中通入SO 气体,产生白色沉淀 沉淀一定为BaSO
3 2 2 3
向2mL0.1mol/L的FeCl 溶液中加入1mL0.1mol/L的KI溶液,充 Fe3+与I−的反应有
3
第Ⅰ卷(选择题,共45分) D
分反应后,再滴入KSCN溶液,溶液变红 一定限度
一、选择题(本题共15小题,每小题只有一个选项符合题意) 7.下列反应的离子方程式正确的是
1.化学与生产生活密切相关。下列叙述错误的是 A.碘化亚铁溶液与等物质的量的氯气:2Fe2++2I-+2Cl 2Fe3++I +4Cl-
2 2
A.华为“麒麟980”芯片的主要成分是硅
B.向硫化钠溶液通入足量二氧化硫:S2-+2SO +2H OH S+2HSO-
B.酸雨是pH<5.6的雨水,主要是氮、硫的氧化物大量排放引起的 2 2 2 3
C.工业生产的玻璃和水泥,均需用石灰石作原料 C.向次氯酸钙溶液通入足量二氧化碳:ClO-+CO
2
+H
2
OHClO+HCO-
3
D.石墨烯和制医用口罩的聚丙烯纤维都是有机高分子材料 D.铜与稀硝酸:Cu+4H++2NO- Cu2++2NO +2H O
3 2 2
2.下列化学用语表达正确的是 8.纸电池是未来电池发展的一个重要研究方向。某研究小组利
用铜片和镁片、硫酸铜溶液、隔离膜制作的简易纸电池如图
A.甲基的电子式: 所示,下列说法正确的是
A.b的电极反应为Cu2++2e−=Cu
B.电极a的电势比电极b高
B.CH 4 分子的空间填充模型: C.a电极表面产生气泡
D.Cu2+向b电极迁移
C.乙烯的结构简式:CH CH
2 2
9.下列各图所示实验设计能达到相应实验目的的是
D. 的键线式:
3.下列说法正确的是
A.简单氢化物的稳定性:CH >NH >H O
4 3 2
B.一氯代物的种类:正戊烷>异戊烷>新戊烷
C.沸点:正丁烷>异丁烷>丙烷
D.羟基氢原子的活泼性:CH COOH>CH CH OH>H O
3 3 2 2
① ② ③ ④
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.14g乙烯和丁烯的混合气体中所含原子总数为3N A.用图①制备并收集乙酸乙酯
A
B.一定条件下2molSO 和1molO 充分反应,转移的电子数为4N B.用图②验证Cl、Br、I非金属性的强弱
2 2 A
C.46g组成为C H O的有机物,C-H键数目一定为5N C.用图③验证非金属性:NCSi
2 6 A
D.100mL0.1mol/L的乙酸溶液中所含H+总数为0.01N D.用图④除去甲烷中的乙烯
A
5.下列除去杂质的方法中,正确的是 10.向某容积一定的密闭绝热容器中充入2molNO和1molO
2
,一定条件
选项 物质(括号内为杂质) 去除杂质的方法 下发生反应:2NO(g)O
2
(g)2NO
2
(g)(忽略其余反应),其反应速
率与反应时间关系如下图所示,下列说法正确的是
A 粗盐(MgCl ) 加入适量的KOH溶液、过滤
2
A.该反应为吸热反应
B CO (SO ) 饱和Na CO 溶液、洗气
2 2 2 3 B.N点时,反应已达平衡状态
C NH 3 (H 2 O) 无水CaCl 2 、干燥 C.点M到点N过程中,速率增大的主要原因是反应放热使温度升高
D 乙酸乙酯(乙酸) 饱和Na CO 溶液、分液 D.M→N→P的过程中,NO的浓度先增大后减小
2 3
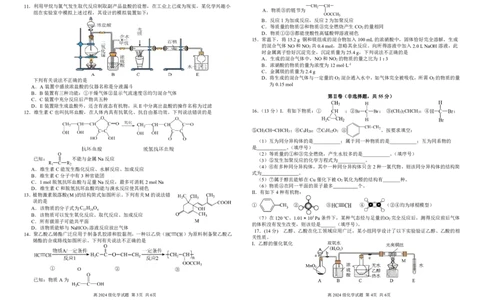
高2024级化学试题 第1页 共6页 高2024级化学试题 第2页 共6页11.利用甲烷与氯气发生取代反应制取副产品盐酸的设想,在工业上已成为现实。某化学兴趣小
A.物质③的链节为
组在实验室中模拟上述过程,其设计的模拟装置如下:
B.反应1为加成反应,反应2为加聚反应
C.等质量的物质②和物质③完全燃烧产生CO 的量相同
2
D.物质①②③都能使酸性高锰酸钾溶液褪色
15.常温下,将15.2g 铜和镁组成的混合物加入100mL的浓硝酸中,固体恰好完全溶解,生成
的混合气体NO和NO 共0.4mol,忽略其余反应。向所得溶液中加入2.0LNaOH溶液,此
2
时金属离子恰好沉淀完全,沉淀质量为25.4g,下列说法不正确的是
A.生成的混合气体中,NO和NO
2
的物质的量之比为1:3
B.浓硝酸的物质的量为浓度为12mol·L-1
C.金属镁的质量为2.4g
D.将生成的混合气体与一定量的O 混合通入水中,如气体完全被吸收,所需O 的物质的量
下列有关说法不正确的是 2 2
为 0.15mol
A.A装置中盛放浓盐酸的仪器名称是分液漏斗
B.B装置有三种功能:①干燥气体②显示气流速度③均匀混合气体
第Ⅱ卷(非选择题,共55分)
C.C装置中充分反应后产物共五种
D.E装置除生成盐酸外,还含有液态有机物,从E中分离出盐酸的操作名称为过滤
12.维生素C也叫抗坏血酸,在人体内具有抗氧化、抗自由基功效。下列说法错误的是 16.(13分)Ⅰ.有如下物质:① ;② ; ③(CH 3 ) 2 CHCH 3 ;④ ;
⑤CH CH=CHCH ;⑥C H ;⑦C H O;⑧ 。按要求填空:
3 3 9 20 5 12
(1)互为同分异构体的是___________;属于同一种物质的是___________;互为同系物的
是 。(填序号)
(2)等质量的①和③完全燃烧,产生水较多的是___________。(填序号)
已知: 不能与金属Na反应
(3)⑤发生加聚反应的化学方程式为___________。
(4)⑥有多种同分异构体,其中一种同分异构体只含2种一氯代物,则该同分异构体的结构简
A.维生素C能发生酯化反应、水解反应、加成反应
式为 。
B.维生素C分子中有3种官能团
(5)⑦属于醇且能够在Cu催化下被O 氧化为醛的结构有 种。
C.1mol脱氢抗坏血酸与足量Na反应,最多可消耗2molNa 2
(6)物质⑧在同一平面的原子最多 个。
D.维生素C和脱氢抗坏血酸均能与溴水反应使其褪色
Ⅱ.有如下4种有机物:
13.植物激素脱落酸(M)的结构简式如图所示。下列有关M的说法错
误的是
① ② ③ ④ (②④均为球棍模型)
A.该物质的分子式为C H O
15 20 4
B.该物质可以发生氧化反应、取代反应、加成反应
(7)在120℃、1.01×105Pa条件下,某种气态烃与足量的O 完全反应后,测得反应前后气体
C.所有碳原子可能共平面 2
的体积没有发生改变,则该烃是______(填序号)。
D.该物质能够与NaHCO 溶液反应放出气体
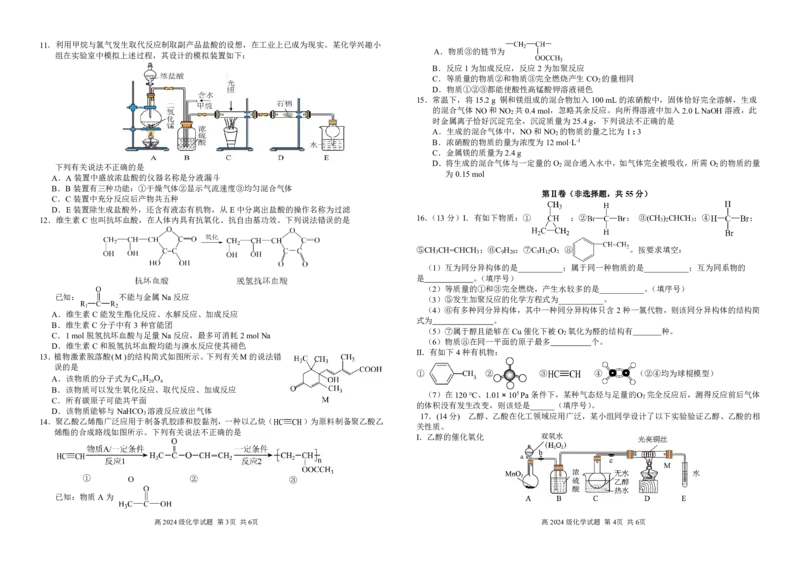
3 17.(14分) 乙醇、乙酸在化工领域应用广泛,某小组同学设计了以下实验验证乙醇、乙酸的相
14.聚乙酸乙烯酯广泛应用于制备乳胶漆和胶黏剂,一种以乙炔( )为原料制备聚乙酸乙
关性质。
烯酯的合成路线如图所示。下列有关说法不正确的是
Ⅰ.乙醇的催化氧化
① O ② ③
已知:物质A为
高2024级化学试题 第3页 共6页 高2024级化学试题 第4页 共6页(1)盛装MnO 的仪器名称为 ,A中发生的反应方程式为 。 实验编 NO 初始浓度/ CO初始浓度/ 催化剂的比表面积
2
T/C
(2)C中热水的作用是 。 号 (molL-1) (molL-1) (m2g-1)
(3)装入实验药品后,打开活塞a、b、c,在铜丝的中间部分加热,通过控制活塞a和b,间歇 a 280 1.2010-3 5.8010-3 82
性地通入氧气,可在D装置中硬质玻璃管处观察到铜丝的实验现象是 。 b 280 1.2010-3 5.8010-3 124
(4)将制得的乙醛溶液加入溴水中,溴水褪色。其原因是溴水能够将乙醛氧化为乙酸,试写出该 c 350 x 5.8010-3 82
请回答:
反应的化学方程式 。
①表中x=___________;
Ⅱ.乙酸的酯化
②此实验验证的影响因素除了催化剂的比表面积,还有___________,
在甲试管中加入无水乙醇,边振荡试管边慢慢加入浓硫酸和乙
能证明该因素对反应速率的影响规律的实验编号为__________。
酸,再加入几片碎瓷片。按右图连接好装置,用酒精灯小心加 (4)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原
热,将产生的蒸气经导管通到饱和Na 2 CO 3 溶液的液面上。 理如图所示,其总反应式为:2CH 3 OH+3O 2 +4OH−=2CO 3 2−+6H 2 O,
(5)为了探究甲试管中反应的历程,采用同位素示踪法,选 则电极A的反应式为 。
用了由18O组成的无水乙醇(CH CH 18OH)参与反应,则该
3 2 19.(15分)异丁酸乙酯( )主要用于配制奶油及草莓,樱桃等水果型香精,
反应的化学方程式为 。
它的一种工业合成流程如下图所示:
(6)乙试管中观察到的现象为 。
(7)饱和碳酸钠溶液的主要作用是___________(填字母)。
a.中和乙酸 b.溶解乙醇
c.降低乙酸乙酯在水中的溶解度 d.便于乙酸乙酯与溶液的分层
(8)如果用4.8g乙醇(CH CH 18OH)和3.0g乙酸在催化剂条件下发生上述反应,充分反应后,
3 2
实际产量
若产率为70%,则实际制得乙酸乙酯的质量是 g。 实(际产率= ×1000 )
理论产量 0
18.(13分)工业生产通常需要考虑能耗、速率、限度、环境保护、经济效益等多方面因素。请
回答:
(1)己知断裂1mol化学键需要的能量如下表所示:
化学键 H—H N—H N N
能量/kJ 436 391 946
工业合成氨,若生成2molNH
3
,则放出 kJ热量。 已知:R—Cl+NaOH水R—OH+NaCl。
△
(2)消除污染物NO,可在一定条件下用CO和NO发生反应2CO(g)+2NO(g) N (g)+2CO (g), 请回答下列问题:
2 2
在恒容密闭容器中充入4molCO和4molNO发生反应,回答下列问题: (1)Ⅰ的结构简式为 ,反应④属于 反应。
①为了提高反应的速率,下列措施可行的是___________。 (2)II的官能团名称为 。
A.升高温度 B.使用催化剂 C.充入氦气 D.移除CO (3)③反应的化学方程式是 。
2
②若恒容容器的体积为2L,2min后n(N )=0.8mol,则此段时间内v(NO)=________,CO的转化
(4)Ⅲ和Ⅶ在浓硫酸作用下加热也可生成酯,则该反应的化学方程式为 ,浓硫酸的作
2
用为 。
率为 。
(5)下列关于有机物VII的说法中,正确的是 (填标号)。
③下列事实能够说明该反应达到化学平衡状态的是___________(填字母)。
a.既能与Na反应,又能与NaOH反应 b.能发生取代、加成反应
A.2v 正 (CO)=v 逆 (N 2 ) c.与乙酸互为同系物 d.属于不饱和烃
B.断开1个N N键同时形成2个CO 2 分子 (6)已知:碳原子数相同的羧酸和酯互为同分异构体。同时符合下列条件的物质Ⅷ的同分异构
C.NO和CO的物质的量之比为1:1 体有 种,任写出一种同分异构体的结构简式 。
D.混合气体的平均相对分子质量不再变化 ①能与NaHCO
3
反应生成CO
2
(3)已知增大催化剂的比表面积可提高反应2CO(g)+2NO(g) N (g)+2CO (g)的速率。为了验 ②含有两个—CH 3
2 2
证某些因素对上述化学反应速率的影响规律,某同学设计了三组实验,如表所示:
高2024级化学试题 第5页 共6页 高2024级化学试题 第6页 共6页