文档内容
可能用到的相对原子质量:
A.从 到 , 为
H-1、C-12、N-14、O-16、Ne—20 Na-23、Mg-24、Al-27、S-32、Cl-35.5、K-39、Ca-
40、Mn-55、Fe-56、Cu-64、Zn-65、Ag-108、Ba-137 B.若混合气体密度不变时,该反应达平衡状态
1.化学与生活、科技、信息等有着密切的关系,下列说法正确的是
C.平衡时向容器中充入 ,反应速率不变
A.太空实验室的硅电池板将太阳能直接转换为电能
D. 时,反应处于平衡状态
B.宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
5.X、Y、Z、W是原子序数依次增大的4种短周期元素,X是不含中子的元素,Y的单质是空气中含量最多的
C.“火树银花合,星桥铁锁开”中涉及的焰色反应是化学变化
成分,Z的最外层电子数是X和Y最外层电子数之和,W的原子半径是短周期主族元素中最大的。下列说法错
D.碳纳米材料是一类有机高分子材料,主要包括富勒烯、碳纳米管等
误的是
2.反应Cl+H O=HCl+ HClO 生成的HClO具有杀菌消毒的作用。下列化学用语的表达正确的是
2 2 A.由X、Z、W三种元素形成的化合物中含有离子键和共价键
A.HClO 的电子式:
B.X和Y形成的化合物YX 中各原子均达8电子稳定结构
3
C.Y、Z、W形成的简单离子半径大小顺序为Y>Z>W
B.原子结构示意图 可表示 Cl-,也可表示 Cl-
D.元素Z的气态氢化物热稳定性比Y的强
6.一定温度下,在恒容密闭容器中进行可逆反应 ,下列可以作为反应到达化学平衡状
C.用电子式表示HCl的形成过程: 态标志的有
①单位时间内生成1mol 的同时生成1mol
D.水分子结构模型:
②1molH-H键断裂的同时有2molH-I键断裂
③密闭容器中混合气体密度不再变化
3.反应 在不同条件下化学反应速率,其中反应最快的是
④密闭容器中混合气体的平均相对分子质量不再变化
A. B. ⑤用HI、 、 的物质的量浓度变化表示的化学反应速率之比为2:1:1的状态
C. D. ⑥ 的浓度不再随时间发生变化
⑦密闭容器中混合气体的颜色不再变化
4.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。 可转化成有机物实现碳 A.3个 B.4个 C.5个 D.6个
7.下列实验的操作、现象和所得结论都正确的是
实验操作 现象 实验结论
循环。在体积为1L的密闭容器中,充入 和 ,一定条件下反应:
红热的铁与水蒸气反应后的固体物
固体物质中不
A 质,用稀硫酸溶解,滴入几滴KSCN 未显红色
含+3价铁元素
溶液
,测得 和 的浓度随时间变化如下图所示。下列说法不
向某溶液先滴加硝酸酸化,再滴加 原溶液中一定
B 出现白色沉淀
溶液 含有
正确的是
将纯Al片与纯Mg片用导线连接,浸 Al片表面产生大量气 金属性:
C
入到氢氧化钠溶液中 泡 Mg>Al
滴加 溶液时,
D 某溶液中先滴加 溶液,再加足 出现白色沉淀,再加足 溶液中含有Cl-
量稀HNO 量稀HNO,沉淀不溶
3 3
解
A.A B.B C.C D.D
8.用下列装置或操作进行相应实验,能达到实验目的的是
试卷第1页,共3页D.向硫化钠溶液通入足量二氧化硫:
装置
11.水合肼(N H·H O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+
或操 2 4 2
作
2NH ===NH·H O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
3 2 4 2
B.验证非金属性:
目的 A.制备
装置
或操
作
A.装置甲中试剂X可以选择生石灰 B.装置乙作为反应过程的安全瓶
C.装置丙制备水合肼时氨气从b口进入 D.装置丁可用于吸收多余的尾气
C.探究氧化性:
目的 D.制取NO 12.用硫酸渣(主要成分为Fe O、SiO)制备铁基颜料铁黄(FeOOH)的一种工艺流程如图。
2 3 2
A.A B.B C.C D.D
9. 为阿伏加德罗常数的值,下列说法正确的是
A.1mol 与足量氧气反应可以产生 个 分子
已知:“还原”时,发生反应FeS+14Fe3++8H O=2SO +15Fe2++16H+;FeS 与HSO 不反应。
2 2 2 2 4
B.常温下,将2.7g铝片投入足量的浓硫酸中,铝失去的电子数为
下列有关说法不正确的是
C.120g 和 的固体混合物中含有的阳离子数为
A.“酸溶”时适当提高硫酸浓度可加快反应速率
B.“还原”时氧化产物与还原产物的物质的量之比为2:15
D. ,当生成标况下6.72L 时转移电子数为
C.“过滤I”所得滤液中存在的阳离子主要有Fe2+和H+
10.下列反应的离子方程式正确的是
D.“沉降、氧化”时发生的离子方程式:4Fe2++8NH·H O+O=8NH +4FeOOH↓+2H O
3 2 2 2
A.碘化亚铁溶液与等物质的量的氯气:
13.利用微生物燃料电池(MFC)可以将废水中的 降解为N。某课题组设计出如图所示的微生物燃料电池进
2
B.用NaSO 溶液吸收少量Cl:
2 3 2
行同步硝化和反硝化脱氮研究,下列说法不正确的是
C.等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1:2混合:
2 4 4
试卷第2页,共3页c.常温下Y的单质呈固态,M的单质呈气态
(3)Y的最高价氧化物对应的水化物的浓溶液与Cu反应的化学方程式为 ;
(4)E的简单氢化物与Q单质反应是工业生产硝酸的重要反应,方程式为 ;
(5)以Pt为电极,R的最高价氧化物对应的水化物为电解质溶液,T的最简单氢化物与Q单质构成燃料电池,该
电池的负极反应式为 ;
(6)M的单质可用于检验运输E的简单氢化物管道是否泄露,若泄露将产生白烟,其原理为 (用化学方程
表示)。
A.好氧电极b上发生的反硝化反应为2 +10e-+12H+=N ↑+6H O
2 2
16.(14分).某温度下CO 加氢制甲醇的的总反应为CO(g)+3H(g)⇌CHOH(g)+HO(g),该反应为放热反应,
2 2 2 3 2
B.好氧电极b上的副反应为O+4e-+4H+=2H O
2 2 在固定容积为2.0 L的密闭容器中充入0.8 mol的CO 和2.4 mol的H,测得CO 和CHOH的物质的量随时间变
2 2 2 3
C.交换膜c为质子交换膜,质子从电极a区域通过质子交换膜移向电极b区域 化如图。
请回答:
D.理论上每消耗1molC 6 H 12 O 6 ,可以处理 的物质的量为4.8mol (1)对于该反应,反应物的化学键断裂要吸收的能量
(填“大于”、“小于”或“等于”)生成物的化学键形成要放出
14.一定量 和 的混合物投入 的稀 中,固体完全溶解后,生成标准状况下 的能量。
(2)下列措施能加快反应速率的是 (填序号,下同)。
A.往容器中充入N
2
( 的还原产物仅此一种)。再向反应后的溶液中加入2mol/L的 溶液,要使铜元素与铁元素 B.往容器充入H 2
C.及时分离出CHOH
3
D.减小容器体积
完全转化为 、 或 沉淀,所加入的 溶液的体积最少是 E.选择高效的催化剂
(3)2 min内CHOH的反应速率为 。
3
A. B. C. D. (4)恒温恒容条件下,能说明反应已达平衡状态的是 。
A.CO(g)体积分数保持不变
二、解答题 2
B.容器中气体压强保持不变
15(16分).X、Y、Z、M、Q、R、E、T是八种短周期主族元素,其原子半径及主要化合价如下表所示:
C.容器中CHOH浓度与HO浓度之比为1∶1
3 2
元素代号 X Y Z M Q R E T
D.混合气体的密度保持不变
E.H 的生成速率是HO生成速率的3倍
原子半径 2 2
0.160 0.102 0.143 0.099 0.074 0.186 0.075 0.077
(5)该反应平衡时CO 的转化率为 。
2
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,
主要化合价
、
、 、 、
其总反应式为: ,则电极A的反应式为 。
17(14分).二氯化砜( )又名磺酰氯,熔点为-54.1℃,沸点69.1℃,常
(1)Q在周期表中的位置是 ,R与Q按原子个数比为 形成的化合物的电子式为 。
(2)Y、M两种元素相比较非金属性较强的是 (填元素符号),下列事实能证明这一结论的是 (选填
温较稳定,遇水剧烈反应,100℃以上易分解。主要用作氯化剂或氯磺化剂。实验室可利用 和 在活性炭
字母序号)。
a.简单氢化物的水溶液酸性:
催化下发生反应: ,得到少量 ,装置如图(部分夹持装置已省略)。
b.Fe分别与M和Y单质反应生成的产物中Fe的化合价:
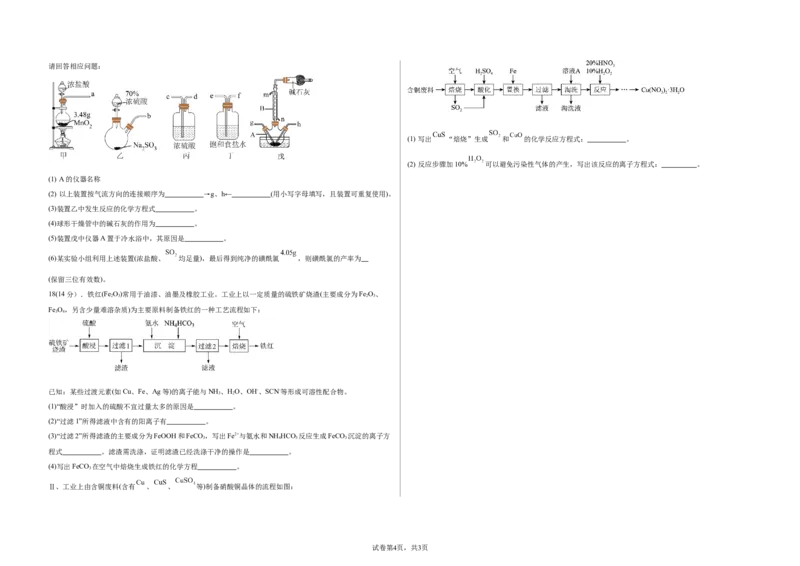
试卷第3页,共3页请回答相应问题:
(1) 写出 “焙烧”生成 和 的化学反应方程式: 。
(2) 反应步骤加10% 可以避免污染性气体的产生,写出该反应的离子方程式: 。
(1) A的仪器名称
(2) 以上装置按气流方向的连接顺序为 →g、h← (用小写字母填写,且装置可重复使用)。
(3)装置乙中发生反应的化学方程式 。
(4)球形干燥管中的碱石灰的作用为 。
(5)装置戊中仪器A置于冷水浴中,其原因是 。
(6)某实验小组利用上述装置(浓盐酸、 均足量),最后得到纯净的磺酰氯 ,则磺酰氯的产率为
(保留三位有效数)。
18(14分).铁红(Fe O)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为Fe O、
2 3 2 3
Fe O,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
3 4
已知:某些过渡元素(如Cu、Fe、Ag等)的离子能与NH 、HO、OH-、SCN-等形成可溶性配合物。
3 2
(1)“酸浸”时加入的硫酸不宜过量太多的原因是 。
(2)“过滤1”所得滤液中含有的阳离子有 。
(3)“过滤2”所得滤渣的主要成分为FeOOH和FeCO,写出Fe2+与氨水和NH HCO 反应生成FeCO 沉淀的离子方
3 4 3 3
程式 。滤渣需洗涤,证明滤渣已经洗涤干净的操作是 。
(4)写出FeCO 在空气中焙烧生成铁红的化学方程 。
3
Ⅱ、工业上由含铜废料(含有 、 、 等)制备硝酸铜晶体的流程如图:
试卷第4页,共3页1.A 2.B 3.A 4.B 5.B6.A 7.C8.C9.D10.B11.C
12.D13.D14.B
15.(1) 第二周期第ⅥA族
(2) Cl b
(3)
(4)
(5) (6)
16.(1)小于 (2)BDE (3) 0.1 mol/(L·min) (4)ABE (5)75%
(6)2CH OH+3O+4OH−=2 +6HO CHOH-6e−+8OH−= +6HO
3 2 2 3 2
17.(1)三颈烧瓶
(2) aefcd或dcb dcb或aefcd
(3) H SO (浓) +Na SO =Na SO +SO+H O (4)吸收未反应的SO 和Cl,进行尾气
2 4 2 3 2 4 2 2 2 2
处理同时可以防止空气中的水蒸气进入装置戊导致磺酰氯水解
(5)制备SO Cl 的反应为放热反应,SO Cl 沸点低,温度过高易气化且易分解
2 2 2 2
(6)75.0%
18.(1)过量太多会增加沉淀过程氨水的用量
(2)H+、Fe2+和Fe3+
(3) 最后一次洗涤液体,用稀盐酸
酸化后再滴入几滴BaCl 溶液,若无白色沉淀产生,说明滤渣已经洗涤干净
2
(4)
答案第1页,共2页