文档内容
虹口区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2020.1
考生注意:1. 本试卷满分60分,理化合卷用时100分钟;
2. 答案必须填写在答题卡上。
相对原子质量:H–1 C–12 O–16 Ca–40
六、选择题(共20分)
下列各题均只有一个正确选项,请将正确选项的代号用 2B铅笔填涂在答题纸相应位置
上,更改答案时,用橡皮擦去,重新填涂。
27. 空气中含量最多的气体是
A. 氮气 B. 氧气 C. 二氧化碳 D. 水蒸气
28. 属于纯净物的是
A. 加碘盐 B. 苏打水 C. 米醋 D. 蒸馏水
29. 与C 互为同素异形体的是
60
A. 活性炭 B. 石墨 C. 木炭 D. 铅笔芯
30. 引起温室效应的气体是
A. 二氧化碳 B.二氧化硫 C. 氮气 D. 氧气
31. 放入水中能形成溶液的是
A. 粉笔灰 B. 奶粉 C. 橄榄油 D. 白砂糖
32. 过程中包含化学变化的是
A. 燃烧燃料 B. 砍柴伐木 C. 裁剪布料 D. 冲洗碗筷
33. 一些水果的pH如下,其中酸性最强的是
A.苹果:4.9 B. 柠檬:3.0 C. 菠萝:5.1 D. 荔枝:5.0
34. 属于氧化物的是
A. 液氧 B. 水 C. 臭氧 D. 碳酸
35. 物质燃烧的现象描述正确的是
A. 硫在氧气中燃烧发出淡蓝色火焰 B. 碳在氧气中燃烧发出红光
C. 镁带在空气屮燃烧发出耀眼的白光 D. 磷在空气中燃烧产生白色烟雾
36. 点燃篝火时,将木柴架空些,目的是
A. 加快散热速度 B. 提高空气中氧气的含量C. 降低木柴着火点 D. 增大木柴与空气的接触面积
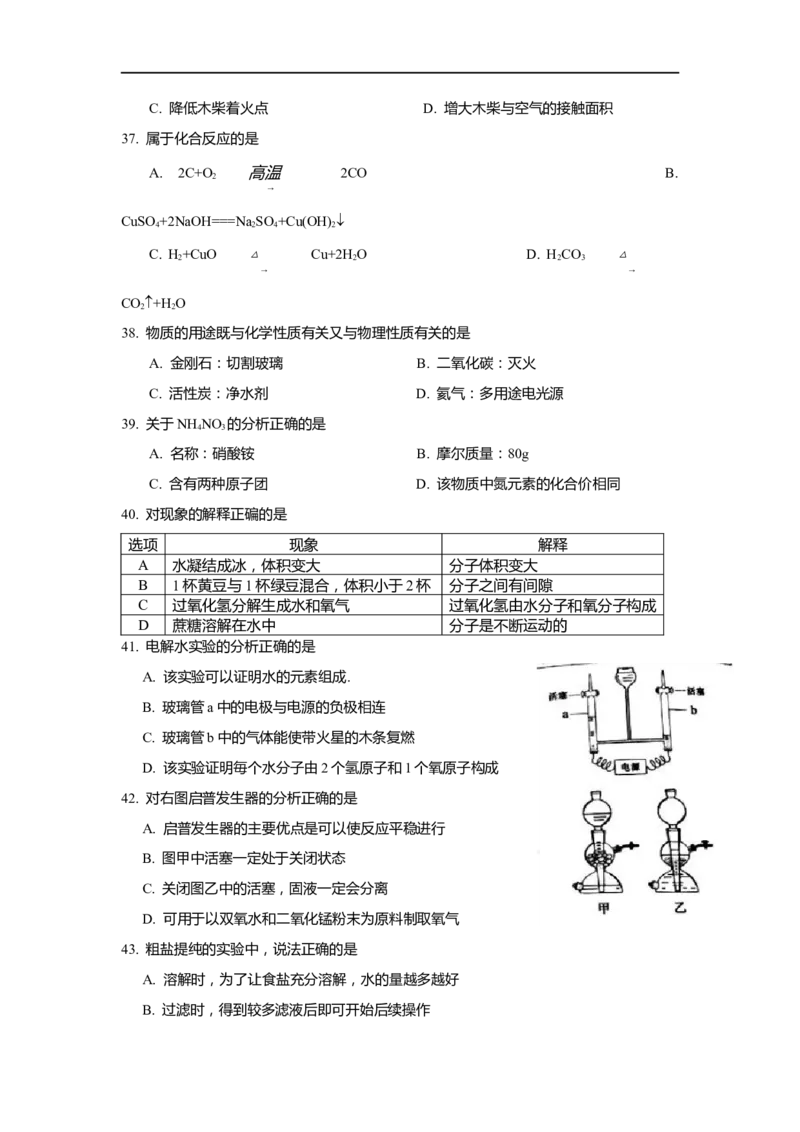
37. 属于化合反应的是
A. 2C+O 高温 2CO B.
2
→
CuSO +2NaOH===NaSO +Cu(OH)
4 2 4 2
C. H+CuO △ Cu+2H O D. H CO △
2 2 2 3
→ →
CO+H O
2 2
38. 物质的用途既与化学性质有关又与物理性质有关的是
A. 金刚石:切割玻璃 B. 二氧化碳:灭火
C. 活性炭:净水剂 D. 氦气:多用途电光源
39. 关于NH NO 的分析正确的是
4 3
A. 名称:硝酸铵 B. 摩尔质量:80g
C. 含有两种原子团 D. 该物质中氮元素的化合价相同
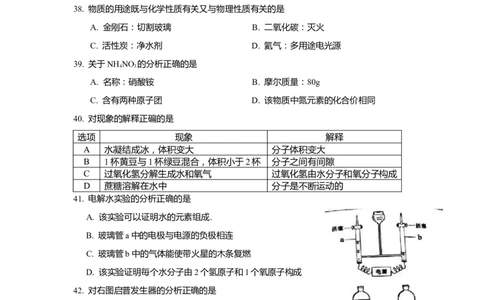
40. 对现象的解释正碥的是
选项 现象 解释
A 水凝结成冰,体积变大 分子体积变大
B 1杯黄豆与1杯绿豆混合,体积小于2杯 分子之间有间隙
C 过氧化氢分解生成水和氧气 过氧化氢由水分子和氧分子构成
D 蔗糖溶解在水中 分子是不断运动的
41. 电解水实验的分析正确的是
A. 该实验可以证明水的元素组成.
B. 玻璃管a中的电极与电源的负极相连
C. 玻璃管b中的气体能使带火星的木条复燃
D. 该实验证明毎个水分子由2个氢原子和1个氧原子构成
42. 对右图启普发生器的分析正确的是
A. 启普发生器的主要优点是可以使反应平稳进行
B. 图甲中活塞一定处于关闭状态
C. 关闭图乙中的活塞,固液一定会分离
D. 可用于以双氧水和二氧化锰粉末为原料制取氧气
43. 粗盐提纯的实验中,说法正确的是
A. 溶解时,为了让食盐充分溶解,水的量越多越好
B. 过滤时,得到较多滤液后即可开始后续操作C. 蒸发时,待液体完全蒸干后才能停止加热
D. 粗盐提纯可以除去泥沙等难溶性杂质
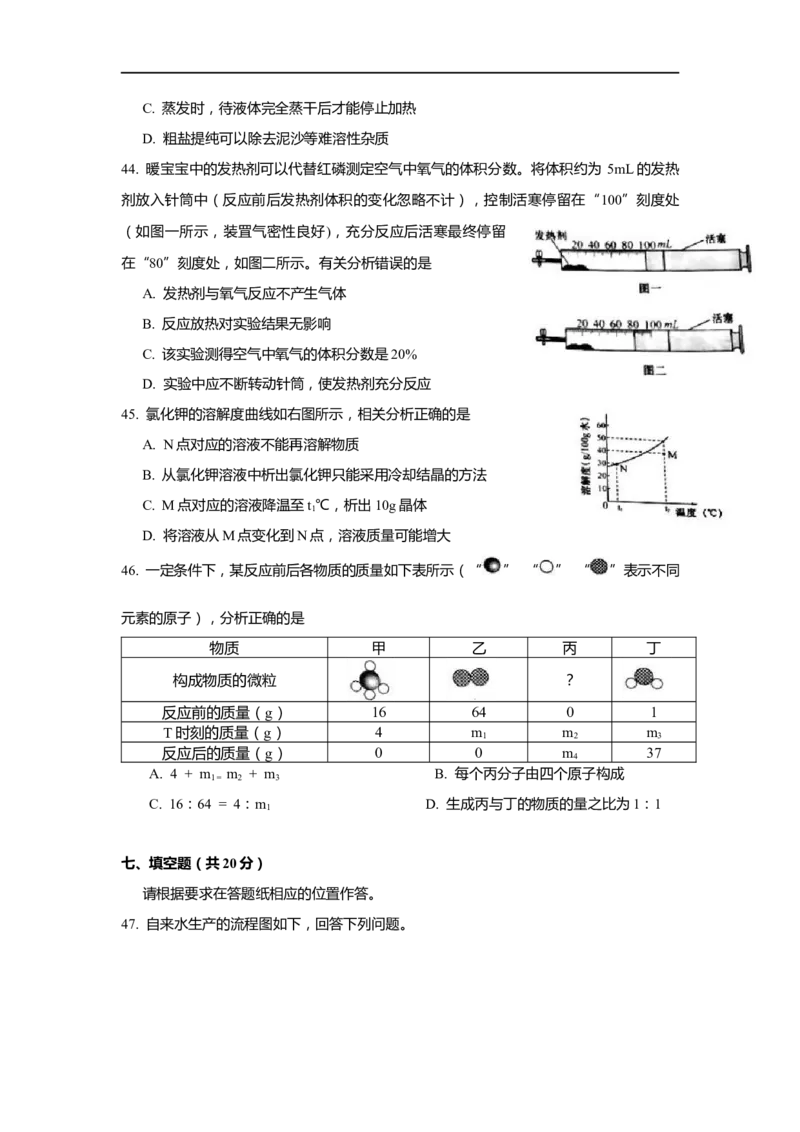
44. 暖宝宝中的发热剂可以代替红磷测定空气中氧气的体积分数。将体积约为 5mL的发热
剂放入针筒中(反应前后发热剂体积的变化忽略不计),控制活寒停留在“100”刻度处
(如图一所示,装罝气密性良好),充分反应后活寒最终停留
在“80”刻度处,如图二所示。有关分析错误的是
A. 发热剂与氧气反应不产生气体
B. 反应放热对实验结果无影响
C. 该实验测得空气中氧气的体积分数是20%
D. 实验中应不断转动针筒,使发热剂充分反应
45. 氯化钾的溶解度曲线如右图所示,相关分析正确的是
A. N点对应的溶液不能再溶解物质
B. 从氯化钾溶液中析出氯化钾只能采用冷却结晶的方法
C. M点对应的溶液降温至t℃,析出10g晶体
1
D. 将溶液从M点变化到N点,溶液质量可能增大
46. 一定条件下,某反应前后各物质的质量如下表所示(“ ” “ ” “ ”表示不同
元素的原子),分析正确的是
物质 甲 乙 丙 丁
构成物质的微粒 ?
反应前的质量(g) 16 64 0 1
T时刻的质量(g) 4 m m m
1 2 3
反应后的质量(g) 0 0 m 37
4
A. 4 + m m + m B. 每个丙分子由四个原子构成
1 = 2 3
C. 16:64 = 4:m D. 生成丙与丁的物质的量之比为1:1
1
七、填空题(共20分)
请根据要求在答题纸相应的位置作答。
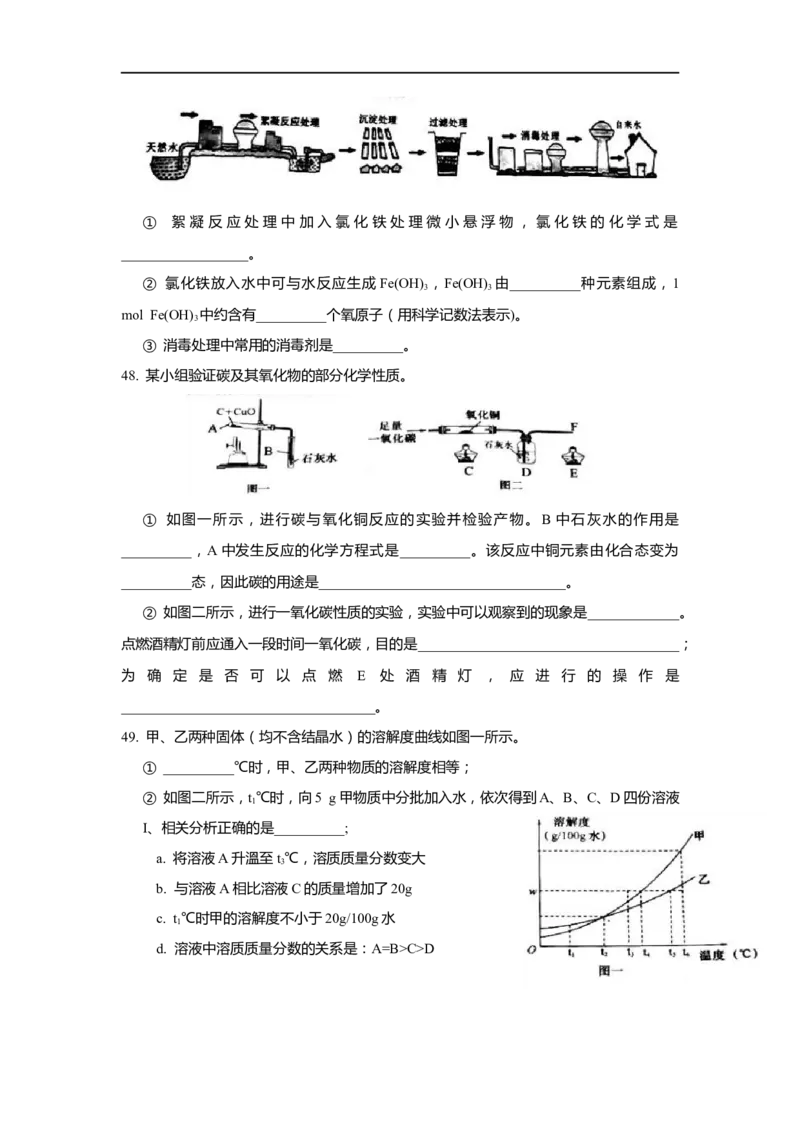
47. 自来水生产的流程图如下,回答下列问题。① 絮 凝 反 应 处 理 中 加 入 氯 化 铁 处 理 微 小 悬 浮 物 , 氯 化 铁 的 化 学 式 是
__________________。
② 氯化铁放入水中可与水反应生成 Fe(OH) ,Fe(OH) 由__________种元素组成,1
3 3
mol Fe(OH) 中约含有__________个氧原子(用科学记数法表示)。
3
③ 消毒处理中常用的消毒剂是__________。
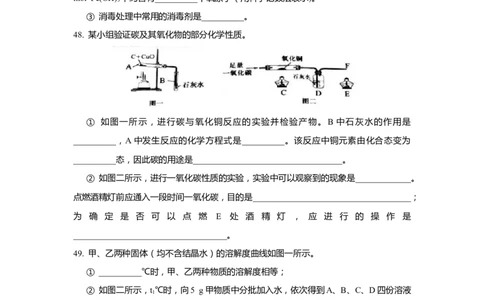
48. 某小组验证碳及其氧化物的部分化学性质。
① 如图一所示,进行碳与氧化铜反应的实验并检验产物。B 中石灰水的作用是
__________,A中发生反应的化学方程式是__________。该反应中铜元素由化合态变为
__________态,因此碳的用途是___________________________________。
② 如图二所示,进行一氧化碳性质的实验,实验中可以观察到的现象是_____________。
点燃酒精灯前应通入一段时间一氧化碳,目的是_____________________________________;
为 确 定 是 否 可 以 点 燃 E 处 酒 精 灯 , 应 进 行 的 操 作 是
____________________________________。
49. 甲、乙两种固体(均不含结晶水)的溶解度曲线如图一所示。
① __________℃时,甲、乙两种物质的溶解度相等;
② 如图二所示,t℃时,向5 g甲物质中分批加入水,依次得到A、B、C、D四份溶液
1
I、相关分析正确的是__________;
a. 将溶液A升溫至t℃,溶质质量分数变大
3
b. 与溶液A相比溶液C的质量增加了20g
c. t ℃时甲的溶解度不小于20g/100g水
1
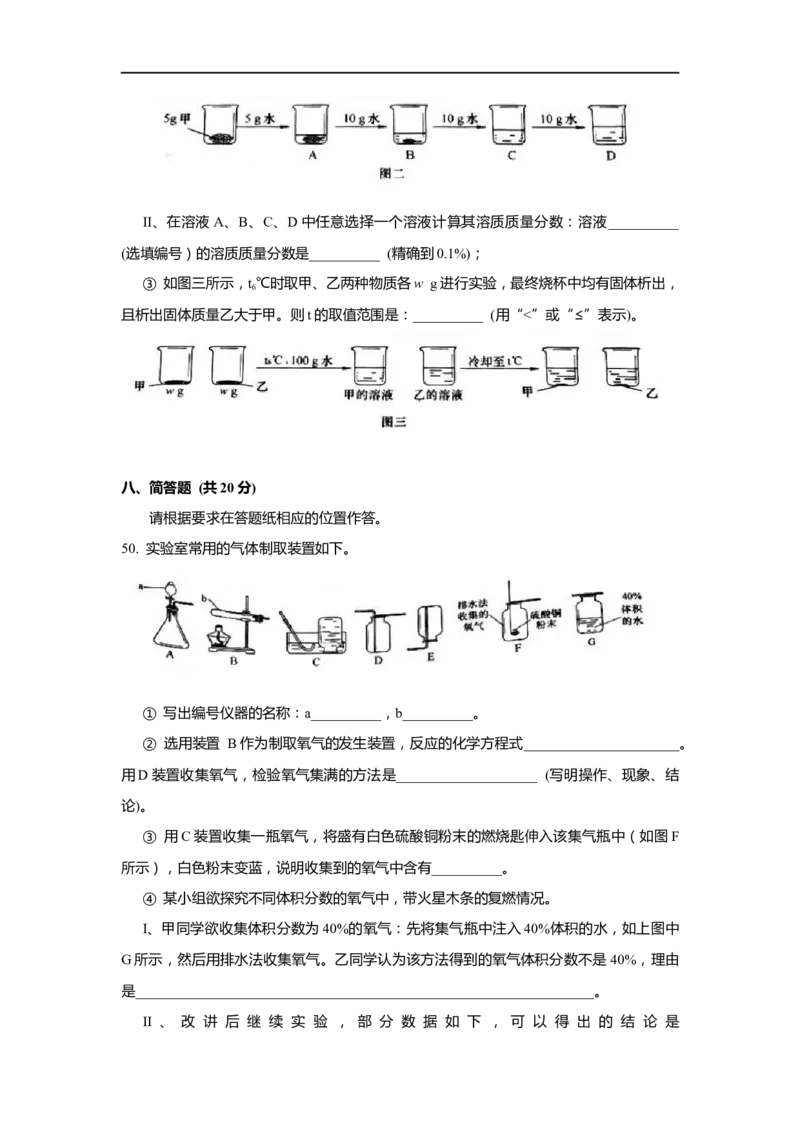
d. 溶液中溶质质量分数的关系是:A=B>C>DII、在溶液A、B、C、D中任意选择一个溶液计算其溶质质量分数:溶液__________
(选填编号)的溶质质量分数是__________ (精确到0.1%);
③ 如图三所示,t℃时取甲、乙两种物质各w g进行实验,最终烧杯中均有固体析出,
6
且析出固体质量乙大于甲。则t的取值范围是:__________ (用“<”或“≤”表示)。
八、简答题 (共20分)
请根据要求在答题纸相应的位置作答。
50. 实验室常用的气体制取装置如下。
① 写出编号仪器的名称:a__________,b__________。
② 选用装置 B作为制取氧气的发生装置,反应的化学方程式______________________。
用D装置收集氧气,检验氧气集满的方法是____________________ (写明操作、现象、结
论)。
③ 用C装置收集一瓶氧气,将盛有白色硫酸铜粉末的燃烧匙伸入该集气瓶中(如图F
所示),白色粉末变蓝,说明收集到的氧气中含有__________。
④ 某小组欲探究不同体积分数的氧气中,带火星木条的复燃情况。
I、甲同学欲收集体积分数为40%的氧气:先将集气瓶中注入40%体积的水,如上图中
G所示,然后用排水法收集氧气。乙同学认为该方法得到的氧气体积分数不是40%,理由
是_________________________________________________________________。
II 、 改 讲 后 继 续 实 验 , 部 分 数 据 如 下 , 可 以 得 出 的 结 论 是_____________________________。
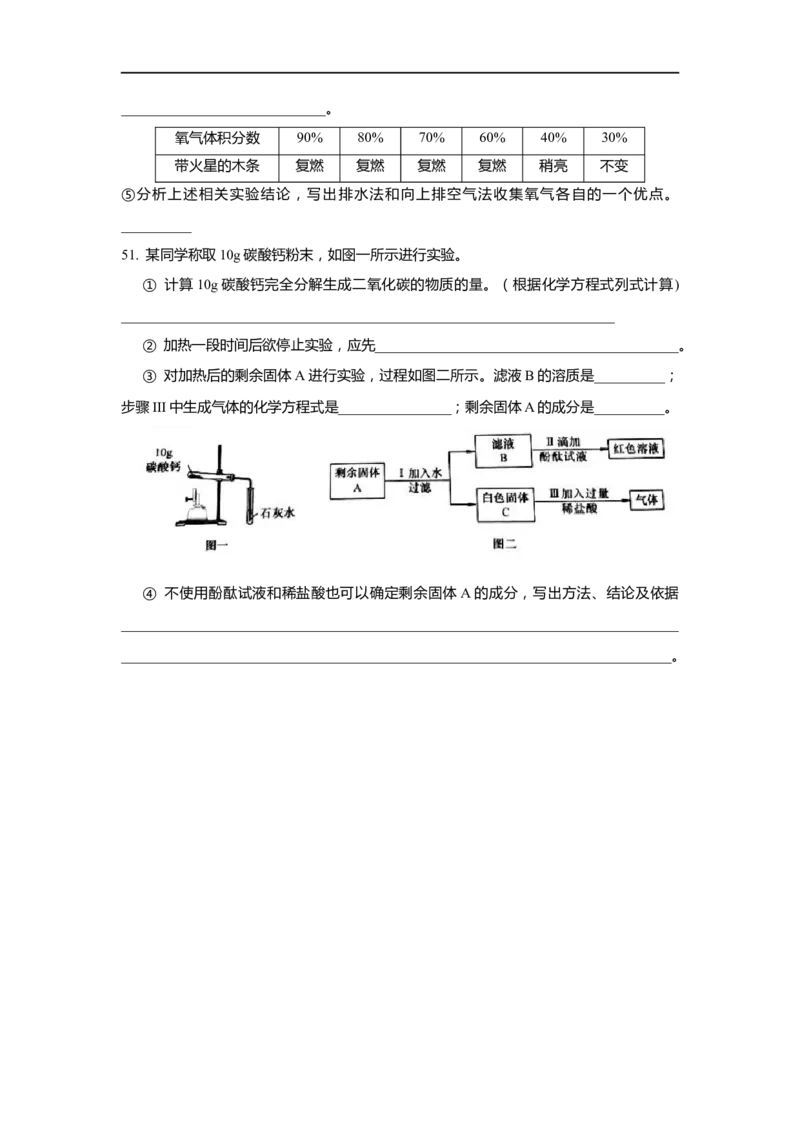
氧气体积分数 90% 80% 70% 60% 40% 30%
带火星的木条 复燃 复燃 复燃 复燃 稍亮 不变
⑤分析上述相关实验结论,写出排水法和向上排空气法收集氧气各自的一个优点。
__________
51. 某同学称取10g碳酸钙粉末,如囹一所示进行实验。
① 计算10g碳酸钙完全分解生成二氧化碳的物质的量。(根据化学方程式列式计算)
______________________________________________________________________
② 加热一段时间后欲停止实验,应先___________________________________________。
③ 对加热后的剩余固体A进行实验,过程如图二所示。滤液B的溶质是__________;
步骤III中生成气体的化学方程式是________________;剩余固体A的成分是__________。
④ 不使用酚酞试液和稀盐酸也可以确定剩余固体A的成分,写出方法、结论及依据
_______________________________________________________________________________
______________________________________________________________________________。