文档内容
专题11 探究性实验
目录
【题型一】氢氧化钠变质探究
【题型二】 废液成分探究
【题型三】混合气体与定量分析
【题型四】 酸碱盐实验探究
【题型五】 物质推断与定量分析
题型一 氢氧化钠变质探究
1.(2023·上海宝山·统考二模)实验室现有一瓶敞口放置一段时间的20%的氢氧化钠溶液(室温),需知道其
是否变质,再进行处理及回收利用。甲乙两组探究性学习小组同学为此开展以下活动。
【理论分析】该氢氧化钠溶液可能已经变质
(1)氢氧化钠可能变质的原因的化学方程式是___________。
【甲组实验】
(2)利用物质的化学性质探究氢氧化钠溶液是否变质及变质程度
实验步骤及现象 实验结论
步骤1:取少许样品,滴加BaCl 溶液,观察到___________; 证明氢氧化钠已变质
2
步骤2:继续步骤1,滴加BaCl 溶液至过量,再___________(填实验操作及现 证明氢氧化钠部分变
2
象)。 质
【乙组实验】利用物质的溶解性探究氢氧化钠溶液是否变质及变质程度
资料:下表为氢氧化钠和碳酸钠在水中和酒精中的部分溶解度。
温度 水中S(g/100g) 酒精中S(g/100g)
碳酸
氢氧化钠 氢氧化钠 碳酸钠
钠
20℃ 109 21.5 17.3 不溶40℃ 129 49 40 不溶
(3)40℃时,碳酸钠在水中的溶解度为___________;
(4)原20%的氢氧化钠溶液是室温下的___________溶液(选填“饱和”“不饱和”);
取样品溶液10g蒸发,将所得固体全部放入温度为___________℃的10g酒精中,充分振荡,固体部分溶解,
证明氢氧化钠已变质且部分变质。
【处理与回收】将该瓶部分变质的氢氧化钠溶液回收再利用
(5)请你和学习小组一起完成回收氢氧化钠的实验方案:
实验目的 实验操作 实验结论
回收氢氧化
___________ 回收得到氢氧化钠溶液
钠
题型二 废液成分探究
1.(2023·上海金山·统考二模 节选)(4)用盐酸和碳酸钙制备CO 产生了大量废液。通过以下探究制定废液
2
处理方案。
I.探究废液成分。
推测废液所含溶质:推测一:CaCl ;推测二:CaCl 和HCl。
2 2
用一种药品验证哪种推测成立,可选择_____(填标号)
A.NaOH溶液 B.AgNO 溶液 C.锌粒 D.CuSO 溶液
3 4
实验测得废液中的溶质是CaCl 和HCl。
2
Ⅱ.废液的处理:决定用Na CO 除去它们。
2 3
【提出问题】如何估算Na CO 固体的用量?
2 3
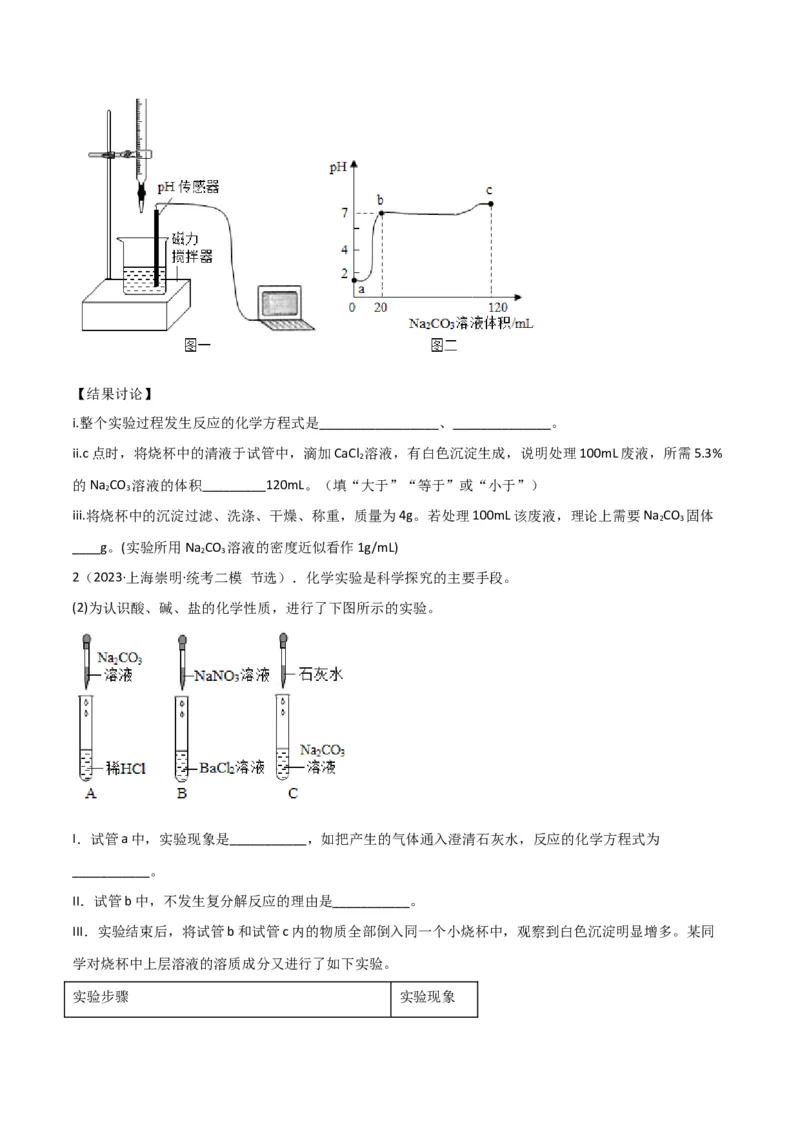
【进行实验】取100mL废液样品于烧杯中,逐滴滴加5.3%的Na CO 溶液,用pH传感器测定滴加过程中溶
2 3
液的pH。实验测得部分数据如图二所示。【结果讨论】
i.整个实验过程发生反应的化学方程式是_________________、______________。
ii.c点时,将烧杯中的清液于试管中,滴加CaCl 溶液,有白色沉淀生成,说明处理100mL废液,所需5.3%
2
的Na CO 溶液的体积_________120mL。(填“大于”“等于”或“小于”)
2 3
iii.将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g。若处理100mL该废液,理论上需要Na CO 固体
2 3
____g。(实验所用Na CO 溶液的密度近似看作1g/mL)
2 3
2(2023·上海崇明·统考二模 节选).化学实验是科学探究的主要手段。
(2)为认识酸、碱、盐的化学性质,进行了下图所示的实验。
I.试管a中,实验现象是___________,如把产生的气体通入澄清石灰水,反应的化学方程式为
___________。
II.试管b中,不发生复分解反应的理由是___________。
III.实验结束后,将试管b和试管c内的物质全部倒入同一个小烧杯中,观察到白色沉淀明显增多。某同
学对烧杯中上层溶液的溶质成分又进行了如下实验。
实验步骤 实验现象取少量上层溶液于试管中,滴加过量稀盐酸 无明显现象
另取少量上层溶液于试管中,滴加少量硫酸钠溶
有白色沉淀
液
上述实验可知,烧杯中上层溶液的溶质成分是___________
3.(2023·上海静安·统考二模)用如图装置完成下列实验(夹持仪器略去,K 、K 均关闭)。
1 2
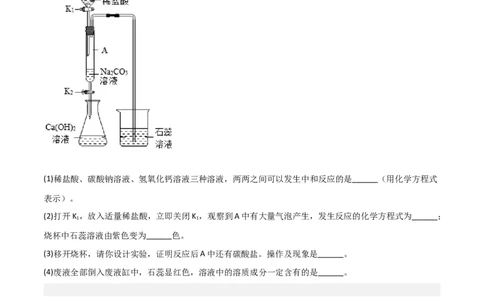
(1)稀盐酸、碳酸钠溶液、氢氧化钙溶液三种溶液,两两之间可以发生中和反应的是______(用化学方程式
表示)。
(2)打开K ,放入适量稀盐酸,立即关闭K ,观察到A中有大量气泡产生,发生反应的化学方程式为______;
1 1
烧杯中石蕊溶液由紫色变为______色。
(3)移开烧杯,请你设计实验,证明反应后A中还有碳酸盐。操作及现象是______。
(4)废液全部倒入废液缸中,石蕊显红色,溶液中的溶质成分一定含有的是______。题型三 混合气体与定量分析
1.(2023·上海杨浦区·统考二模)为进一步确定湖边收集的气体的组成,同学们进行了以下探究过程,请
你参与并协助他们完成相关学习任务。
【提出猜想】收集的气体中可能含有CH 、CO 、CO和H O
4 2 2
【查阅资料】 ;
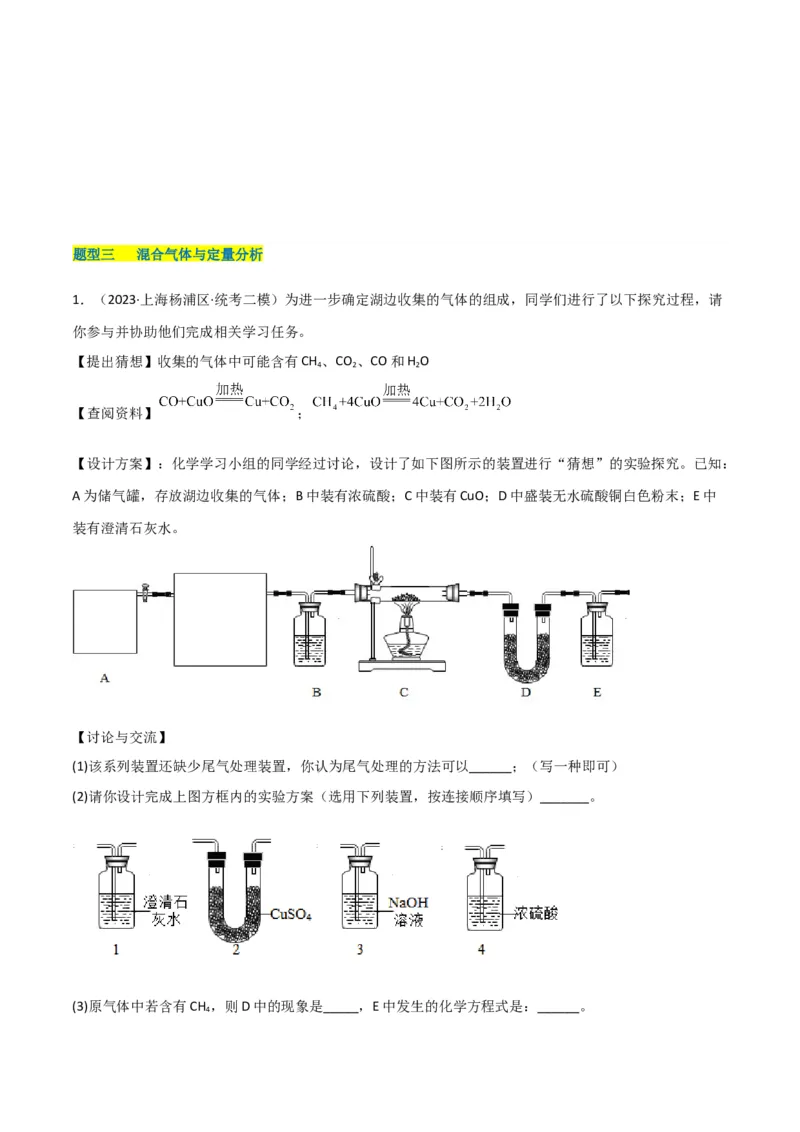
【设计方案】:化学学习小组的同学经过讨论,设计了如下图所示的装置进行“猜想”的实验探究。已知:
A为储气罐,存放湖边收集的气体;B中装有浓硫酸;C中装有CuO;D中盛装无水硫酸铜白色粉末;E中
装有澄清石灰水。
【讨论与交流】
(1)该系列装置还缺少尾气处理装置,你认为尾气处理的方法可以______;(写一种即可)
(2)请你设计完成上图方框内的实验方案(选用下列装置,按连接顺序填写)_______。
(3)原气体中若含有CH ,则D中的现象是_____,E中发生的化学方程式是:______。
4(4)老师认为以上设计仍有缺陷,不能确定______气体是否存在。
(5)小王同学和小李同学想通过定量实验的方法检验尚不能确定的气体,于是对实验方案进行了改进,E装
置中的试剂改为足量的X溶液,可达到更好的吸收效果。则X为_____,试验后为证明X有剩余,可以通过
加入______和_____验证。
(6)同时对D、E装置在实验前后的质量进行称量,数据记入下表中:
反应前 反应后
D装置 100g 103.6g
E装置 120g 125.5g
你认为根据上述数据计算后能否得出原气体中含有CO的结论?请简要分析_____。
(7) 实验中若试剂用量充足调换B跟D的位置,对测定结果有无影响?_____(填“有”或“无”)。
题型四 酸碱盐实验
1.(2023·上海嘉定·统考二模)某兴趣小组同学学习了酸、碱和盐的知识后,进行了如下的实验研究:
实验一:探究稀酸的化学性质。
(1)试管Ⅰ中的现象是溶液变红,说明溶液呈______性。
(2)试管II 中反应的化学方程式为的______。
(3)试管III 中的现象是______,说明氧化铁属于______(选填“酸性氧化物”或“碱性氧化物”)。
(4)实验中发现试管II 中固体全部溶解,试管IV中产生白色沉淀,白色沉淀的化学式为______接着向试管V
中滴加氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图乙所示。则试管IV 中的溶质
有______;图乙中a~b段对应溶液中一定发生反应的化学方程式为______。C点后沉淀质量不再增加的原
因是______。实验二:通过实验证明二氧化碳能与氢氧化钠反应,并检验生成了碳酸盐。25℃时,氢氧化钠和碳酸钠在
乙醇中的溶解度如下表所示。
物质 NaOH Na CO
2 3
溶解度(g/100乙醇) 17.3 <0.01
利用如图所示装置进行实验(该装置气密性良好;乙醇不参与反应)。
步骤1:打开K ,关闭K ,从a口通入二氧化碳,看到饱和氢氧化钠的乙醇溶液中产生大量沉淀,停止通
1 2
二氧化碳;
步骤2:从a口通入氮气,直至排净装置中的二氧化碳;
步骤3:关闭K ,打开K ,向甲装置的试管中滴入足量的稀盐酸。
1 2
(5)步骤1装置甲的试管中能看到沉淀的原因是_______。
(6)步骤2中,通入氮气,排净装置甲中二氧化碳的目的是_______。
(7)步骤3乙中能看到的现象是______,反应的化学方程式是________。
2(2023·上海黄埔区·统考二模) 如图是实验室常用的气体发生装置。
(1)双氧水和二氧化锰混合制取氧气的化学方程式是______;反应的基本类型是______;收集氧气可以
用向上排气法,该方法所利用的氧气的物理性质是______。
的
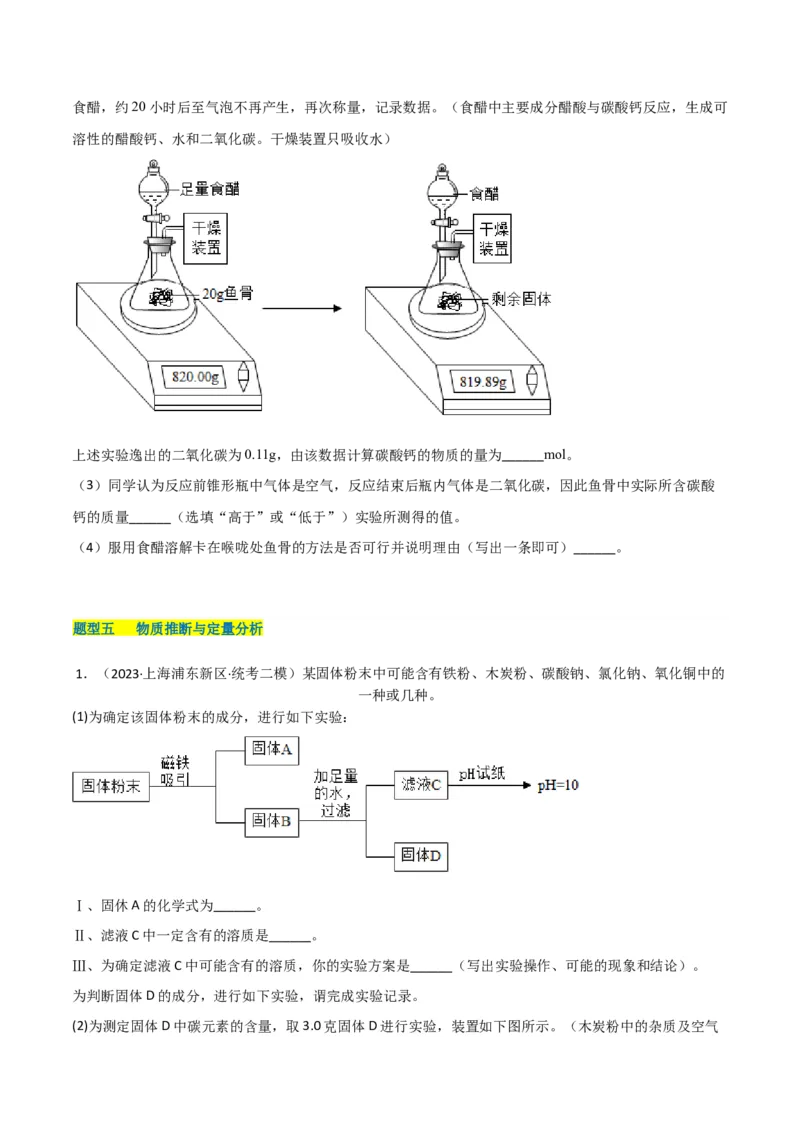
(2)下图是测定某鱼骨中碳酸钙质量 实验。取20g鱼骨加入锥形瓶中,放在电子天平上称量;加入足量食醋,约20小时后至气泡不再产生,再次称量,记录数据。(食醋中主要成分醋酸与碳酸钙反应,生成可
溶性的醋酸钙、水和二氧化碳。干燥装置只吸收水)
上述实验逸出的二氧化碳为0.11g,由该数据计算碳酸钙的物质的量为______mol。
(3)同学认为反应前锥形瓶中气体是空气,反应结束后瓶内气体是二氧化碳,因此鱼骨中实际所含碳酸
钙的质量______(选填“高于”或“低于”)实验所测得的值。
(4)服用食醋溶解卡在喉咙处鱼骨的方法是否可行并说明理由(写出一条即可)______。
题型五 物质推断与定量分析
1.(2023·上海浦东新区·统考二模)某固体粉末中可能含有铁粉、木炭粉、碳酸钠、氯化钠、氧化铜中的
一种或几种。
(1)为确定该固体粉末的成分,进行如下实验:
Ⅰ、固休A的化学式为______。
Ⅱ、滤液C中一定含有的溶质是______。
Ⅲ、为确定滤液C中可能含有的溶质,你的实验方案是______(写出实验操作、可能的现象和结论)。
为判断固体D的成分,进行如下实验,谓完成实验记录。
(2)为测定固体D中碳元素的含量,取3.0克固体D进行实验,装置如下图所示。(木炭粉中的杂质及空气中CO 对实验的影响忽略不计)
2
通入足量O ,点燃酒精灯,使固体充分燃烧,反应结束后继续通入O 至乙中质量不再增加。实验前后乙装
2 2
置中溶液增重4.4g,丙中始终未出现浑浊。
Ⅰ、写出乙处反应的化学方程式_________________________。
Ⅱ、根据乙装置中溶液增重4.4g,能否确定固体D中碳元素的含量,请分析说明______。
2.(2023·上海松江区·统考二模)某碳酸钠样品中可能含硫酸钠、氯化钡、碳酸钙中的一种或几种杂质,
对碳酸钠样品中杂质的成分进行如下探究:
由上述流程和相关现象可知,该样品的杂质中一定含有氯化钡和硫酸钠。
(1)操作A是______,现象C是______
(2)写出生成白色沉淀的一个化学方程式______
(3)溶液B中一定含有的溶质是______
(4)另取10.6g该碳酸钠样品加入100g稀盐酸,恰好完全反应,生成4.4g二氧化碳。根据数据能否确定样品
中含有碳酸钙,请分析说明______
3(2023·上海黄埔区·统考二模). 某溶液M中可能含氢氧化钠、碳酸钠、硫酸钠。为验证其成分,进行
如下实验。(1)实验1:取样于试管中,滴入酚酞溶液,观察到溶液变红。请分析说明,用该方法证明溶液M中含
有氢氧化钠的可行性。______
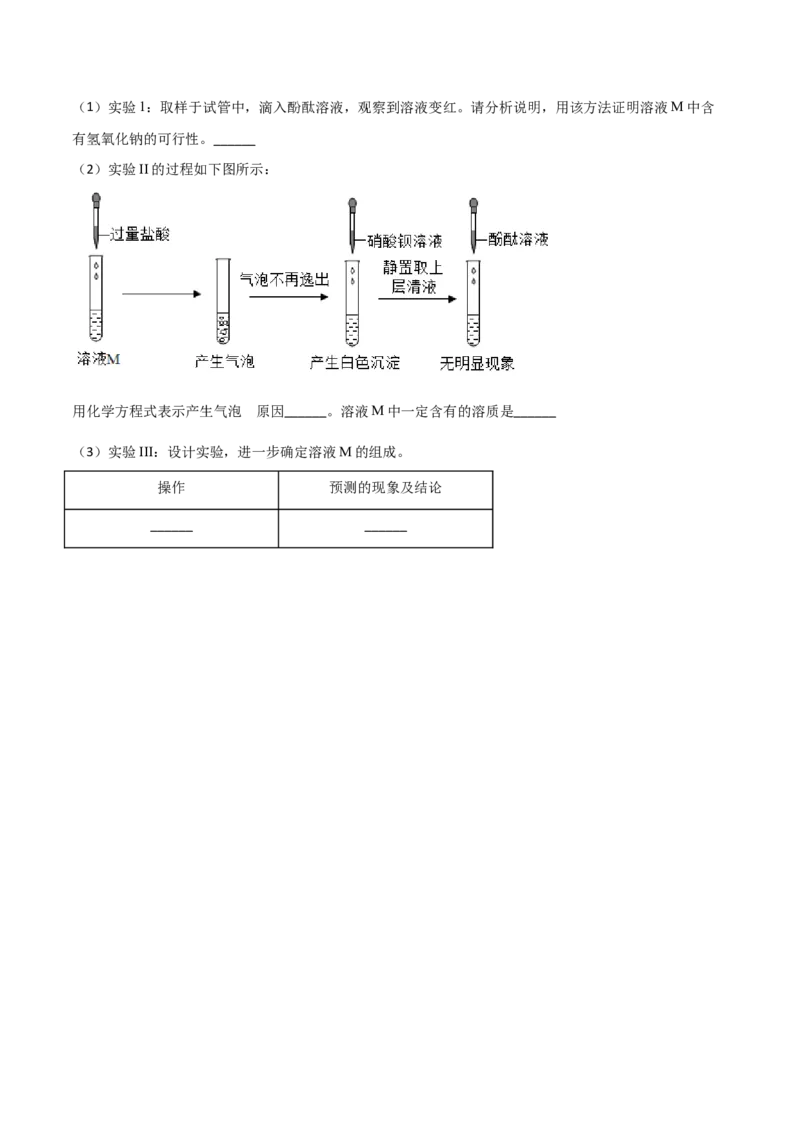
(2)实验II的过程如下图所示:
的
用化学方程式表示产生气泡 原因______。溶液M中一定含有的溶质是______
(3)实验III:设计实验,进一步确定溶液M的组成。
操作 预测的现象及结论
______ ______