文档内容
高一化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题
区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:必修第一册前两章。
5.可能用到的相对原子质量:H1 C12 O16 Na23 Cl35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的)
1. 为实现“双碳目标”,我国新兴了很多 综合利用技术。其中电催化还原 的一种反应为
,该反应属于
A. 复分解反应 B. 置换反应 C. 化合反应 D. 氧化还原反应
【答案】D
【解析】
【详解】A.复分解反应是由两种化合物互相交换成分,生成另外两种化合物的反应,
不是复分解反应,A不选;
B.置换反应是单质与化合物反应生成另外的单质和化合物的化学反应,
不是置换反应,B不选;
C.化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,
不是化合反应,C不选;D. 中C元素和O元素的化合价发生变化,属于氧化还原反应,D选;
答案选D。
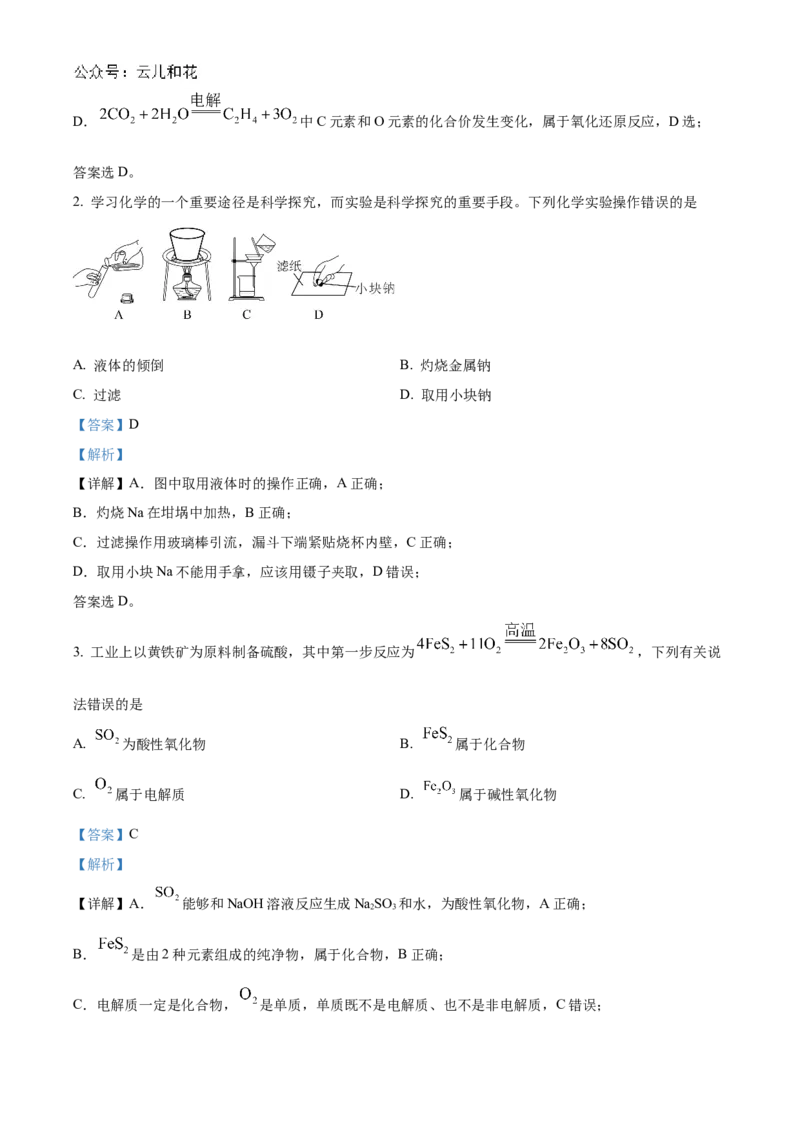
2. 学习化学的一个重要途径是科学探究,而实验是科学探究的重要手段。下列化学实验操作错误的是
A. 液体的倾倒 B. 灼烧金属钠
C. 过滤 D. 取用小块钠
【答案】D
【解析】
【详解】A.图中取用液体时的操作正确,A正确;
B.灼烧Na在坩埚中加热,B正确;
C.过滤操作用玻璃棒引流,漏斗下端紧贴烧杯内壁,C正确;
D.取用小块Na不能用手拿,应该用镊子夹取,D错误;
答案选D。
3. 工业上以黄铁矿为原料制备硫酸,其中第一步反应为 ,下列有关说
法错误的是
A. 为酸性氧化物 B. 属于化合物
C. 属于电解质 D. 属于碱性氧化物
【答案】C
【解析】
【详解】A. 能够和NaOH溶液反应生成NaSO 和水,为酸性氧化物,A正确;
2 3
B. 是由2种元素组成的纯净物,属于化合物,B正确;
C.电解质一定是化合物, 是单质,单质既不是电解质、也不是非电解质,C错误;D. 和盐酸反应生成FeCl 和HO,属于碱性氧化物,D正确;
3 2
故选C。
4. 中科院化学所在离子液体包 型微乳液研究方面取得重要成果,微乳液中分散液滴的直径在
之间,下列分散系中分散质直径与其相同的是
A. 氯化钠溶液 B. 氢氧化铝胶体 C. 泥水 D. 清澈的河水
【答案】B
【解析】
【分析】分散质粒子直径在 之间的分散系属于胶体;
【详解】A.氯化钠溶液属于溶液,其分散质粒子直径小于1nm,A错误;
在
B.氢氧化铝胶体属于胶体,其分散质粒子直径 之间,B正确;
C.泥水属于悬浊液,其分散质粒子直径大于100nm,C错误;
D.清澈的河水属于溶液,其分散质粒子直径小于1nm,D错误;
故选B。
5. 下列物质在水溶液中的电离方程式正确的是
A. B.
C. D.
【答案】C
【解析】
【详解】A.NH NO 电离方程式为: ,A错误;
4 3
B.BaCl 的电离方程式为: ,B错误;
2
C.NaHCO 是盐,属于强电解质,电离方程式为: ,C正确;
3
D.KAl(SO ) 是盐,属于强电解质,电离方程式为: ,D错误;
4 2
答案选C。
6. 下列有关钠及其化合物的说法正确的是A. 可置换出 溶液中的
B. 久置于空气中最终产物为
C. 属于碱性氧化物
D. 可加热除去 固体中混有的
【答案】D
【解析】
【详解】A. 投入 溶液中, 先与水反应生成 , 与 反应生成
,无法置换出 溶液中的 ,A项错误;
B. 在空气中放置先与氧气反应生成 , 再与水反应生成 , 再与 反应
生成 , 风化生成 ,B项错误;
C. 不属于碱性氧化物,为过氧化物,C项错误;
D. 受热易分解,可加热除去 固体中混有的 ,D项正确;
故选D。
7. 下列关于氯及其化合物的叙述中错误的是
A. 常温常压下, 是黄绿色气体
B. 氯水和液氯的成分完全相同
C. 在光照条件下易发生分解
D. 含氯漂白液的有效成分为
【答案】B
【解析】
【详解】A.常温常压下, 是黄绿色气体,A项正确;B.氯水是氯气的水溶液,其中含 、 、 、 、 、 、 (极少),属于混合物,
液氯中只有 分子,氯水和液氯的成分不相同,B项错误;
C. 见光分解成 和 ,C项正确;
D.含氯漂白液的主要成分为氯化钠和次氯酸钠,有效成分为 ,D项正确;
故选B。
的
8. 下列各组澄清透明溶液中,能大量共存 离子组是
.
A 、 、 、
B. 、 、
C. 、 、 、
D. 、 、 、
【答案】A
【解析】
【详解】A.各离子之间不会发生离子反应,能够大量共存,A项符合题意;
B. 与 反应生成 沉淀,不能大量共存,B项不符合题意;
C. 与 反应生成 和 ,不能大量共存,C项不符合题意;
D. 与 反应生成 沉淀,不能大量共存,D项不符合题意;
故选A。
9. 物质的性质决定用途,下列两者对应关系正确的是
A. ——治疗胃酸过多症 B. ——食品脱氧剂
C. ——消毒剂 D. 胶体——自来水消毒
【答案】C【解析】
【详解】A.碳酸钠溶液碱性较强,一般用碳酸氢钠治疗胃酸过多症,A错误;
B. 不与 反应,但能与水反应,可用作干燥剂,B错误;
C. 可用于自来水消毒,C正确;
D. 胶体具有吸附性,可吸附水中悬浮的不溶性小颗粒杂质使之沉降,但不能杀菌消毒,D错误;
答案选C。
10. 下列离子方程式中书写正确的是
A. 溶于水:
B. 向 溶液中滴加少量盐酸:
C. 醋酸除水垢:
D. 向石灰乳中加入 溶液:
【答案】B
【解析】
【详解】A. 溶于水生成HCl和HClO,HClO是弱酸,保留化学式,离子方程式为:
,A错误;
B.向 溶液中滴加少量盐酸反应生成NaHCO ,离子方程式为: ,B正确;
3
C.醋酸除水垢是醋酸和碳酸钙反应生成醋酸钙、二氧化碳和水,醋酸是弱酸,不拆成离子,离子方程式
为: ,C错误;
D.向石灰乳中加入 溶液反应生成碳酸钙沉淀和氢氧化钾,石灰乳是氢氧化钙浊液,大部分氢氧化
钙以固体形式存在,保留化学式,离子方程式为: ,D错误;
故选B。11. 在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
【答案】D
【解析】
【详解】A. 具有强氧化性, 在 中燃烧只能生成 ,A错误;
B. 难溶于水,常温下不能与水反应生成 ,B错误;
C. 在 中点燃,生成 ,C错误;
D.向 溶液中通入 生成 ,向 溶液中通入 生成 ,D正确;
故选D。
12. 下列“实验结论”与“实验操作及现象”对应正确的是
选项 实验操作及现象 实验结论
A 收集一试管气体,“扇闻”闻到刺激性气味 该气体一定为
B 取少量待测液于试管中,加入适量 溶液,生成白色沉淀 该溶液中一定含有
取少量待测液于试管中,加入适量 溶液,生成白色沉
C 该溶液中一定含有
淀
D 取少量待测液于试管中,滴加几滴紫色石蕊试液,溶液呈红色 该溶液中一定含有
A. A B. B C. C D. D
【答案】D
【解析】【详解】A.有刺激性气味的气体不一定是 ,也可以是SO 等,A错误;
2
B.亚硫酸钡、碳酸钡、氯化银都是白色沉淀,向某溶液中加入 溶液,生成白色沉淀,溶液中不一
定含有 ,B错误;
C.碳酸银也是白色沉淀,向某溶液中加入 溶液,生成白色沉淀,该溶液中不一定含有 ,C错
误;
D.溶液呈酸性,溶液中一定含有 ,D正确;
答案选D。
13. 已知氯酸钠与浓盐酸反应生成氯气: ,下列关于该反应
的说法正确的是(用 表示阿伏加德罗常数的值)
A. 中含有 数目为
B. 中含有离子数目为
C. 常温常压下,每生成 转移电子数目为
D. 标准状况下, 中含氢原子数目为
【答案】C
【解析】
【详解】A. 是由 和 组成,不含有 ,A项错误;
B. 的物质的量为 , 中含有离子数目为 ,B项错误;
C.常温常压下, 的物质的量为 ,每生成 转移电子数目为 ,C项正确;
D.标准状况下, 不是气体,不能用气体摩尔体积计算水的物质的量,D项错误;
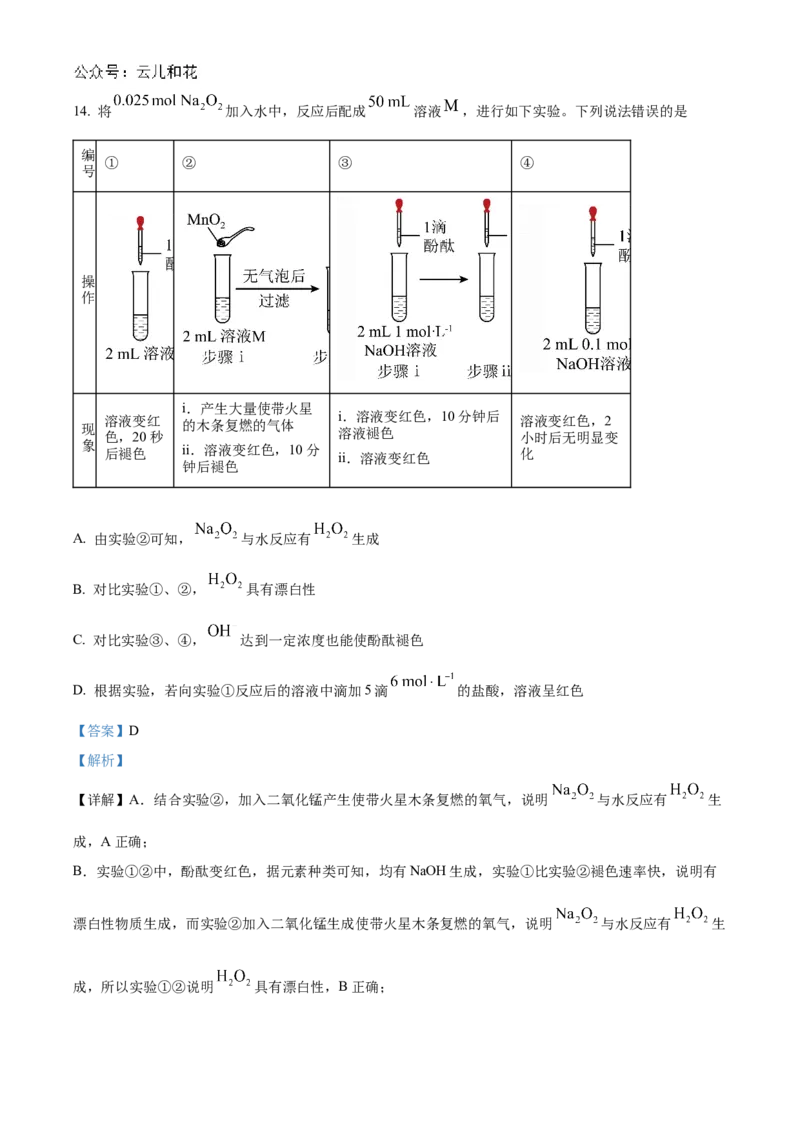
答案选C。14. 将 加入水中,反应后配成 溶液 ,进行如下实验。下列说法错误的是
编
① ② ③ ④
号
操
作
i.产生大量使带火星
溶液变红
i.溶液变红色,10分钟后
溶液变红色,2
现 色,20秒 的木条复燃的气体 溶液褪色 小时后无明显变
象
ii.溶液变红色,10分
后褪色 ii.溶液变红色 化
钟后褪色
A. 由实验②可知, 与水反应有 生成
B. 对比实验①、②, 具有漂白性
C. 对比实验③、④, 达到一定浓度也能使酚酞褪色
D. 根据实验,若向实验①反应后的溶液中滴加5滴 的盐酸,溶液呈红色
【答案】D
【解析】
【详解】A.结合实验②,加入二氧化锰产生使带火星木条复燃的氧气,说明 与水反应有 生
成,A正确;
B.实验①②中,酚酞变红色,据元素种类可知,均有NaOH生成,实验①比实验②褪色速率快,说明有
漂白性物质生成,而实验②加入二氧化锰生成使带火星木条复燃的氧气,说明 与水反应有 生
成,所以实验①②说明 具有漂白性,B正确;C.对比实验③、④可知, 的 溶液能使酚酞先变红后褪色,加入盐酸中和部分 后
溶液又恢复红色,实验①中 的 溶液不能使酚酞褪色,综合推断, 达到一定浓度也
能使酚酞褪色,C正确;
D.实验①中溶液褪色的主要原因是生成强氧化性的过氧化氢,将有色物质氧化为无色物质,与 溶
液浓度大小没有关系,向实验①反应后溶液中滴加5滴 的盐酸,消耗的是溶液中的 ,所
以溶液不会变红,D错误;
故选D。
二、非选择题(本题共4小题,共58分)
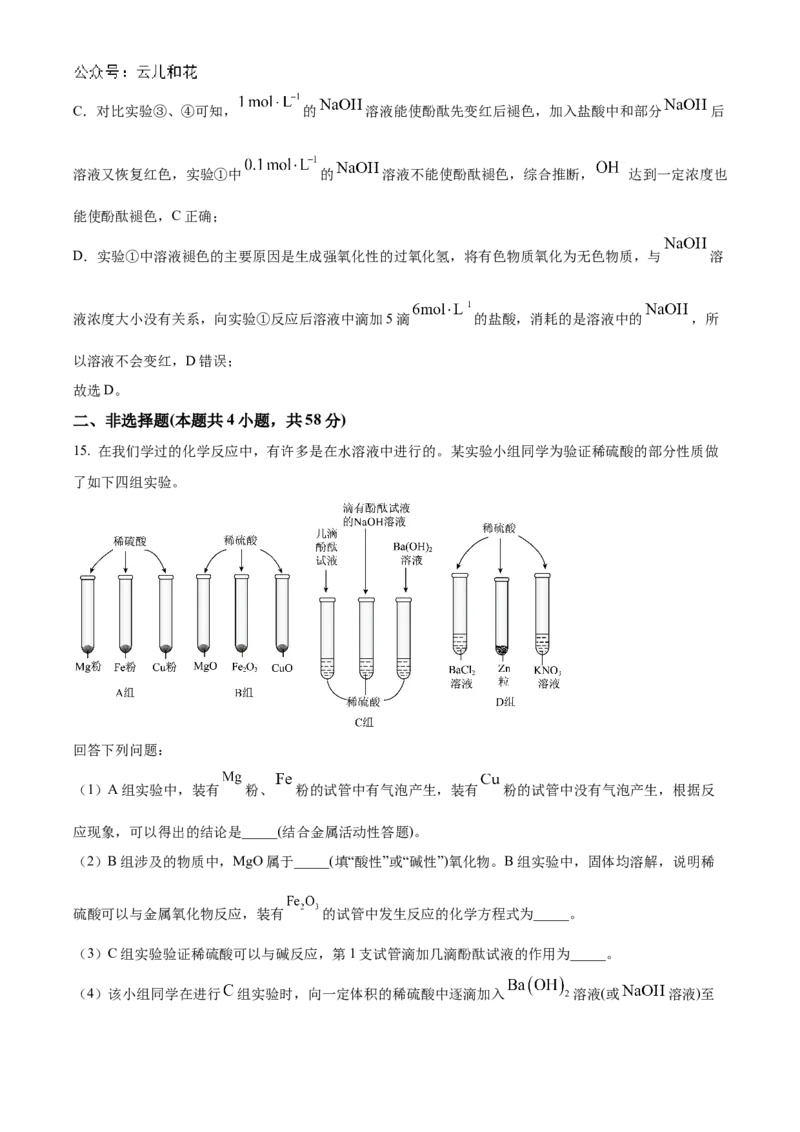
15. 在我们学过的化学反应中,有许多是在水溶液中进行的。某实验小组同学为验证稀硫酸的部分性质做
了如下四组实验。
回答下列问题:
(1)A组实验中,装有 粉、 粉的试管中有气泡产生,装有 粉的试管中没有气泡产生,根据反
应现象,可以得出的结论是_____(结合金属活动性答题)。
(2)B组涉及的物质中,MgO属于_____(填“酸性”或“碱性”)氧化物。B组实验中,固体均溶解,说明稀
硫酸可以与金属氧化物反应,装有 的试管中发生反应的化学方程式为_____。
(3)C组实验验证稀硫酸可以与碱反应,第1支试管滴加几滴酚酞试液的作用为_____。
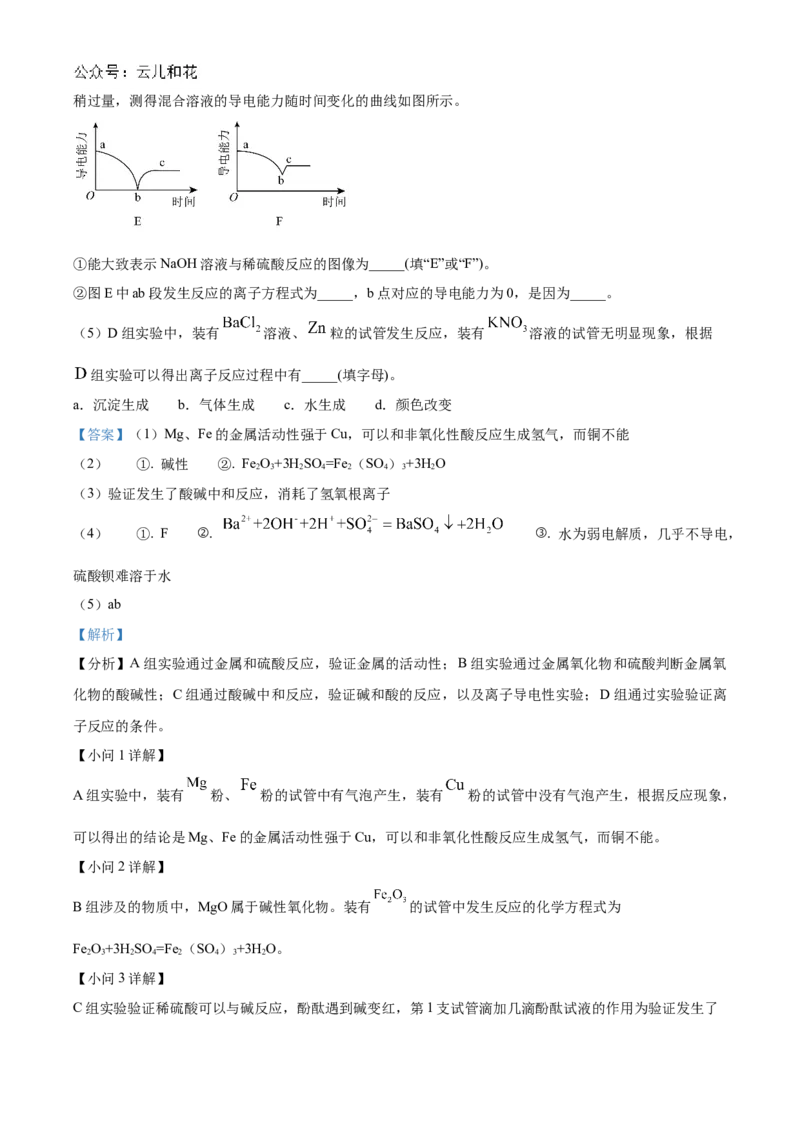
(4)该小组同学在进行 组实验时,向一定体积的稀硫酸中逐滴加入 溶液(或 溶液)至稍过量,测得混合溶液的导电能力随时间变化的曲线如图所示。
①能大致表示NaOH溶液与稀硫酸反应的图像为_____(填“E”或“F”)。
②图E中ab段发生反应的离子方程式为_____,b点对应的导电能力为0,是因为_____。
(5)D组实验中,装有 溶液、 粒的试管发生反应,装有 溶液的试管无明显现象,根据
组实验可以得出离子反应过程中有_____(填字母)。
a.沉淀生成 b.气体生成 c.水生成 d.颜色改变
【答案】(1)Mg、Fe的金属活动性强于Cu,可以和非氧化性酸反应生成氢气,而铜不能
(2) ①. 碱性 ②. Fe O+3H SO =Fe (SO )+3H O
2 3 2 4 2 4 3 2
(3)验证发生了酸碱中和反应,消耗了氢氧根离子
(4) ①. F ②. ③. 水为弱电解质,几乎不导电,
硫酸钡难溶于水
(5)ab
【解析】
【分析】A组实验通过金属和硫酸反应,验证金属的活动性;B组实验通过金属氧化物和硫酸判断金属氧
化物的酸碱性;C组通过酸碱中和反应,验证碱和酸的反应,以及离子导电性实验;D组通过实验验证离
子反应的条件。
【小问1详解】
A组实验中,装有 粉、 粉的试管中有气泡产生,装有 粉的试管中没有气泡产生,根据反应现象,
可以得出的结论是Mg、Fe的金属活动性强于Cu,可以和非氧化性酸反应生成氢气,而铜不能。
【小问2详解】
B组涉及的物质中,MgO属于碱性氧化物。装有 的试管中发生反应的化学方程式为
Fe O+3H SO =Fe (SO )+3H O。
2 3 2 4 2 4 3 2
【小问3详解】
C组实验验证稀硫酸可以与碱反应,酚酞遇到碱变红,第1支试管滴加几滴酚酞试液的作用为验证发生了酸碱中和反应,消耗了氢氧根离子。
【小问4详解】
该小组同学在进行 组实验时,向一定体积的稀硫酸中逐滴加入 溶液和硫酸反应生成硫酸钡和
水,正好反应时导电能力接近于0,故E为氢氧化钡和硫酸反应,F为 溶液和硫酸反应。
①能大致表示NaOH溶液与稀硫酸反应的图像为F。
②图E中ab段为 溶液和硫酸反应生成硫酸钡和水,发生反应的离子方程式为
,b点对应的导电能力为0,是因为水为弱电解质,几乎不
导电,硫酸钡难溶于水。
【小问5详解】
D组实验中,装有 溶液加入硫酸反应生成硫酸钡沉淀, 粒和硫酸反应生成氢气,装有 溶
液加入硫酸既没有沉淀,也没有气体,故试管无明显现象,根据 组实验可以得出离子反应过程中有沉淀
生成或气体生成,故选ab。
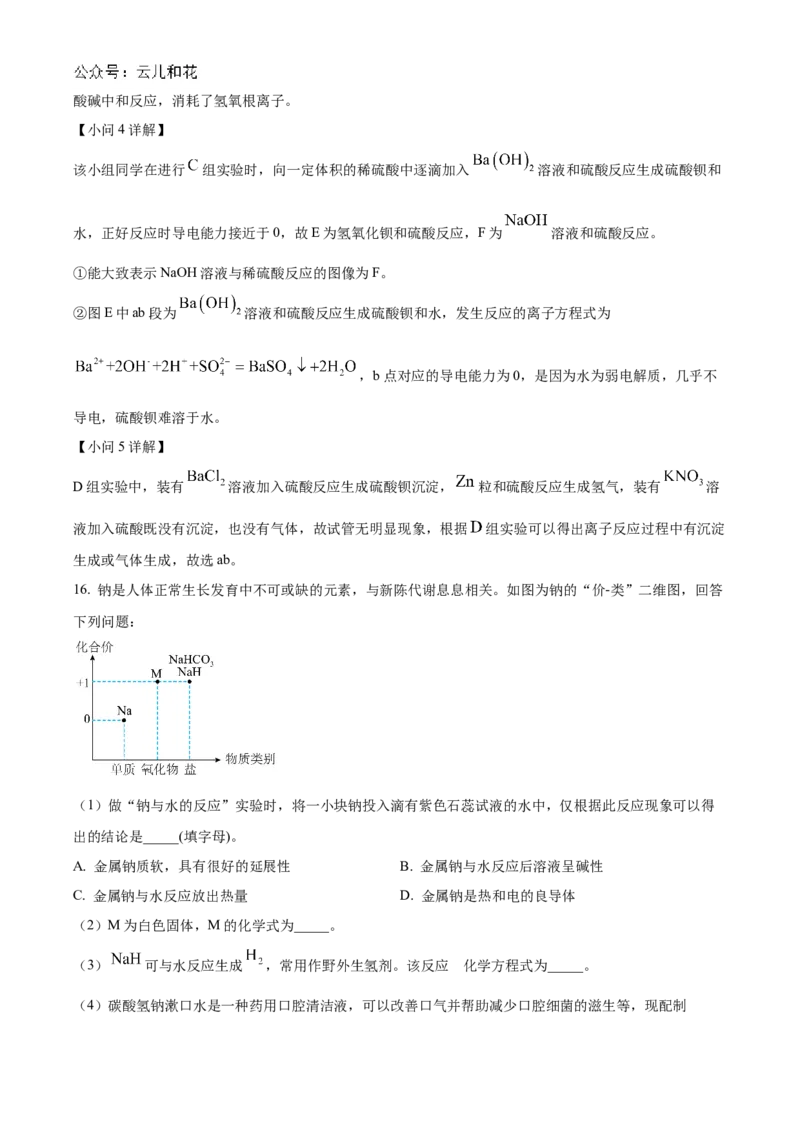
16. 钠是人体正常生长发育中不可或缺的元素,与新陈代谢息息相关。如图为钠的“价-类”二维图,回答
下列问题:
(1)做“钠与水的反应”实验时,将一小块钠投入滴有紫色石蕊试液的水中,仅根据此反应现象可以得
出的结论是_____(填字母)。
A. 金属钠质软,具有很好的延展性 B. 金属钠与水反应后溶液呈碱性
C. 金属钠与水反应放出热量 D. 金属钠是热和电的良导体
(2)M为白色固体,M的化学式为_____。
的
(3) 可与水反应生成 ,常用作野外生氢剂。该反应 化学方程式为_____。
(4)碳酸氢钠漱口水是一种药用口腔清洁液,可以改善口气并帮助减少口腔细菌的滋生等,现配制碳酸氢钠漱口水,操作过程如图所示。
①需用托盘天平称量的 的质量为_____g。
②“操作1”中 溶于水溶液温度_____(填“升高”或“降低”),故需待溶液温度恢复至室温再转
移。
③“操作2”中玻璃棒的作用为_____;“操作4”中待液面距离刻度线_____ 处,改用胶头滴管逐滴滴
加至溶液凹液面与刻度线相切。
④下列操作会使所配溶液物质的量浓度偏小的是_____(填字母)。
A.“操作2”中容量瓶使用前未干燥
B.“操作3”中烧杯洗涤液未转移到容量瓶中
C.“操作5”摇匀后静置,发现液面低于刻度线,继续加水至凹液面与刻度线相切
【答案】(1)BC (2)NaO
2
(3)
(4) ①. 5.0g ②. 降低 ③. 引流 ④. 1~2 ⑤. B
【解析】
【分析】银白色金属钠在空气中被氧气氧化,生成白色固体NaO,
2
【小问1详解】
A.钠投入滴有紫色石蕊试液的水中,没有表现质软,具有延展性,A不符合题意;
B.钠与水剧烈反应生成氢氧化钠与氢气,溶液呈碱性,溶液变蓝色,B符合题意;
C.金属钠与水反应放出氢气,小球在水面上迅速游动,可以得出反应放出热量,C符合题意;
D.金属钠与水剧烈反应生成氢氧化钠与氢气,但没有表现热和电的良导体,D不符合题意;
故选BC。
【小问2详解】
根据分析,M为NaO;
2
【小问3详解】中钠为+1价,氢元素的化合价为-1价,氢离子容易失云电子,作还原剂反应的化学方程式为
;
【小问4详解】
①配制 ,需要的 的质量,m=nM=cVM=0.06mol·L-1×1L×84g·mol-
1=5.04g,托盘天平称量的 的质量为5.0g;
② 溶于水吸热,溶液温度降低;
③“操作2”中玻璃棒的作用为引流;“操作4”中待液面距离刻度线1~2 处,改用胶头滴管逐滴滴加至溶
液凹液面与刻度线相切。
④A.“操作2”中容量瓶使用前未干燥,不影响浓度,A错误;
B.“操作3”中烧杯洗涤液未转移到容量瓶中,有溶质未转移到容量瓶,浓度偏低,B正确;
C.“操作5”摇匀后静置,发现液面低于刻度线,继续加水至凹液面与刻度线相切,加水过量,浓度偏低,
C错误;
故选B;
17. 食品添加剂的使用一定要严格按照标准执行。回答下列问题:
Ⅰ.白酒新国标中指出,不得使用非谷物食用酒精和食品添加剂。
(1)酒精的化学名称为乙醇( ),乙醇属于_____(填字母)。
A. 电解质 B. 氧化物 C. 化合物 D. 碱
(2)乙醇在空气中燃烧的化学方程式为_____。
(3)将一小块钠投入乙醇中,会缓慢产生氢气,发生反应的化学方程式为
,其中还原剂为_____(填化学式),每生成 ,转
移_____电子。
Ⅱ.葡萄酒酿制过程中,添加适量 既可以起到杀菌的作用,又可以作为抗氧化剂。
(4) 作为抗氧化剂是利用其_____(填“还原性”或“氧化性”)。(5) 可以与 气体发生反应生成 和 ,写出该反应的化学方程式并用单线桥表示电子转移的
方向和数目:_____。
(6)已知反应:① ;② 。
配平反应②:_____, 、 、 的还原性由强到弱的顺序为_____。
【答案】(1)C (2)C HOH+3O 2CO+3H O
2 5 2 2 2
(3) ①. Na ②. 4N
A
(4)还原性 (5)
(6) ①. 2Fe3++2I-=2Fe2++I ②. > >
2
【解析】
【小问1详解】
乙醇是非电解质,属于化合物,C正确;
【小问2详解】
乙醇在空气中燃烧生成二氧化碳和水,反应的化学方程式为:C HOH+3O 2CO+3H O;
2 5 2 2 2
【小问3详解】
Na与乙醇反应生成乙醇钠和氢气, ,Na的化合价由0价
升高到+1价,失去电子是还原剂,生成1molH 转移2mol电子,每生成2molH 转移4N 电子;
2 2 A
【小问4详解】
SO 具有还原性,可以做抗氧化剂;
2
【
小问5详解】
可以与HS气体发生反应生成S和HO,反应中HS失去电子,SO 得到电子,用单线桥表示的电子
2 2 2 2
转移方向和数目是: ;【小问6详解】
根据得失电子守恒、原子守恒和电荷守恒,Fe3+与I-反应的离子方程式为:2Fe3++2I-=2Fe2++I ;还原剂的还
2
原性大于还原产物,由①可知还原性SO >I-,由②可知还原性I->Fe2+,得出还原性由强到弱的顺序是:
2
> > 。
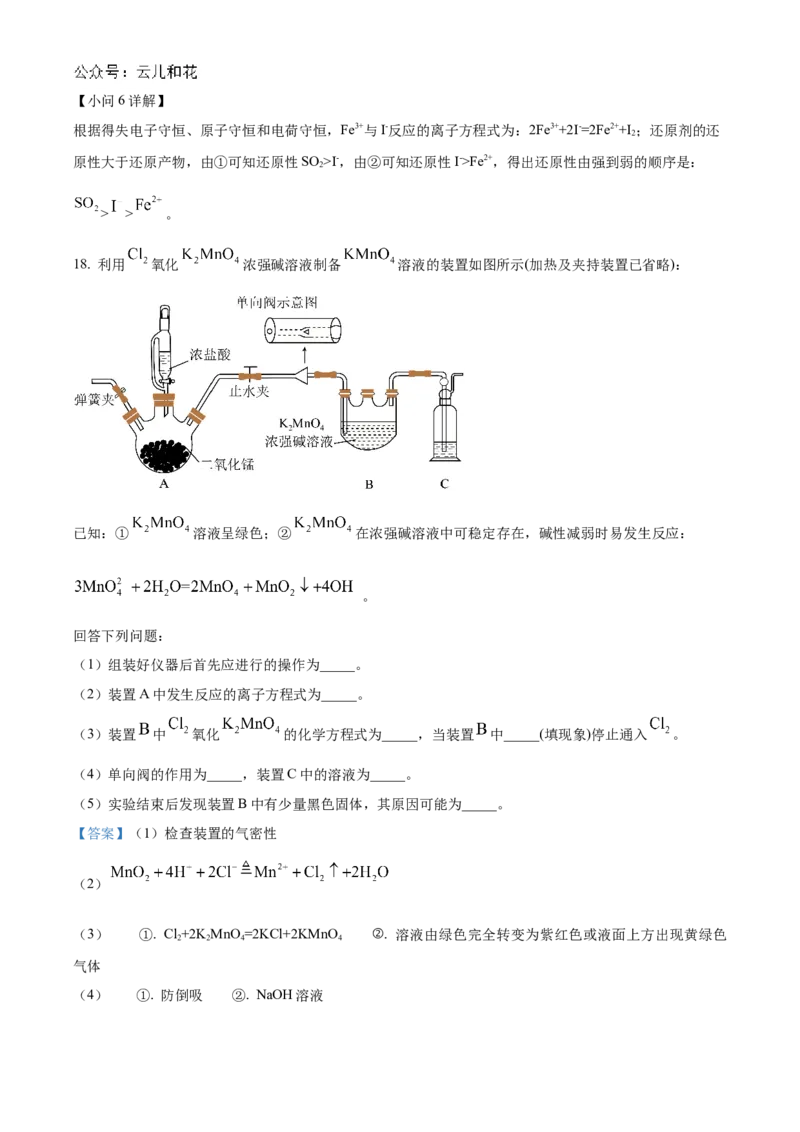
18. 利用 氧化 浓强碱溶液制备 溶液的装置如图所示(加热及夹持装置已省略):
已知:① 溶液呈绿色;② 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
。
回答下列问题:
(1)组装好仪器后首先应进行的操作为_____。
(2)装置A中发生反应的离子方程式为_____。
(3)装置 中 氧化 的化学方程式为_____,当装置 中_____(填现象)停止通入 。
(4)单向阀的作用为_____,装置C中的溶液为_____。
(5)实验结束后发现装置B中有少量黑色固体,其原因可能为_____。
【答案】(1)检查装置的气密性
(2)
(3) ①. Cl+2K MnO =2KCl+2KMnO ②. 溶液由绿色完全转变为紫红色或液面上方出现黄绿色
2 2 4 4
气体
(4) ①. 防倒吸 ②. NaOH溶液(5)浓盐酸易挥发,生成的氯气中混有HCl,直接导致B中溶液碱性减弱, 与水反应生成MnO
2
【解析】
【分析】由实验装置图可知,装置A中二氧化锰与浓盐酸共热反应制备氯气,浓盐酸具有挥发性,制得的
氯气中混有氯化氢,氯化氢会与装置B中浓碱反应导致碱性减弱,锰酸根离子在溶液中发生歧化反应,所
以实验时应在A、B之间增加盛有饱和食盐水的洗气瓶除去氯化氢,装置B中氯气与浓强碱溶液中的锰酸
钾反应制备高锰酸钾,装置C中盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气。
【小问1详解】
对于涉及气体制备的实验,组装好仪器后首先应进行的操作为:检查装置的气密性。
【小问2详解】
装置A中二氧化锰与浓盐酸共热反应制备氯气,离子方程式为:
。
【小问3详解】
由分析可知,装置B中氯气与浓强碱溶液中的锰酸钾反应制备高锰酸钾,反应的化学方程式为
Cl+2K MnO =2KCl+2KMnO ,由方程式可知,当装置B中绿色的锰酸钾溶液完全转变为紫红色高锰酸钾
2 2 4 4
溶液或液面上方出现黄绿色气体时,说明锰酸钾完全反应,应停止通氯气。
【小问4详解】
由示意图可知,单向阀只允许气体从左流向右,不允许溶液从右流向左,可以起到防倒吸的作用。装置C
中盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气。
【小问5详解】
已知 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
,生成MnO 黑色固体,则实验结束后发现装置B中有少量
2
黑色固体,其原因可能为:浓盐酸易挥发,生成的氯气中混有HCl,直接导致B中溶液碱性减弱,
与水反应生成MnO 。
2