文档内容
湖南省 2021 年普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在本试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
H:1C:12 N:14 O:16 F:19 Na:23 Mg:24Si:28 Cl:35.5 Ge:73 Br:80 I:127
一、选择题:本题共 10小题,每小题 3分,共 30 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 下列有关湘江流域的治理和生态修复的措施中,没有涉及到化学变化的是
A. 定期清淤,疏通河道
B. 化工企业“三废”处理后,达标排放
C. 利用微生物降解水域中的有毒有害物质
D. 河道中的垃圾回收分类后,进行无害化处理
2. 下列说法正确的是
A. 糖类、蛋白质均属于天然有机高分子化合物
B. FeO粉末在空气中受热,迅速被氧化成Fe O
3 4
C. SO 可漂白纸浆,不可用于杀菌、消毒
2
D. 镀锌铁皮的镀层破损后,铁皮会加速腐蚀
3. 下列实验设计不能达到实验目的的是
实验目的 实验设计
A 检验溶液中FeSO 是否被氧化 取少量待测液,滴加KSCN 溶液,观察溶液颜色变化
4
B 净化实验室制备的Cl 气体依次通过盛有饱和NaCl溶液、浓H SO 的洗气瓶
2 2 4
C 测定NaOH溶液的pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
第1页 | 共12页D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
A. A B. B C. C D. D
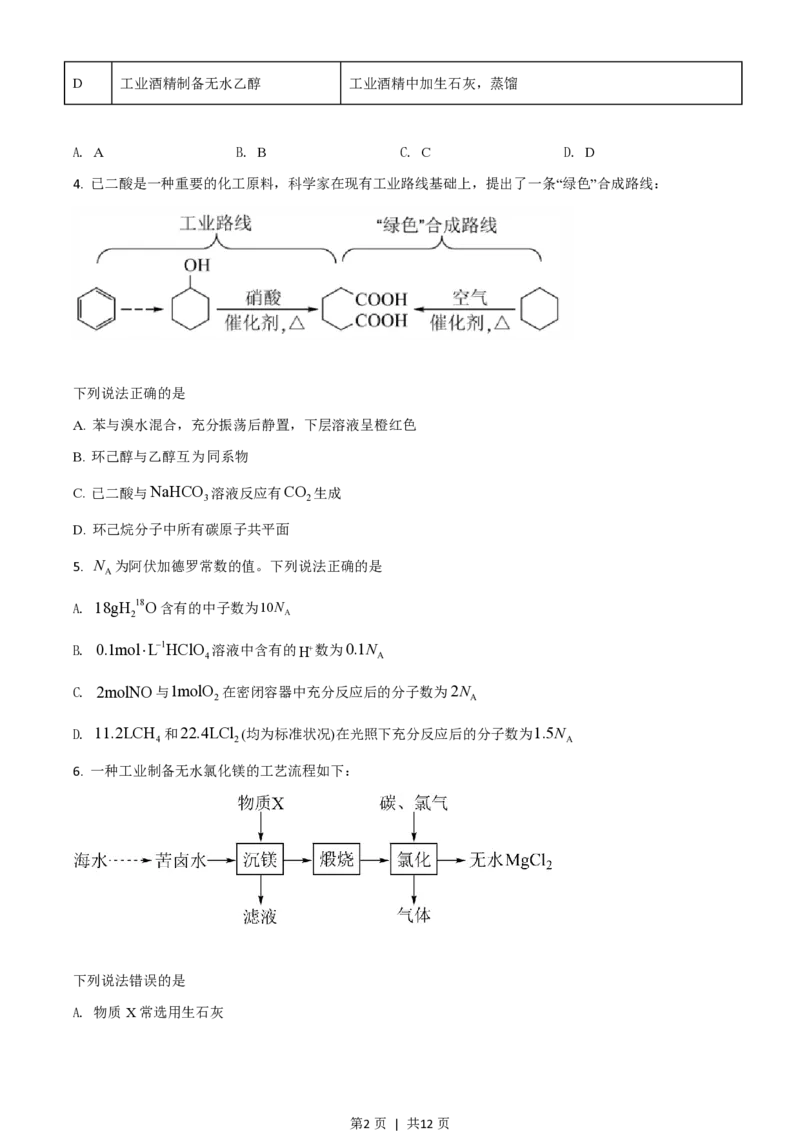
4. 已二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线:
下列说法正确的是
A. 苯与溴水混合,充分振荡后静置,下层溶液呈橙红色
B. 环己醇与乙醇互为同系物
C. 已二酸与NaHCO 溶液反应有CO 生成
3 2
D. 环己烷分子中所有碳原子共平面
5. N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 18gH 18O含有的中子数为10N
2 A
B. 0.1mol×L-1HClO 溶液中含有的H+数为0.1N
4 A
C. 2molNO与1molO 在密闭容器中充分反应后的分子数为2N
2 A
D. 11.2LCH 和22.4LCl (均为标准状况)在光照下充分反应后的分子数为1.5N
4 2 A
6. 一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是
A. 物质X常选用生石灰
第2页 | 共12页B. 工业上常用电解熔融MgCl 制备金属镁
2
高温
C. “氯化”过程中发生的反应为MgO+C+Cl MgCl +CO
2 2
D. “煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
7. W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数之和,Z的
最外层电子数为K层的一半,W与X可形成原子个数比为2:1的18e-分子。下列说法正确的是
A. 简单离子半径:Z>X>Y
B. W与Y能形成含有非极性键的化合物
C. X和Y的最简单氢化物的沸点:X>Y
D. 由W、X、Y三种元素所组成化合物的水溶液均显酸性
8. KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
3
Δ
6I +11KCIO +3H O 6KHIO +5KCl+3Cl 。下列说法错误的是
2 3 2 3 2 2
A. 产生22.4L(标准状况)Cl 时,反应中转移10mole-
2
B. 反应中氧化剂和还原剂的物质的量之比为11:6
C. 可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D. 可用酸化的淀粉碘化钾溶液检验食盐中IO-的存在
3
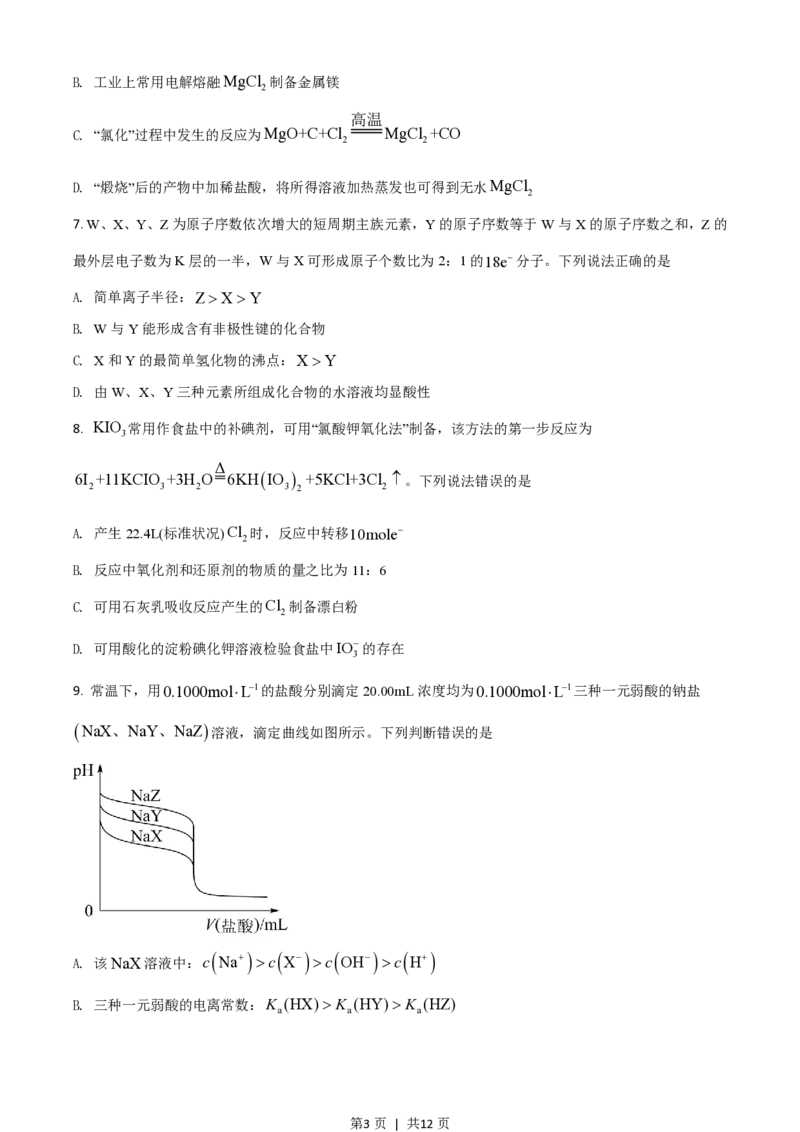
9. 常温下,用0.1000mol×L-1的盐酸分别滴定20.00mL浓度均为0.1000mol×L-1三种一元弱酸的钠盐
NaX、NaY、NaZ
溶液,滴定曲线如图所示。下列判断错误的是
A. 该NaX溶液中:c
Na+
>c
X-
>c
OH-
>c
H+
B. 三种一元弱酸的电离常数:K (HX)> K (HY)> K (HZ)
a a a
第3页 | 共12页C. 当pH=7时,三种溶液中:c
X-
=c
Y-
=c
Z-
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:c
X-
+c
Y-
+c
Z-
=c
H+
-c
OH-
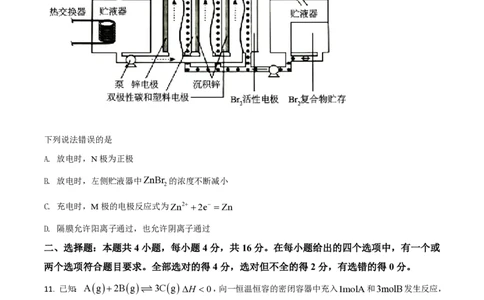
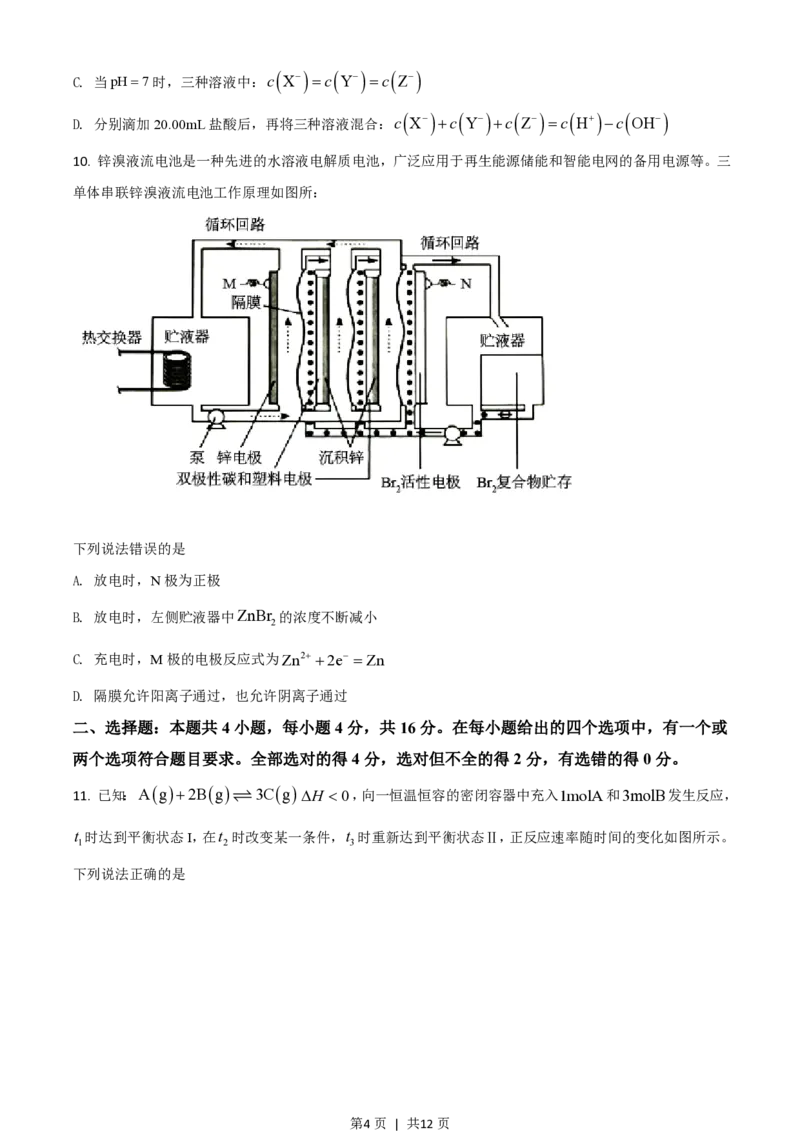
10. 锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网的备用电源等。三
单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A. 放电时,N极为正极
B. 放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C. 充电时,M极的电极反应式为Zn2+ +2e- =Zn
D. 隔膜允许阳离子通过,也允许阴离子通过
二、选择题:本题共 4小题,每小题 4分,共 16 分。在每小题给出的四个选项中,有一个或
两个选项符合题目要求。全部选对的得 4分,选对但不全的得 2分,有选错的得 0分。
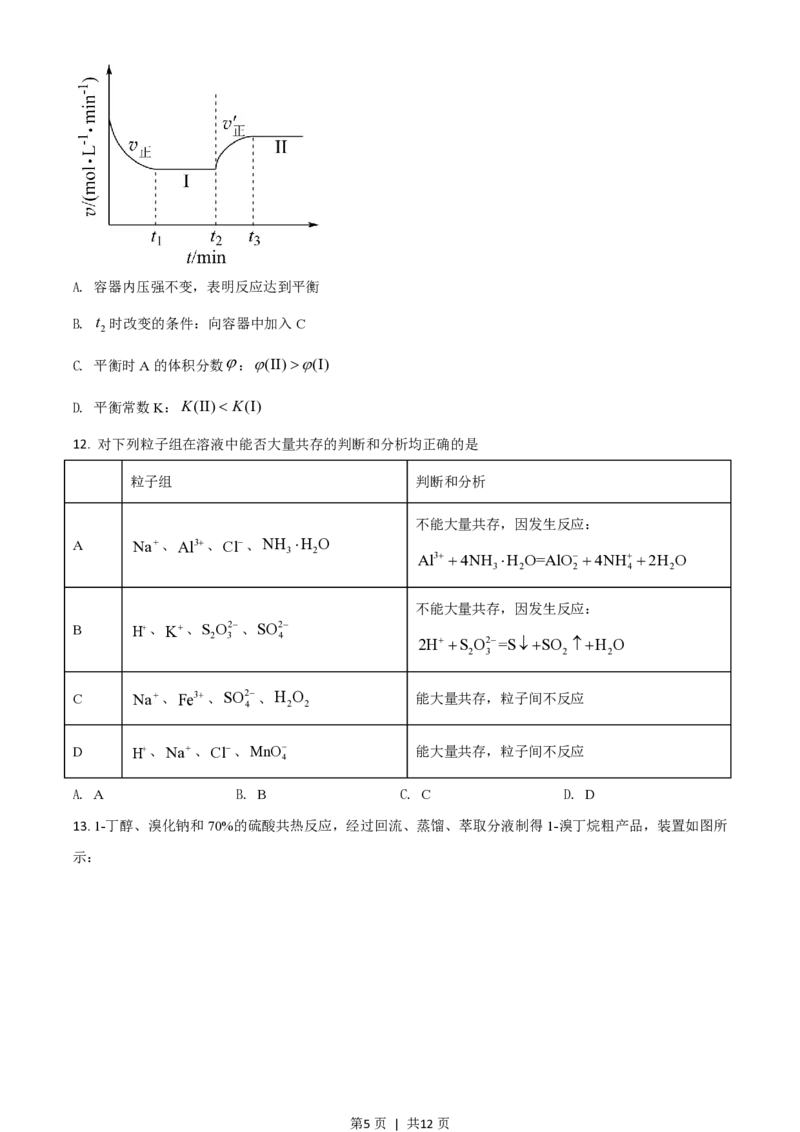
11. 已知:Ag+2Bg ƒ 3Cg DH <0,向一恒温恒容的密闭容器中充入1molA和3molB发生反应,
t 时达到平衡状态I,在t 时改变某一条件,t 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
1 2 3
下列说法正确的是
第4页 | 共12页A. 容器内压强不变,表明反应达到平衡
B. t 时改变的条件:向容器中加入C
2
C. 平衡时A的体积分数 j :j(II)>j(I)
D. 平衡常数K:K(II)< K(I)
12. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A Na+、Al3+、Cl-、NH ×H O
3 2
Al3+ +4NH ×H O=AlO- +4NH+ +2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H+、K+、S O2-、SO2-
2 3 4
2H+ +S O2-=S¯+SO +H O
2 3 2 2
C Na+、Fe3+、SO2-、H O 能大量共存,粒子间不反应
4 2 2
D H+、Na+、Cl-、MnO- 能大量共存,粒子间不反应
4
A. A B. B C. C D. D
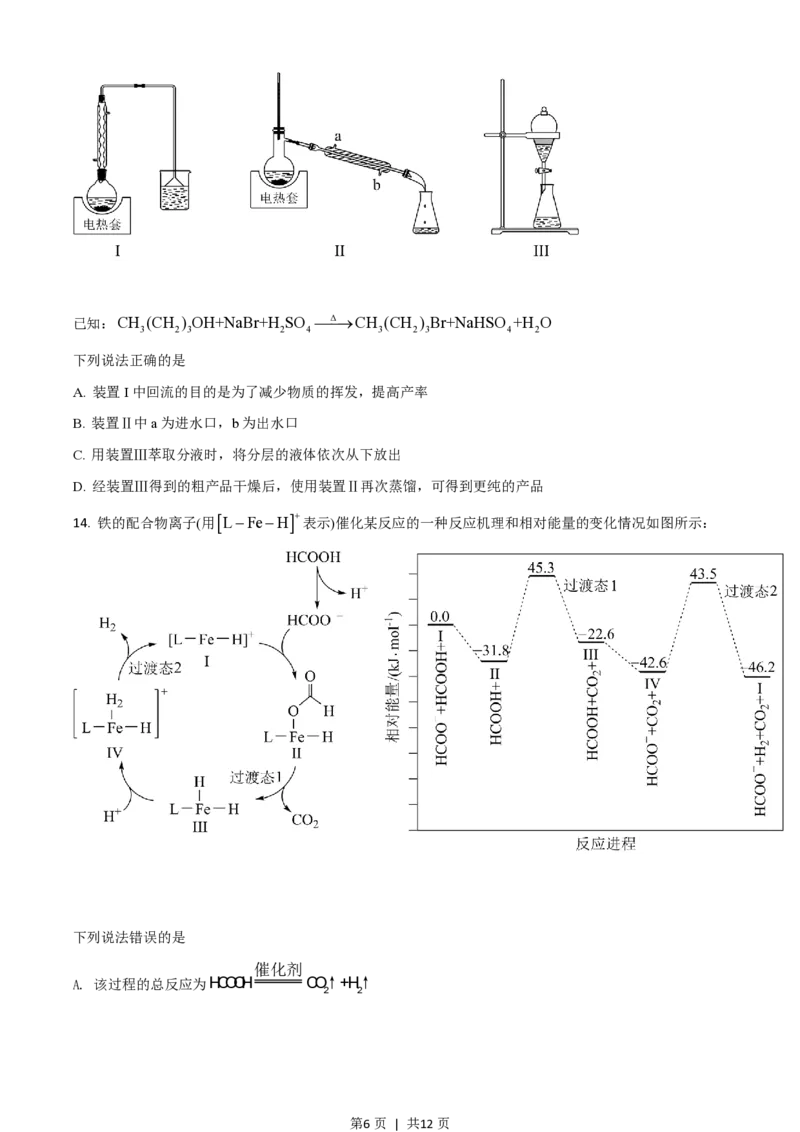
13. 1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴丁烷粗产品,装置如图所
示:
第5页 | 共12页已知:CH (CH ) OH+NaBr+H SO ¾Δ¾®CH (CH ) Br+NaHSO +H O
3 2 3 2 4 3 2 3 4 2
下列说法正确的是
A. 装置I中回流的目的是为了减少物质的挥发,提高产率
B. 装置Ⅱ中a为进水口,b为出水口
C. 用装置Ⅲ萃取分液时,将分层的液体依次从下放出
D. 经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
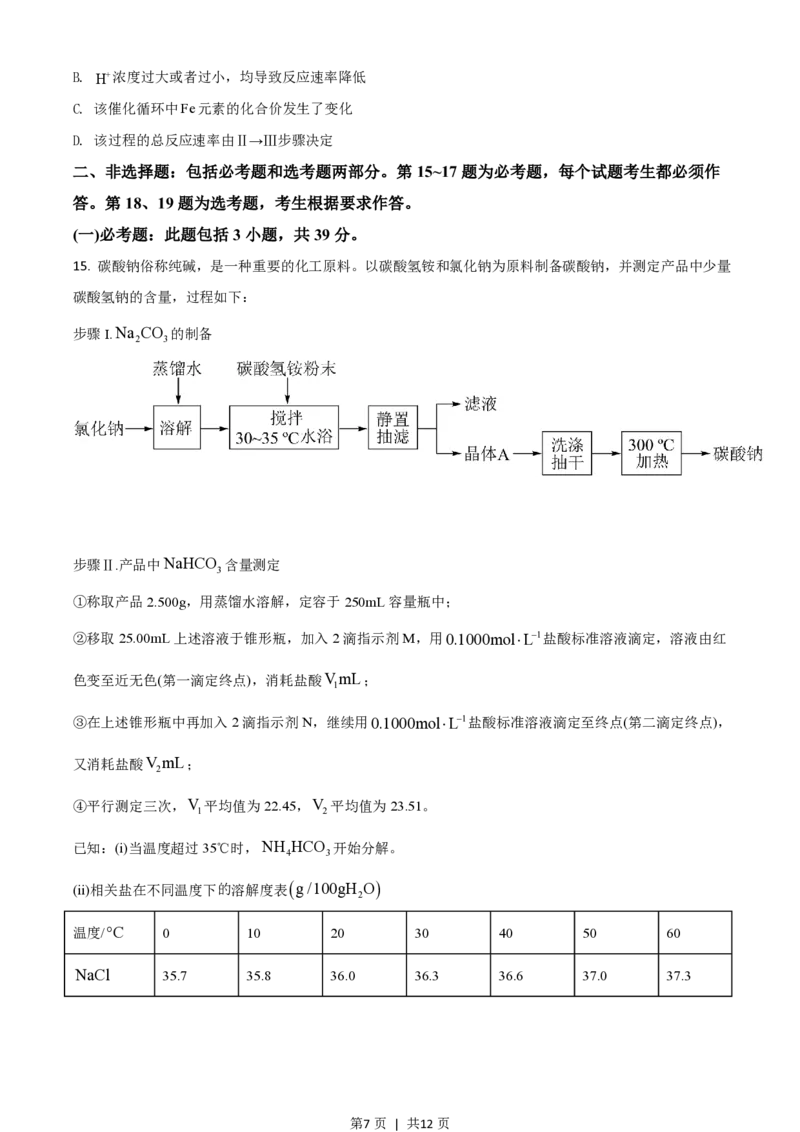
14.
铁的配合物离子(用L-Fe-H+
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
下列说法错误的是
催化剂
A. 该过程的总反应为HCOOH CO↑+H↑
2 2
第6页 | 共12页B. H+浓度过大或者过小,均导致反应速率降低
C. 该催化循环中Fe元素的化合价发生了变化
D. 该过程的总反应速率由Ⅱ→Ⅲ步骤决定
二、非选择题:包括必考题和选考题两部分。第 15~17题为必考题,每个试题考生都必须作
答。第 18、19题为选考题,考生根据要求作答。
(一)必考题:此题包括 3小题,共 39分。
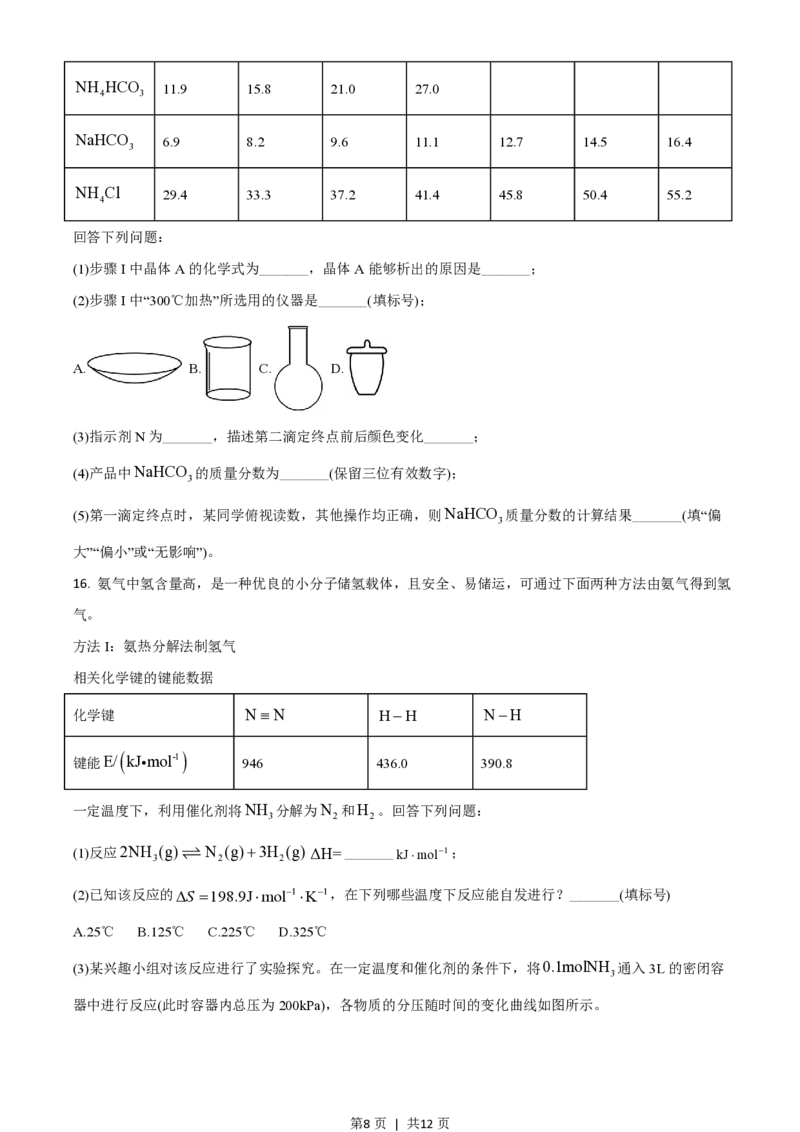
15. 碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量
碳酸氢钠的含量,过程如下:
步骤I.Na CO 的制备
2 3
步骤Ⅱ.产品中NaHCO 含量测定
3
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol×L-1盐酸标准溶液滴定,溶液由红
色变至近无色(第一滴定终点),消耗盐酸VmL;
1
③在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol×L-1盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸V mL;
2
④平行测定三次,V 平均值为22.45,V 平均值为23.51。
1 2
已知:(i)当温度超过35℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表 g/100gH O
2
温度/°C 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
第7页 | 共12页NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是_______;
(2)步骤I中“300℃加热”所选用的仪器是_______(填标号);
A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化_______;
(4)产品中NaHCO 的质量分数为_______(保留三位有效数字);
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO 质量分数的计算结果_______(填“偏
3
大”“偏小”或“无影响”)。
16. 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢
气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键 Nº N H-H N-H
键能E/
kJ g
mol-1
946 436.0 390.8
一定温度下,利用催化剂将NH 分解为N 和H 。回答下列问题:
3 2 2
(1)反应2NH 3 (g) ƒ N 2 (g)+3H 2 (g) ΔH=_______kJ×mol-1;
(2)已知该反应的DS =198.9J×mol-1×K-1,在下列哪些温度下反应能自发进行?_______(填标号)
A.25℃ B.125℃ C.225℃ D.325℃
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH 通入3L的密闭容
3
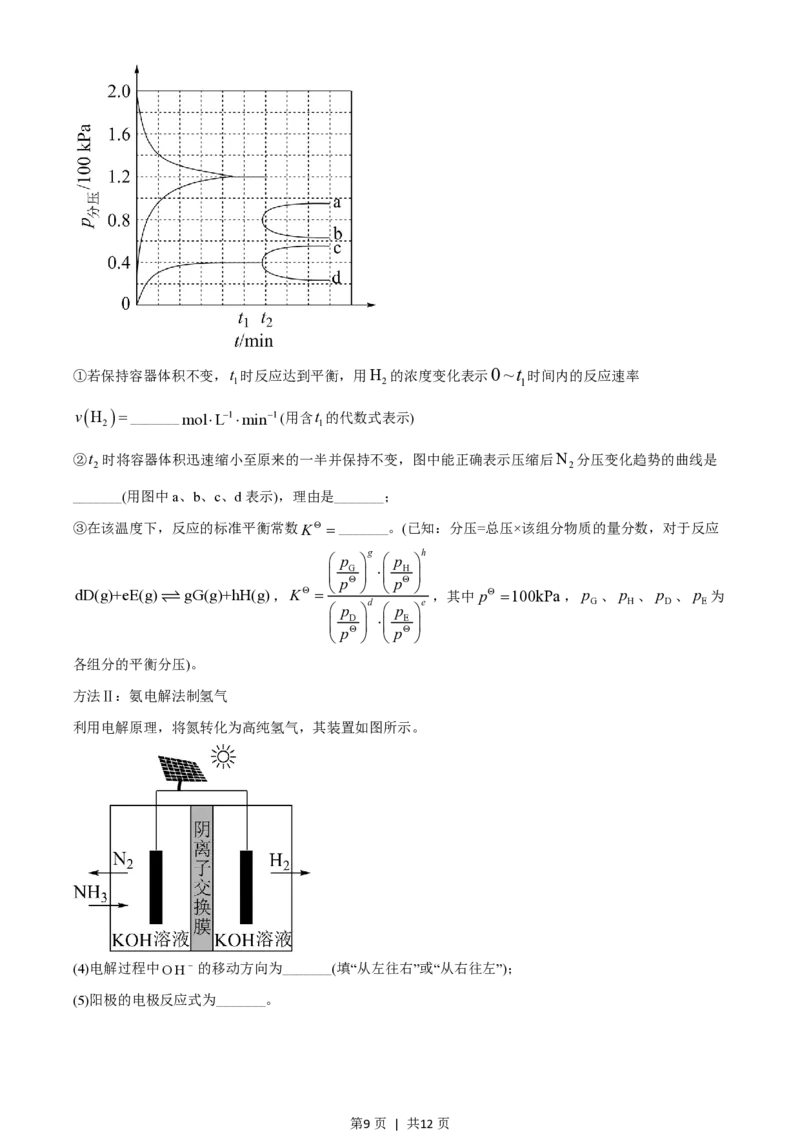
器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
第8页 | 共12页①若保持容器体积不变,t 时反应达到平衡,用H 的浓度变化表示0~t 时间内的反应速率
1 2 1
vH =_______mol×L-1×min-1(用含t
的代数式表示)
2 1
②t 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N 分压变化趋势的曲线是
2 2
_______(用图中a、b、c、d表示),理由是_______;
③在该温度下,反应的标准平衡常数KQ =_______。(已知:分压=总压×该组分物质的量分数,对于反应
g h
æ p ö æ p ö
G × H
ç ÷ ç ÷
è
pQ
ø è
pQ
ø
dD(g)+eE(g) gG(g)+hH(g),KQ = ,其中 pQ =100kPa, p 、 p 、 p 、 p 为
ƒ d e G H D E
æ p ö æ p ö
D × E
ç ÷ ç ÷
è
pQ
ø è
pQ
ø
各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氮转化为高纯氢气,其装置如图所示。
(4)电解过程中OH- 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
第9页 | 共12页KOH溶液KOH溶液
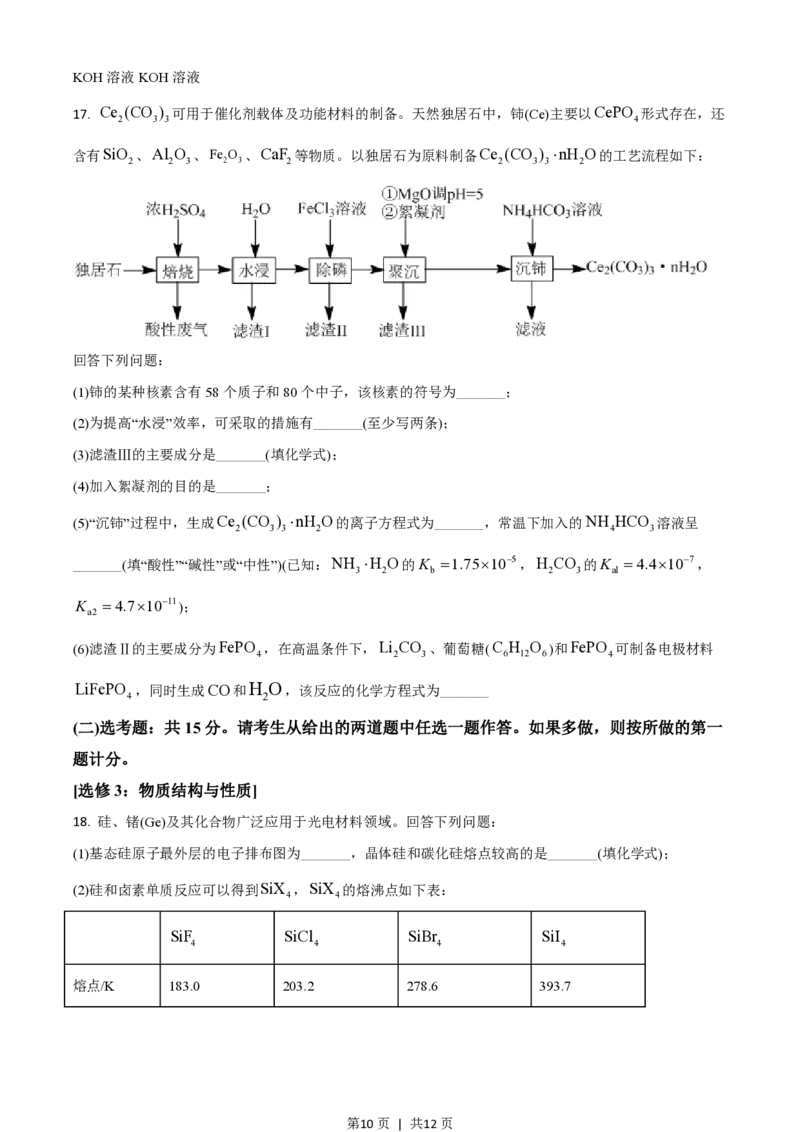
17. Ce (CO ) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO 形式存在,还
2 3 3 4
含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备Ce (CO ) ×nH O的工艺流程如下:
2 2 3 2 3 2 2 3 3 2
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成Ce (CO ) ×nH O的离子方程式为_______,常温下加入的NH HCO 溶液呈
2 3 3 2 4 3
_______(填“酸性”“碱性”或“中性”)(已知:NH ×H O的K =1.75´10-5,H CO 的K =4.4´10-7,
3 2 b 2 3 al
K =4.7´10-11);
a2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,Li CO 、葡萄糖(C H O )和FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和H O,该反应的化学方程式为_______
4 2
(二)选考题:共 15分。请考生从给出的两道题中任选一题作答。如果多做,则按所做的第一
题计分。
[选修 3:物质结构与性质]
18. 硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为_______,晶体硅和碳化硅熔点较高的是_______(填化学式);
(2)硅和卤素单质反应可以得到SiX ,SiX 的熔沸点如下表:
4 4
SiF SiCl SiBr SiI
4 4 4 4
熔点/K 183.0 203.2 278.6 393.7
第10页 | 共12页沸点/K 187.2 330.8 427.2 560.7
①0℃时,SiF 、SiCl 、SiBr 、SiI 呈液态的是____(填化学式),沸点依次升高的原因是_____,气态
4 4 4 4
SiX 分子的空间构型是_______;
4
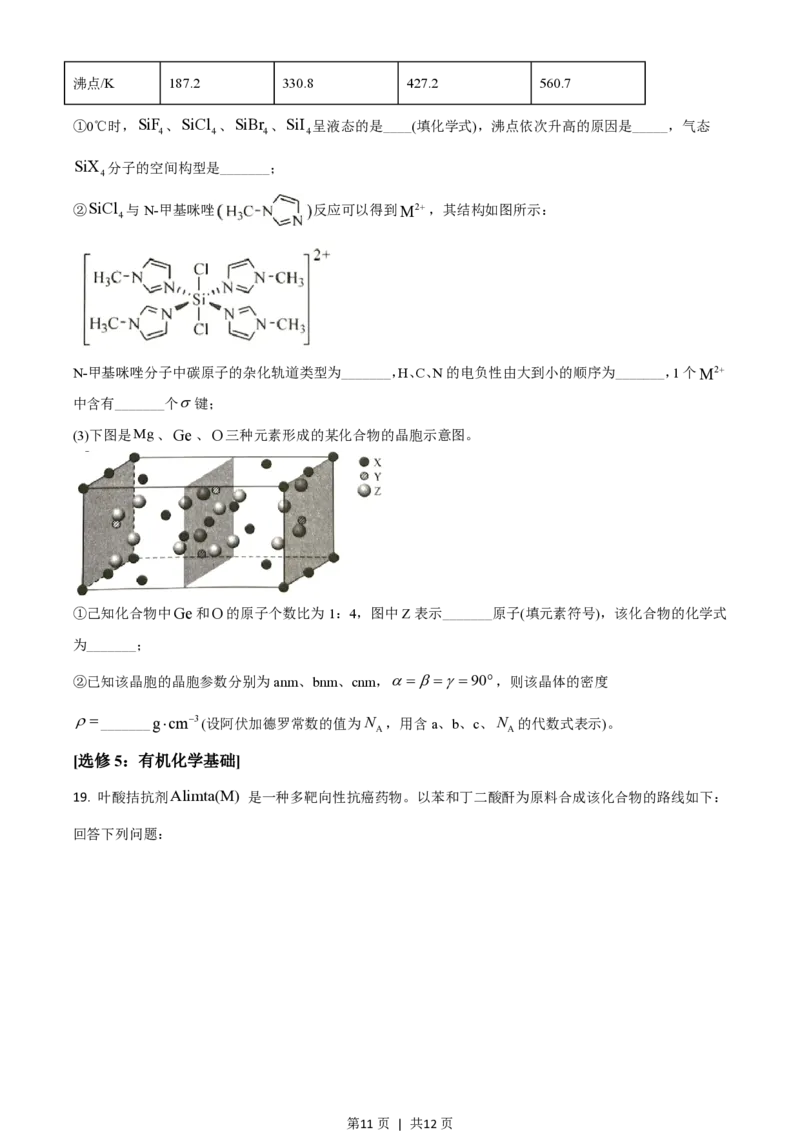
②SiCl 与N-甲基咪唑 反应可以得到M2+,其结构如图所示:
4
N-甲基咪唑分子中碳原子的杂化轨道类型为_______,H、C、N的电负性由大到小的顺序为_______,1个M2+
中含有_______个s键;
(3)下图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。
①己知化合物中Ge和O的原子个数比为1:4,图中Z表示_______原子(填元素符号),该化合物的化学式
为_______;
②已知该晶胞的晶胞参数分别为anm、bnm、cnm,a=b=g=90°,则该晶体的密度
r=_______g×cm-3(设阿伏加德罗常数的值为N ,用含a、b、c、N 的代数式表示)。
A A
[选修 5:有机化学基础]
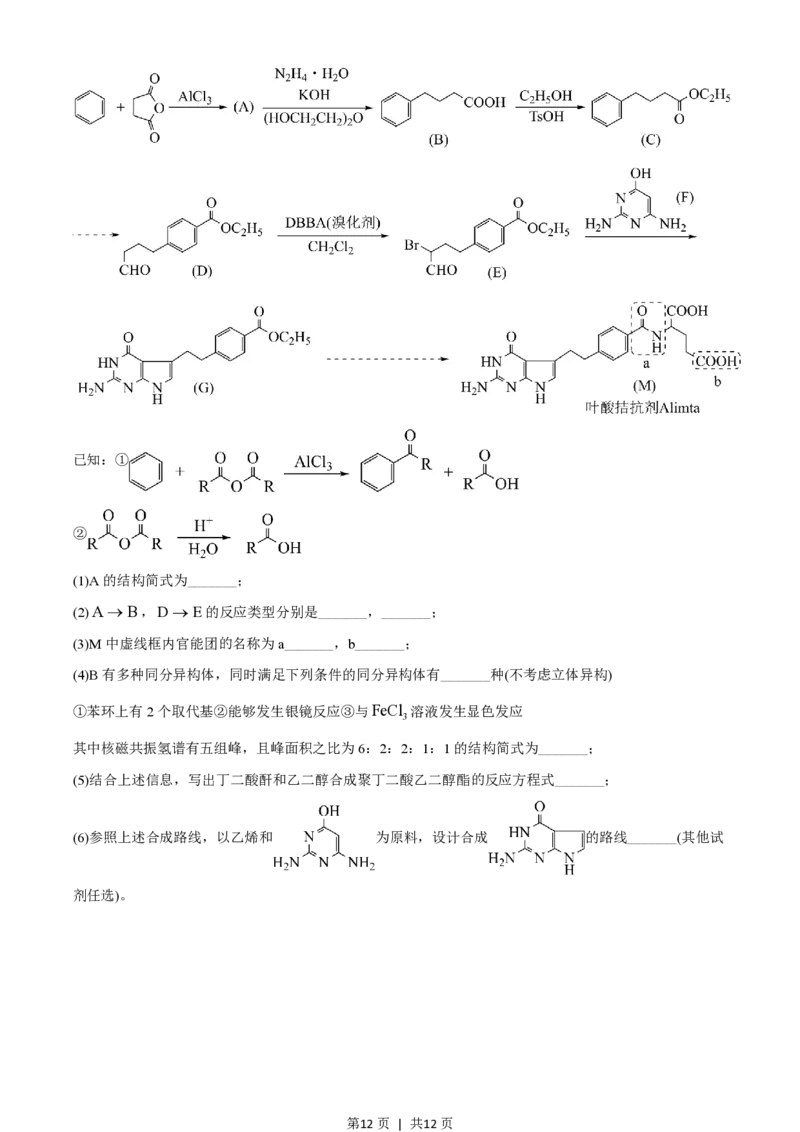
19. 叶酸拮抗剂Alimta(M) 是一种多靶向性抗癌药物。以苯和丁二酸酐为原料合成该化合物的路线如下:
回答下列问题:
第11页 | 共12页已知:①
②
(1)A的结构简式为_______;
(2)A®B,D®E的反应类型分别是_______,_______;
(3)M中虚线框内官能团的名称为a_______,b_______;
(4)B有多种同分异构体,同时满足下列条件的同分异构体有_______种(不考虑立体异构)
①苯环上有2个取代基②能够发生银镜反应③与FeCl 溶液发生显色发应
3
其中核磁共振氢谱有五组峰,且峰面积之比为6:2:2:1:1的结构简式为_______;
(5)结合上述信息,写出丁二酸酐和乙二醇合成聚丁二酸乙二醇酯的反应方程式_______;
(6)参照上述合成路线,以乙烯和 为原料,设计合成 的路线_______(其他试
剂任选)。
第12页 | 共12页