文档内容
2021年福建省新高考化学试卷
一、选择题:本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.(4分)建盏是久负盛名的陶瓷茶器,承载着福建历史悠久的茶文化。关于建盏,下列
说法错误的是( )
A.高速烧结过程包含复杂的化学变化
B.具有耐酸碱腐蚀、不易变形的优点
C.制作所用的黏土原料是人工合成的
D.属硅酸盐产品,含有多种金属元素
2.(4分)豆甾醇是中药半夏中含有的一种天然物所,其分子结构如图所示。关于豆甾醇,
下列说法正确的是( )
A.属于芳香族化合物
B.含有平面环状结构
C.可发生取代反应和加成反应
D.不能使酸性KMnO 溶液褪色
4
3.(4分)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1.12L C H 所含极性共价键的数目为0.2N
2 4 A
B.12g NaHSO 晶体中阴、阳离子总数为0.2N
4 A
C.0.1mol CH 与足量Cl 反应生成CH Cl的分子数为0.1N
4 2 3 A
D.电解熔融MgCl 制2.4g Mg,电路中通过的电子数为0.1N
2 A
4.(4分)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)
如图:
第1页 | 共8页下列说法错误的是
A.FeSO 的分解产物X为FeO
4
B.本流程涉及复分解反应
C.HNO 的沸点比H SO 的低
3 2 4
D.制备使用的铁锅易损坏
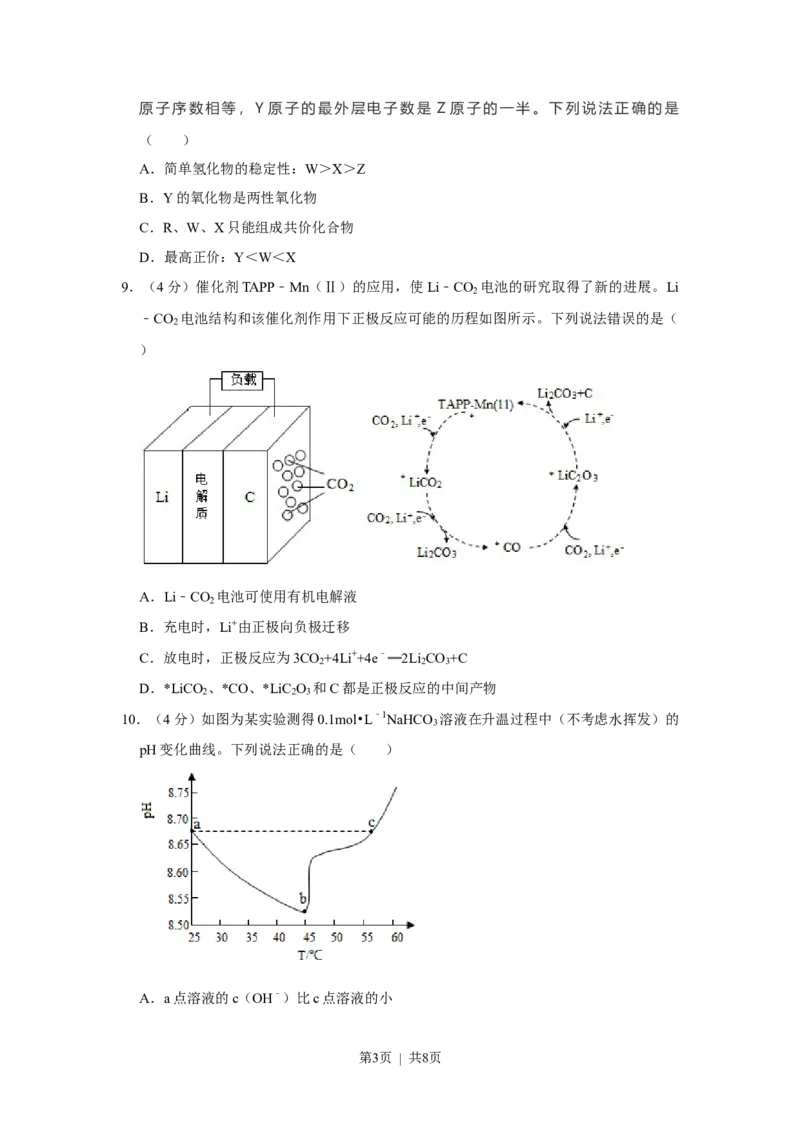
5.(4分)实验室配制碘水时,通常将I 溶于KI溶液:I (aq)+I﹣(aq) I ﹣(aq)。
2 2 3
关于该溶液,下列说法正确的是( ) ⇌
A.KI的电子式为
B.滴入淀粉溶液,不变蓝
C.加水稀释,平衡逆向移动
D.加少量AgNO 固体,平衡正向移动
3
6.(4分)室温下,下列各组离子一定能与指定溶液共存的是( )
A.0.2mol•L﹣1的NH Cl溶液:Na+、K+、SO 2﹣、SiO 2﹣
4 4 3
B.0.2mol•L﹣1的FeCl 溶液:NH +、Ca2+、Br﹣、SCN﹣
3 4
C.0.2mol•L﹣1的H SO 溶液:Mg2+、Fe2+、NO ﹣、Cl﹣
2 4 3
D.0.2mol•L﹣1的Ba(OH) 溶液:Na+、K+、Cl﹣、ClO﹣
2
7.(4分)利用下列装置和试剂进行实验,不能达到实验目的的是( )
A B C D
比较Zn与Cu的金属性 除去Cl 中的HCl并 制取乙酸乙酯(必要时 实验室制取氯气
2
强弱 干燥 可加沸石)
A.A B.B C.C D.D
8.(4分)某种食品膨松剂由原子序数依次增大的 R、W、X、Y、Z五种主族元素组
成。五种元素分处三个短周期,X、Z 同主族,R、W、X 的原子序数之和与 Z 的
第2页 | 共8页原子序数相等,Y 原子的最外层电子数是 Z 原子的一半。下列说法正确的是
( )
A.简单氢化物的稳定性:W>X>Z
B.Y的氧化物是两性氧化物
C.R、W、X只能组成共价化合物
D.最高正价:Y<W<X
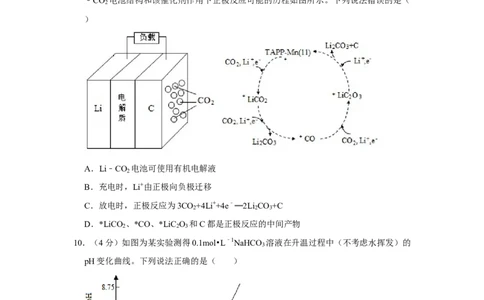
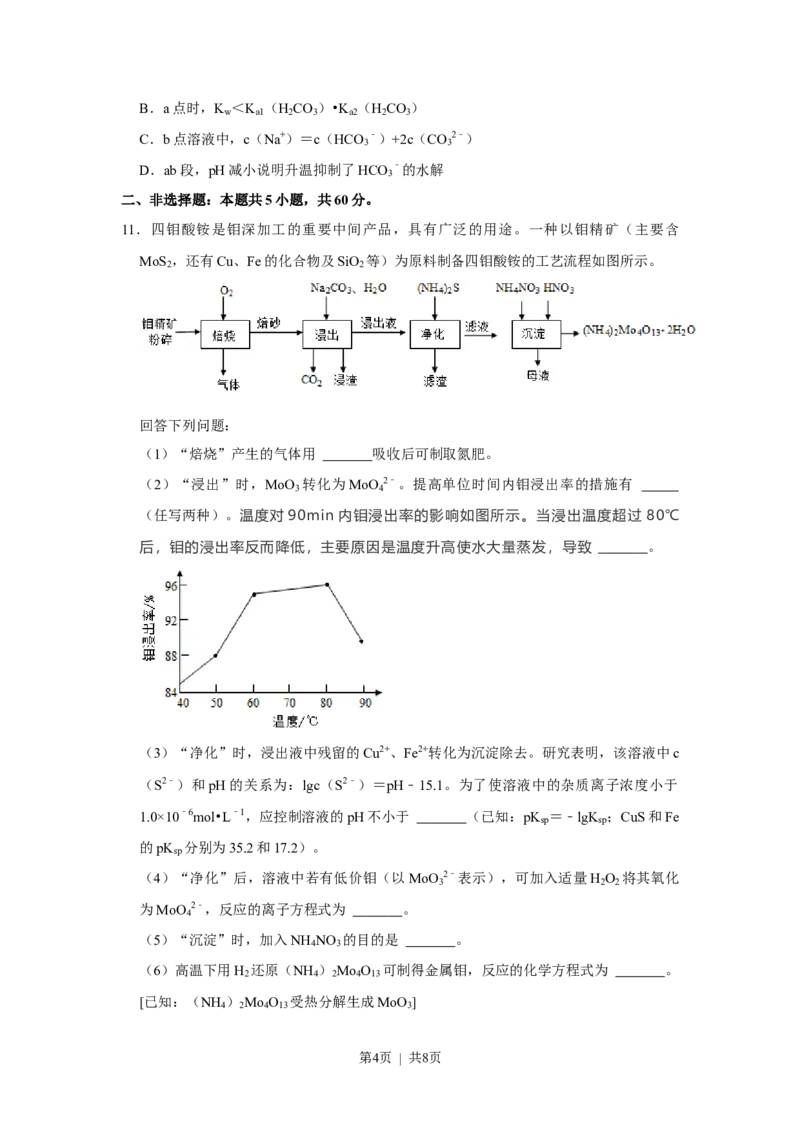
9.(4分)催化剂TAPP﹣Mn(Ⅱ)的应用,使Li﹣CO 电池的研究取得了新的进展。Li
2
﹣CO 电池结构和该催化剂作用下正极反应可能的历程如图所示。下列说法错误的是(
2
)
A.Li﹣CO 电池可使用有机电解液
2
B.充电时,Li+由正极向负极迁移
C.放电时,正极反应为3CO +4Li++4e﹣═2Li CO +C
2 2 3
D.*LiCO 、*CO、*LiC O 和C都是正极反应的中间产物
2 2 3
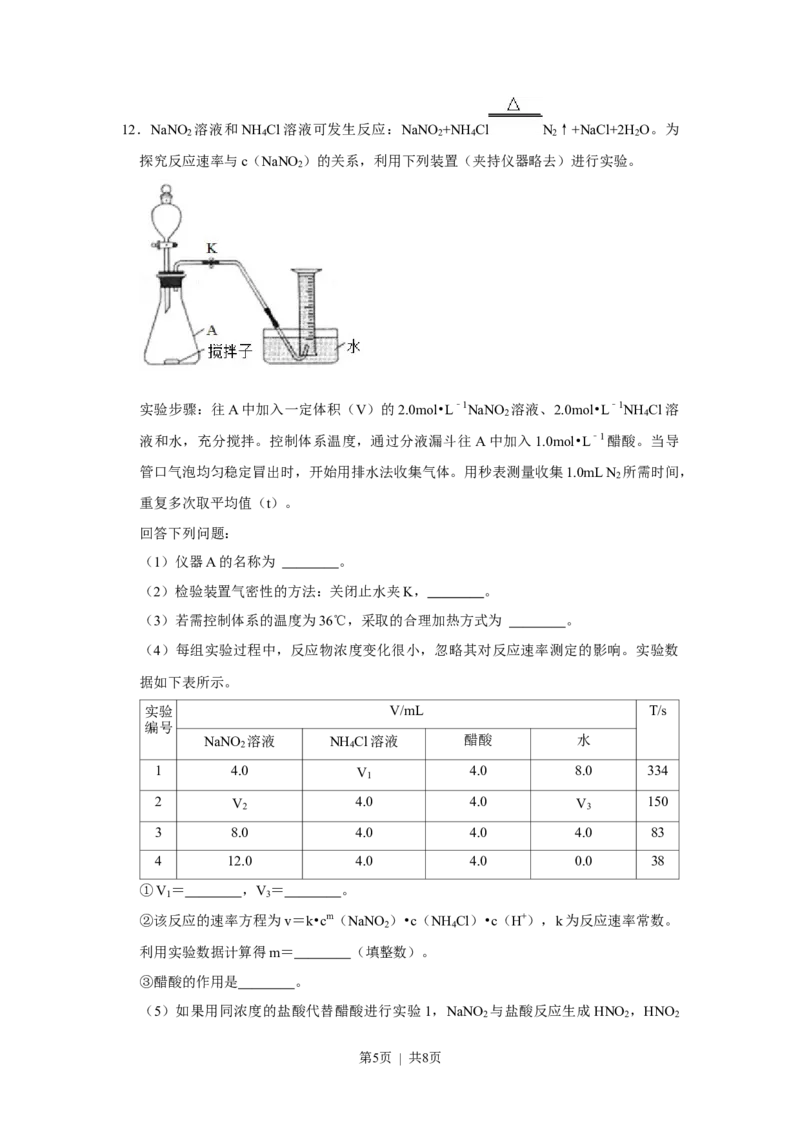
10.(4分)如图为某实验测得0.1mol•L﹣1NaHCO 溶液在升温过程中(不考虑水挥发)的
3
pH变化曲线。下列说法正确的是( )
A.a点溶液的c(OH﹣)比c点溶液的小
第3页 | 共8页B.a点时,K <K (H CO )•K (H CO )
w a1 2 3 a2 2 3
C.b点溶液中,c(Na+)=c(HCO ﹣)+2c(CO 2﹣)
3 3
D.ab段,pH减小说明升温抑制了HCO ﹣的水解
3
二、非选择题:本题共5小题,共60分。
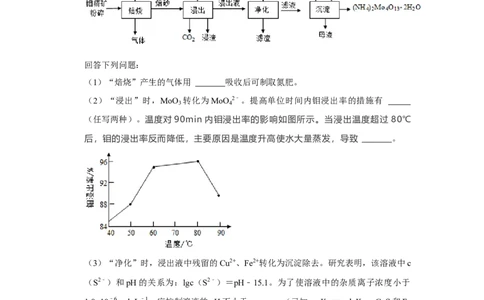
11.四钼酸铵是钼深加工的重要中间产品,具有广泛的用途。一种以钼精矿(主要含
MoS ,还有Cu、Fe的化合物及SiO 等)为原料制备四钼酸铵的工艺流程如图所示。
2 2
回答下列问题:
(1)“焙烧”产生的气体用 吸收后可制取氮肥。
(2)“浸出”时,MoO 转化为MoO 2﹣。提高单位时间内钼浸出率的措施有
3 4
(任写两种)。温度对 90min 内钼浸出率的影响如图所示。当浸出温度超过 80℃
后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致 。
(3)“净化”时,浸出液中残留的Cu2+、Fe2+转化为沉淀除去。研究表明,该溶液中c
(S2﹣)和pH的关系为:lgc(S2﹣)=pH﹣15.1。为了使溶液中的杂质离子浓度小于
1.0×10﹣6mol•L﹣1,应控制溶液的pH不小于 (已知:pK =﹣lgK ;CuS和Fe
sp sp
的pK 分别为35.2和17.2)。
sp
(4)“净化”后,溶液中若有低价钼(以MoO 2﹣表示),可加入适量H O 将其氧化
3 2 2
为MoO 2﹣,反应的离子方程式为 。
4
(5)“沉淀”时,加入NH NO 的目的是 。
4 3
(6)高温下用H 还原(NH ) Mo O 可制得金属钼,反应的化学方程式为 。
2 4 2 4 13
[已知:(NH ) Mo O 受热分解生成MoO ]
4 2 4 13 3
第4页 | 共8页12.NaNO 溶液和NH Cl溶液可发生反应:NaNO +NH Cl N ↑+NaCl+2H O。为
2 4 2 4 2 2
探究反应速率与c(NaNO )的关系,利用下列装置(夹持仪器略去)进行实验。
2
实验步骤:往A中加入一定体积(V)的2.0mol•L﹣1NaNO 溶液、2.0mol•L﹣1NH Cl溶
2 4
液和水,充分搅拌。控制体系温度,通过分液漏斗往 A中加入1.0mol•L﹣1醋酸。当导
管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集1.0mL N 所需时间,
2
重复多次取平均值(t)。
回答下列问题:
(1)仪器A的名称为 。
(2)检验装置气密性的方法:关闭止水夹K, 。
(3)若需控制体系的温度为36℃,采取的合理加热方式为 。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数
据如下表所示。
实验 V/mL T/s
编号
NaNO 溶液 NH Cl溶液 醋酸 水
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
①V = ,V = 。
1 3
②该反应的速率方程为v=k•cm(NaNO )•c(NH Cl)•c(H+),k为反应速率常数。
2 4
利用实验数据计算得m= (填整数)。
③醋酸的作用是 。
(5)如果用同浓度的盐酸代替醋酸进行实验1,NaNO 与盐酸反应生成HNO ,HNO
2 2 2
第5页 | 共8页分解产生等物质的量的两种气体。反应结束后,A中红棕色气体逐渐变浅,装置中还能
观察到的现象有 。HNO 分解的化学方程式为 。
2
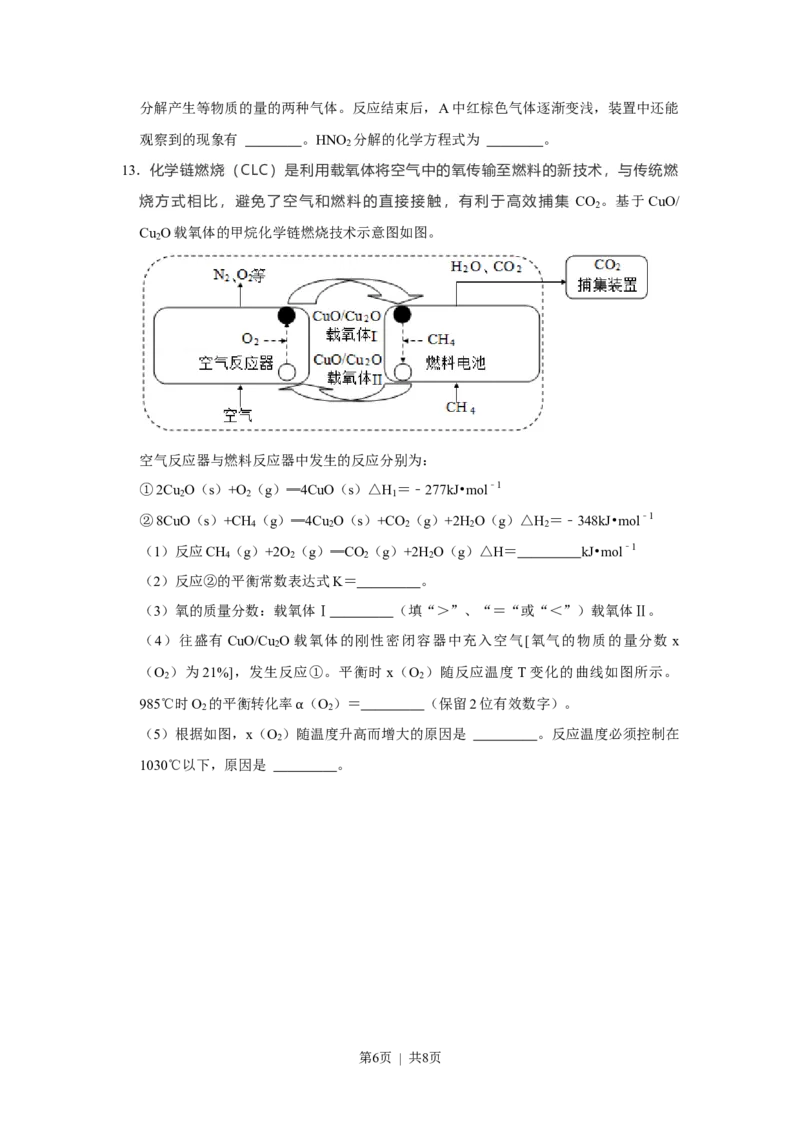
13.化学链燃烧(CLC)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃
烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 CO 。基于CuO/
2
Cu O载氧体的甲烷化学链燃烧技术示意图如图。
2
空气反应器与燃料反应器中发生的反应分别为:
①2Cu O(s)+O (g)═4CuO(s)△H =﹣277kJ•mol﹣1
2 2 1
②8CuO(s)+CH (g)═4Cu O(s)+CO (g)+2H O(g)△H =﹣348kJ•mol﹣1
4 2 2 2 2
(1)反应CH (g)+2O (g)═CO (g)+2H O(g)△H= kJ•mol﹣1
4 2 2 2
(2)反应②的平衡常数表达式K= 。
(3)氧的质量分数:载氧体Ⅰ (填“>”、“=“或“<”)载氧体Ⅱ。
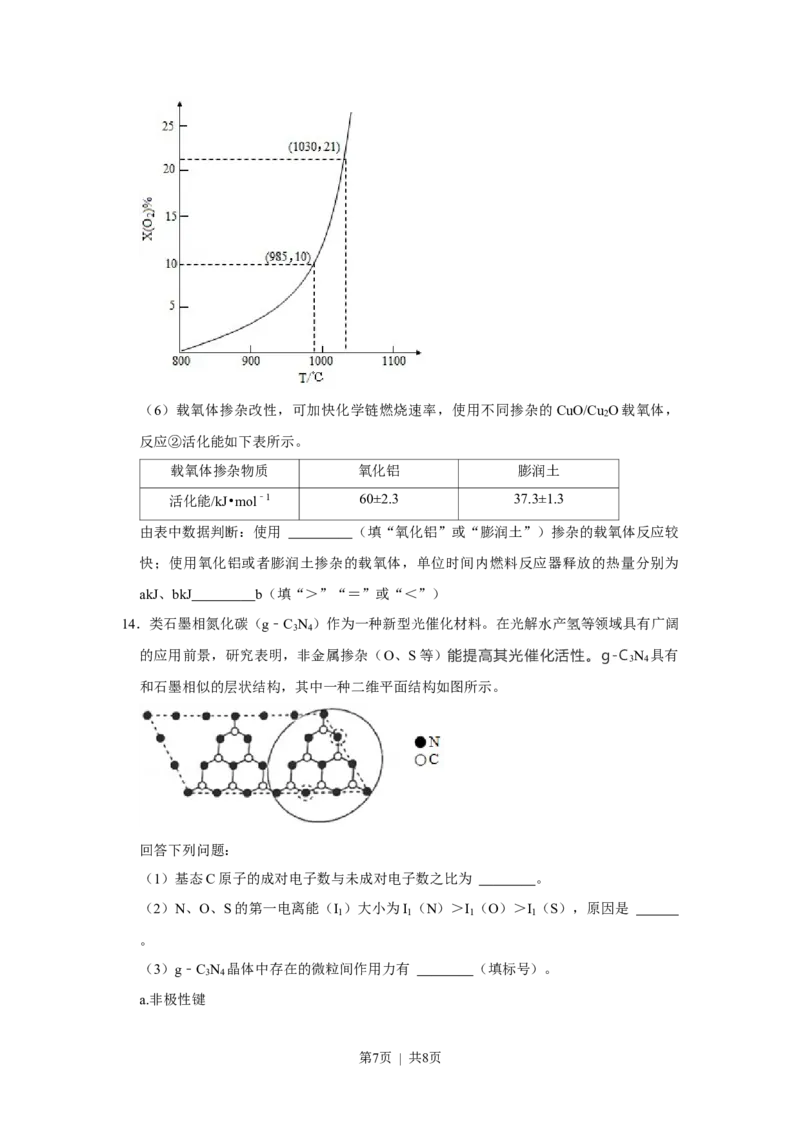
(4)往盛有 CuO/Cu O 载氧体的刚性密闭容器中充入空气[氧气的物质的量分数 x
2
(O )为21%],发生反应①。平衡时x(O )随反应温度T变化的曲线如图所示。
2 2
985℃时O 的平衡转化率 (O )= (保留2位有效数字)。
2 2
(5)根据如图,x(O
2
)α随温度升高而增大的原因是 。反应温度必须控制在
1030℃以下,原因是 。
第6页 | 共8页(6)载氧体掺杂改性,可加快化学链燃烧速率,使用不同掺杂的CuO/Cu O载氧体,
2
反应②活化能如下表所示。
载氧体掺杂物质 氧化铝 膨润土
活化能/kJ•mol﹣1 60±2.3 37.3±1.3
由表中数据判断:使用 (填“氧化铝”或“膨润土”)掺杂的载氧体反应较
快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为
akJ、bkJ b(填“>”“=”或“<”)
14.类石墨相氮化碳(g﹣C N )作为一种新型光催化材料。在光解水产氢等领域具有广阔
3 4
的应用前景,研究表明,非金属掺杂(O、S等)能提高其光催化活性。g-C N 具有
3 4
和石墨相似的层状结构,其中一种二维平面结构如图所示。
回答下列问题:
(1)基态C原子的成对电子数与未成对电子数之比为 。
(2)N、O、S的第一电离能(I )大小为I (N)>I (O)>I (S),原因是
1 1 1 1
。
(3)g﹣C N 晶体中存在的微粒间作用力有 (填标号)。
3 4
a.非极性键
第7页 | 共8页b.金属键
c. 键
d.π范德华力
(4)g﹣C N 中,C原子的杂化轨道类型为 ,N原子的配位数为 。
3 4
(5)每个基本结构单元(图中实线圈部分)中两个 N原子(图中虚线圈所示)被
O原子代替,形成O掺杂的g-C N (OPCN)。OPCN的化学式为 。
3 4
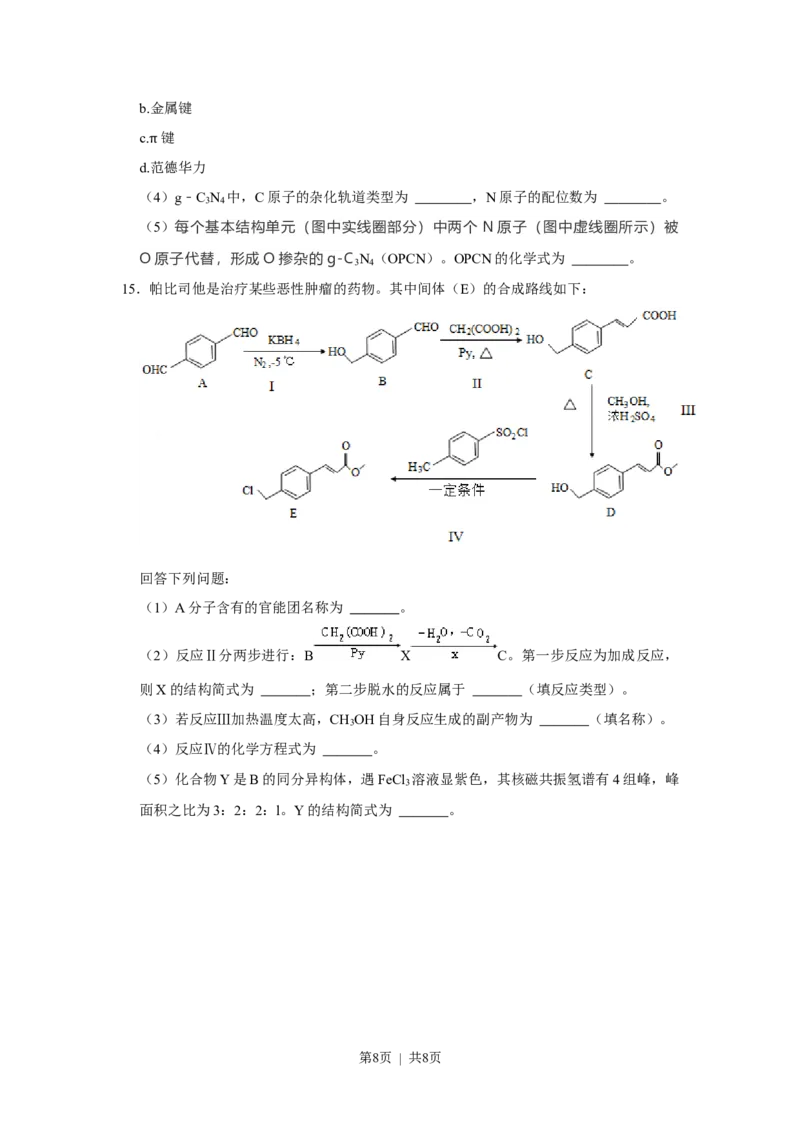
15.帕比司他是治疗某些恶性肿瘤的药物。其中间体(E)的合成路线如下:
回答下列问题:
(1)A分子含有的官能团名称为 。
(2)反应Ⅱ分两步进行:B X C。第一步反应为加成反应,
则X的结构简式为 ;第二步脱水的反应属于 (填反应类型)。
(3)若反应Ⅲ加热温度太高,CH OH自身反应生成的副产物为 (填名称)。
3
(4)反应Ⅳ的化学方程式为 。
(5)化合物Y是B的同分异构体,遇FeCl 溶液显紫色,其核磁共振氢谱有4组峰,峰
3
面积之比为3:2:2:l。Y的结构简式为 。
第8页 | 共8页