文档内容
2024 年上海市普通高中学业水平等级性考试化学试卷
(考试时间 60分钟,满分 100分)
注意:试卷为回忆版。试题来自网络,非官方渠道,学科网不对真实性负责,请自行鉴别。
一、氟及其化合物
氟元素及其化合物具有广泛用途。
1. 下列关于氟元素的性质说法正确的是
A. 原子半径最小 B. 原子第一电离能最大
C. 元素的电负性最强 D. 最高正化合价为+7
2. 下列关于18F与19F说法正确的是
A. 是同种核素 B. 是同素异形体
C. 19F比18F多一个电子 D. 19F比18F多一个中子
3. 萤石(CaF )与浓硫酸共热可制备HF气体,写出该反应的化学方程式:_______,该反应中体现浓硫酸
2
的性质是_______。
A.强氧化性 B.难挥发性 C.吸水性 D.脱水性
4. 液态氟化氢(HF)的电离方式为:3HF ƒ X+HF 2 ,其中X为_______。HF 2 的结构为F-H L F-,其中
F-与HF依靠_______相连接。
5. 回答下列问题:
(1)氟单质常温下能腐蚀Fe、Ag等金属,但工业上却可用Cu制容器储存,其原因是_______。
PtF 是极强的氧化剂,用Xe和PtF 可制备稀有气体离子化合物,六氟合铂氙[XeF]+Pt F - 的制备方
6 6 2 11
式如图所示
(2)上述反应中的催化剂为_______。
A. PtF B. PtF- C. F- D. XeF+
6 7
(3)上述过程中属于氧化还原反应的是_______。
第1页/共6页
学科网(北京)股份有限公司A. ② B. ③ C. ④ D. ⑤
(4)氟气通入氙(Xe)会产生XeF、XeF、XeF 三种氟化物气体。现将1mol的Xe和9mol的F 同时通
2 4 6 2
入50L的容器中,反应10min后,测得容器内共有8.9mol气体,且三种氟化物的比例为
XeF :XeF :XeF =1:6:3,则l0min内XeF 的速率vXeF = _______。
2 4 6 4 4
二、粗盐水的精制
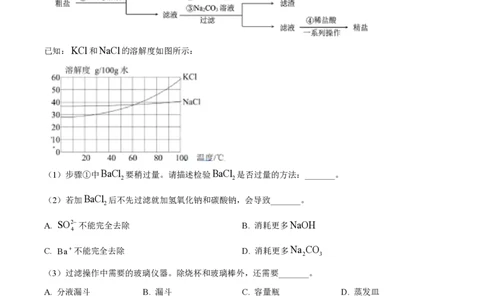
6. 粗盐中含有SO2-,K+,Ca2+,Mg2+等杂质离子,实验室按下面的流程进行精制:
4
已知:KCl和NaCl的溶解度如图所示:
(1)步骤①中BaCl 要稍过量。请描述检验BaCl 是否过量的方法:_______。
2 2
(2)若加BaCl 后不先过滤就加氢氧化钠和碳酸钠,会导致_______。
2
A. SO2-不能完全去除 B. 消耗更多NaOH
4
C. Ba+不能完全去除 D. 消耗更多Na CO
2 3
(3)过滤操作中需要的玻璃仪器。除烧杯和玻璃棒外,还需要_______。
A. 分液漏斗 B. 漏斗 C. 容量瓶 D. 蒸发皿
(4)步骤④中用盐酸调节pH至3~4,除去的离子有_______。
(5)“一系列操作”是指_______。
A. 蒸发至晶膜形成后,趁热过滤 B. 蒸发至晶膜形成后,冷却结晶
C. 蒸发至大量晶体析出后,趁热过滤 D. 蒸发至大量晶体析出后,冷却结晶
(6)请用离子方程式表示加入盐酸后发生的反应_______。
另有两种方案选行粗盐提纯。
第2页/共6页
学科网(北京)股份有限公司方案2:向粗盐水中加入石灰乳[主要成分为Ca(OH) ]除去Mg2+,再通入含NH ,CO 的工业废气除去
2 3 2
Ca2+;
方案3:向粗盐水中加入石灰乳除去Mg2+,再加入碳酸钠溶液除去Ca2+。
(7)相比于方案3,方案2的优点是_______。
(8)已知粗盐水中MgCl 含量为0.38g×L-1,CaCl 含量为1.11g×L-1,现用方案3提纯10L该粗盐
2 2
水,求需要加入石灰乳(视为CaO)和碳酸钠的物质的量_______。
三、溴化铝的性质
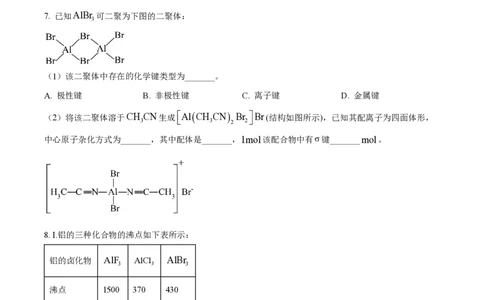
7. 已知AlBr 可二聚为下图的二聚体:
3
(1)该二聚体中存在的化学键类型为_______。
A. 极性键 B. 非极性键 C. 离子键 D. 金属键
(2)将该二聚体溶于CH
3
CN生成é
ë
AlCH
3
CN
2
Br
2
ù
û
Br(结构如图所示),已知其配离子为四面体形,
中心原子杂化方式为_______,其中配体是_______,1mol该配合物中有σ键_______mol。
8. I.铝的三种化合物的沸点如下表所示:
铝的卤化物 AlF AlCl AlBr
3 3 3
沸点 1500 370 430
(1)解释三种卤化物沸点差异的原因_______。
(2)已知反应Al
2
Br
6
(l)
ƒ
2Al(g)+6Br(g) ΔH
。
①Al
2
Br
6
(s)
ƒ
Al
2
Br
6
(l) ΔH
1
②Al(s)
ƒ
Al(g) ΔH
2
第3页/共6页
学科网(北京)股份有限公司③Br
2
(l)
ƒ
Br
2
(g) ΔH
3
④Br
2
(g)
ƒ
2Br(g) ΔH
4
⑤2Al(s)+3Br
2
(l)
ƒ
Al
2
Br
6
(s) ΔH
5
则ΔH=_______。
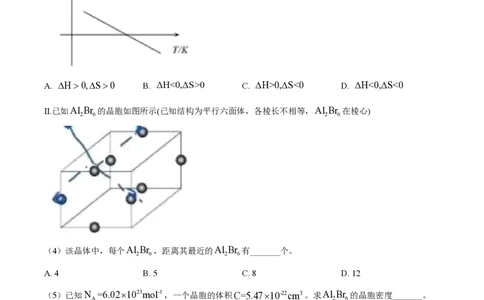
(3)由图可知,若该反应自发,则该反应的_______。
A. DH >0,DS>0 B. ΔH<0,ΔS>0 C. ΔH>0,ΔS<0 D. ΔH<0,ΔS<0
II.已如Al Br 的晶胞如图所示(已知结构为平行六面体,各棱长不相等,Al Br 在棱心)
2 6 2 6
(4)该晶体中,每个Al Br ,距离其最近的Al Br 有_______个。
2 6 2 6
A. 4 B. 5 C. 8 D. 12
(5)已知N =6.02´1023mol-1,一个晶胞的体积C=5.47´10-22cm3。求Al Br 的晶胞密度_______。
A 2 6
(6)AlBr 水解可得Al(OH) 胶体,请解释用Al(OH) 可净水的原因_______。
3 3 3
(7)用上述制得的胶体做电泳实验时,有某种胶体粒子向阴极移动,该粒子可能是_______。
x+ 3x-
A. émAl(OH) ×nAl3+×(3n-x)Br-ù B. émAl(OH) ×nBr-×xAl3+ù
ë 3 û ë 3 û
x- x-
C. émAl(OH) ×nOH-×(n-x)H+ù D. émAl(OH) ×nAl3+×(n-x)Br-ù
ë 3 û ë 3 û
四、瑞格列奈的制备
第4页/共6页
学科网(北京)股份有限公司9. 瑞格列奈的制备。
(1)瑞格列奈中的含氧官能团除了羧基、醚键,还存在_______。
(2)反应①的反应类型为_______。
A. 还原反应 B. 消去反应 C. 取代反应 D. 氧化反应
(3)反应②的试剂和条件是_______。
(4)D的分子式是C H OF,画出D的结构简式_______。
11 13
(5)化合物D有多种同分异构体,写出满足下列条件的D的同分异构体的结构简式_______。
i.芳香族化合物,可以发生银镜反应;
ii.核磁共振氢谱中显示出3组峰,其峰面积之比为6:6:1。
(6)G对映异构体分离后才能发生下一步反应
①G中有_______个手性碳
②已知 ,用 和谷氨酸可制备
,该物质可用于分离对映异构体。谷氨酸的结构简式为:_______。检验谷氨酸
的试剂是_______。
A. 硝酸 B. 茚三酮 C. NaOH D. NaHCO
3
(7)用 与G可直接制取H。但产率变低,请分析原因_______。
(8)以 和CH MgBr合成 _______。
3
五、珊瑚的形成与保护
10. 已知:Ca2++2HCO 3 - ƒ CaCO 3 +H 2 CO 3
第5页/共6页
学科网(北京)股份有限公司①HCO- H++CO2-
3 ƒ 3
②Ca2++CO2- CaCO
3 ƒ 3
③HCO-+H+ H CO
3 ƒ 2 3
(1)以下能判断总反应达到平衡状态的是_______。
c
HCO-
3
A. 钙离子浓度保持不变 B. 保持不变
c
CO2-
3
C. v Ca2+ =v CaCO D. v H CO :v HCO- =2:1
正 逆 3 正 2 3 逆 3
(2)pH增大有利于珊瑚的形成,请解释原因_______。
(3)已知H CO 的K =4.2´10-7,K =5.6´10-11,K (CaCO )=2.8´10-9,c(H+)=8.4´10-9mol×L-1,
2 3 al a2 sp 3
c HCO- =1´10-4mol×L-1,cH CO 为_______。当c Ca2+ =_______mol×L-1时,开始产生CaCO 沉
3 2 3 3
淀。
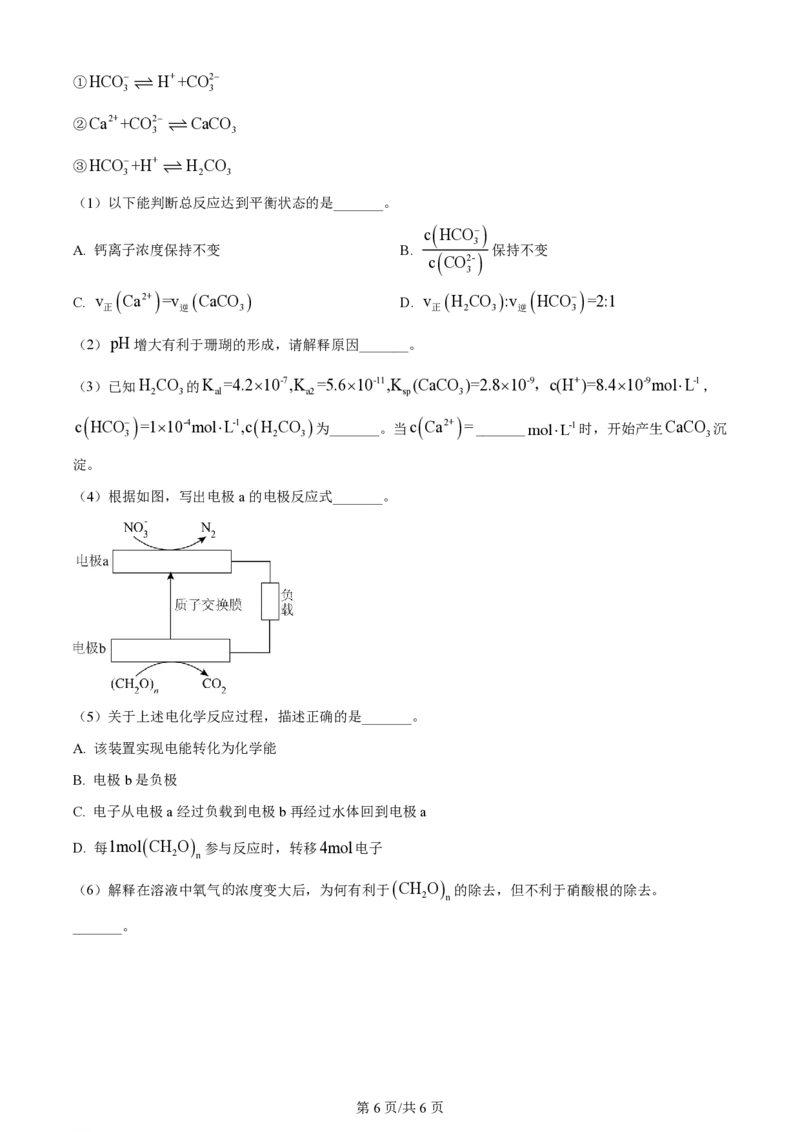
(4)根据如图,写出电极a的电极反应式_______。
(5)关于上述电化学反应过程,描述正确的是_______。
A. 该装置实现电能转化为化学能
B. 电极b是负极
C. 电子从电极a经过负载到电极b再经过水体回到电极a
D.
每1molCH O
参与反应时,转移4mol电子
2 n
(6)解释在溶液中氧气的浓度变大后,为何有利于
CH O
的除去,但不利于硝酸根的除去。
2 n
_______。
第6页/共6页
学科网(北京)股份有限公司