文档内容
机密★启用前
2024 年海南省普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题|卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Li-7 ⅳO-16 Cl-35.5 K-39 Mn-55 Fe-56 Cu-64 Zn-
65
一、选择题:本题共 8小题,每小题 2分,共 16分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学为实现社会可持续发展贡献巨大。下列说法错误的是
A. 以竹代塑,可减少白色污染 B. 使用人工合成杀虫剂,对环境无影响
C. 无纸化办公,可减少人工合成油墨的使用 D. 使用无磷洗涤剂,可减少水体污染
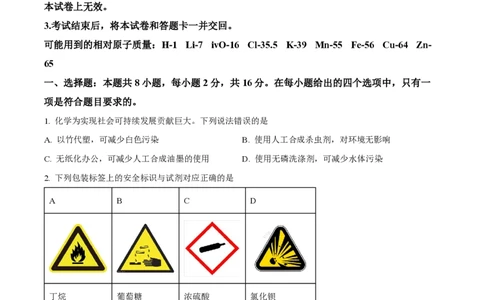
2. 下列包装标签上的安全标识与试剂对应正确的是
A B C D
丁烷 葡萄糖 浓硫酸 氯化钡
A. A B. B C. C D. D
3. 高分子物质与我们生活息息相关。下列说法错误的是
A. 糖原(成分类似于淀粉)可转化为葡萄糖
B. 聚合物 是CH =CH 的加聚物
2 2
C. 畜禽毛羽(主要成分为角蛋白)完全水解可以得到氨基酸
第1页/共10页
学科网(北京)股份有限公司D. 聚合物 的单体是HOOCCH COOH和CH CH OH
2 4 3 2
CH CH OH
3 2
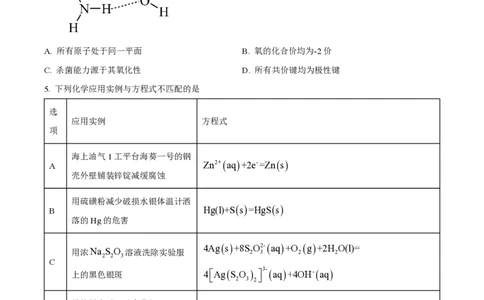
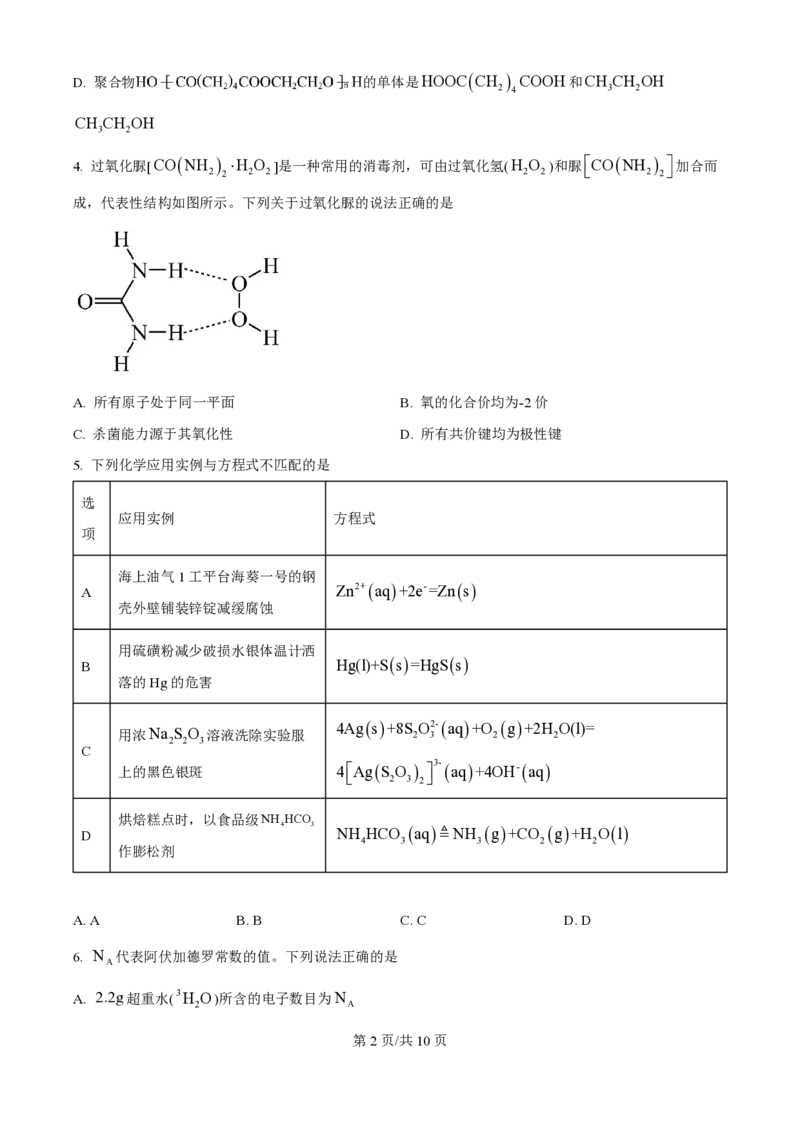
4. 过氧化脲[CONH 2 2 ×H 2 O 2 ]是一种常用的消毒剂,可由过氧化氢(H 2 O 2 )和脲é ë CONH 2 2 ù û 加合而
成,代表性结构如图所示。下列关于过氧化脲的说法正确的是
A. 所有原子处于同一平面 B. 氧的化合价均为-2价
C. 杀菌能力源于其氧化性 D. 所有共价键均为极性键
5. 下列化学应用实例与方程式不匹配的是
选
应用实例 方程式
项
海上油气1工平台海葵一号的钢
A
Zn2+aq+2e-=Zns
壳外壁铺装锌锭减缓腐蚀
用硫磺粉减少破损水银体温计洒
B
Hg(l)+Ss=HgSs
落的Hg的危害
4Ags+8S O2-aq+O g+2H O(l)=
用浓Na S O 溶液洗除实验服 2 3 2 2
2 2 3
C
上的黑色银斑 4éAgS O ù 3-aq+4OH-aq
ë 2 3 2 û
烘焙糕点时,以食品级NH HCO
D 4 3 NH 4 HCO 3 aq @ NH 3 g+CO 2 g+H 2 Ol
作膨松剂
A. A B. B C. C D. D
6. N 代表阿伏加德罗常数的值。下列说法正确的是
A
A. 2.2g超重水(3H O)所含的电子数目为N
2 A
第2页/共10页
学科网(北京)股份有限公司B. 1L 0.1mol×L-1 NaClO溶液中ClO-的数目为0.1N
A
C. 过量C与1mol SiO 充分反应转移电子数目为3N
2 A
D. 1mol Cl 与足量CH 发生取代反应生成HCl分子的数目为2N
2 4 A
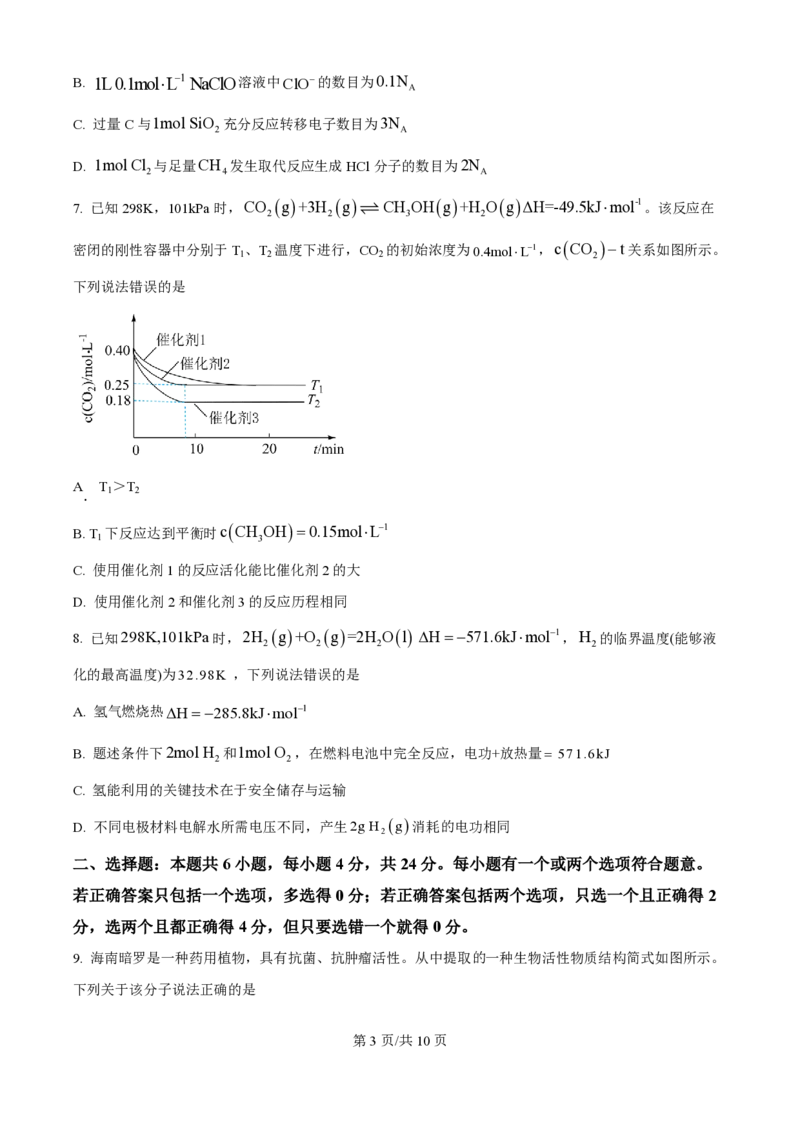
7. 已知298K,101kPa时,CO 2 g+3H 2 g ƒ CH 3 OHg+H 2 OgΔH=-49.5kJ×mol-1。该反应在
密闭的刚性容器中分别于T 、T 温度下进行,CO
的初始浓度为0.4mol×L-1,cCO -t关系如图所示。
1 2 2 2
下列说法错误的是
A T >T
. 1 2
B. T
下反应达到平衡时cCH OH=0.15mol×L-1
1 3
C. 使用催化剂1的反应活化能比催化剂2的大
D. 使用催化剂2和催化剂3的反应历程相同
8. 已知298K,101kPa时,2H g+O g=2H Ol DH=-571.6kJ×mol-1,H 的临界温度(能够液
2 2 2 2
化的最高温度)为32.98K ,下列说法错误的是
A. 氢气燃烧热DH=-285.8kJ×mol-1
B. 题述条件下2mol H 和1mol O ,在燃料电池中完全反应,电功+放热量= 571.6kJ
2 2
C. 氢能利用的关键技术在于安全储存与运输
D. 不同电极材料电解水所需电压不同,产生2g H g消耗的电功相同
2
二、选择题:本题共 6小题,每小题 4分,共 24 分。每小题有一个或两个选项符合题意。
若正确答案只包括一个选项,多选得 0分;若正确答案包括两个选项,只选一个且正确得 2
分,选两个且都正确得 4分,但只要选错一个就得 0分。
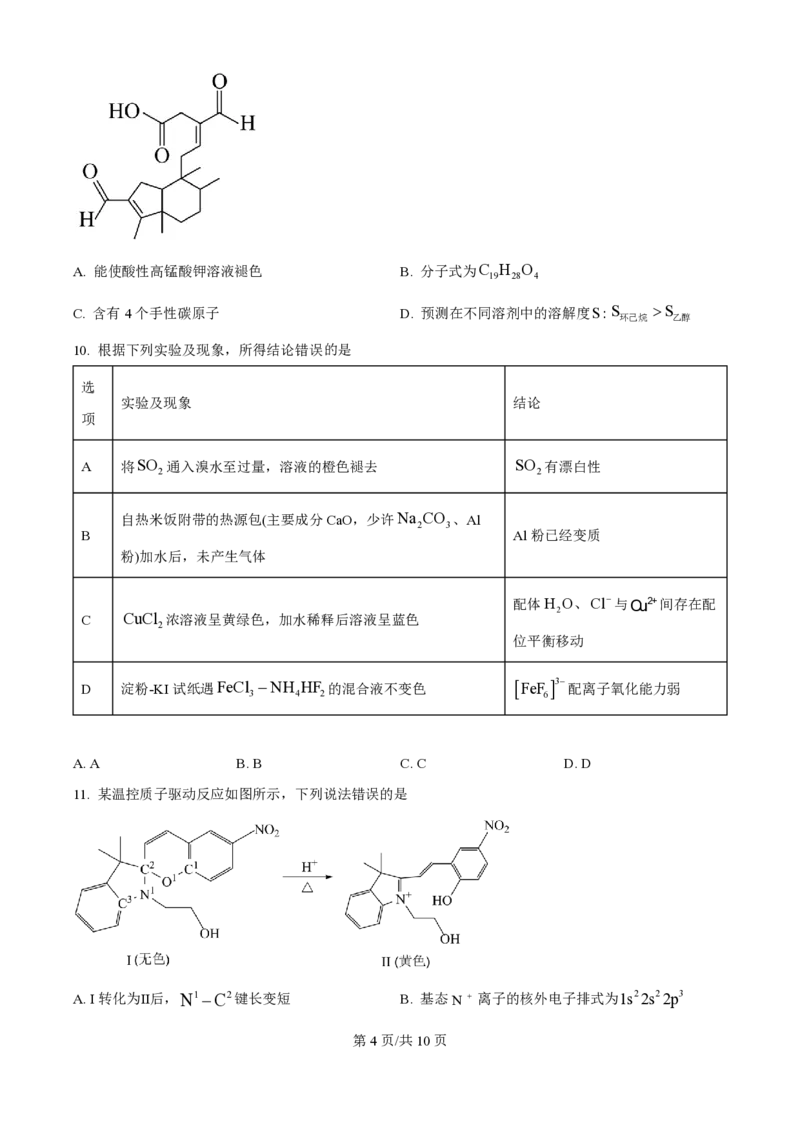
9. 海南暗罗是一种药用植物,具有抗菌、抗肿瘤活性。从中提取的一种生物活性物质结构简式如图所示。
下列关于该分子说法正确的是
第3页/共10页
学科网(北京)股份有限公司A. 能使酸性高锰酸钾溶液褪色 B. 分子式为C H O
19 28 4
C. 含有4个手性碳原子 D. 预测在不同溶剂中的溶解度S:S >S
环己烷 乙醇
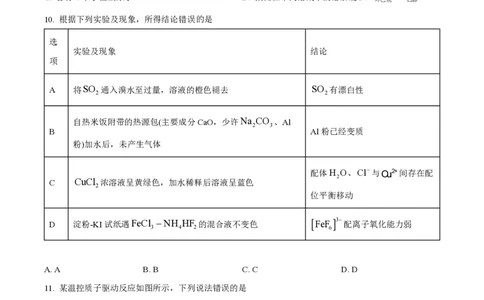
10. 根据下列实验及现象,所得结论错误的是
选
实验及现象 结论
项
A 将SO 通入溴水至过量,溶液的橙色褪去 SO 有漂白性
2 2
自热米饭附带的热源包(主要成分CaO,少许Na CO 、Al
2 3
B Al粉已经变质
粉)加水后,未产生气体
配体H O、Cl-与Cu2+间存在配
2
C CuCl 浓溶液呈黄绿色,加水稀释后溶液呈蓝色
2
位平衡移动
D 淀粉-KI试纸遇FeCl -NH HF 的混合液不变色 FeF 3- 配离子氧化能力弱
3 4 2 6
A. A B. B C. C D. D
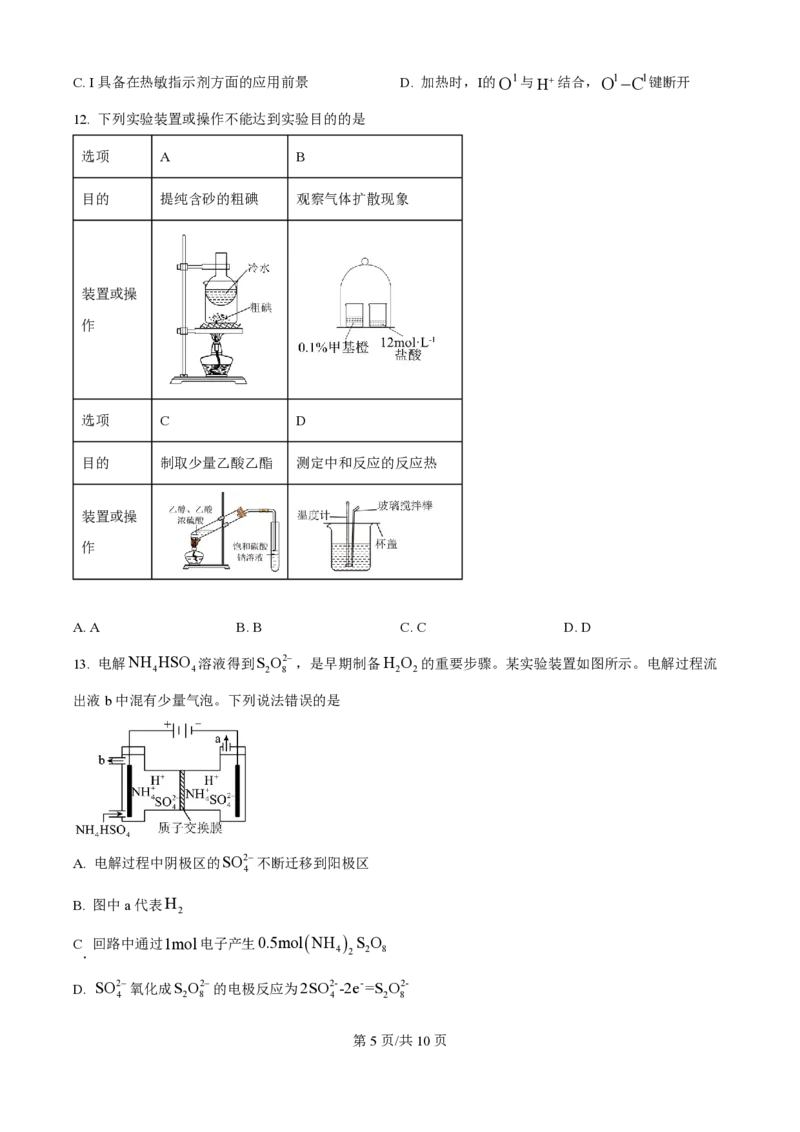
11. 某温控质子驱动反应如图所示,下列说法错误的是
A. I转化为Ⅱ后,N1-C2键长变短 B. 基态N + 离子的核外电子排式为1s22s22p3
第4页/共10页
学科网(北京)股份有限公司C. I具备在热敏指示剂方面的应用前景 D. 加热时,Ⅰ的O1与H+结合,O1-C1键断开
12. 下列实验装置或操作不能达到实验目的的是
选项 A B
目的 提纯含砂的粗碘 观察气体扩散现象
装置或操
作
选项 C D
目的 制取少量乙酸乙酯 测定中和反应的反应热
装置或操
作
A. A B. B C. C D. D
13. 电解NH HSO 溶液得到S O2-,是早期制备H O 的重要步骤。某实验装置如图所示。电解过程流
4 4 2 8 2 2
出液b中混有少量气泡。下列说法错误的是
A. 电解过程中阴极区的SO2-不断迁移到阳极区
4
B. 图中a代表H
2
C 回路中通过1mol电子产生0.5molNH S O
. 4 2 2 8
D. SO2-氧化成S O2-的电极反应为2SO2--2e-=S O2-
4 2 8 4 2 8
第5页/共10页
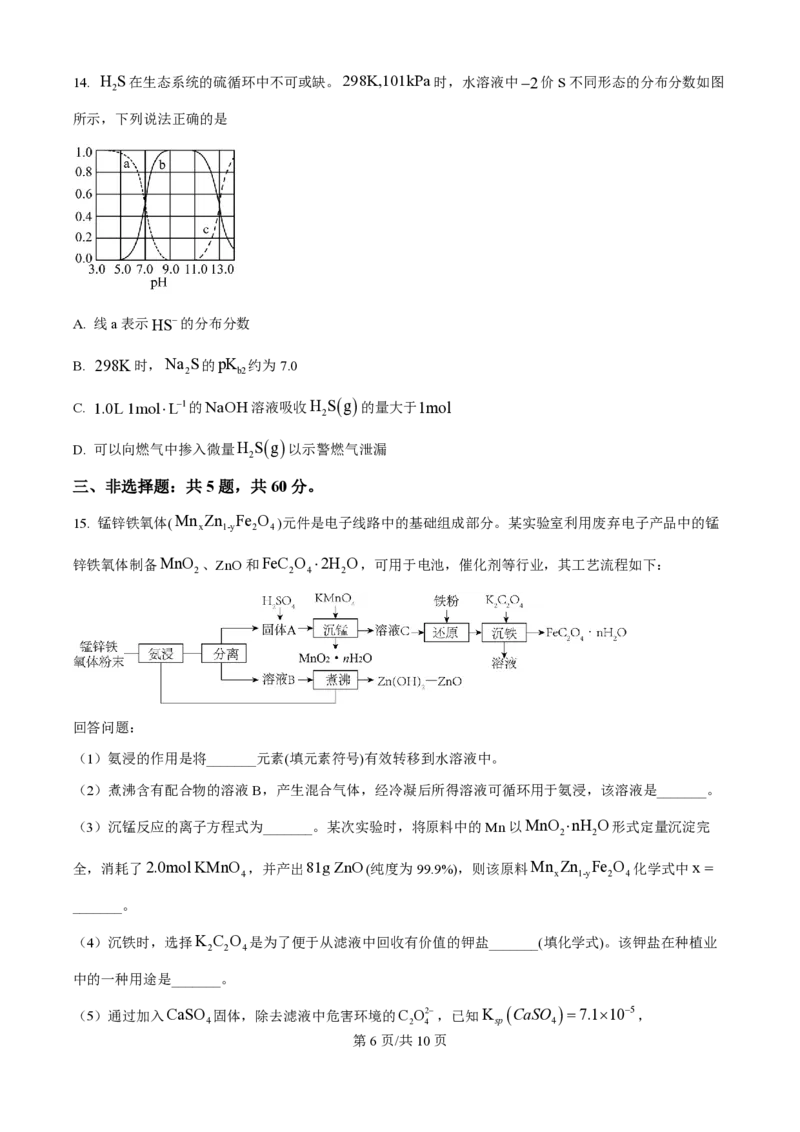
学科网(北京)股份有限公司14. H S在生态系统的硫循环中不可或缺。298K,101kPa时,水溶液中-2价S不同形态的分布分数如图
2
所示,下列说法正确的是
A. 线a表示HS-的分布分数
B. 298K时,Na S的pK 约为7.0
2 b2
C. 1.0L 1mol×L-1的NaOH溶液吸收H Sg 的量大于1mol
2
D. 可以向燃气中掺入微量H Sg 以示警燃气泄漏
2
三、非选择题:共 5题,共 60分。
15. 锰锌铁氧体(Mn Zn Fe O )元件是电子线路中的基础组成部分。某实验室利用废弃电子产品中的锰
x 1-y 2 4
锌铁氧体制备MnO 、ZnO和FeC O ×2H O,可用于电池,催化剂等行业,其工艺流程如下:
2 2 4 2
回答问题:
(1)氨浸的作用是将_______元素(填元素符号)有效转移到水溶液中。
(2)煮沸含有配合物的溶液B,产生混合气体,经冷凝后所得溶液可循环用于氨浸,该溶液是_______。
(3)沉锰反应的离子方程式为_______。某次实验时,将原料中的Mn以MnO ×nH O形式定量沉淀完
2 2
全,消耗了2.0mol KMnO ,并产出81g ZnO(纯度为99.9%),则该原料Mn Zn Fe O 化学式中x =
4 x 1-y 2 4
_______。
(4)沉铁时,选择K C O 是为了便于从滤液中回收有价值的钾盐_______(填化学式)。该钾盐在种植业
2 2 4
中的一种用途是_______。
(5)通过加入CaSO 固体,除去滤液中危害环境的C O2-,已知K CaSO =7.1´10-5,
4 2 4 sp 4
第6页/共10页
学科网(北京)股份有限公司K sp CaC 2 O 4 =2.3´10-9。反应CaSO 4 s+C 2 O 4 2-aq ƒ CaC 2 O 4 s+SO2 4 -aq 的平衡常数为
_______。
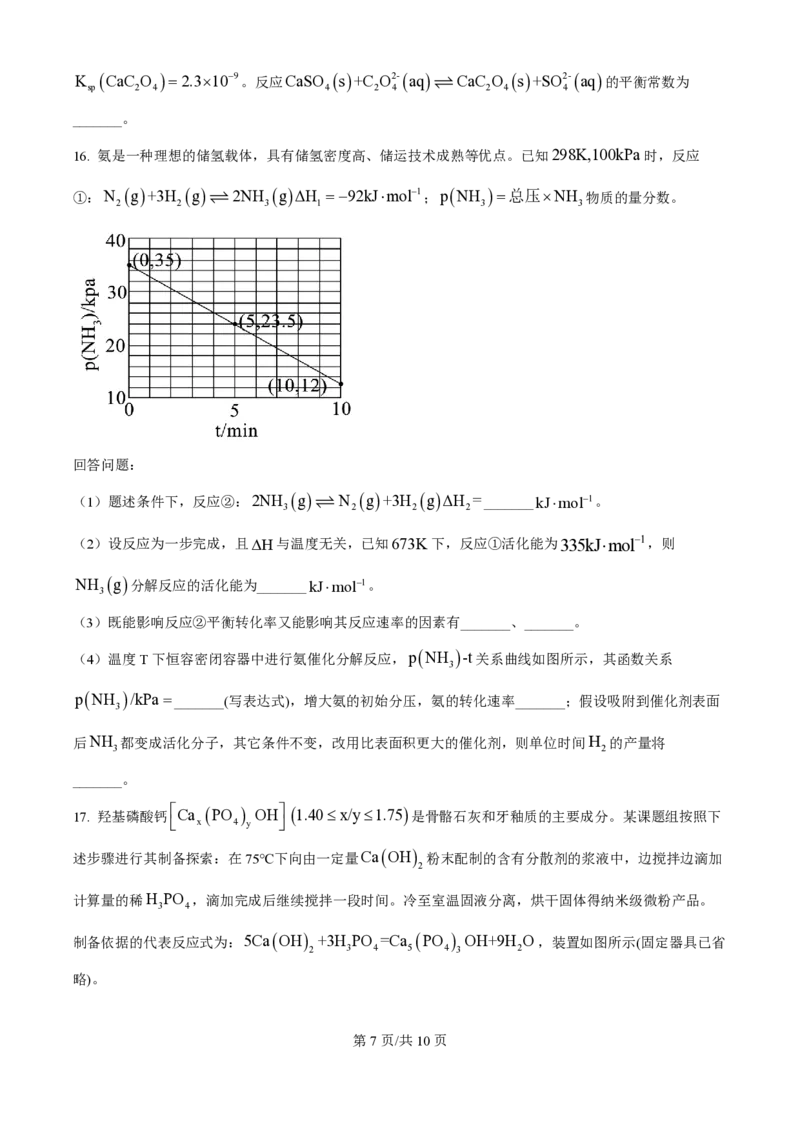
16. 氨是一种理想的储氢载体,具有储氢密度高、储运技术成熟等优点。已知298K,100kPa时,反应
①:N 2 g+3H 2 g ƒ 2NH 3 gΔH 1 =-92kJ×mol-1;pNH 3 =总压´NH 3 物质的量分数。
回答问题:
(1)题述条件下,反应②:2NH
3
g
ƒ
N
2
g+3H
2
gΔH
2
=_______kJ×mol-1。
(2)设反应为一步完成,且DH与温度无关,已知673K下,反应①活化能为335kJ×mol-1,则
NH g 分解反应的活化能为_______kJ×mol-1。
3
(3)既能影响反应②平衡转化率又能影响其反应速率的因素有_______、_______。
(4)温度T下恒容密闭容器中进行氨催化分解反应,pNH -t关系曲线如图所示,其函数关系
3
pNH /kPa =_______(写表达式),增大氨的初始分压,氨的转化速率_______;假设吸附到催化剂表面
3
后NH 都变成活化分子,其它条件不变,改用比表面积更大的催化剂,则单位时间H 的产量将
3 2
_______。
17. 羟基磷酸钙
éCa PO OHù 1.40£x/y£1.75
是骨骼石灰和牙釉质的主要成分。某课题组按照下
ë x 4 y û
述步骤进行其制备探索:在75℃下向由一定量CaOH
粉末配制的含有分散剂的浆液中,边搅拌边滴加
2
计算量的稀H PO ,滴加完成后继续搅拌一段时间。冷至室温固液分离,烘干固体得纳米级微粉产品。
3 4
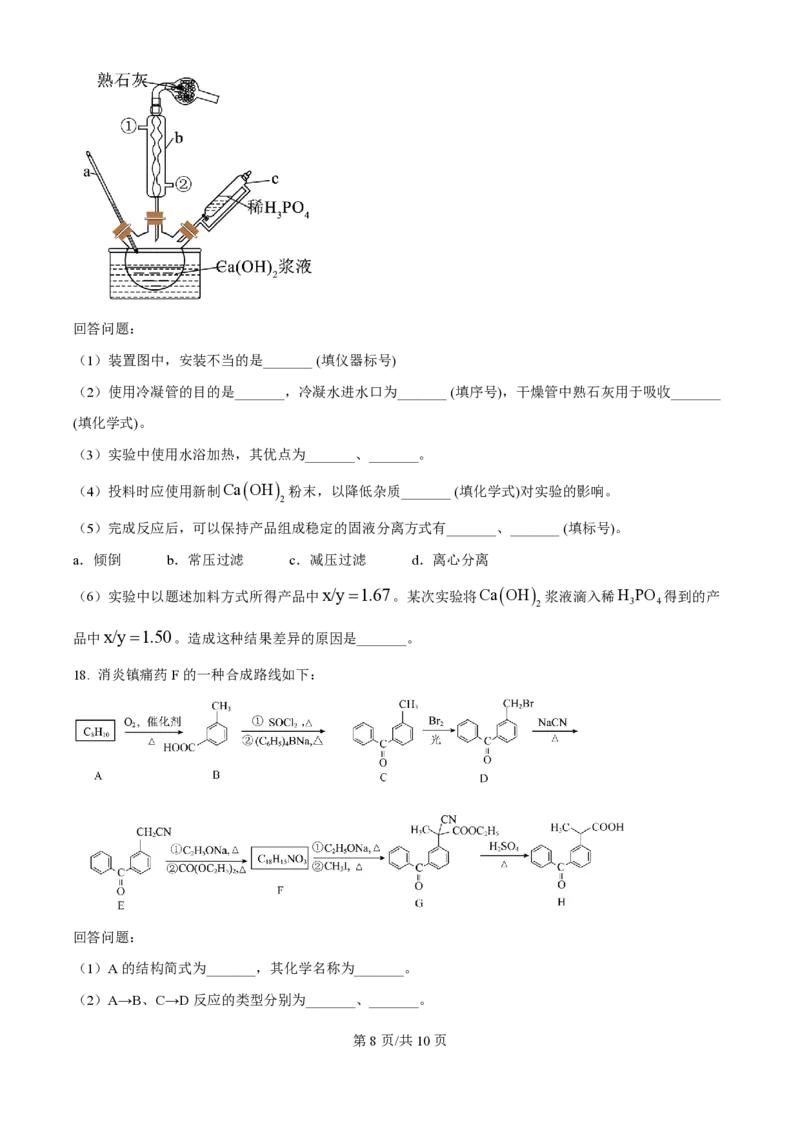
制备依据的代表反应式为:5CaOH +3H PO =Ca PO OH+9H O,装置如图所示(固定器具已省
2 3 4 5 4 3 2
略)。
第7页/共10页
学科网(北京)股份有限公司回答问题:
(1)装置图中,安装不当的是_______ (填仪器标号)
(2)使用冷凝管的目的是_______,冷凝水进水口为_______ (填序号),干燥管中熟石灰用于吸收_______
(填化学式)。
(3)实验中使用水浴加热,其优点为_______、_______。
(4)投料时应使用新制CaOH
粉末,以降低杂质_______ (填化学式)对实验的影响。
2
(5)完成反应后,可以保持产品组成稳定的固液分离方式有_______、_______ (填标号)。
a.倾倒 b.常压过滤 c.减压过滤 d.离心分离
(6)实验中以题述加料方式所得产品中x/y=1.67。某次实验将CaOH 浆液滴入稀H PO 得到的产
2 3 4
品中x/y=1.50。造成这种结果差异的原因是_______。
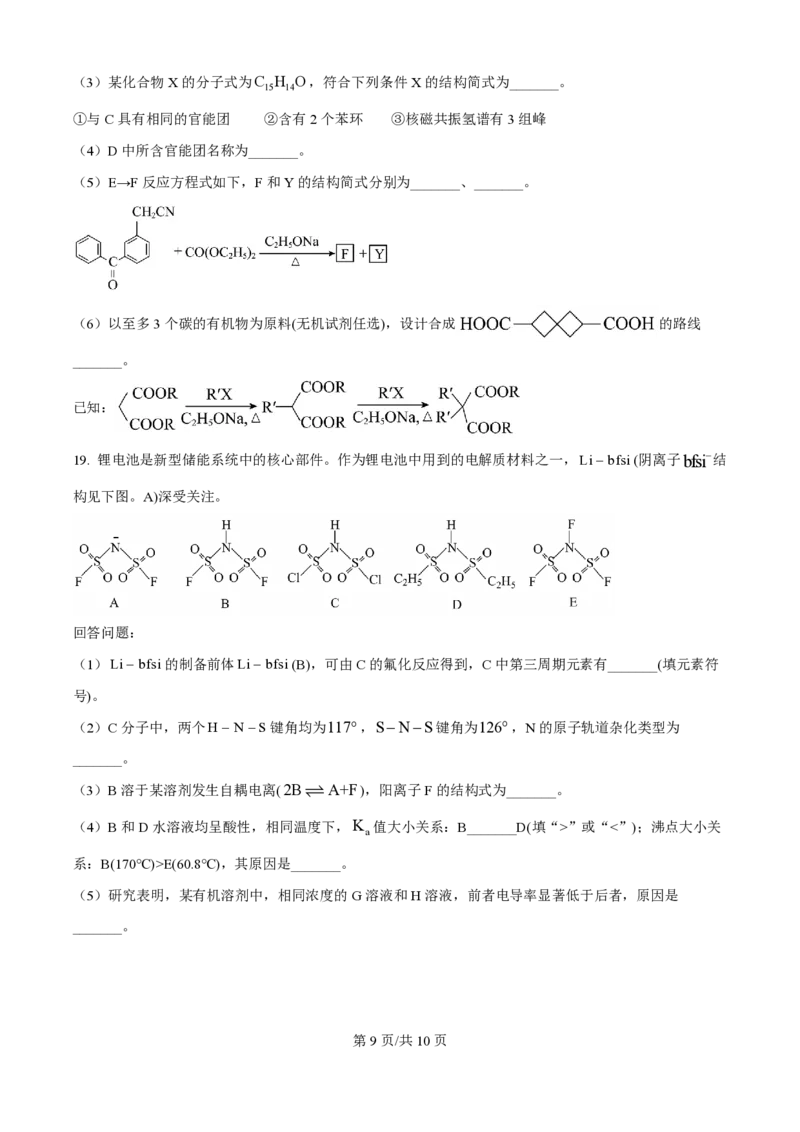
18. 消炎镇痛药F的一种合成路线如下:
回答问题:
(1)A的结构简式为_______,其化学名称为_______。
(2)A→B、C→D反应的类型分别为_______、_______。
第8页/共10页
学科网(北京)股份有限公司(3)某化合物X的分子式为C H O,符合下列条件X的结构简式为_______。
15 14
①与C具有相同的官能团 ②含有2个苯环 ③核磁共振氢谱有3组峰
(4)D中所含官能团名称为_______。
(5)E→F反应方程式如下,F和Y的结构简式分别为_______、_______。
(6)以至多3个碳的有机物为原料(无机试剂任选),设计合成 的路线
_______。
已知:
19. 锂电池是新型储能系统中的核心部件。作为锂电池中用到的电解质材料之一,Li-bfsi(阴离子bfsi-结
构见下图。A)深受关注。
回答问题:
(1)Li-bfsi的制备前体Li-bfsi(B),可由C的氟化反应得到,C中第三周期元素有_______(填元素符
号)。
(2)C分子中,两个H - N -S键角均为117°,S-N-S键角为126°,N的原子轨道杂化类型为
_______。
(3)B溶于某溶剂发生自耦电离(2B
ƒ
A+F),阳离子F的结构式为_______。
(4)B和D水溶液均呈酸性,相同温度下,K 值大小关系:B_______D(填“>”或“<”);沸点大小关
a
系:B(170℃)>E(60.8℃),其原因是_______。
(5)研究表明,某有机溶剂中,相同浓度的G溶液和H溶液,前者电导率显著低于后者,原因是
_______。
第9页/共10页
学科网(北京)股份有限公司(6)Li OHCl在固体离子电导方面具有潜在的应用前景。其两种晶型中,一种取长方体形晶胞(图1,
2
长方体棱长为a、b、c),另一种取立方体形晶胞(图2,Cl居于立方体中心,立方体棱长为d)。图中氢原子
皆己隐去。
①立方体形晶胞所代表的晶体中部分锂离子(●Li)位置上存在缺位现象,锂离子的总缺位率为_______;该
晶型中氯离子周围紧邻的锂离子平均数目为_______。
②两种晶型的密度近似相等,则c=_______。(以含a、b和d的代数式表达)
第10页/共10页
学科网(北京)股份有限公司