【2026版三维高考设计高中化学人教版培优课时训练word电子版第48讲沉淀溶解平衡图像
 48讲沉淀溶解平衡图像
48讲沉淀溶解平衡图像
一、选择题(本题包括7小题,每小题只有一个选项符合题意)
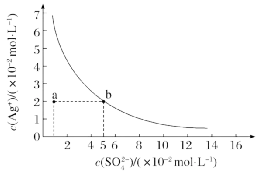
1.某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是()
A.含有大量S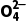 的溶液中肯定不存在Ag+
的溶液中肯定不存在Ag+
B.Ag2SO4的溶度积常数(Ksp)为1×10-3
C.0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
2.硫化镉(CdS)是一种难溶于水的黄色颜料,在水溶液中存在如下沉淀溶解平衡:CdS(s)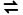 Cd2+(aq)+S2-(aq) ΔH>0,其沉淀溶解平衡曲线如图所示。下列说法错误的是()
Cd2+(aq)+S2-(aq) ΔH>0,其沉淀溶解平衡曲线如图所示。下列说法错误的是()
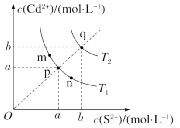
A.图中温度:T1<T2
B.图中各点对应的Ksp的关系为Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
3.T ℃时,向5 mL a mol·L-1 BaCl2溶液中逐滴加入0.1 mol·L-1 Na2CO3溶液,滴加过程中溶液的-lg c(B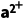 )与Na2CO3溶液体积(V)的关系如图所示。下列说法正确的是[已知:lg 5=0.7,Ksp(BaSO4)=1.0×10-10]()
)与Na2CO3溶液体积(V)的关系如图所示。下列说法正确的是[已知:lg 5=0.7,Ksp(BaSO4)=1.0×10-10]()
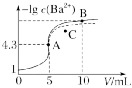
A.A、B两点溶液中c(B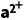 )之比为2 000∶3
)之比为2 000∶3
B.a=10-4.3
C.T ℃时,C点对应的含BaCO3的分散系很稳定
D.若用相同浓度的Na2SO4溶液代替Na2CO3溶液,则图像在A点后的变化曲线如虚线部分
4.在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是()
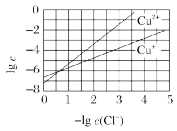
A.Ksp(CuCl)的数量级为10-7
B.除Cl-的反应为Cu+Cu2++2Cl- 2CuCl
2CuCl
C.加入Cu越多,Cu+浓度越高,除去Cl-的效果越好
D.2Cu+(aq)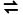 Cu2+(aq)+Cu(s)平衡常数很大,反应趋于完全
Cu2+(aq)+Cu(s)平衡常数很大,反应趋于完全
5.已知:Ka1(H2S)=10-7.1,Ka2(H2S)=10-14.7,Ksp(CuS)=10-36,Ksp(ZnS)=10-24.8;金属离子完全沉淀时c≤10-5 mol·L-1。处理含Cu2+、Zn2+的废水过程中始终保持H2S饱和,即c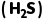 =0.1 mol·L-1。废水体系中pH与-lg c(HS-)、-lg c(S2-)的关系如图所示(浓度单位是 mol·L-1)。下列说法正确的是()
=0.1 mol·L-1。废水体系中pH与-lg c(HS-)、-lg c(S2-)的关系如图所示(浓度单位是 mol·L-1)。下列说法正确的是()
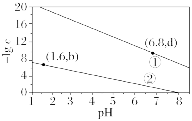
A.①为pH与-lg c(HS-)的关系线
B.pH=1的废水中,Cu2+不能完全沉淀
C.d=9.2
D.要完全沉淀Zn2+,溶液pH≥3.5
6.常温下,取一定量的PbI2固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如图所示。下列有关说法正确的是()
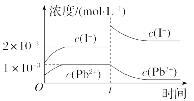
A.常温下,PbI2的Ksp为2×10-6
B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,沉淀溶解平衡向沉淀生成的方向移动,Pb2+的浓度减小
C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI2的Ksp增大
D.常温下,Ksp(PbS)=8×10-28,向PbI2的悬浊液中加入Na2S溶液,反应PbI2(s)+S2-(aq)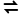 PbS(s)+2I-(aq)的平衡常数为5×1018
PbS(s)+2I-(aq)的平衡常数为5×1018
7.(2024·渭南模拟)常温下,已知MCO3、M(OH)2的沉淀溶解平衡曲线如图所示,溶液中M2+和阴离子(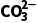 、OH-)浓度的负对数分别用pM和pR表示。
、OH-)浓度的负对数分别用pM和pR表示。

已知:100.6≈4。下列说法正确的是()
A.曲线XY代表的是MCO3
B.M(OH)2的Ksp为4.0×10-12
C.在MCO3饱和溶液中加少量Na2CO3固体,M2+、OH-浓度均减小
D.阴影区域内,可析出M(OH)2,而不析出MCO3
二、非选择题(本题包括2小题)
8.已知:pAg=-lg c(Ag+),Ksp(AgCl)=1×10-12。如图是向10 mL AgNO3溶液中逐渐加入0.1 mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积变化的图像(实线)。根据图像回答下列问题[提示:Ksp(AgCl)>Ksp(AgI)]:
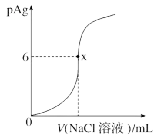
(1)原AgNO3溶液的物质的量浓度为mol·L-1。
(2)图中在x点时加入NaCl溶液的体积为。
(3)相同温度下,AgCl在纯水中的溶解度(填“>”“<”或“=”)在NaCl溶液中的溶解度。
9.(1)金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度[S/(mol·L-1)]如图1所示。

①pH=3时溶液中铜元素的主要存在形式是。
②若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为(填字母)。
A.<1 B.4左右 C.>6
③在Ni2+溶液中含有少量的Co2+杂质, (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是。
通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




