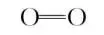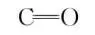【2026版化学苏教版必修第二册练透培优讲义电子版专题6 第二单元 第2课时化学反应中能量变化的原因燃料燃烧释放的能量和氢能的
[核心素养发展目标] 1.能用化学键解释某些吸热反应和放热反应,能进行一些简单的能量变化计算。2.理解化学反应中能量的变化取决于反应物与生成物的总能量的相对大小。3.认识燃料的燃烧效率、保护环境、开发清洁燃料的必要性和重要性。
一、化学反应中能量变化的原因
1.化学反应中能量变化与化学键的关系(微观探析)
(1)化学反应过程
(2)化学反应中能量变化的原因
2.化学反应中能量变化的决定因素(宏观辨识)
|
宏观解释 |
|
|
|
能量变化 示意图 |
|
|
由能量变化示意图知
(1)反应吸收能量而使体系内能量。ΔH为正值,即ΔH0。
(2)反应放出能量而使体系内能量。ΔH为负值,即ΔH0。
(3)可利用能量守恒定律,从宏观角度(即反应物总能量与生成物总能量大小)理解化学反应中能量变化的原因。
思考乙醇汽油是乙醇和普通汽油按一定比例混合配成的新型替代能源。
(1)已知乙醇的结构式为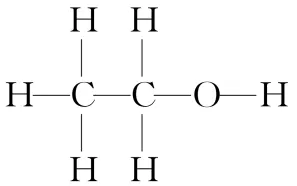 mol乙醇含有共价键的物质的量各是多少?
mol乙醇含有共价键的物质的量各是多少?
____________________________________________________________________________________
(2)1molCO2和1molH2O都有什么化学键?
____________________________________________________________________________________
(3)已知断开或形成1mol化学键的数据如下:
|
化学键 |
C—C |
C—H |
|
H—O |
C—O |
|
|
键能/(kJ·mol-1) |
348 |
413 |
498 |
463 |
351 |
745 |
则1mol乙醇与O2完全燃烧生成CO2和H2O(g)放出的能量是多少?写出计算过程。
____________________________________________________________________________________
1.判断正误
(1)任何化学反应,都有物质变化,同时伴随着能量变化( )
(2)当反应物的总能量大于生成物的总能量时,化学反应吸收热量( )
(3)对于一个化学反应来说,当化学键断裂时吸收的能量大于化学键形成时放出的能量,则反应放热( )
(4)放热反应为“贮存”能量的过程,吸热反应为“释放”能量的过程( )
(5)已知Fe与稀盐酸的反应为放热反应,即Fe的能量大于H2的能量( )
2. 已知反应A+B===C+D的能量变化如图所示(E1、E2均为正值),下列说法正确的是( )
A.该反应吸收的能量为E1–E2
B.该反应只有在加热条件下才能进行
C.A和B的总能量一定高于C和D的总能量
D.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
3.已知2H→H2的能量变化如图所示。下列说法不正确的是( )
A.2H→H2过程中形成的化学键是共价键
B.相同质量的氢气分子的能量比氢原子的能量低
C.2H→H2过程中形成1 mol新化学键放出437.6 kJ的能量
D.1 mol H2离解成2 mol H要放出437.6 kJ热量
4.已知一些化学键的键能数据如下表所示:
|
共价键 |
键能/(kJ·mol-1) |
共价键 |
键能/(kJ·mol-1) |
|
H—H |
436.4 |
C—C |
347.7 |
|
Cl—Cl |
242.7 |
H—Cl |
431.8 |
|
H—O |
462.8 |
N≡N |
941.7 |
(1)化学反应H2+Cl2===2HCl的热化学方程式为。
(2)H2和Cl2反应的能量变化图可用(填“A”或“B”)表示。
(3)H2在Cl2中燃烧的过程主要是能转化为能的过程。
(1)键能:在标准状况下,将1mol气体分子AB(g)解离为气体原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ·mol-1。
(2)物质所含能量越低,物质越稳定,键能越大,断裂其化学键所需能量越高,而形成其化学键所释放的能量也越多,反之亦然。
(3)ΔH=E反应物的键能之和–E生成物的键能之和。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/1FV5DqLWuSuDWXxDC6TcwsQ?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风