【专题突破】原子结构如何决定性质(可下载word版)

要点梳理
1.原子结构与周期表的关系
(1)原子结构与周期表的关系(完成下列表格)
|
周期 |
电子层数 |
每周期第一个元素 |
每周期最后一个元素 |
||
|
原子序数 |
基态原子的简化电子排布式 |
原子序数 |
基态原子的电子排布式 |
||
|
2 |
2 |
3 |
[He]2s1 |
10 |
1s22s22p6 |
|
3 |
3 |
11 |
[Ne]3s1 |
18 |
1s22s22p63s23p6 |
|
4 |
4 |
19 |
[Ar]4s1 |
36 |
1s22s22p63s23p6 3d104s24p6 |
|
5 |
5 |
37 |
[Kr]5s1 |
54 |
1s22s22p63s23p63d10 4s24p64d105s25p6 |
|
6 |
6 |
55 |
[Xe]6s1 |
86 |
1s22s22p63s23p63d104s24p6 4d104f145s25p65d106s26p6 |
(2)每族元素的价层电子排布特点
①主族
|
主族 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
|
排布特点 |
ns1 |
ns2 |
ns2np1 |
ns2np2 |
|
主族 |
ⅤA |
ⅥA |
ⅦA |
|
|
排布特点 |
ns2np3 |
ns2np4 |
ns2np5 |
③过渡元素(副族和第Ⅷ族):(n-1)d1~10ns1~2。
(3)元素周期表的分区与价层电子排布的关系
①周期表的分区
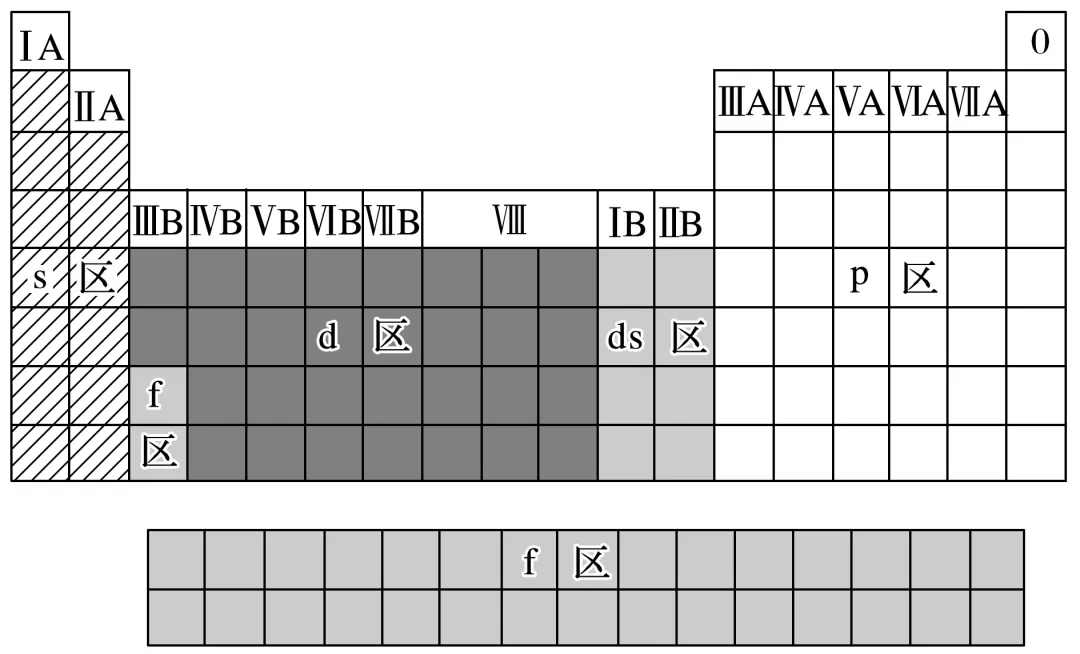
②各区价层电子排布特点
|
分区 |
价层电子排布 |
|
s区 |
ns1~2 |
|
p区 |
ns2np1~6(除氦外) |
|
d区 |
(n-1)d1~9ns1~2(除钯外) |
|
ds区 |
(n-1)d10ns1~2 |
|
f区 |
(n-2)f0~14(n-1)d0~2ns2 |
(1)影响因素电子层数:电子层数越多,原子半径越大核电荷数:电子层数相同,核电荷数越大, 原子半径越小
(2)变化规律
元素周期表中的同周期主族元素从左到右,原子半径逐渐减小;同主族元素从上到下,原子半径逐渐增大。
3.电离能
(1)第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,符号:I1,单位:kJ·mol-1。
(2)规律
①同周期:第一种元素的第一电离能最小,最后一种元素的第一电离能最大,总体呈现从左至右逐渐增大的变化趋势。
②同族元素:从上至下第一电离能逐渐减小。
③同种原子:逐级电离能越来越大(即I1<I2<I3…)。
4.电负性
(1)含义:元素的原子在化合物中吸引键合电子能力的标度。元素的电负性越大,表示其原子在化合物中吸引键合电子的能力越强。
(2)标准:以最活泼的非金属氟的电负性为4.0作为相对标准,计算得出其他元素的电负性(稀有气体未计)。
(3)变化规律
金属元素的电负性一般小于2,非金属元素的电负性一般大于2,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在2左右。
在元素周期表中,同周期从左至右,元素的电负性逐渐增大,同主族从上至下,元素的电负性逐渐减小。
5.对角线规则
在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,如。
【思维火花】
(1)钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能(×)
(2)第2周期主族元素的原子半径随核电荷数的增大依次减小(√)
(3)C、N、O、F四种元素第一电离能从大到小的顺序是N>O>F>C(×)
(4)正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族(√)
(5)价电子排布式为4s24p3的元素位于第4周期ⅤA族,是p区元素(√)
(6)元素的电负性越大,非金属性越强,第一电离能也越大(×)
(7)第3周期所有元素的第一电离能(I1)大小顺序为_________(用元素符号表示)。
(8)Na的逐级电离能中有___次突跃。分别是哪级电离能发生突跃? _____、____。
(9)F、Cl、Br、I的第一电离能由大到小的顺序为______,电负性由大到小的顺序为_____。
【答案】 (7)Na<Al<Mg<Si<S<P<Cl<Ar
(8)2 I2≫I1I10≫I9
(9)F>Cl>Br>I F>Cl>Br>I
关于元素周期表的应用技巧,敬请点击:
【高考热点】多维剖析元素周期表(律)的应用(本文12985字,可下载word版)
典题精练
1.表1是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
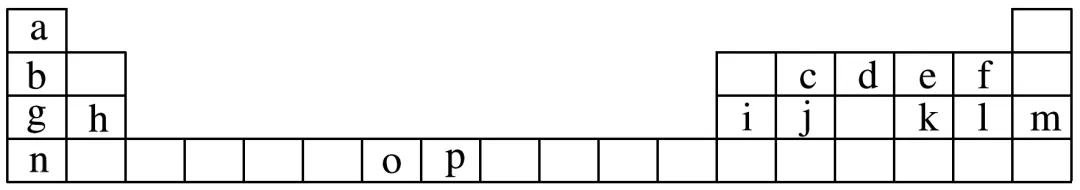
表1
(1)元素p为26号元素,请写出其基态原子电子排布式:__________。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因: _______________。
(3)o、p两元素的部分电离能数据如表2:
|
元素 电离能/kJ·mol-1 |
o |
p |
|
I1 |
717 |
759 |
|
I2 |
1 509 |
1 561 |
|
I3 |
3 248 |
2 957 |
表2
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________。
(4)第3周期8种元素单质熔点高低的顺序如图1所示,其中电负性最大的是_____(填图1中的序号)。
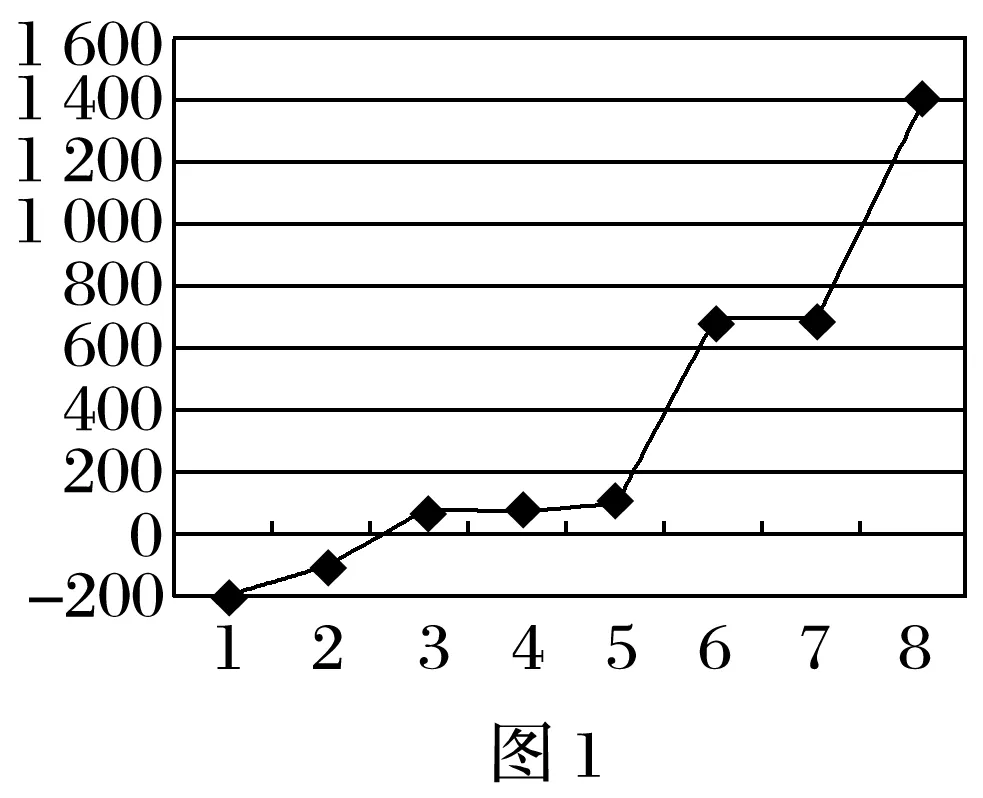
(5)表1中所列的某主族元素的电离能情况如图2所示,则该元素是__________(填元素符号)。
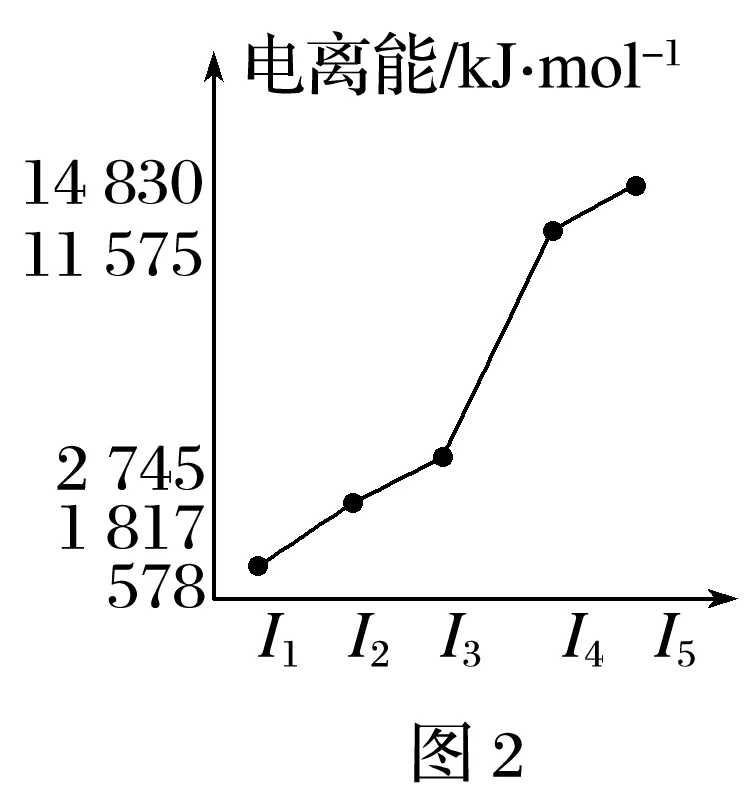
【答案】(1)1s22s22p63s23p63d64s2(或[Ar]3d64s2)
(2)电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量
(3)Mn2+的3d轨道电子排布为半充满状态,比较稳定
(4)2 (5)Al
【解析】 (2)h为Mg元素,Mg单质在空气中燃烧发出耀眼的白光,电子从能量较高的轨道跃迁到能量较低的轨道时以光(子)的形式释放能量。(3)o元素为Mn,其基态原子电子排布式为1s22s22p63s23p63d54s2,Mn2+的基态电子排布式为1s22s22p63s23p63d5,其3d能级为半充满状态,相对比较稳定,当其失去第3个电子时比较困难,而Fe2+的基态电子排布式为1s22s22p63s23p63d6,其3d能级再失去一个电子即为半充满状态,故其失去第3个电子比较容易。(4)第3周期8种元素分别为钠、镁、铝、硅、磷、硫、氯、氩,其单质中钠、镁、铝形成金属晶体,熔点依次升高;硅形成原子晶体;磷、硫、氯、氩形成分子晶体,且常温下磷、硫为固体,氯气、氩为气体,8种元素熔点最低的为氩,其次为氯,其中电负性最大的为氯。(5)由图可知,该元素的电离能I4 远大于I3,故为第ⅢA族元素,应为Al。
2.根据信息回答下列问题:
不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
电负性值 |
1.0 |
1.5 |
2.0 |
2.5 |
3.5 |
4.0 |
0.9 |
1.5 |
1.8 |
2.1 |
2.5 |
3.0 |
(2)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围_____。
(3)请归纳元素的电负性和金属性、非金属性的关系是_____________。
(4)推测AlF3、AlCl3、AlBr3是离子化合物还是共价化合物:
AlF3__________________,AlCl3____________________,AlBr3________________。
【答案】 (1)两 Be(OH)2+2H+===Be2++2H2O
Be(OH)2+2OH-===BeO2-2+2H2O
(2)0.9~1.5
(3)非金属性越强,电负性越大;金属性越强,电负性越小
(4)离子化合物 共价化合物 共价化合物
3.明代宋应星所著《天工开物》中已经记载了我国古代用炉甘石(主要成分为ZnCO3)和煤冶锌工艺,锌的主要用途是制造锌合金和作为其他金属的保护层。回答下列问题:
(1)Zn基态原子核外电子排布式为________________。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①与SO2-4互为等电子体的阴离子化学式为________(写出一种)。
②氨的热稳定性强于膦(PH3),原因是_________________。
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu<IZn的原因是_______________。
(4)《本草纲目》中记载炉甘石(主要成分为ZnCO3)可止血、消肿毒、生肌、明目等。Zn、C、O的电负性由大至小的顺序是________________。
【答案】 (1)1s22s22p63s23p63d104s2(或[Ar]3d104s2) (2)①PO3-4(或ClO-4) ②氮元素的非金属性强于磷元素 (3)锌失去的是全充满的4s2电子,铜失去的是4s1电子 (4)O>C>Zn
【解析】 (1)Zn是30号元素。位于元素周期表第4周期ⅡB族,故其基态原子核外电子排布式为1s22s22p63s23p63d104s2(或[Ar]3d104s2)。(2)①SO2-4为5原子32个价电子微粒,故与其互为等电子体的阴离子有PO3-4、ClO-4等。②氮元素的非金属性强于磷元素,故氨的热稳定性比膦强。(3)Cu与Zn的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu<IZn的原因是锌失去的是全充满的4s2电子,铜失去的是4s1电子。(4)通常非金属性越强的元素其电负性越大,且一般情况下,非金属的电负性比金属的电负性大,故Zn、C、O电负性由大至小的顺序是O>C>Zn。
为便于友友们阅读,现将各个合集的代表作展示如下,欢迎赐教:
(1)《氧化还原反应》合集:热点梳理:有关氧化还原反应的热考点
(2)《物质的量》合集:雾点警示:你知道摩尔命题有哪些魔坑吗
(3)《物质结构、元素周期律》合集:【克难秘技】巧解晶体投影、妙定粒子坐标
(4)《电化学》合集:“四步曲”搞定新情境下原电池电极反应式的书写
(5)《化学平衡、化学反应速率》合集:【同步教辅】《化学反应原理》专题复习之《化学平衡综合应用》
(6)《电解质溶液》合集:重点明示:有关弱电解质的三大考点
(7)《化学实验》合集:热点提升:常见两类实验,破解设计方案
(8)《有机化学》合集:热点专攻:如何巧解有机合成综合题
(9)《我的育人理念》合集:考后寄语:高考,人生的跳板而已
(10)《我的文学作品》合集:周末驿站:那个中午,我收到了3封情书
(11)《诗歌》合集:教师节抒怀诗词两首
特别提示:点击“合集”(操作方法见精选文章《本公众号使用说明书》)可以得到某合集所有考点的word版。


百度网盘:【专题突破】原子结构如何决定性质(可下载word版).doc
链接: https://pan.baidu.com/s/10XG4GSqYFX0qsDgtWEqvdw
提取码: 52cb
 夜雨聆风
夜雨聆风