JACI|AI如何重新解读哮喘遗传风险?
 这篇文章发表于2026年4月1日,第一完成单位为浙江大学医学院附属邵逸夫医院呼吸与危重症医学科。研究主要想解决一个问题:哮喘为什么会受遗传因素影响,以及能不能用人工智能把这些遗传风险找得更准。作者整合了欧洲人群中超大规模哮喘遗传数据,并结合嗜酸性粒细胞这一和哮喘密切相关的免疫指标,使用传统统计方法和基于Transformer的深度学习模型一起筛选风险变异。
这篇文章发表于2026年4月1日,第一完成单位为浙江大学医学院附属邵逸夫医院呼吸与危重症医学科。研究主要想解决一个问题:哮喘为什么会受遗传因素影响,以及能不能用人工智能把这些遗传风险找得更准。作者整合了欧洲人群中超大规模哮喘遗传数据,并结合嗜酸性粒细胞这一和哮喘密切相关的免疫指标,使用传统统计方法和基于Transformer的深度学习模型一起筛选风险变异。
研究目的
数 据
- GBMI 哮喘 GWAS 数据
包含欧洲血统人群中 121,940 例哮喘患者 和 1,254,131 名对照,是文章中最核心的哮喘遗传数据之一。 - MVP 哮喘 GWAS 数据
包含欧洲血统人群中 36,823 例哮喘患者 和 398,278 名对照,用于和 GBMI 数据进行大型 Meta 分析。 - UK Biobank/TAGC 哮喘数据
包含 88,486 例哮喘患者 和 447,859 名对照,主要用于深度学习模型训练相关分析。 - 血细胞性状 GWAS 数据
来自 746,667 人的跨种族血细胞遗传研究,文章重点使用其中欧洲人群的嗜酸性粒细胞数据,样本量为 474,237 人。 - CHOP 儿童哮喘验证队列
用于多基因风险评分验证,包括两个独立队列:
CHOP-HM 队列:1,302 例哮喘患者,2,636 名对照。
CHOP-GSA 队列:2,446 例哮喘患者,3,666 名对照。
模型构建
方法一:大规模哮喘 GWAS Meta 分析
作者首先把 GBMI 和 MVP 两个大型欧洲人群哮喘 GWAS 数据合并,进行固定效应 Meta 分析。简单理解,就是把两个大型数据库中的哮喘遗传信号整合到一起,提高统计效能,让原本在单个数据集中不够显著的风险位点更容易被发现。通过这一步,作者识别出大量与哮喘相关的全基因组显著位点,其中包含不少过去没有报道过的新位点,说明单纯整合更大规模数据,仍然可以扩展哮喘的遗传图谱。
方法二:哮喘与血细胞性状的遗传相关性分析
由于哮喘和免疫炎症密切相关,作者进一步比较了哮喘与多种血细胞指标之间的遗传相关性,包括淋巴细胞、单核细胞、嗜酸性粒细胞、中性粒细胞、白细胞等。结果发现,嗜酸性粒细胞与哮喘的遗传相关性最强。这一步的意义在于,它不是随便选择一个免疫指标来联合分析,而是先用遗传相关性证明:嗜酸性粒细胞确实和哮喘共享较强的遗传基础,因此后续把嗜酸性粒细胞作为辅助性状是有生物学依据的。
方法三:MTAG 多性状联合分析
MTAG 的作用是把哮喘和嗜酸性粒细胞两个相关性状放在一起分析,利用它们之间共享的遗传信息来提高发现能力。通俗来说,如果某个遗传变异在哮喘中信号不够强,但它同时也影响嗜酸性粒细胞,那么 MTAG 可以借助这个“共同线索”把它重新识别出来。文章中,作者把哮喘作为主要性状,把嗜酸性粒细胞作为辅助性状,最终发现了一批新的哮喘相关位点,说明联合免疫表型可以帮助补充传统 GWAS 的不足。
方法四:condFDR 条件假发现率分析
condFDR 也是一种利用两个相关性状进行遗传位点挖掘的方法。它的核心逻辑是:如果一个变异不仅和哮喘有关,同时也和嗜酸性粒细胞有关,那么这个变异是真实哮喘风险位点的可能性就更高。作者用嗜酸性粒细胞信息对哮喘 GWAS 结果进行重新排序和筛选,从而发现更多潜在哮喘相关位点。这个方法特别适合挖掘“单独看哮喘不够显著,但结合免疫指标后变得可信”的遗传信号。
方法五:Transformer 深度学习模型 InsightGWAS
文章最有创新性的部分,是作者建立了一个基于 Transformer 的深度学习框架 InsightGWAS,用来增强哮喘遗传变异的识别。这个模型不是只看传统 GWAS 的 P 值,而是同时整合效应值、样本量、等位基因频率、连锁不平衡信息、eQTL、染色质开放性、转录因子结合位点、功能注释和致病性评分等多层信息。简单理解,就是让 AI 同时学习“统计学信号”和“生物学功能信号”,从而判断哪些变异更可能与哮喘真正相关。结果显示,InsightGWAS 发现了更多候选位点,提示深度学习可以作为传统 GWAS 的补充工具。
方法六:多方法交叉验证新位点
为了避免单一方法带来的假阳性,作者把 Meta 分析、MTAG、condFDR 和 InsightGWAS 的结果放在一起比较。重点关注那些能被多种方法同时发现或支持的位点。这样做的好处是,如果一个位点既能被传统 GWAS 发现,又能被多性状分析支持,还能被深度学习模型识别,那么它的可信度就更高。文章最终筛选出一批跨方法一致的新位点,并进一步关注了 TNFRSF9、PIK3CD、NEGR1、AHR 等具有明确生物学意义的候选基因。
结果解读
Fig1 研究整体设计流程
文章先从三个大规模哮喘遗传数据库出发,分别进行常规 GWAS Meta 分析、哮喘与嗜酸性粒细胞的跨性状联合分析,以及基于 Transformer 的深度学习分析。随后,作者把不同方法筛选出的哮喘风险位点进行比较,并进一步构建多基因风险评分,最后在两个独立的儿童哮喘队列中验证预测效果。整体来看,Fig1 主要说明这项研究不是单纯做一个 GWAS,而是把“大样本统计分析 + 免疫相关性状 + 深度学习 + 独立队列验证”串成了一个完整分析流程。
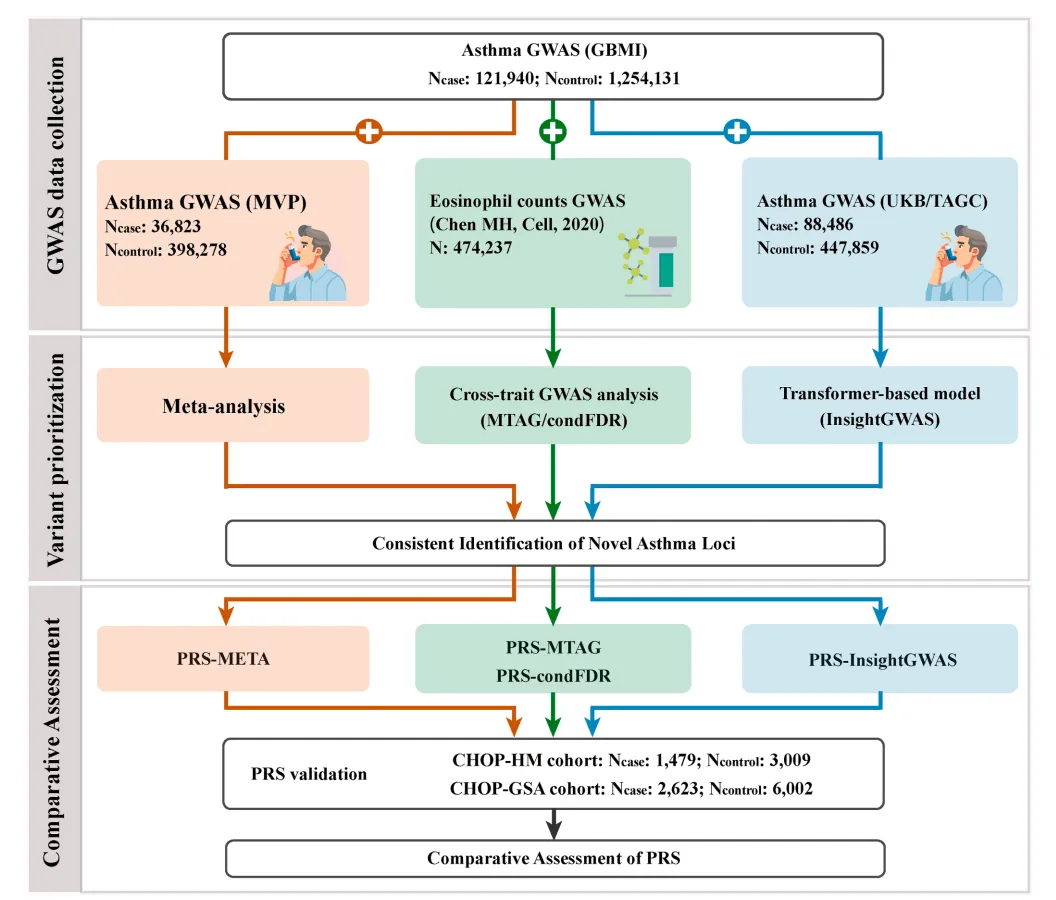
Fig2 新哮喘风险位点的全基因组定位
Fig2 展示了哮喘 GWAS Meta 分析得到的全基因组关联结果,以及几个代表性新位点的局部放大图。曼哈顿图中超过显著阈值的信号代表与哮喘风险显著相关的遗传区域,说明作者通过整合 GBMI 和 MVP 数据发现了大量哮喘相关位点。后面的局部图重点展示了 AHR、TNFRSF9、NEGR1、PIK3CD 等候选基因附近的风险变异,提示这些基因可能参与哮喘发生,尤其与免疫调控、炎症反应、气道反应性和环境刺激应答有关。
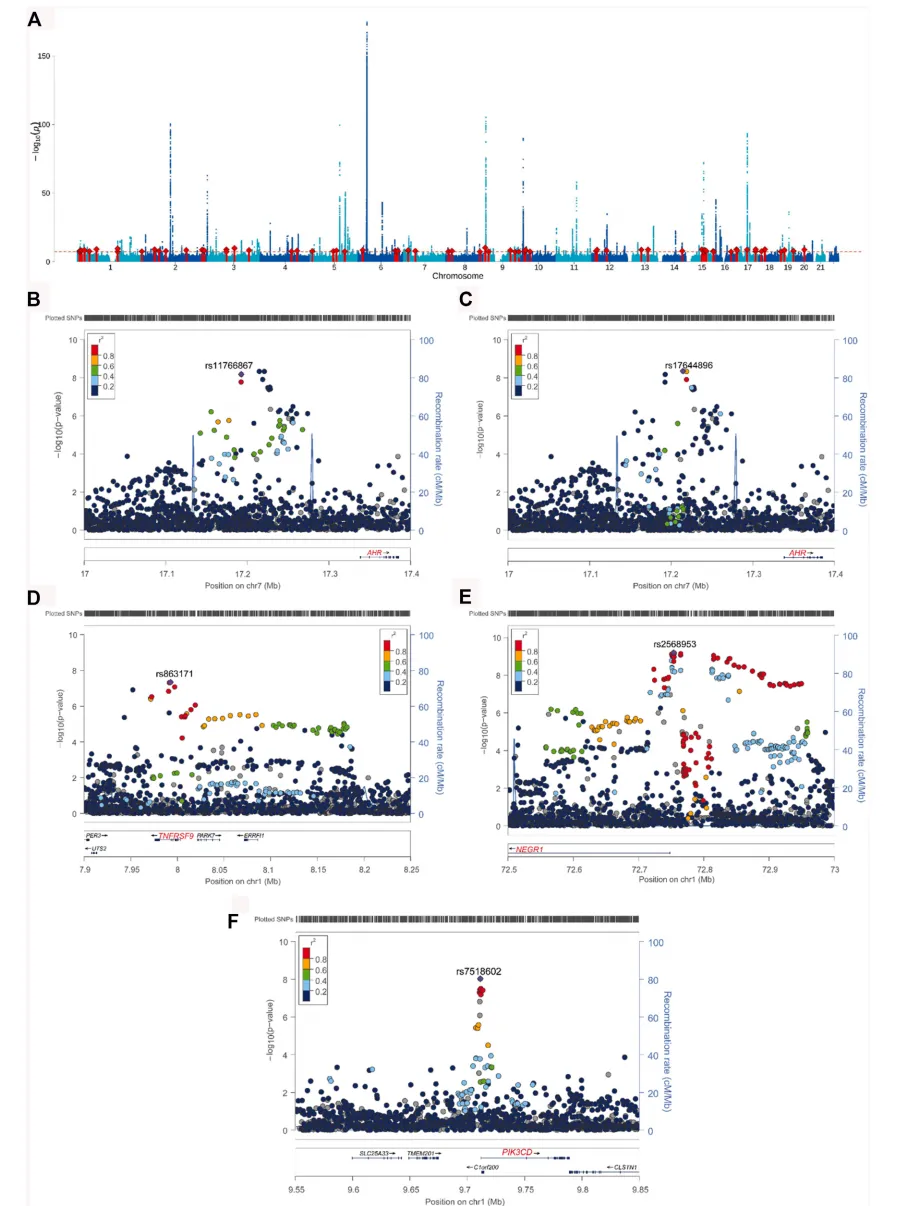
Fig3 多种方法共同支持的新风险位点
Fig3 用交集图展示了 Meta 分析、condFDR、MTAG 和 InsightGWAS 四种方法识别到的哮喘相关位点之间的重叠关系。可以看到,InsightGWAS 发现的候选位点数量最多,而部分位点同时被传统统计方法和深度学习方法识别出来。作者重点关注这些跨方法重复出现的位点,因为它们的可信度更高。这个结果说明,深度学习不是简单替代传统 GWAS,而是可以作为补充方法,帮助挖掘传统统计方法容易遗漏的遗传信号。
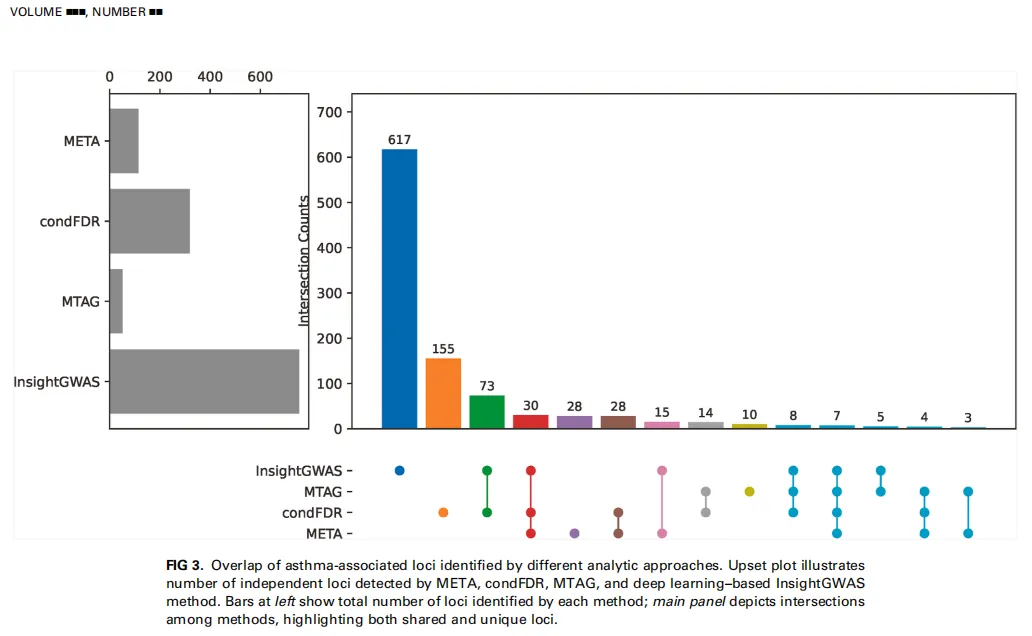
Fig4 不同方法构建的遗传风险评分表现
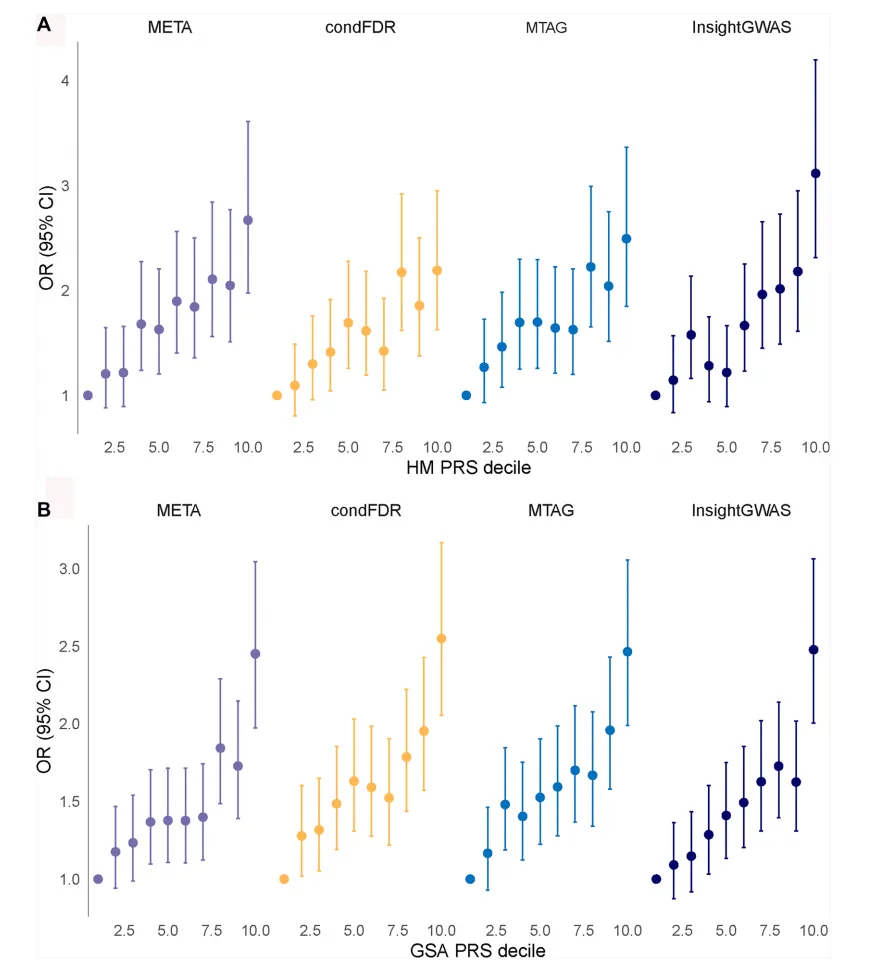
Fig4 比较了不同方法筛选出的遗传位点构建多基因风险评分后,对哮喘风险的预测能力。横坐标是遗传风险评分从低到高分成的不同等级,纵坐标是对应的哮喘风险。整体趋势是,随着风险评分升高,哮喘发生风险也逐渐升高,说明这些遗传位点确实具有一定预测价值。尤其是基于 InsightGWAS 筛选位点构建的评分,在部分验证队列中表现更好,提示深度学习筛出的位点不仅有统计意义,也可能更接近真实疾病相关信号。
总 结
Fig1 研究设计的核心价值
这项研究最大的特点,是把传统大样本 GWAS、跨性状统计方法和深度学习模型结合起来,而不是只依赖单一分析策略。作者认为,哮喘是一个高度复杂的多基因疾病,单纯增加样本量虽然有帮助,但很难完全解释疾病遗传结构。因此,通过引入嗜酸性粒细胞这一与哮喘密切相关的免疫表型,再结合 AI 模型进行变异优先级排序,可以从多个角度补充传统 GWAS 的不足。
Fig2 新风险位点提供了新的机制线索
作者在讨论中强调,研究发现的多个新位点具有明确的生物学意义。例如 PIK3CD 与免疫细胞功能、气道高反应性和炎症细胞募集有关;AHR 与黏膜免疫、环境刺激反应以及不同类型的炎症通路有关;TNFRSF9 和 NEGR1 可能与肥胖相关哮喘亚型有关。这说明这些新位点不只是统计学上的显著信号,而是可能指向哮喘不同亚型背后的真实机制。
Fig3 多方法重复出现的位点更可信
讨论部分特别强调,很多新位点不仅在 Meta 分析中出现,还能被 MTAG、condFDR 或 InsightGWAS 支持。也就是说,这些位点并不是某一种方法“偶然筛出来”的结果,而是在不同分析框架下都能得到验证。对于生信分析来说,这一点非常重要,因为复杂疾病研究中单一方法容易产生假阳性,而多方法交叉验证可以显著提高候选基因和候选位点的可信度。
Fig4 遗传风险评分具有一定转化潜力
作者认为,多基因风险评分的结果进一步支持了这些位点的实际价值。尤其是在两个独立儿童哮喘队列中,风险评分越高,哮喘风险整体越高,说明这些遗传变异可以帮助区分不同风险人群。虽然目前这种评分还不能直接用于临床诊断,但它为未来哮喘风险分层、早期筛查和精准预防提供了基础。

论文链接:
https://doi.org/10.1016/j.jaci.2026.03.016
 夜雨聆风
夜雨聆风




