供稿 | 别开枪-是我
审稿 | 吉星

2018 年 4 月,FDA 批准了一个叫 Fostamatinib 的小分子药物,商品名 Tavalisse™,适应症是慢性免疫性血小板减少症(ITP)——一种自身抗体攻击血小板、导致出血风险升高的自身免疫病。开发它的 Rigel 制药花了十几年才走完审批,市场反响不温不火:ITP 是个小市场,已有药物不少,Fostamatinib 只是多了一个选项。
最近帮合作者做一个药物重定位的项目 (这是其中一个案列), 我尝试使用小龙虾 + claude code 进行自动搜索文献、GEO 的转录组数据搜集和分析,查询各个公开数据库锁定靶点和候选分子、最终锁定 43 个候选药物并进行 300 轮配对比较——这个平平无奇的 ITP 药物以 100% 的胜率碾压所有对手,冲到 ANCA 相关性血管炎(AAV)候选药物排行榜的第一名。
AI 在 400 篇文献中看到了人类审稿人可能需要数月才能拼出的图谱。
ANCA 血管炎:一场针对自家血管的免疫风暴
要理解 Fostamatinib 为什么能排第一,要从 ANCA 血管炎的病理机制说起。
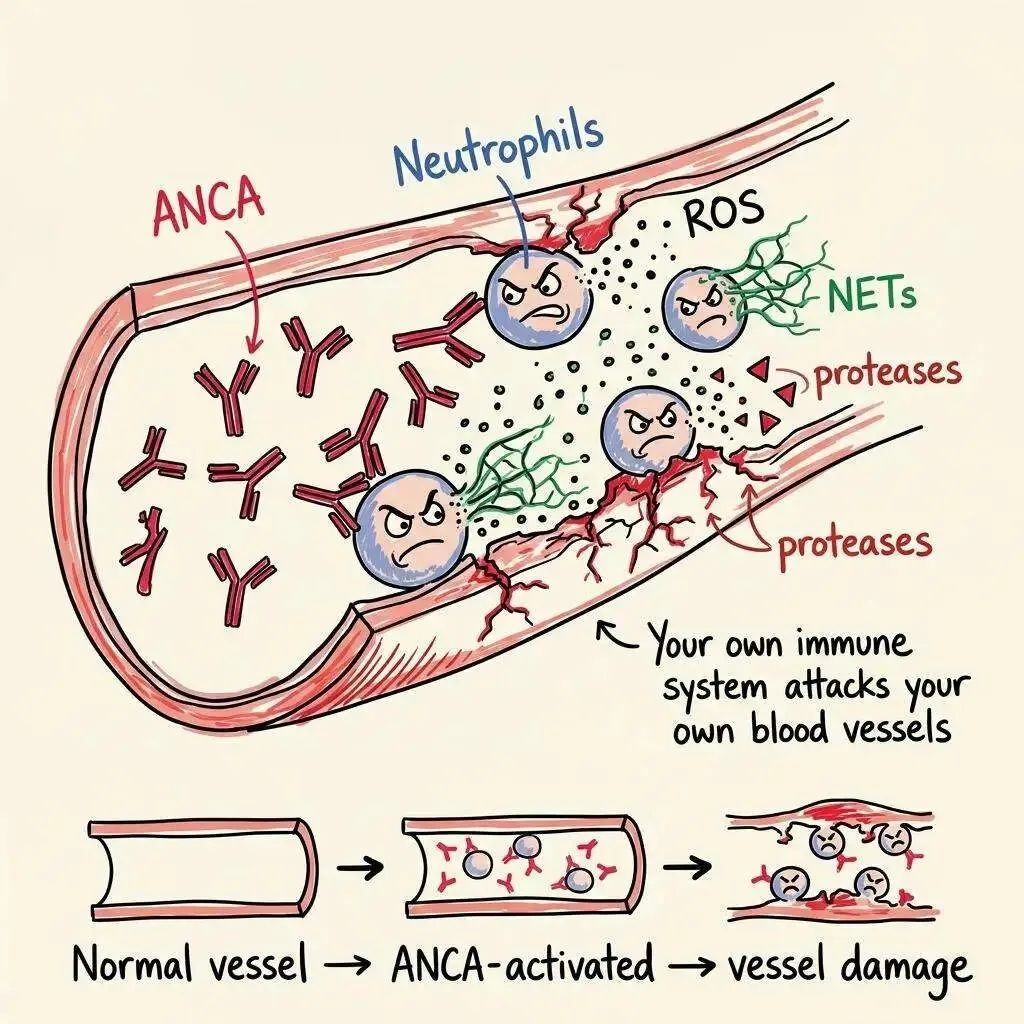
ANCA 血管炎的全称是"抗中性粒细胞胞质抗体相关性血管炎"——名字拗口,但病理逻辑清晰明了:患者体内产生一种自身抗体(ANCA),这种抗体靶向中性粒细胞表面的特定蛋白质(主要是 MPO 或 PR3)。抗体结合中性粒细胞后,通过 Fc 段与中性粒细胞表面的 Fc 受体(FcγR)交联,启动一连串胞内信号,把中性粒细胞从"巡逻兵"变成"自杀式炸弹"。
被 ANCA 激活的中性粒细胞不再安分地在血管里巡逻,而是牢牢粘附在血管内壁上,向血管壁释放活性氧、蛋白酶、中性粒细胞胞外陷阱(NETs)。小血管壁被反复攻击,坏死性炎症层层叠加。最终,肾小球新月体形成,肺泡出血,皮肤紫癜——这些都是 AAV 最典型的临床表现。
现有治疗是什么?利妥昔单抗或环磷酰胺——本质上是"关闭整个免疫系统"。好比你家厨房着火了,治疗方案是把整栋楼的电闸拉掉。火确实灭了,但你也什么都不能用了。感染风险飙升,长期副作用显著。
所以学术界一直在想:有没有办法只关掉"着火的那条线路",而不是拉整栋楼的电闸?
关掉"那条线路"的前提是——找到它的开关。
信号级联:从抗体到破坏的传导链
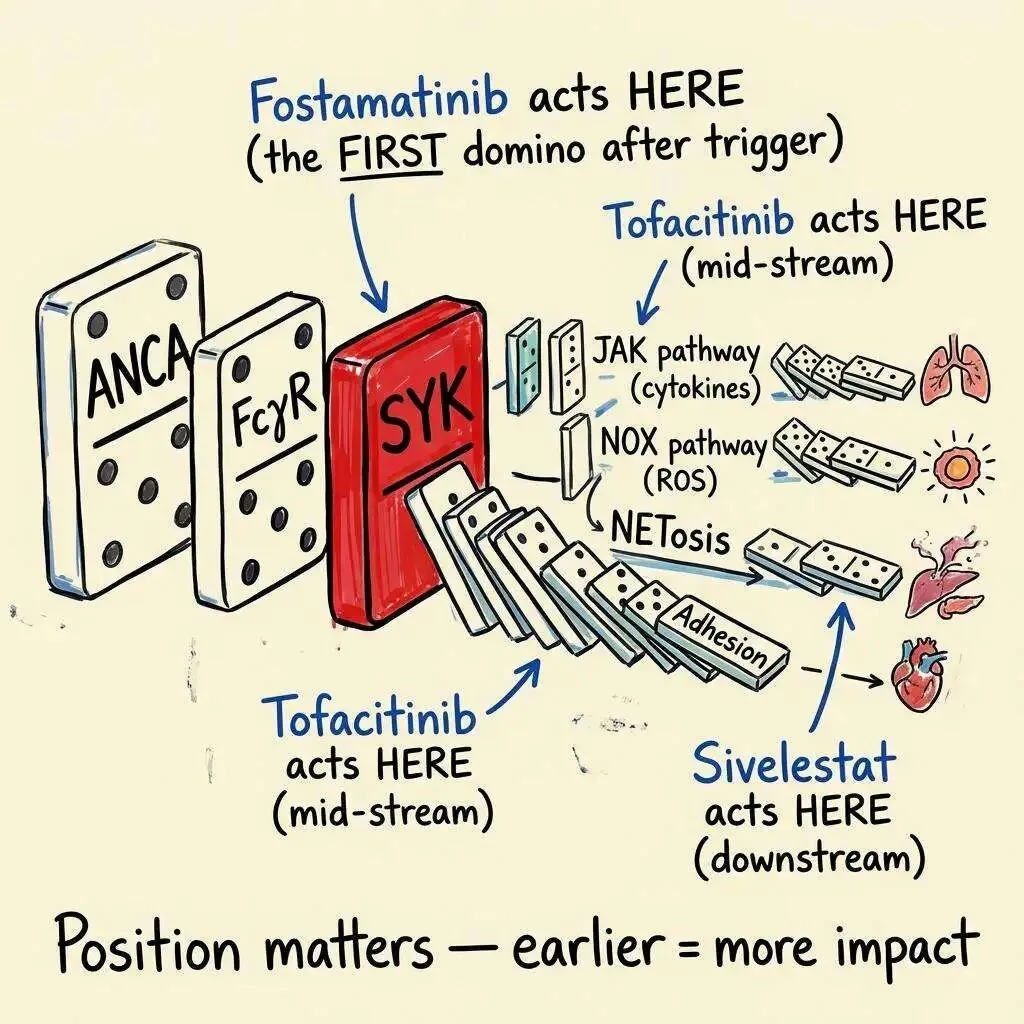
ANCA 激活中性粒细胞的过程不是一步到位的。它是一个信号级联——像多米诺骨牌一样,一环触发下一环:
ANCA 抗体 → 结合 FcγR → 激活胞内激酶 → 激活 NADPH 氧化酶 → 产生活性氧 → 脱颗粒 → NETosis → 粘附 → 血管壁损伤
在这条级联中,不同的靶点处于不同的位置。Tofacitinib(排名第三的候选药物)靶向的 JAK1/3 在这条级联的中下游——主要负责传递细胞因子的信号。GKT137831(排名第六)靶向的 NOX1/2 在级联的中游——负责活性氧的产生。Sivelestat(排名第二)靶向的中性粒细胞弹性蛋白酶更靠下游——保护被蛋白酶攻击的血管壁糖萼。
每一个靶点都有它的道理,每一个都经过文献验证,每一个都在某些动物模型中展示了疗效。
但它们都不在级联的最上游。
SYK:级联的第一张骨牌
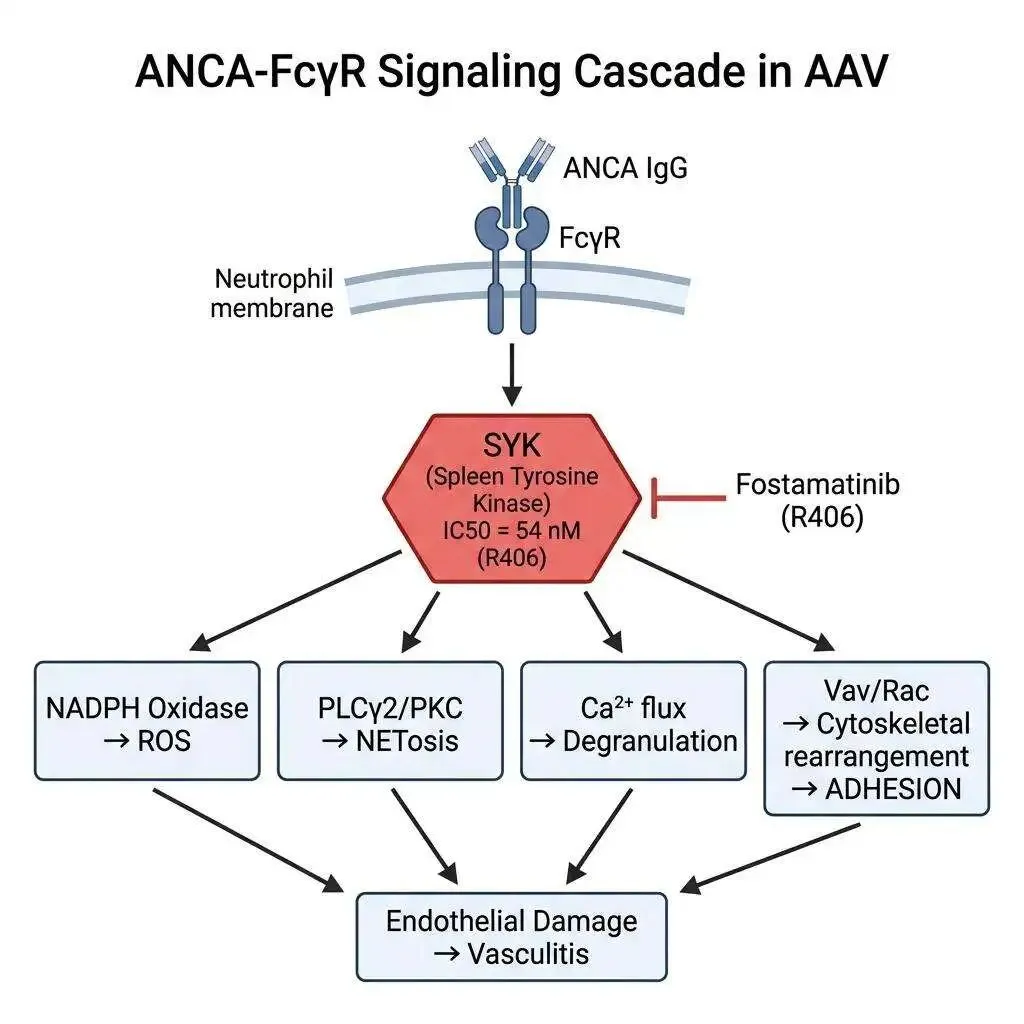
在 FcγR 的胞内信号中,ANCA 抗体与 FcγR 交联后,第一个被磷酸化的激酶不是 JAK,不是 PKC,不是 Rac——而是一个叫 SYK(脾酪氨酸激酶,spleen tyrosine kinase)的分子。
SYK 的磷酸化发生在 FcγR 被交联后的几秒钟内。它不依赖于任何其他中间信号——SYK 直接与 FcγR 的 ITAM 基序结合并自磷酸化。一旦 SYK 被激活,它就像一个总调度,同时向四个方向发出信号:
NADPH 氧化酶组装 → 产生活性氧(ROS) PLCγ2 → PKC → 触发 NETosis 钙动员 → 脱颗粒 Vav/Rac → 细胞骨架重排 → 粘附
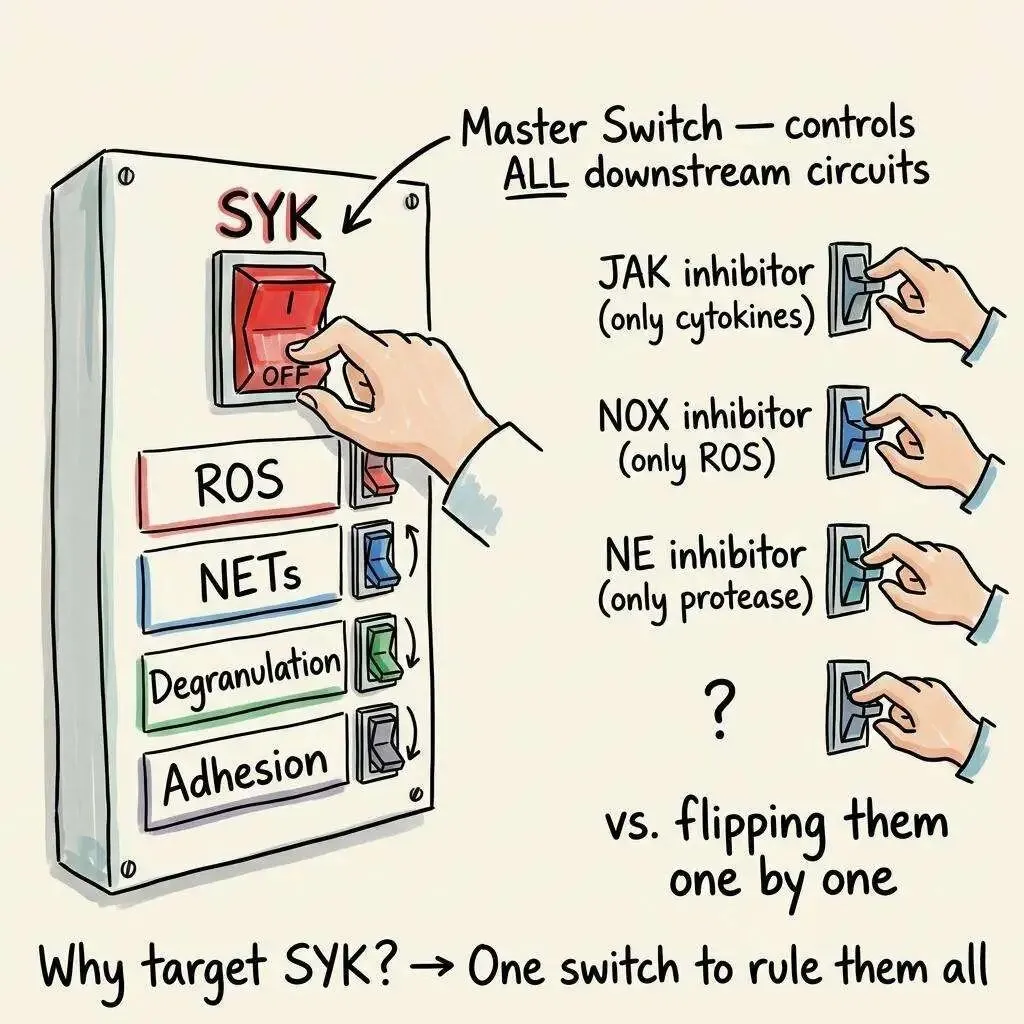
四条下游通路,全部从 SYK 这一个节点分叉出去。关闭 SYK,就同时关闭了活性氧、NETosis、脱颗粒、粘附——整条级联的所有破坏性输出。
这就是信号通路"位置"的力量。JAK 只管细胞因子那条线,NOX 只管活性氧那条线,NE 只管蛋白酶那条线——它们各自管各自的。SYK 管的是所有这些线路的总开关。
Fostamatinib(更准确地说,它的活性代谢物 R406)以 54 纳摩尔的 IC₅₀ 抑制 SYK。54 nM 意味着极强的靶点亲和力。而且 R406 对 SYK 的选择性约为 JAK2 的 10 倍——不是一颗散弹,而是相当精准的打击。
一个 FDA 已经批准了的、可以口服的、安全性数据已经有了的药物,恰好精准地命中了 ANCA 血管炎信号级联最顶端的那个节点。
这是概率的巧合,还是分子药理学的内在逻辑?
四条独立证据线
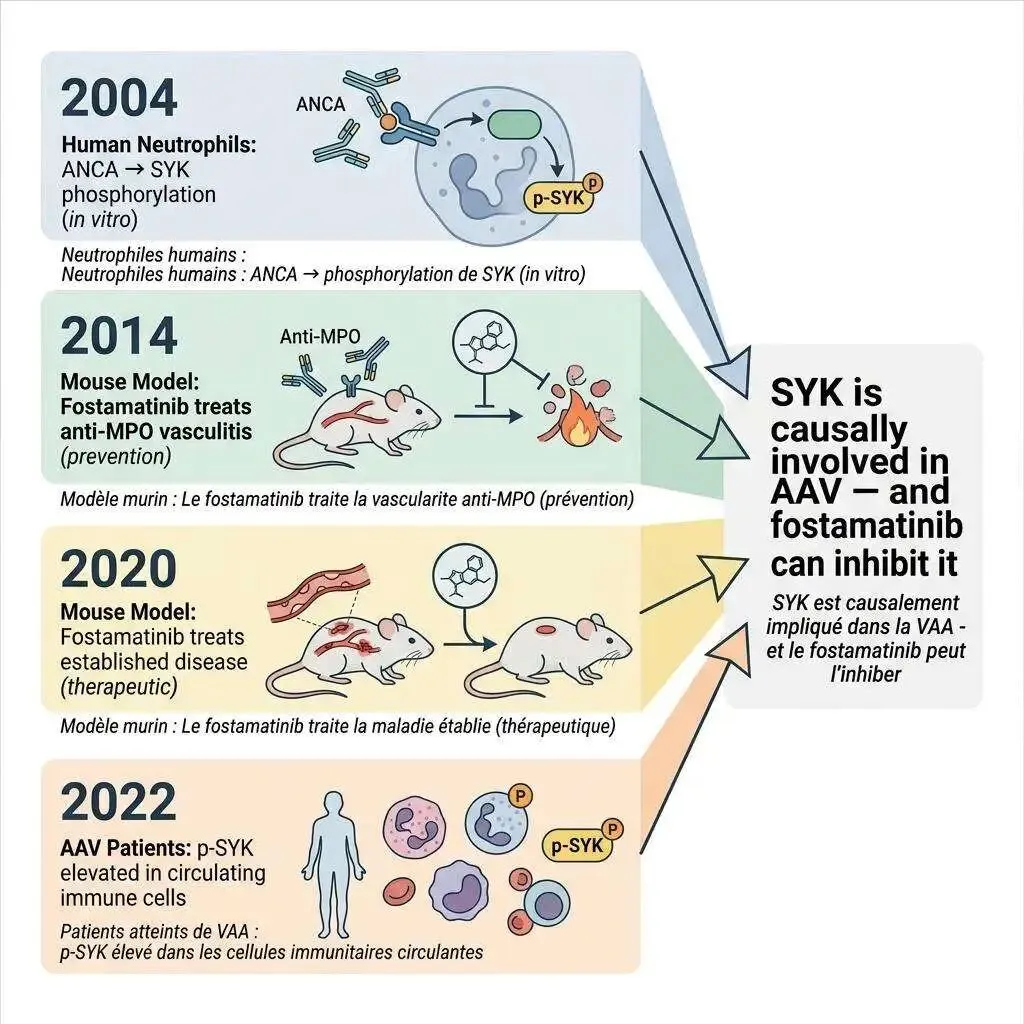
如果说 SYK 的"通路位置"是理论上的优势,那么让 Fostamatinib 真正脱颖而出的,是四条独立的实验证据——覆盖了从试管到动物到患者的全部层次。
第一条线:2004 年,人类中性粒细胞被 ANCA 激活后 SYK 被磷酸化
2004 年,发表在 Journal of the American Society of Nephrology 上的一项研究首次回答了一个基础问题:ANCA 抗体是否真的能激活中性粒细胞中的 SYK?
答案是肯定的。研究者用 anti-MPO 和 anti-PR3 IgG 处理人类中性粒细胞,观察到 SYK 在 Y348 位点发生了剂量依赖性的磷酸化。这意味着 ANCA → FcγR → SYK 这条通路在人类细胞中是真实存在的——不是从其他疾病类推的,而是用 ANCA 抗体、在人类中性粒细胞上、直接测量到的。
第二条线:2014 年,Fostamatinib 在 anti-MPO 血管炎小鼠模型中有效
十年后,McAdoo 等人在 Lancet 发表了一项决定性的研究。他们在抗 MPO 自身免疫性血管炎小鼠模型中测试了 Fostamatinib(R788)。这个模型能复现人类 AAV 的两大核心病理:新月体肾小球肾炎和肺出血。
结果:Fostamatinib 以 10 mg/kg BID 给药,显著减少了蛋白尿、肾小球新月体形成和肺出血评分。
在排名前五的 43 个候选药物中,这是唯一一个在 AAV 的标准动物模型中被直接测试并证明有效的。其他候选药物的动物数据要么来自脓毒症模型(Sivelestat),要么来自其他自身免疫模型(Tofacitinib 在类风湿关节炎中),但没有任何一个在 anti-MPO 血管炎模型中被测试过。
这条证据线的权重怎么强调都不过分:它是唯一的直接疾病模型证据。
第三条线:2020 年,Fostamatinib 对"已建立"的血管炎也有效
2014 年的研究可以被质疑:也许 Fostamatinib 只是预防了血管炎的发生,而不是治疗了已有的炎症。在临床中,患者来看病的时候疾病已经发生了,预防性给药毫无意义。
McAdoo 团队在 2020 年 Kidney International 的第二项研究直接回应了这个质疑。他们设计了一个"治疗窗口"实验——先让小鼠发展出血管炎,然后再开始给 Fostamatinib。结果:即便在疾病已经建立之后开始治疗,Fostamatinib 仍然有效。
这把 Fostamatinib 从"预防剂"升级为"治疗剂"——在临床场景中更有意义的定位。
第四条线:2022 年,AAV 患者循环免疫细胞中 SYK 确实被激活
以上三条证据有一个共同的局限:它们要么来自体外实验,要么来自小鼠模型——都不是人体内的直接观察。
2022 年,Tanna 等人在 Arthritis & Rheumatology 发表了一项关键的人群数据。他们采集了 AAV 患者的外周血,用磷酸化流式细胞术测量了循环单核细胞和中性粒细胞中的 p-SYK 水平。结果:AAV 患者的 p-SYK 显著高于健康对照组。
这意味着 SYK 不仅"在试管里可以被 ANCA 激活"(2004 年数据),也不仅"在小鼠里被激活了"(2014/2020 年数据),而是在活着的 AAV 患者体内就是激活状态的。
四条证据线:试管 → 小鼠预防 → 小鼠治疗 → 患者验证。从 2004 年到 2022 年,跨越 18 年,四个独立研究团队,四种不同的实验范式,指向同一个结论。
在 43 个候选药物中,没有第二个拥有如此完整的证据链。
为什么是第一而不是"第一等"

读到这里,一个自然的问题是:如果 Fostamatinib 的证据这么强,为什么它没有进入 AAV 临床试验?
答案很简单:因为从来没有人试过。
截至 2026 年,ClinicalTrials.gov 上没有任何一项将 SYK 抑制剂用于 AAV 的注册临床试验。相比之下,Tofacitinib(排名第三的 JAK 抑制剂)已经有 4 项 AAV 相关的注册试验。
这是一个吊诡的局面:证据这么强的候选药物反而在临床开发上最落后。背后的原因可能是多重的——SYK 抑制剂在 AAV 中的研究主要来自学术实验室而非制药公司;Rigel 制药的商业重心一直在血液学和免疫学的其他方向;AAV 是一个罕见病,市场规模不大,主动开展试验的商业动机不强。
但"没有临床试验数据"不等于"不值得做临床试验"。这两者之间的区别至关重要。Fostamatinib 不是因为失败了而没有进 AAV 临床试验,而是因为根本没有人做过——这是一个证据的空白(gap),而不是一个证据的否定(refutation)。
一瓢冷水
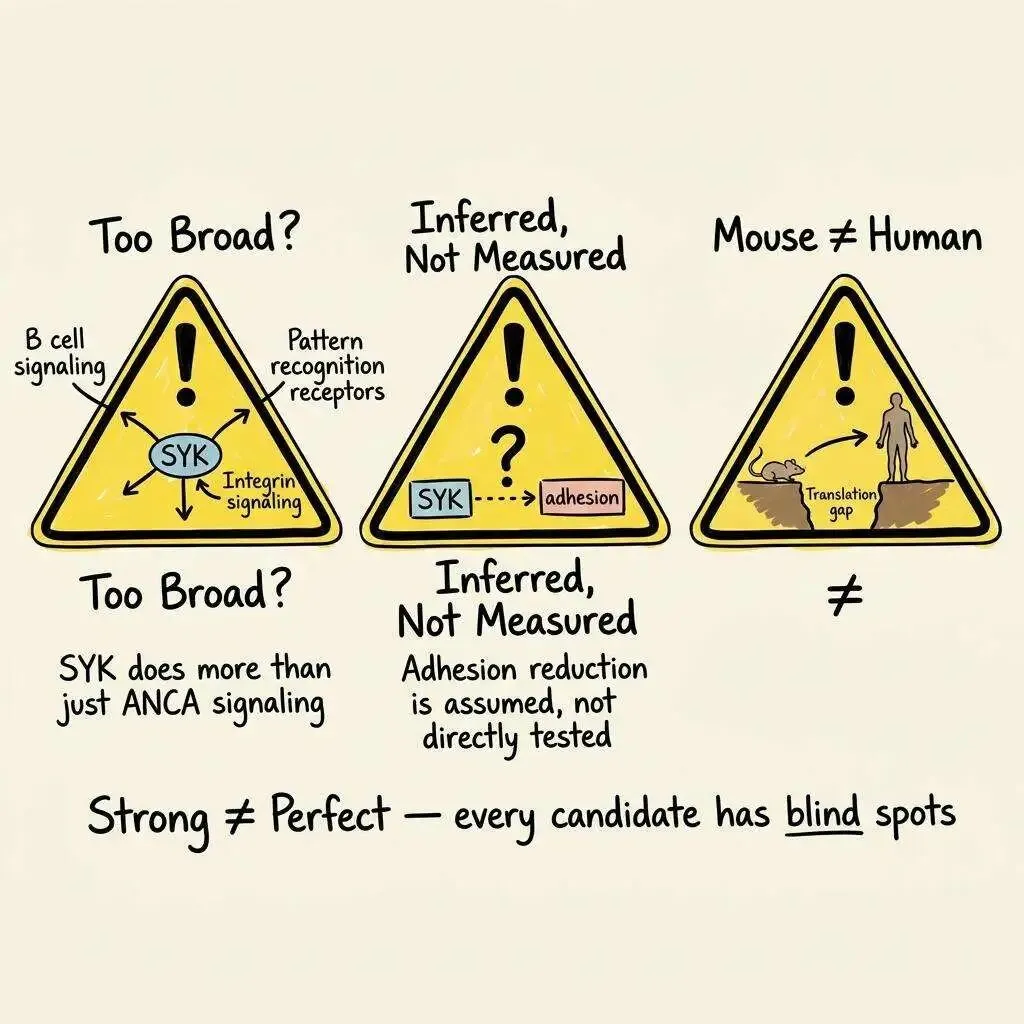
强不代表完美。在对 Fostamatinib 保持兴奋的同时,必须直面几个严肃的风险。
风险一:SYK 可能"管得太宽"。
SYK 不仅仅在 ANCA-FcγR 通路中发挥作用。它参与 B 细胞受体信号传导、模式识别受体信号传导、整合素信号传导——几乎所有涉及免疫受体的激酶级联都有 SYK 的影子。这意味着抑制 SYK 不只是"关掉 ANCA 那条线路",而可能同时关掉多条免疫防线。
一个 2024 年的信号值得注意:在镰刀细胞贫血小鼠中,Fostamatinib 被报道引发了血栓炎症反应。虽然镰刀细胞贫血和 AAV 的病理环境截然不同,但它提醒我们:SYK 抑制在特定凝血紊乱的背景下可能有意想不到的风险。AAV 患者是否存在类似的凝血激活基线,需要在临床试验中被仔细监测。
不过,Fostamatinib 已经在 ITP 患者中积累了多年的安全性数据。已知的主要副作用是高血压和贫血——可管理,非致命。ITP 的获批意味着其安全窗口至少是可以接受的。但 ITP 患者通常不处于系统性炎症状态,AAV 患者则不同。同一个剂量在更"火热"的免疫环境中是否安全,需要实际数据来回答。
风险二:粘附抑制是推断的,不是直接测量的。
Fostamatinib 的核心叙事是"SYK → 细胞骨架重排 → 中性粒细胞粘附"。但仔细审视证据链会发现:McAdoo 的两项小鼠研究测量的主要终点是蛋白尿、新月体和肺出血——这些是疾病整体结局的读数,而不是粘附本身的读数。
中性粒细胞沿血管壁的粘附减少,目前是从一般中性粒细胞生物学推断的,而不是在 AAV 条件下用 Fostamatinib 直接测量的。这个推断合理吗?非常合理——SYK → Vav/Rac → 肌动蛋白重排 → 粘附是教科书级的通路。但"教科书级的合理"和"实验证实"之间,始终有一道沟。
风险三:临床翻译的不确定性。
从小鼠到人,失败率之高已经不需要多说。AAV 的 anti-MPO 小鼠模型虽然是同类中最好的,但它不能完全复现人类 AAV 的复杂性——特别是人类疾病的慢性复发特征和多器官受累模式。
三个递进的实验
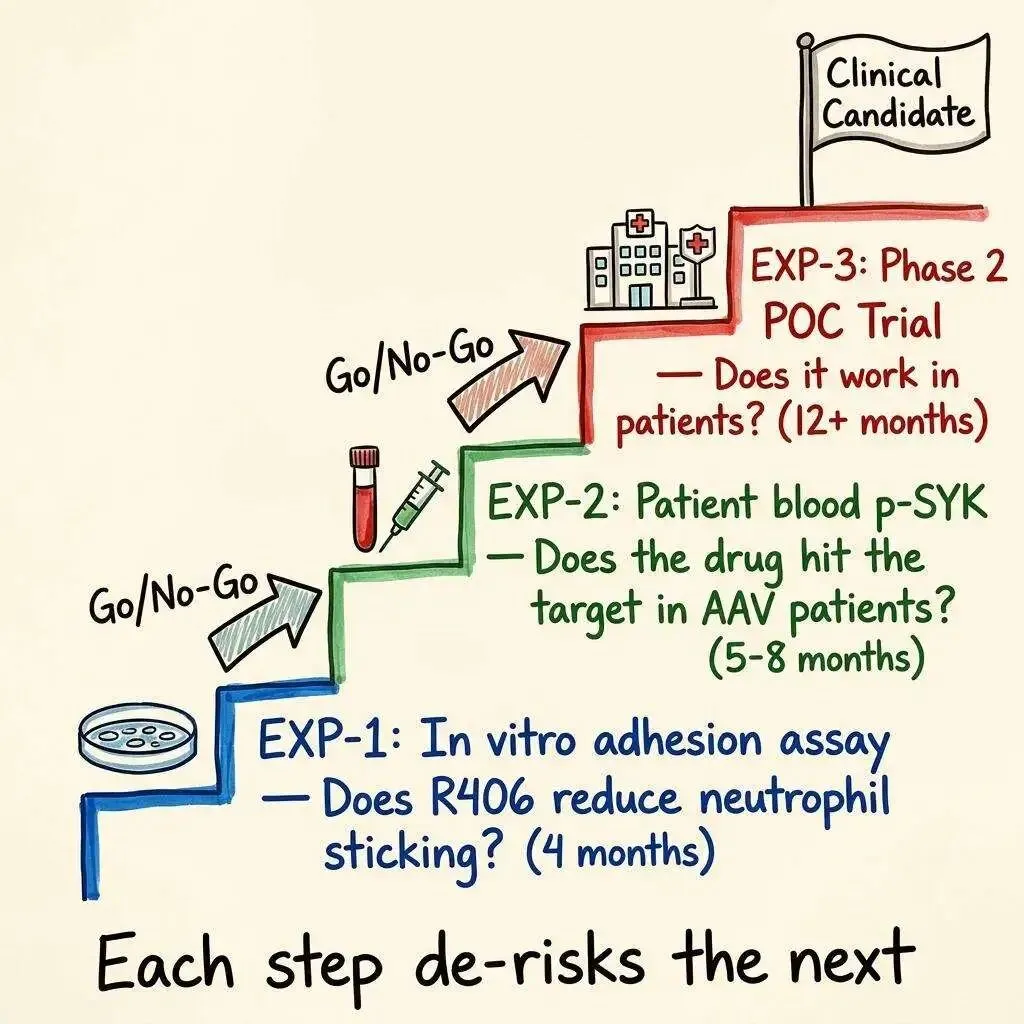
要把 Fostamatinib 从"最强候选"变为"可以写入临床试验申请"的分子,需要回答三个层层递进的问题,每一个都为下一个铺路。
实验一:Fostamatinib 能直接减少 ANCA 条件下中性粒细胞对内皮的粘附吗?
这是为了填补"粘附是推断的"那个缝隙。取人脐静脉内皮细胞(HUVEC)作为内皮层,用 ANCA 激活人中性粒细胞,然后以三个剂量梯度(0.1μM、1μM、10μM)加入 R406。读数:粘附中性粒细胞计数。关键判据:EC₅₀ 是否低于 100 mg BID 剂量下的血浆游离药物浓度(约 3μM)?如果低于,意味着 ITP 批准剂量就能达到有效粘附抑制。
是风险最低、信息密度最高的第一步。
实验二:AAV 患者外周血中的 p-SYK 能被 Fostamatinib 压下来吗?
2022 年 Tanna 的研究已经证明 AAV 患者的 p-SYK 是升高的。下一步是直接验证药物的靶标抑制:招募 20 名活动期 AAV 患者,给 Fostamatinib 150 mg BID 两周,Day 0 和 Day 14 取血,流式细胞术测 CD15⁺CD16⁺ 中性粒细胞中的 p-SYK MFI。配 10 名健康对照。
判成标准:p-SYK 降低 ≥ 50%。
这是一个药效学(PD)研究,不是疗效试验。它回答的不是"病好了没有",而是"药打到靶了没有"。如果 p-SYK 没有被压下来,后面的一切都不用做了。如果被压下来了,就有了 Phase 2 的药效学基盘。
取决于患者招募速度。
实验三:Phase 2 概念验证试验设计
如果前两个实验都是阳性的,就有了充分的理由去设计一个真正的临床试验。这不是"应该做"的建议,而是一个基于数据的必然推进——因为到那时,你手握的证据是:
54 nM 的靶点亲和力(ChEMBL), 人类中性粒细胞中 ANCA 确实激活 SYK(2004), 小鼠 AAV 模型中预防和治疗均有效(2014, 2020), 患者免疫细胞中 SYK 确实是激活的(2022), R406 在体外粘附实验中有效(实验一), Fostamatinib 在 AAV 患者血中压低了 p-SYK(实验二)。
六条证据线,跨越 20 年,完整覆盖了从生化到临床前到人体的所有验证层。
这是一个极少见的"由内而外"的药物重定位故事:不是先有临床观察再倒推机制(如伟哥从心血管药变为 ED 药),而是先有完整的机制证据链再推向临床——更慢,但更扎实。
所处的位置
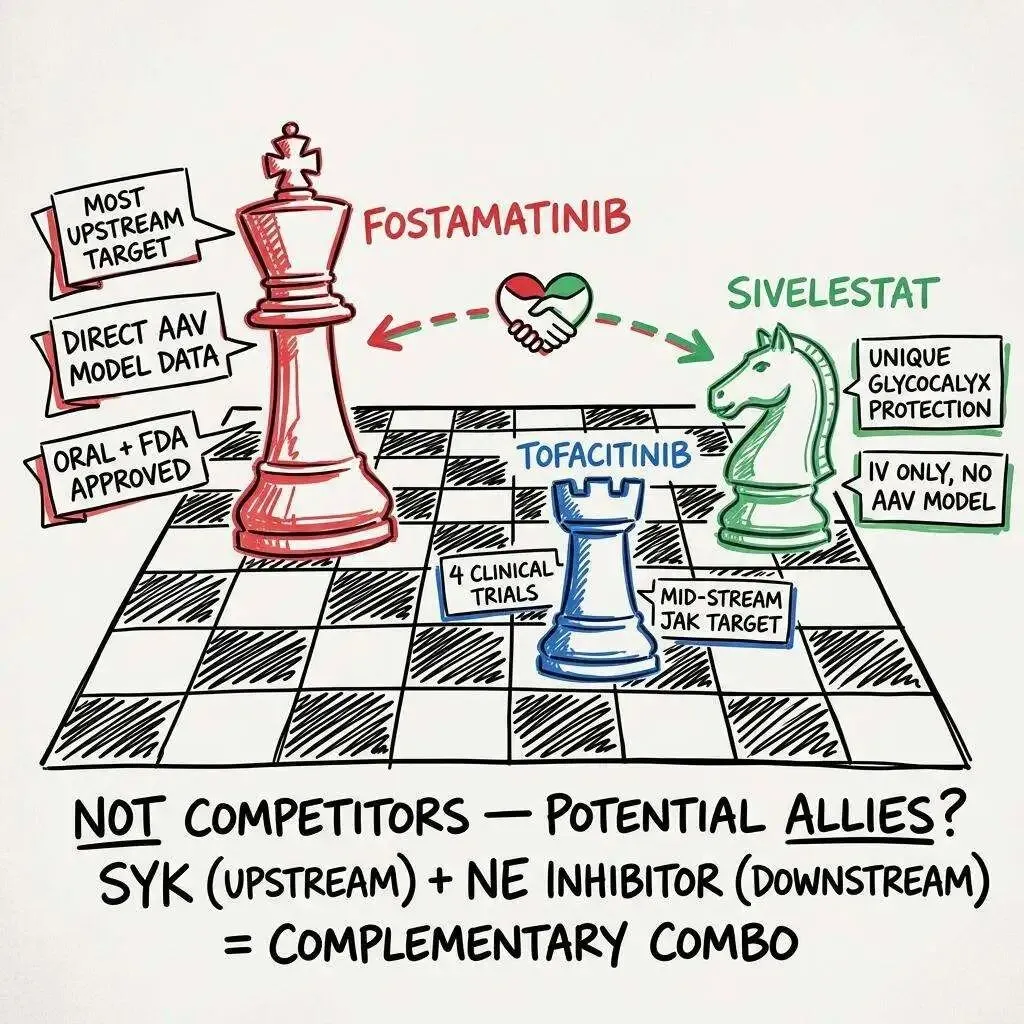
在 ANCA 血管炎的药物重定位棋盘上,Fostamatinib 占据的不只是排名第一的位置,而是一个独特的战略生态位。
Tofacitinib(排名第三)有 4 项注册临床试验——在临床开发的维度上遥遥领先。但 Tofacitinib 的 JAK 抑制发生在信号级联的中下游:它管的是细胞因子受体以后的事。ANCA → FcγR → SYK 这条通路的激活,Tofacitinib 几乎不干预。
Sivelestat(排名第二)拥有独特的糖萼保护机制——在概念新颖性上无出其右。但它的所有证据都来自脓毒症和 ARDS 模型,零条来自自身免疫性血管炎模型。而且 Sivelestat 是 IV 制剂,半衰期只有 2-3 小时——对 AAV 这种慢性病来说几乎不具备临床可行性。
Fostamatinib 的差异化在于三个属性的交集:最上游的靶点 × 直接的 AAV 模型数据 × 口服给药 + FDA 已批准安全性。这三个属性中任何一个单独拿出来都不算稀奇,但三者同时成立的候选药物,在 43 个候选里只有这一个。
更有趣的是,Fostamatinib 与其他候选药物之间并不完全是竞争关系。SYK 处于级联最上游,Sivelestat 保护的是下游的血管壁——理论上,"SYK 抑制 + NE 抑制"是一个上下游互补的组合策略。关闭总开关的同时在末端加一层保护,逻辑上比两者择一更完整。虽然这种联合方案目前纯属推测,但它暗示了一种可能性:AAV 的最优治疗策略可能不是选一个"最好的靶点",而是一个精心设计的多靶点组合。
综合评分:它比 Sivelestat 强在哪里
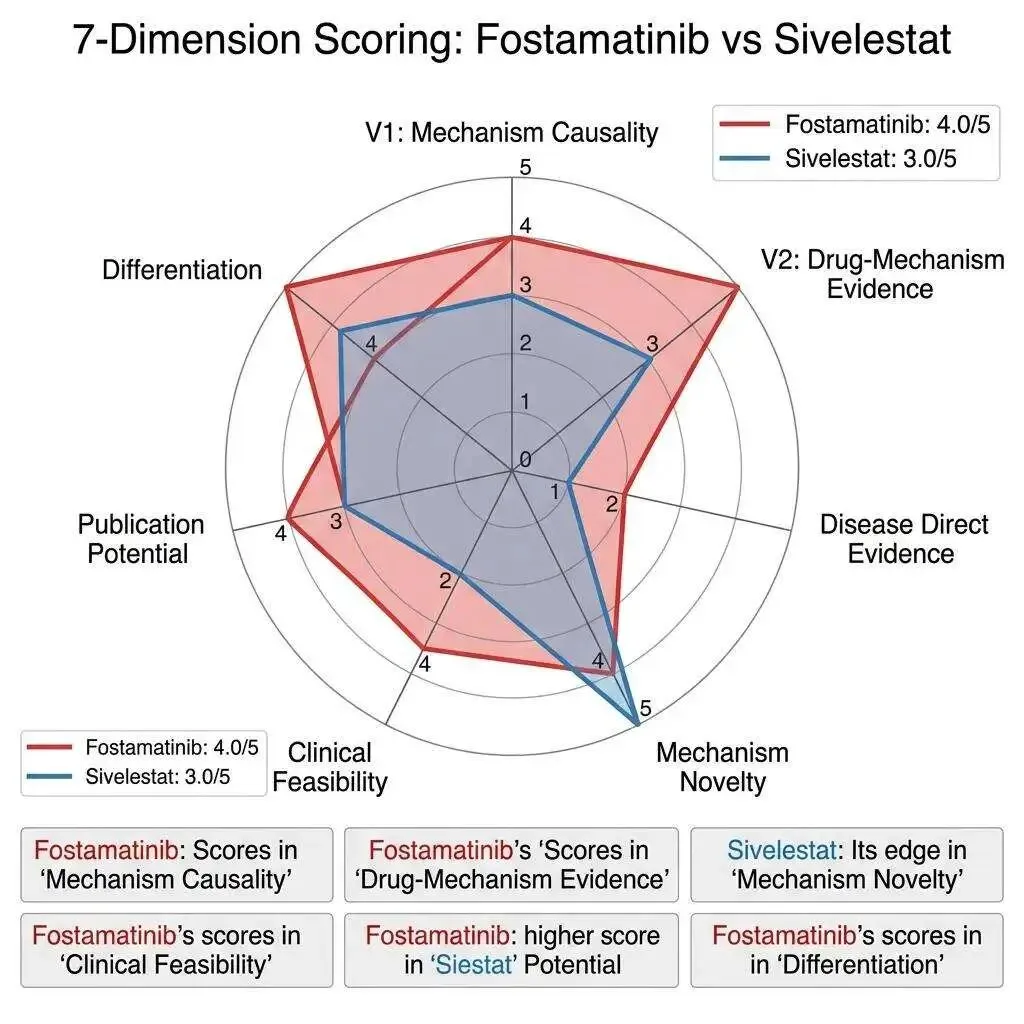
在报告使用的七维评分体系中,Fostamatinib 的总分是 4.0/5——显著高于 Sivelestat 的 3.0/5。差距主要体现在三个维度:
药物 - 机制证据(V2):5/5 vs. 3/5。Fostamatinib 有四条独立证据线覆盖从生化到患者的全部层次,而 Sivelestat 的证据全部来自脓毒症/ARDS 模型,"类推距离"太远。
疾病直接证据:2/5 vs. 1/5。虽然两者都没有人体 AAV 临床数据,但 Fostamatinib 有两项 anti-MPO 小鼠模型研究(McAdoo 2014, 2020)+ 患者免疫细胞 p-SYK 数据(Tanna 2022)。Sivelestat 在 AAV 模型中的数据是零。
临床可行性:4/5 vs. 2/5。口服、已批准、半衰期 14.6 小时 vs. IV、仅日本批准、半衰期 2-3 小时。在慢性自身免疫病的治疗场景中,这不是"方便不方便"的问题,而是"能不能真正做临床试验"的问题。
唯一一个 Sivelestat 胜出的维度是机制新颖性(5/5 vs. 4/5)——糖萼保护作为 AAV 治疗策略确实闻所未闻,而 SYK 抑制虽然在 AAV 中未被探索过,但 SYK 本身在免疫学中已经被研究了几十年。新颖性不等于证据强度,但它意味着更高的发表价值和更大的科学惊喜因子。
它最终意味着什么

Fostamatinib 的故事和 Sivelestat 代表了药物重定位的两种截然不同的范式。
Sivelestat 是探路者——它可能是第一个证明"糖萼保护"在 AAV 中行得通的概念验证工具,但它自身不太可能成为 AAV 的治疗药物。它的价值在于打通一条新通路,然后让更好的分子来接棒。
Fostamatinib 则是候选人——一个有真实可能性自身成为 AAV 治疗药物的分子。它口服给药,半衰期合理,安全性已知,剂量可以从 ITP 批准剂量直接外推。如果 Phase 2 POC 试验成功,从"候选人"到"获批药物"的路径虽然漫长但清晰可见。
这是一个罕见的情形:通常在药物重定位中,你要么有好的机制假说但缺乏直接疾病模型数据,要么有临床观察但缺乏机制解释。Fostamatinib 两者都有——缺的只是最后一步:有人在 AAV 患者身上按下"开始"键。
在药物开发的世界里,有一种特殊的悲哀叫做"被证据支持但没人推进"。无数有潜力的分子不是因为错误而被搁置,而是因为商业逻辑、资源分配、学术关注度等与科学无关的因素,静静地待在文献中无人问津。
Fostamatinib 在 AAV 中的位置正处于这个危险地带。四条独立证据线已经铺好了路,但路的尽头还没有人踏出第一步。
54 纳摩尔的亲和力。100% 的配对胜率。两项发表在 Lancet 和 Kidney International 上的阳性动物实验。一群 AAV 患者免疫细胞中亮着的 p-SYK 信号。一切都在说:这条路值得走。
但在没有人体临床试验数据之前,这一切仍然是——逻辑自洽的、多线验证的、但尚未在真正的患者身上被检验的——假说。
只不过,它是 43 个假说中站得最稳的那一个。
小结
SYK——中性粒细胞的信号级联中第一个被磷酸化的分子——可能是 AAV 治疗中一个被严重低估的"总开关"。
Fostamatinib 是一个 2018 年 FDA 批准的 SYK 抑制剂,原本用于免疫性血小板减少症。但在一条针对 ANCA 血管炎的药物重定位管线中,它以 100% 的配对胜率(14W/0L)碾压了其他 42 个候选药物。核心原因不是因为它本身多特别,而是因为它精准命中了 ANCA-FcγR 信号通路的最顶端——SYK。
四条独立证据线跨越 18 年,从人类中性粒细胞体外实验(2004)→ 小鼠 AAV 模型预防(2014)→ 小鼠 AAV 模型治疗(2020)→ AAV 患者免疫细胞验证(2022),全部指向同一个结论。
"在 43 个候选药物中,Fostamatinib 是唯一一个在 ANCA 血管炎的标准动物模型中被直接测试并证明有效的。"
最吊诡的是:拥有最强证据的候选药物,在临床开发上反而是最大的空白。ClinicalTrials.gov 上零项 AAV 相关 SYK 抑制剂试验。所有的拼图都摆好了,但还没有人把最后一块放上去。综合评分 4.0/5——在 43 个候选药物的最高分。不是概念验证工具,而是一个有真实可能性成为治疗药物的分子。前提是,有人愿意启动那个 Phase 2 试验。
重要参考文献
McAdoo S, et al. SYK inhibition in experimental autoimmune vasculitis. Lancet 2014; 383: 2031-2037. doi: 10.1016/s0140-6736(14)60335-4 McAdoo S, et al. Spleen tyrosine kinase inhibition is an effective treatment for established vasculitis in a pre-clinical model. Kidney Int 2020; 97: 1043-1053. doi: 10.1016/j.kint.2019.12.014[1] Tanna A, et al. Syk Activation in Circulating and Tissue Innate Immune Cells in ANCA-associated Vasculitis. Arthritis Rheumatol 2022; 74: 1533-1544. doi: 10.1002/art.42321[2] Tanna A, et al. Activation of Syk in neutrophils by antineutrophil cytoplasm antibodies. J Am Soc Nephrol 2004; 15: 2198-2204. doi: 10.1097/01.asn.0000113241.98702.77[3] R406 reduces LPS-induced neutrophil activation. Cell Immunol 2024. doi: 10.1016/j.cellimm.2024.104860[4] SYK inhibition restores myeloid homeostasis in COVID-19. Sci Adv 2023. doi: 10.1126/sciadv.ade8272[5] Fostamatinib attenuates lupus in FcγRIIb⁻/⁻ mice. Cell Death Discov 2025. doi: 10.1038/s41420-025-02342-x[6] Short-term fostamatinib in sickle cell mice. Blood 2024. doi: 10.1182/blood-2024-205346[7] Investigational SYK inhibitors for autoimmune diseases. Exp Opin Invest Drugs 2022. doi: 10.1080/13543784.2022.2040014[8] Rigel Pharmaceuticals. FDA NDA 209255 (fostamatinib). 2018. ChEMBL compound record: CHEMBL2103830[9] :::
10.1016/j.kint.2019.12.014: https://doi.org/10.1016/j.kint.2019.12.014
[2]10.1002/art.42321: https://doi.org/10.1002/art.42321
[3]10.1097/01.asn.0000113241.98702.77: https://doi.org/10.1097/01.asn.0000113241.98702.77
[4]10.1016/j.cellimm.2024.104860: https://doi.org/10.1016/j.cellimm.2024.104860
[5]10.1126/sciadv.ade8272: https://doi.org/10.1126/sciadv.ade8272
[6]10.1038/s41420-025-02342-x: https://doi.org/10.1038/s41420-025-02342-x
[7]10.1182/blood-2024-205346: https://doi.org/10.1182/blood-2024-205346
[8]10.1080/13543784.2022.2040014: https://doi.org/10.1080/13543784.2022.2040014
[9]CHEMBL2103830: https://www.ebi.ac.uk/chembl/compound_report_card/CHEMBL2103830/
 夜雨聆风
夜雨聆风