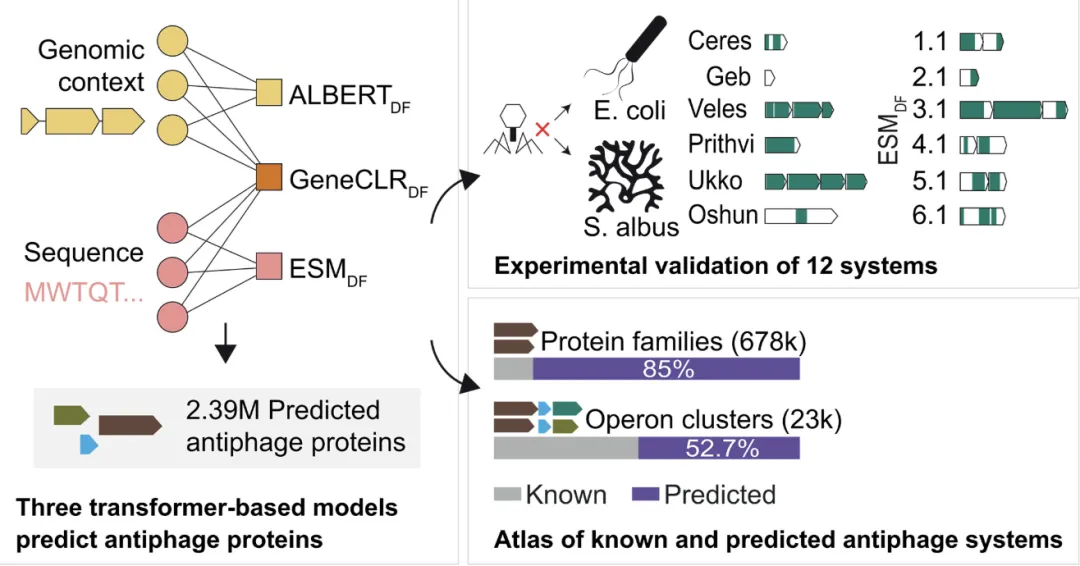
细菌编码了高度多样化的抗病毒防御系统,目前已有超过250种系统通过实验验证,涵盖广泛的分子机制。随着计算与实验筛选的持续推进,新的防御系统不断被发现,表明其真实多样性远超当前认知。然而,抗噬菌体防御系统的整体规模与组成仍未被系统解析。 尽管多样性尚不明确,已知防御系统在蛋白序列与基因组结构层面呈现出一定共性特征,例如特定功能结构域,以及在“防御岛”或前噬菌体区域的富集。这提示抗噬菌体系统可通过跨机制的模式进行识别,而不仅依赖传统的序列同源性。 2026年4月2日,法国巴斯德所Aude Bernheim 团队在《Science 》发表研究,构建了三种互补的蛋白质与基因组语言模型,实现对抗噬菌体系统的规模化识别, 系统发掘出海量新型抗噬菌体蛋白,构建了细菌抗噬菌体防御系统图谱数据库 ,显著拓展了对细菌免疫体系的整体认知 。 主要结果 (1)开发三种互补的深度学习模型,突破传统同源性搜索局限,实现泛基因组尺度的抗噬菌体功能预测: a)ALBERTDF:基于局部基因组上下文推断防御功能,不依赖蛋白序列; b)ESMDF:基于蛋白质语言模型,从氨基酸序列中提取特征; c)GeneCLRDF:整合序列与基因组信息,性能最佳,在基准测试中达到99%精确率和92%召回率。 (2)通过在大肠杆菌和白色链霉菌中的实验验证,鉴定出12种此前未知的抗噬菌体防御系统,证实模型预测的可靠性。 (3)新发现系统涵盖多种功能结构域(如脱氧核酸酶、肽酶等),并包含此前未与抗病毒免疫相关的蛋白类型,表明模型能够捕捉超越已知机制的功能特征。 (4)在超过32,000个细菌基因组中进行系统预测,结果显示平均约1.5%的基因参与抗病毒防御,其中超过85%的蛋白家族此前未被注释为免疫相关。 (5)共预测约239万个抗噬菌体蛋白,形成约23,000个操纵子家族,其中绝大多数为全新防御单元。 (6)基于上述结果构建细菌抗病毒免疫图谱(atlas),揭示一个远超既往认知的广阔防御体系,并通过交互式平台公开共享。 研究意义 (1)提出了用于大规模发现抗噬菌体防御系统的深度学习框架,并构建了系统性的细菌抗噬菌体免疫图谱。 (2)该方法显著拓展了对细菌免疫多样性的认识,并为后续的功能研究与机制解析提供了重要基础。 Ernest Mordret et al. ,Protein and genomic language models uncover the unexplored diversity of bacterial immunity.Science392,eadv8275(2026). DOI:10.1126/science.adv8275