在癌症诊疗的复杂战场上,“原发灶不明肿瘤(Carcinoma of Unknown Primary, CUP)”如同迷雾中的暗礁,让无数患者和医生举步维艰。今天要讲述的,正是这样一位在迷雾中突围的患者——从颈部肿物的初现,到AI技术点亮诊疗方向,再到历经多线治疗达到疾病缓解,孙女士的故事,是AI赋能癌症精准医疗的生动案例。
在2021年的某天,孙女士突然发现她的颈部出现一个肿物,那时她并未在意,可在一年后当她走进医院对肿物进行穿刺检测时,结果如同一记重锤,打破了生活的平静。孙女士2022年7月的CT报告结果显示:颈部、纵隔有多发增大的淋巴结,双肺有少许慢性炎性灶,左肾存在囊肿。三天后,孙女士拿到肿物穿刺病理报告,结果提示右颈部转移的低分化腺癌,结合免疫组化结果,确诊为低分化腺癌,病理诊断明确肿瘤亚型,但没有肿瘤的来源,医生尝试用免疫组化的各项指标结果进行匹配,却始终无法明确肿瘤具体的原发部位。“原发不明”,这四个字像一块石头压在患者和家属的心头,不知道病灶从哪里来,又该如何精准治疗?迷茫如同潮水将他们淹没。
就在治疗一筹莫展时,孙女士在2022年8月做的NGS基因检测结果带来了关键线索:HER2 基因有两处激活突变,CDKN2A、CDKN2B 基因缺失,TP53 基因突变,肿瘤突变负荷(TMB)高达14.7Muts/Mb,提示免疫治疗敏感。紧接着,AI驱动的肿瘤预测报告也有了结果,通过对孙女士的基因特征、免疫组化等多维度数据分析,肿瘤来源的范围大幅缩小,最终,肺腺癌被列为高概率倾向类型。虽然肿瘤预测不能直接确诊肿瘤来源,但在原发灶不明肿瘤的诊疗中扮演着至关重要的“导航”角色,它通过大数据分析排除干扰项,为医生提供了重要的决策参考,让后续治疗更具针对性,避免了盲目尝试治疗带来的身体损伤和时间消耗。
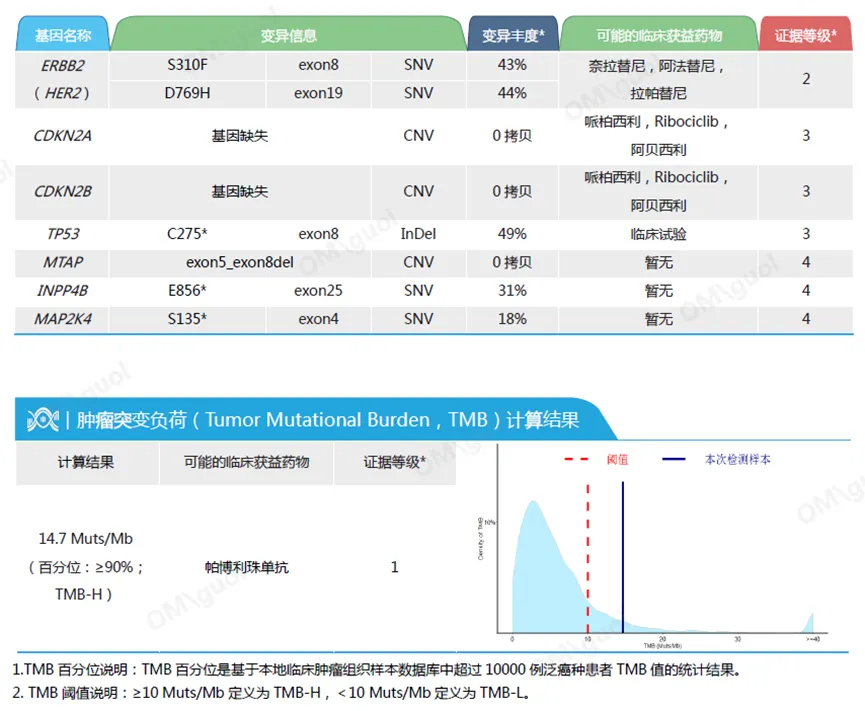
图1 患者基因检测结果
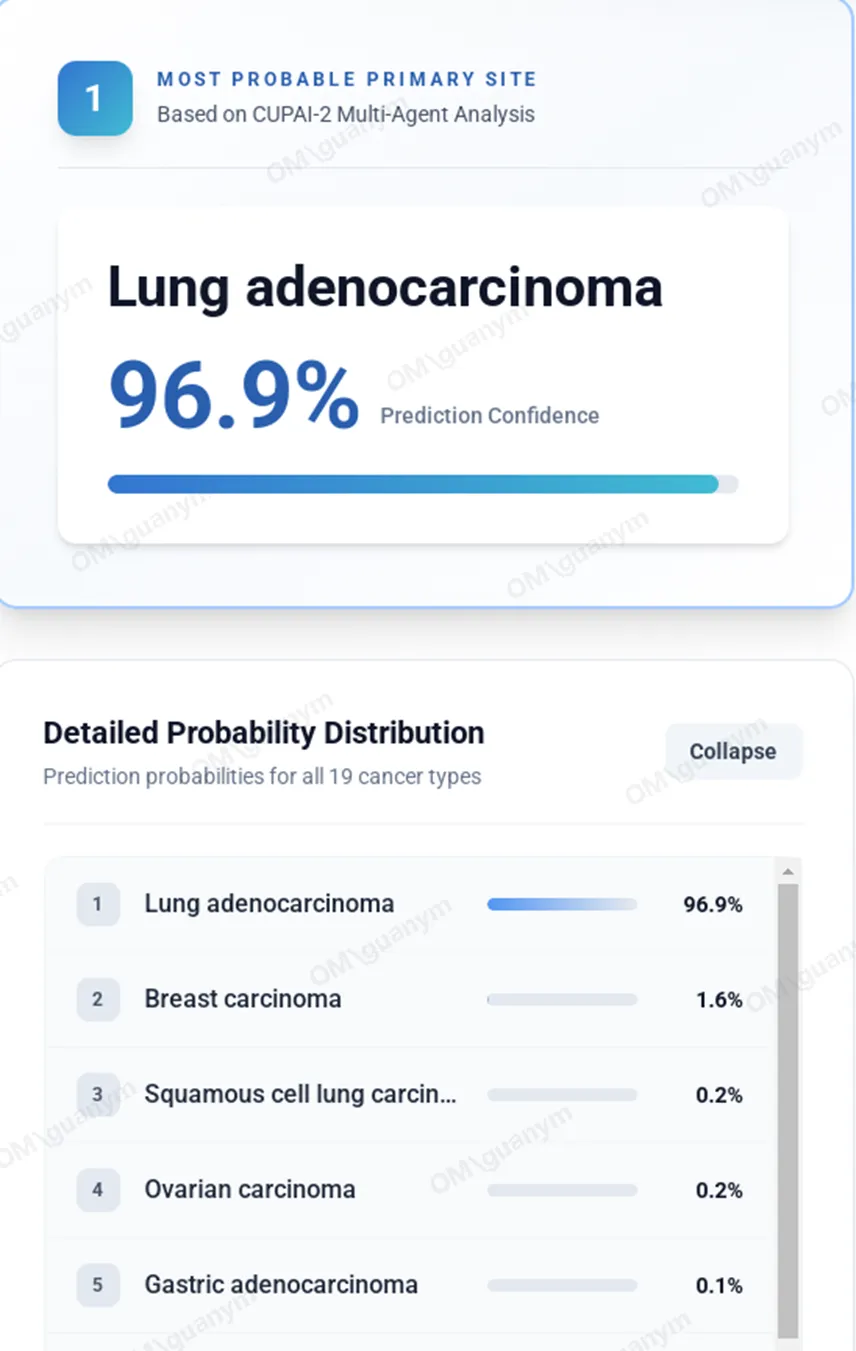
图2 患者肿瘤类型预测结果
基于NGS的HER2 突变和AI预测的参考方向,2022年9月,医生指导孙女士开始使用一线HER2 靶向药—奈拉替尼进行治疗,期间持续规律复查,治疗至2023年8月,孙女士的疗效已经达到部分缓解(PR),肿瘤得到有效控制。但开始出现耐药迹象,医生根据其TMB-H(14.7 Mut/Mb)特征,调整为二线方案:帕博利珠单抗(K药)联合白蛋白紫杉醇,疗效达到疾病稳定(SD)。2024年4月,孙女士的病情出现了新的变化,临床医生再次结合多方面因素,最终选择了新型的抗体药物偶联物(ADC)—戈沙妥珠单抗,作为三线治疗用药。幸好,第三次更换药物治疗的结果让孙女士和她的家人感到欣慰,医生告诉她体内的转移瘤消失很多,原来直径5厘米的肿瘤已经缩小至0.8厘米,疗效评估再次达到PR,直到最新一次随访,孙女士还在持续用药进行治疗。这场诊疗从不知道如何用药,到使用靶向药、免疫药,再到ADC药物,每一次治疗方案调整的背后,都有基因检测的精准指引和AI预测的方向支撑。

图3 AI解读基因检测结果

图4 AI解读肿瘤预测结果
在孙女士的抗癌历程中,AI通过整合临床、病理、基因等多维度数据,在原发灶不明的困境中为诊疗团队缩小了探索范围,让治疗决策更科学、更高效。而患者的坚持、医生的专业判断与AI技术的结合,共同谱写了这场抗癌逆袭的乐章。如今,越来越多的AI技术正融入癌症诊疗的各个环节——从肿瘤预测到药物筛选,从疗效评估到不良反应预警,AI正在让精准医疗从“理想”走向“现实”。
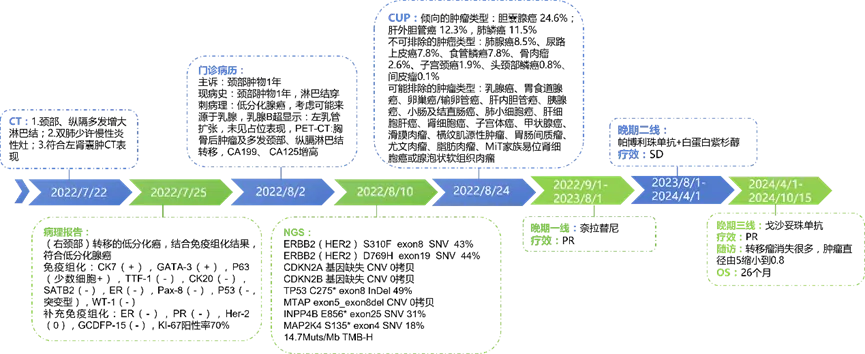
图5 患者诊疗时间轴
免责声明:本文内容仅供癌症病例个性化治疗探讨,不代表至本医疗立场,亦不是治疗方案。在做任何诊疗处理决策前,请谨遵专业医疗建议。
 夜雨聆风
夜雨聆风