2026年4月,英国牛津大学Deborah C.I. Goberdhan教授团队在《Trends in Cell Biology》(IF:18.1)上发表了题为“Generating exosome subtypes: diverse membrane origins and mergers”的观点文章。该研究系统颠覆了细胞外囊泡仅来源于晚期内体的传统观点,首次明确提出循环内体、自噬体、线粒体来源囊泡、高尔基体来源分泌囊泡及核膜来源多囊泡体等多种膜结构均可通过膜融合参与细胞外囊泡亚型的生成。研究发现,不同膜起源通过差异化的货物装载机制(如ESCRT依赖/非依赖、LC3-II介导的LDELS、相分离等)赋予细胞外囊泡独特的生理病理功能,例如Rab11a标记的循环内体细胞外囊泡在营养应激下特异性携带促癌因子AREG。此外,文章揭示了腔内微环境(如蛋白聚集、ER接触位点)在调控细胞外囊泡功能中的关键作用,并指出只有少数特定亚型的细胞外囊泡介导了关键的信号传导功能。该研究为细胞外囊泡异质性的来源提供了全新的理论框架,并为开发亚型特异性检测、阻断及工程化改造策略指明了方向。


细胞外囊泡是细胞间通讯的重要媒介,传统观点认为其仅由晚期内体通过向内出芽形成多囊泡内体后分泌产生。然而,近年研究发现,细胞释放的小细胞外囊泡(sEVs)存在高度异质性,且不同细胞外囊泡亚型可能携带截然不同的生物活性分子,介导差异化的生理病理功能。但细胞外囊泡异质性的来源尚不明确,不同膜区室是否参与细胞外囊泡生成、膜起源如何影响细胞外囊泡功能,以及是否存在亚型特异性的调控机制,仍是领域内亟待解决的核心问题。阐明细胞外囊泡亚型的生成机制,对于精准靶向疾病相关细胞外囊泡及开发新型治疗策略具有重要意义。
本文亮点
1. 首次提出细胞外囊泡膜起源的多样性理论:系统颠覆了“细胞外囊泡仅来源于晚期内体”的传统观点,证明循环内体(Rab11a标记)、自噬体、线粒体来源囊泡及高尔基体来源分泌囊泡均可通过膜融合参与细胞外囊泡生成,扩展了细胞外囊泡亚型的分类框架。
2. 揭示膜起源决定细胞外囊泡亚型功能:发现不同膜起源(如晚期内体 vs. 循环内体)通过差异化的货物装载机制(ESCRT依赖/非依赖、LC3-II介导的LDELS、相分离等)赋予细胞外囊泡独特的生理病理功能,例如Rab11a-细胞外囊泡在营养应激下特异性携带促癌因子AREG。
3. 提出细胞外囊泡亚型靶向策略:强调只有特定细胞外囊泡亚型介导关键信号传导,并指出通过识别膜起源标志物(如Rab GTPases)可实现亚型特异性检测、阻断或工程化改造,为克服当前细胞外囊泡异质性带来的诊断和治疗难题提供了新方向。
图文导读
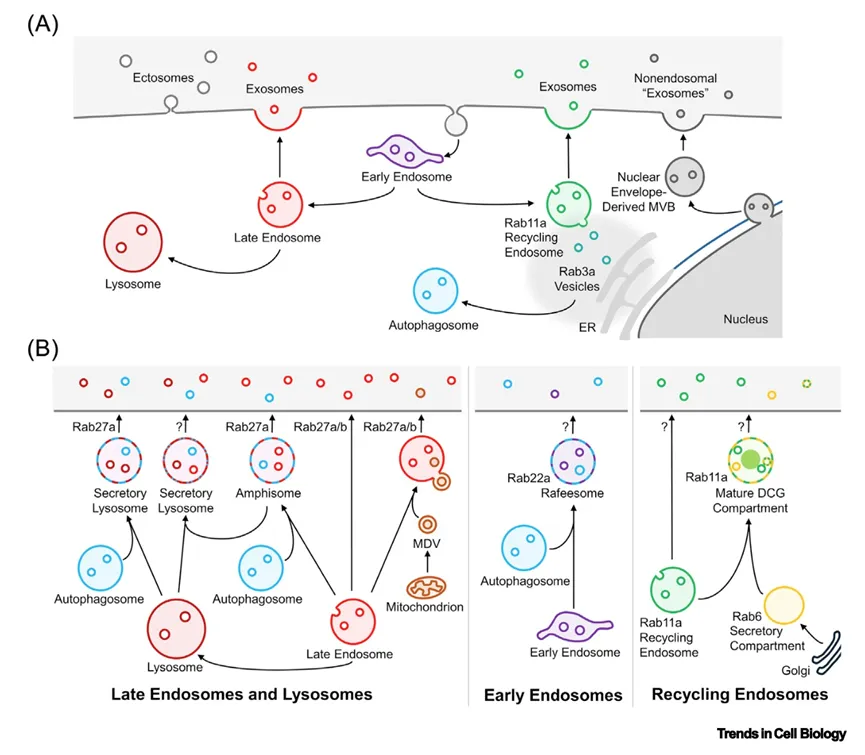
图1(原文 Fig. 1)
小细胞外囊泡和细胞外囊泡的身份受膜起源和膜融合的影响
图片解析:
图1A展示小细胞外囊泡的三种生成途径:质膜出芽形成胞外体、晚期/循环内体融合形成细胞外囊泡、非内体多囊泡体融合形成非内体“细胞外囊泡”;同时显示Rab3a阳性囊泡从Rab11a阳性循环内体出芽,参与自噬体形成。图1B展示非内体膜输入如何增加腔内囊泡多样性:自噬体与晚期内体融合形成amphisome,进一步与溶酶体融合形成分泌性溶酶体;自噬体也可与早期内体融合形成rafeesome;线粒体来源囊泡可将线粒体内膜来源的ILV转移至多囊泡内体;循环内体与高尔基体来源的调节性分泌 compartment融合,形成致密核心颗粒并产生混合膜来源的ILV。
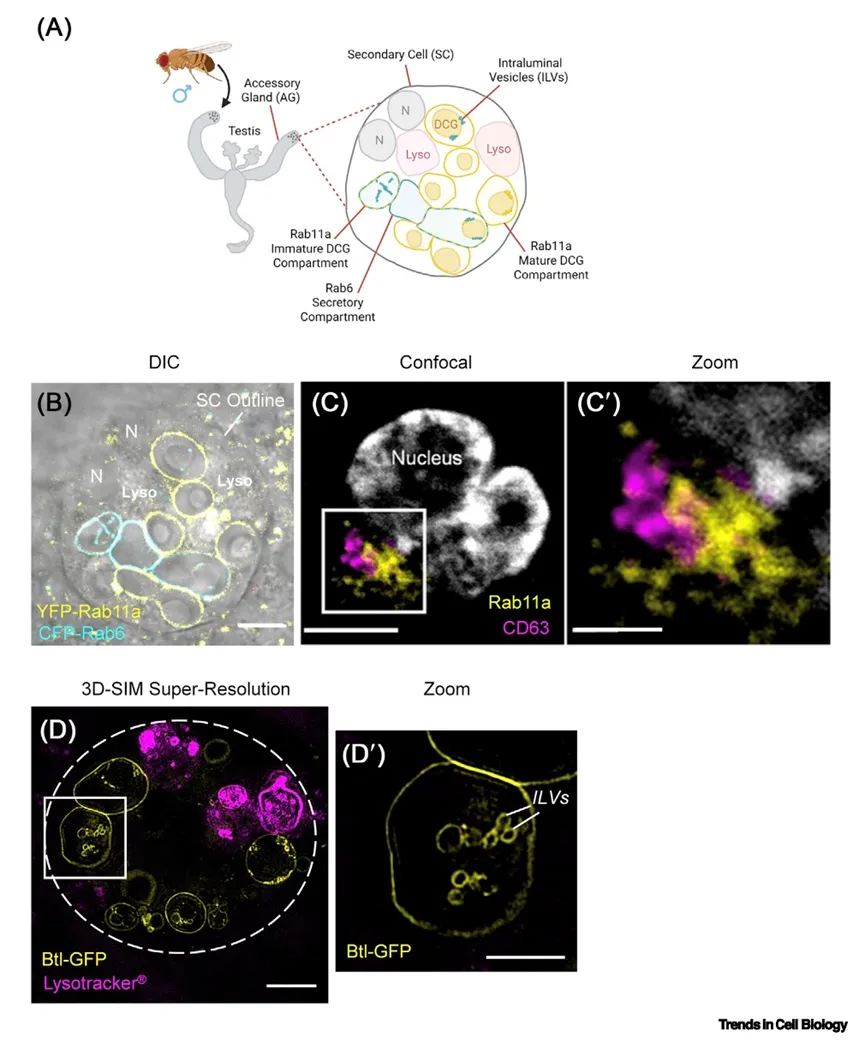
图2(原文 Fig. 2)
果蝇副细胞循环内体中细胞外囊泡的生物发生
图片解析:
图2A为果蝇副细胞细胞外囊泡生物发生模型示意图:双核副细胞嵌入腺上皮,含有溶酶体和Rab6标记的高尔基体来源分泌 compartment,后者与Rab11a标记的内体融合,逐渐转变为Rab11a身份,伴随Rab11a-细胞外囊泡(ILV)生物发生和蛋白聚集事件,形成致密核心颗粒。图2B显示活体副细胞中内源性Rab6和Rab11a蛋白荧光标记,可见分泌/DCG compartment(~5μm直径)和与DCG接触的聚集ILV。图2C-C'显示人HCT116结直肠癌细胞中Rab11a compartment较小,标准光镜无法分辨ILV。图2D-D'显示超分辨3D-SIM显微镜下ILV聚集并与内体限制膜接触,大部分ILV直径<100nm。。
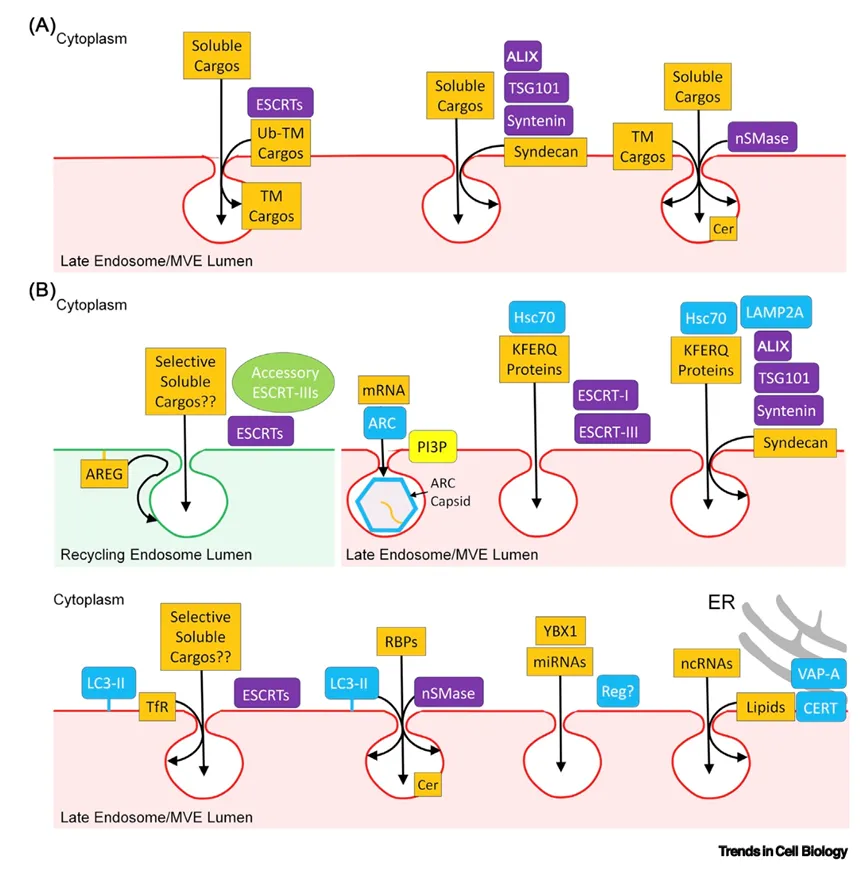
图3(原文 Fig. 3)
内体内腔内囊泡生物发生和货物装载的通用及特殊机制
图片解析:
图3A展示三种通用ILV生物发生机制:ESCRT蛋白依赖性机制(涉及ESCRT-0、-I、-II、-III)、ALIX-Syntenin介导的非核心ESCRT机制(装载Syndecan等跨膜货物)、以及中性鞘磷脂酶介导的神经酰胺依赖性膜变形机制。图3B展示特殊ILV生物发生机制:在循环内体中,辅助ESCRT-III蛋白选择性调节ILV形成,AREG是特异性ILV货物;在晚期内体中,ARC通过PI3P依赖性机制形成衣壳、Hsc70与KFERQ样基序蛋白通过LAMP2A依赖或非依赖机制装载、LC3-II通过ESCRT依赖或nSMase依赖机制促进ILV形成并选择性装载RNA结合蛋白或TfR;YBX1与特定mRNA形成相分离凝聚物被包装入ILV;VAP-A和CERT在内质网-MVE接触位点控制非编码RNA和脂质递送。
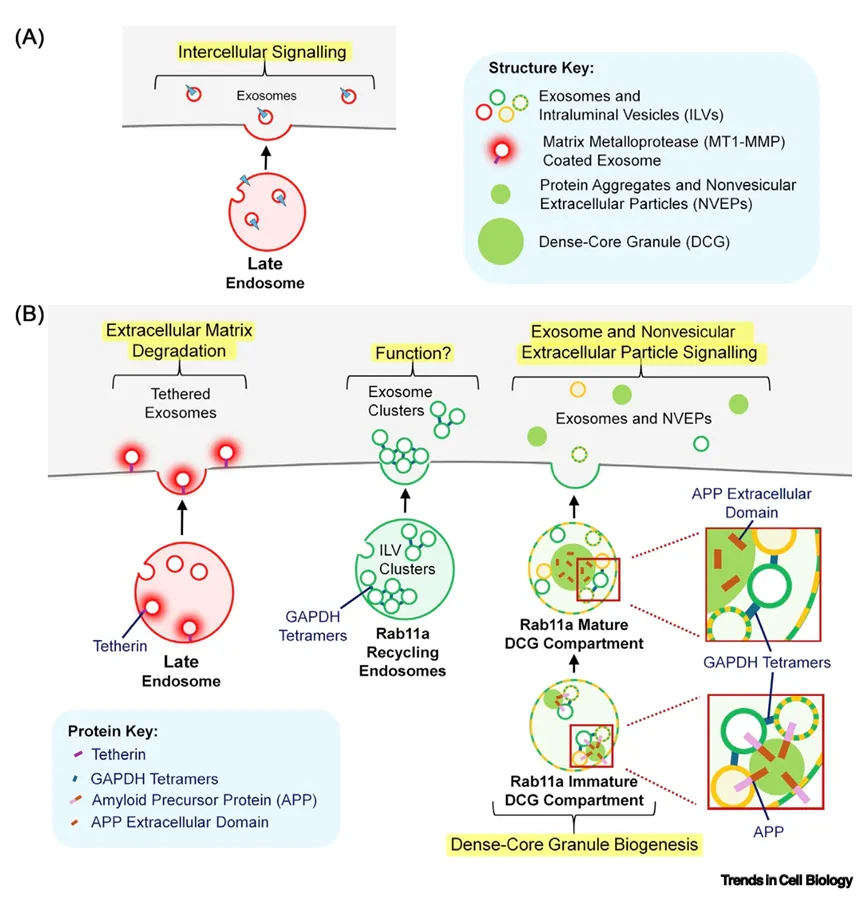
图4(原文 Fig. 4)
微环境相互作用影响腔内囊泡和细胞外囊泡功能
图片解析:
图4A显示所有分泌的ILV(作为细胞外囊泡分泌)在其表面携带膜相关货物,可影响其靶向或信号传导功能。图4B展示特定跨膜蛋白及其他蛋白如何改变囊泡特性与功能:Tetherin的GPI锚使细胞外囊泡相关MT1-MMP能够降解ECM;膜外表面GAPDH促进ILV和细胞外囊泡聚集;跨膜ILV蛋白APP参与致密核心颗粒形成(生理性蛋白聚集事件),需要APP切割并导致其胞外域包装入DCG、胞内域降解。这些聚集事件也可能导致具有增强信号活性的非囊泡胞外颗粒(如supermere)的生成。
总结与展望
不同区室和膜的贡献产生了功能特化的细胞外囊泡亚型。这一发现强调了在健康和疾病中识别并深入表征细胞外囊泡亚型特异性机制的重要性,这比在异质性sEV制剂中筛选亚型标志物更为有效。理解细胞外囊泡亚型生成机制也为研究sEVs提供了新思路:Rab蛋白等低丰度货物可作为细胞外囊泡膜起源的“路标”,揭示介导其生物发生的运输机制。此外,深入研究蛋白聚集体与ILV/细胞外囊泡之间的联系,将有助于理解生理性细胞外囊泡信号传导及其在疾病中的功能障碍。未来聚焦于亚型特异性细胞外囊泡组装机制,将推动鉴定具有关键信号活性的细胞外囊泡,为疾病中选择性检测、阻断或利用细胞外囊泡提供坚实的理论依据。
DOI:
10.1016/j.tcb.2026.03.009.
原文链接:
https://doi.org/10.1016/j.tcb.2026.03.009.
 夜雨聆风
夜雨聆风