01 热稳定蛋白的分析困境
在AI驱动的蛋白设计领域,一个普遍且引人注目的现象是:从头设计的蛋白质往往展现出极高的热稳定性,其熔解温度(Tm)常常轻松超过水的沸点。
这种特性对于许多生物技术应用极具吸引力,例如高温工业催化、或通过热裂解进行快速蛋白纯化。
然而,这种“超常”的稳定性也给研究人员带来了一个分析难题:当蛋白质在常规实验温度下(如95°C)根本不会展开时,我们该如何精确测量并理解其稳定性参数?
传统上,蛋白质的热稳定性研究多集中于自然界的嗜热微生物,通过比较中温与嗜热同源蛋白,揭示了三种主要的稳定性提升模型。这些模型可以通过蛋白质去折叠自由能(ΔGu)随温度变化的曲线来直观展示。
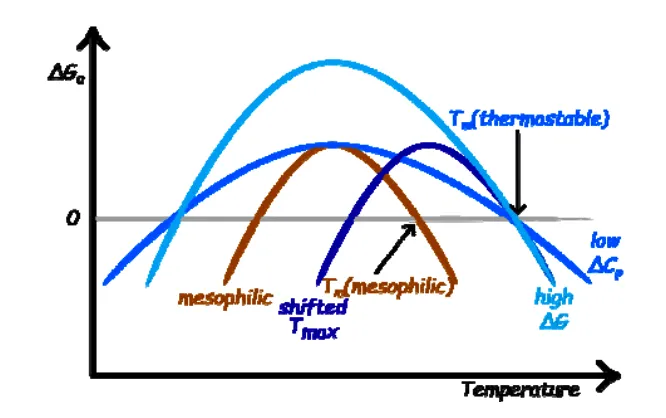
图1:三种可能的蛋白质热稳定性提升机制示意图
一种可能是蛋白在所有温度下都更稳定(曲线整体上移);另一种可能是稳定性峰值向高温偏移;第三种,也是最容易被忽视的一种,是蛋白质对温度的敏感性降低,这表现为去折叠过程中的热容变化(ΔCp)较小。
为了在蛋白工程中准确、高通量地获取这些热力学参数,纳米级差示扫描荧光法(nanoDSF)因其样品用量少、可平行测量多个样本而成为理想选择。
对于热稳定蛋白,通常的策略是加入变性剂(如盐酸胍),通过记录不同变性剂浓度下的热熔解曲线,来外推得到无变性剂条件下的稳定性参数。但这种方法的数据分析复杂,亟需更易用、标准化的工具。
02 CheMelt:一键式热力学分析平台
为了解决这一瓶颈,来自丹麦奥胡斯大学和欧洲分子生物学实验室汉堡分部的研究团队开发了一款名为CheMelt 的在线工具。
该工具专为联合化学与热诱导去折叠数据的全局分析而设计,旨在通过直观的图形用户界面,降低这一强大分析方法的使用门槛。
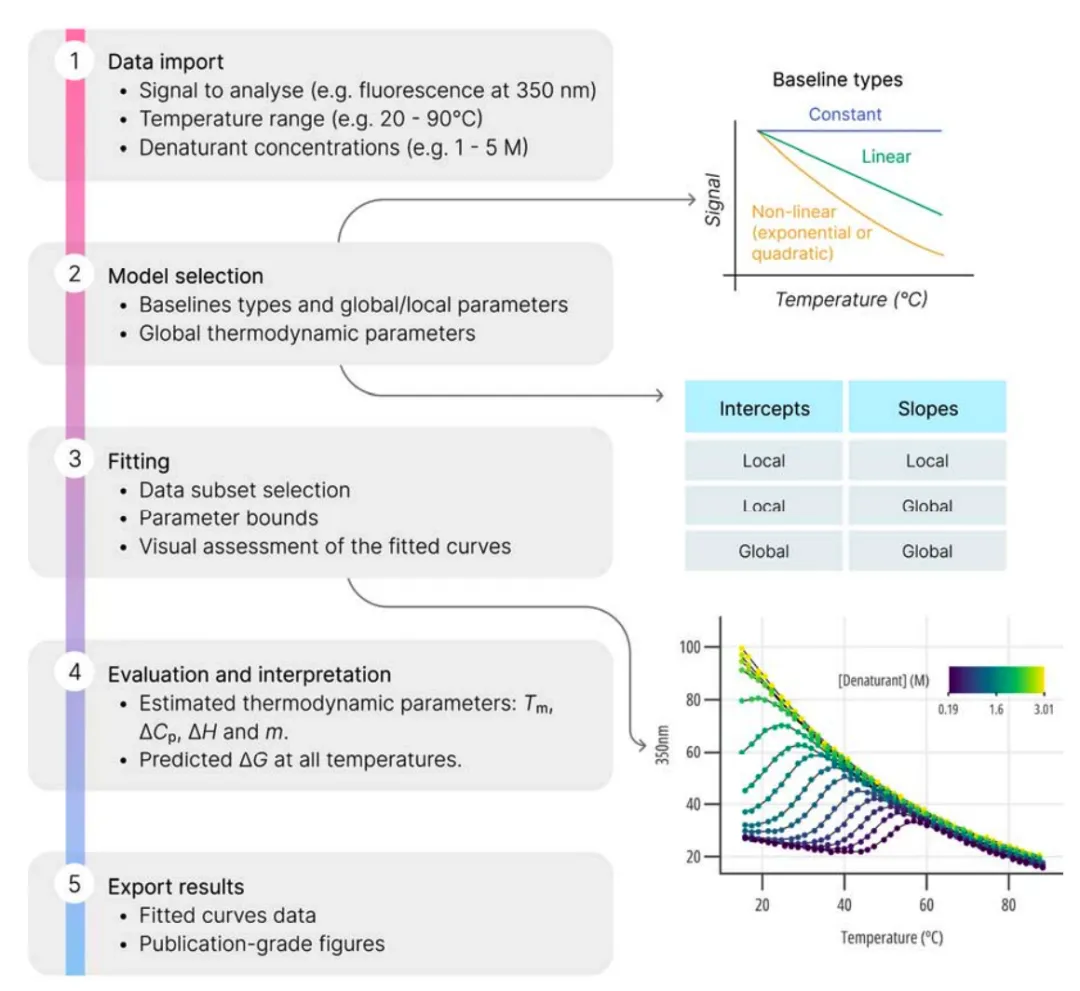
图 2:CheMelt在线工具的五大核心操作步骤
CheMelt的分析流程清晰简洁,主要分为五个步骤:
该工具基于成熟的Python包pychemelt构建,并集成在eSPC生物物理数据分析平台上,方便研究者随时访问使用。
03 验证与挑战:从标准模型到超稳蛋白
研究团队通过三个案例,系统地验证了CheMelt的能力。
案例一,他们重新分析了经典的乙酰辅酶A结合蛋白(ACBP)数据集。CheMelt不仅成功拟合了数据,其提取的热力学参数(如Tm、ΔCp、m值)与先前文献报道高度一致,证明了算法的准确性。
案例二,面对核心挑战——超高热稳定蛋白,团队首先使用模拟数据进行测试。结果显示,即使在没有变性剂时完全观察不到去折叠转变,CheMelt依然能够通过高浓度变性剂下的曲线,准确外推并估算出蛋白质在生理条件下的Tm及其他参数。
真正的考验来自案例三。研究团队选取了35个使用RFdiffusion和ProteinMPNN设计的全新蛋白结合剂(mini-binder),利用nanoDSF进行扫描。
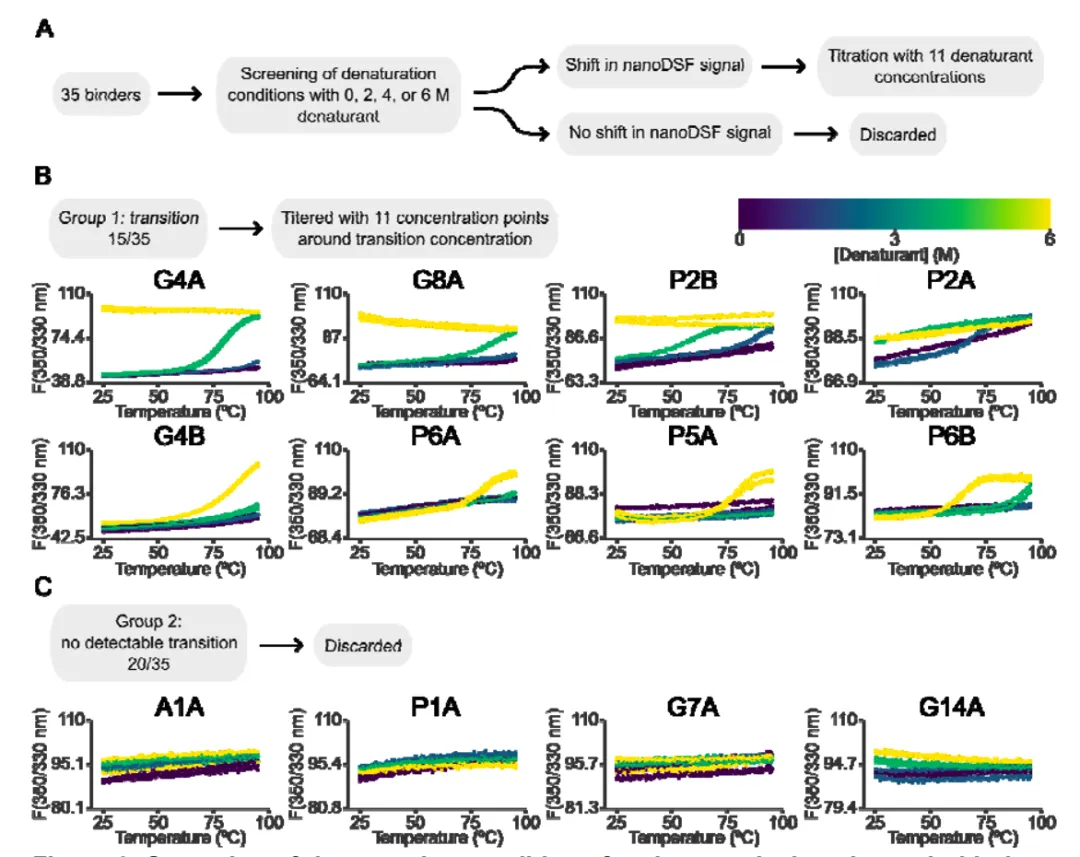
图 3:对35个从头设计蛋白进行变性条件筛选的流程与结果示例
出乎意料的是,其中20个蛋白即使在高温和高浓度变性剂下,也未显示出明显的荧光信号变化。后续的圆二色谱(CD)实验证实,这些蛋白实际上发生了去折叠,只是其芳香族残基在去折叠前后环境变化极小,导致荧光信号“沉默”。
这一现象本身就是一个重要发现,暗示了这些设计蛋白的疏水核心可能具有独特性质。
04 关键发现:低ΔCp是热稳定的“捷径”
在15个显示出可观测熔解转变的蛋白中,CheMelt成功完成了所有数据的高质量全局拟合。
结果显示,这些从头设计蛋白的熔解温度分布在96°C至152°C之间,平均高达122°C,印证了其超高热稳定性。
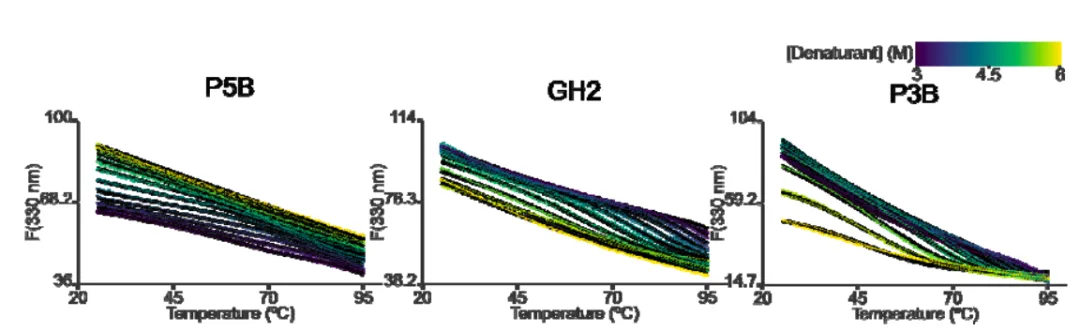
图 4:CheMelt对三个代表性设计蛋白去折叠数据的全局拟合结果
然而,更深入的分析揭示了其稳定性的独特机制。当研究人员将设计蛋白的热容变化(ΔCp)和变性剂依赖性(m值)与天然蛋白数据库比较时,发现了一个显著差异。
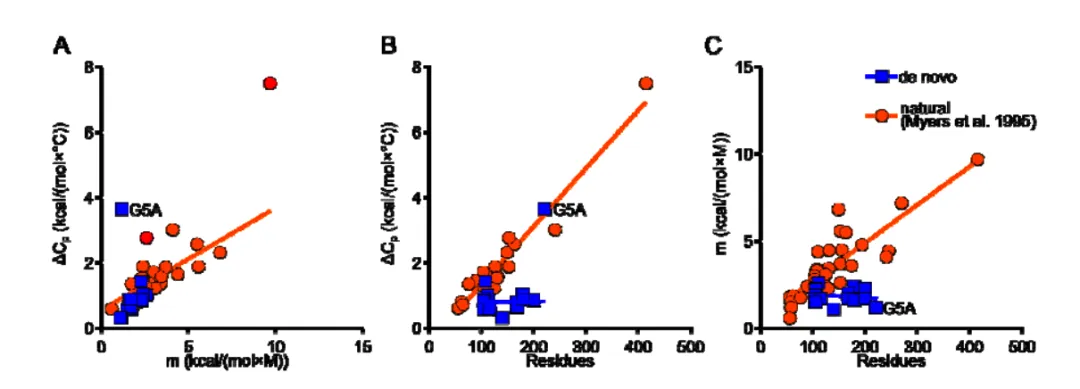
图 5:从头设计蛋白与天然蛋白在ΔCp和m值上的对比
尽管设计蛋白的ΔCp和m值之间存在与天然蛋白相似的相关性,但这两个参数随蛋白链长度增长的斜率明显低于天然蛋白。这意味着,对于相同大小的蛋白,设计蛋白在去折叠时暴露的疏水表面积更少。
ΔCp的大小直接决定了蛋白质稳定性曲线(ΔGu vs. T)的弯曲程度。较低的ΔCp意味着曲线更为平坦,蛋白质的稳定性对温度变化不敏感。
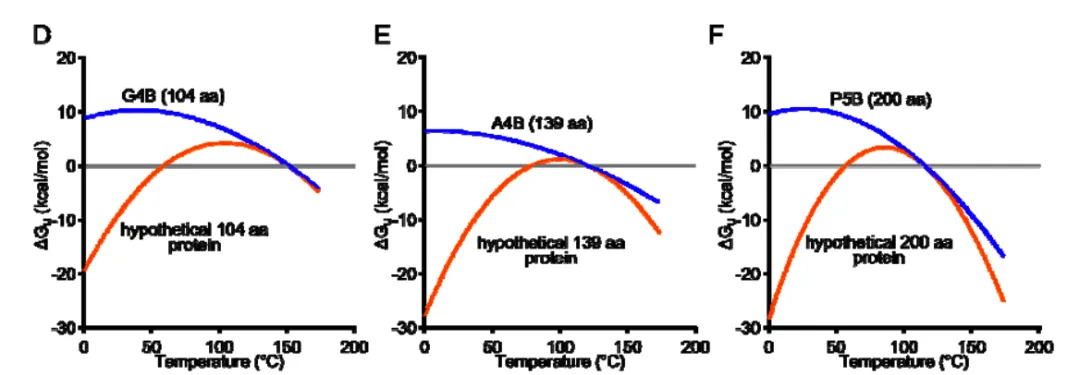
图 6:低ΔCp导致蛋白质稳定性曲线更平坦,从而提升熔解温度
研究表明,这些从头设计的蛋白主要通过降低ΔCp(即降低对温度的敏感性),而非普遍认为的“在所有温度下都具有极高的平衡稳定性”,来实现其惊人的高热熔解温度。
05 行业启示:重新审视“稳定性”的内涵
这项研究对AIDD和蛋白设计领域具有重要启示。
首先,它强调了全面热力学表征的重要性。高熔解温度并不等同于高平衡稳定性。一个通过低ΔCp实现高热稳定性的蛋白,在室温下可能具有相当比例的非折叠状态,这意味着它可能并不具备对抗聚集或蛋白酶解的强健性。
因此,在评价设计蛋白的稳定性时,仅依赖Tm值作为单一指标是片面的。CheMelt这类工具的出现,使得快速、准确地获取完整热力学参数成为可能,为蛋白工程的理性优化提供了关键数据。
其次,研究揭示了当前AI蛋白设计算法(如RFdiffusion + ProteinMPNN)可能存在的某种“设计偏好”。它们倾向于生成具有更紧密、更少疏水残基暴露的疏水核心的蛋白,这或许是算法在追求能量最小化或结构理想化时产生的结果。
理解这一机制,有助于我们未来在设计时更好地平衡热稳定性与其他功能性需求。
【文章原文】
https://arxiv.org/html/2604.09369v1
往期精选
1 AI设计大环肽结合剂登Nature子刊:成功率高达100%
2保姆级最前沿 AI蛋白质设计教程!有浏览器就能学 AlphaFold, RFDiffusion和ProteinMPNN 一网打尽
 夜雨聆风
夜雨聆风