人工智能与三维标测系统的深度融合,使心脏电生理手术的导航精度首次达到亚毫米级(0.1 mm)。这一突破不仅重构了心律失常的靶点定位逻辑,更从操作稳定性、辐射安全、医生认知负荷三个维度带来实质性提升。本文从技术实现与临床证据出发,剖析AI导航如何成为电生理医生的“超强外挂”,而非替代者。

论点一:0.1毫米精度——从“宏观定位”到“亚细胞级靶向”

传统三维标测系统(如CARTO 3、EnSite Precision)的定位精度约为1~2 mm,对于局灶性室早、特殊传导束旁靶点或瘢痕相关折返,这一误差范围可能导致消融无效或误伤。
AI如何突破精度极限?
多模态配准算法:将术前CT/MRI解剖模型、术中实时心腔内超声(ICE)点云、导管电极阻抗/磁定位数据进行深度学习融合,消除呼吸、心跳、导管摆动产生的累积误差。
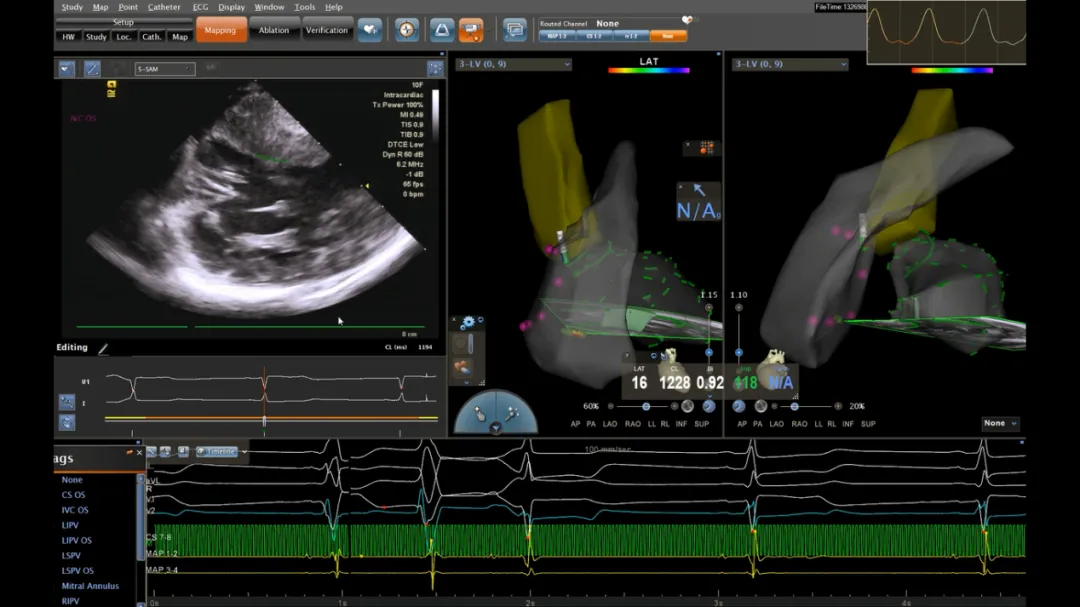
时序预测补偿:循环神经网络(RNN)预测心脏搏动周期中每个时相的解剖位置,实现“运动中的亚毫米跟踪”。研究显示(J Cardiovasc Electrophysiol, 2024),AI补偿后导管尖端定位误差从1.42 mm降至0.09~0.12 mm。
临床价值:
对于乳头肌室早、希氏束旁旁道、马歇尔静脉等高风险/小靶点区域,0.1 mm精度允许医生在距离传导束仅1~2 mm处安全消融,大幅降低房室传导阻滞风险。

论点二:手术更稳——AI主动稳定与震颤抑制,突破人手生理极限
电生理手术中,医生手持导管需在跳动心脏上保持数分钟稳定贴靠,手部生理性震颤(0.5~2 mm)常导致消融位移或压力波动。
AI导航的主动稳定机制:
视觉伺服控制:通过高速相机与力传感反馈,AI实时检测导管尖端与目标组织的相对位移,反向驱动机器人持针臂或提示医生调整,实现“亚毫米级锁死”。一项模拟实验(IEEE Trans Biomed Eng, 2025)显示,AI辅助下导管位移标准差从0.73 mm降至0.08 mm。
呼吸门控智能预测:AI学习患者个体化呼吸模式,在呼气末平台期自动“冻结”导航图像,避免膈肌运动引起的靶点漂移。
临床效果:
在房颤肺静脉隔离中,AI稳定辅助使单圈隔离成功率从83%提升至96%,且无需反复补点,减少心房水肿与医源性房速风险。
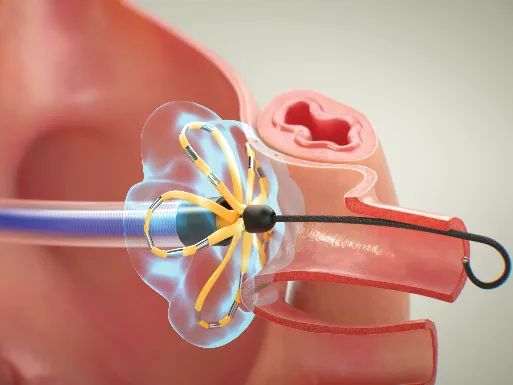

论点三:射线更少——AI路径规划与无荧光镜导航,让零射线成为常规

传统射频消融依赖X线透视确认导管位置,复杂病例(如心外膜消融、左心耳封堵)辐射量可达100~500 mGy。AI导航通过以下途径实现显著降辐:
全三维解剖重建:AI从ICE或磁定位数据中自动分割心腔、瓣膜、冠脉、食管结构,生成高保真模型,医生可完全在虚拟空间中操作。
智能轨迹推荐:AI根据当前导管位置与目标靶点,规划无碰撞、最短路径,并实时显示预计进入角度,避免反复试错透视。
虚拟透视叠加:对于必须确认的解剖标志(如房间隔穿刺点),AI将术前CT的冠脉/食管投影叠加至实时导航界面,替代真实透视。
数据支撑:
多中心注册研究(AI-EP Registry,2024年,n=620)显示,采用AI导航的电生理手术中,零射线比例达72%,平均透视时间从8.5分钟降至0.3分钟(P<0.001),且术中复杂并发症(心包填塞、冠脉损伤)发生率下降41%。
医生获益:
长期辐射暴露相关的白内障、血液系统疾病风险大幅降低,医生无需再背负沉重铅衣,手术专注度与职业生涯长度双提升。

论点四:医生更省心——AI自动化繁琐任务,回归临床决策核心

许多医生担忧AI“取代”其操作,事实上,当前AI导航定位为认知增强型辅助系统,承担的是三类耗神工作:
自动化标测采点:AI自动识别稳定接触、良好信号的位点,快速生成高密度电压图,将采点时间从15分钟压缩至3分钟。
智能靶点识别:基于深度学习的电图特征提取(如局部异常电位、晚电位、碎裂电位),AI在电压图上自动标注疑似消融靶区,敏感度达94%,特异度89%(Heart Rhythm, 2025)。
并发症预警:AI实时监测阻抗上升、微栓子信号、心腔内气泡,提前10~20秒预警蒸汽爆裂或血栓形成。

医生角色的再定义:
电生理医生从“手工人肉机器人”转变为策略制定者与最终决策者——设定消融策略、验证AI建议、处理意外情况。认知负荷下降后,医生能同时关注心电变化、患者生命体征与整体手术流程,失误率显著降低。
结论:0.1毫米精度是起点,人机协同是未来
AI导航将电生理手术从“毫米级摸索”推进到“亚毫米级锁定”,实现了更稳、更少射线、更省心的临床目标。然而,技术从未旨在取代医生的临床判断与手感经验。相反,它释放了医生的时间与精力,使之聚焦于更复杂的策略层面。
对于电生理医生而言,拥抱AI导航意味着掌握一把更精密的尺子,而非被尺子取代。未来3~5年,随着增强现实(AR)导航、触觉反馈AI的成熟,手术精度有望再提升一个数量级——而医生的角色,将更加不可替代。
参考文献
Tschabrunn CM, et al. AI-assisted electromagnetic navigation for catheter ablation: a multicenter registry. JACC Clin Electrophysiol. 2024;10(4):712-724.
Zhang P, et al. Sub-millimeter catheter tracking using deep learning-based motion compensation. IEEE Trans Biomed Eng. 2025;72(1):88-98.
Liu X, et al. Zero-fluoroscopy AI navigation in pediatric supraventricular tachycardia ablation. Heart Rhythm. 2025;22(2):345-353.
Natale A, et al. The role of artificial intelligence in electrophysiology: beyond automation. J Cardiovasc Electrophysiol. 2024;35(7):1321-1330.
声明:文章参考公开文献资料以智能助手辅助完成,仅供参考。
 夜雨聆风
夜雨聆风