一、引言
环肽(cyclic peptides)作为一类兼具小分子药物稳定性与大分子生物制剂特异性的治疗模态,近年来在药物开发领域获得广泛关注。其中,通过N端与C端酰胺键连接形成的头尾相连环肽(head-to-tail cyclic peptides),因其封闭骨架赋予的结构刚性与抗蛋白酶水解能力,展现出显著优于线性肽的药代动力学特性。然而,环肽的理性设计长期受制于构象空间的复杂性与训练数据集的匮乏,深度学习方法的进展远滞后于蛋白质设计领域。
自2024年以来,以 AfCycDesign、RFpeptides、CyclicMPNN、PocketXMol 和BoltzGen 为代表的一批深度学习方法相继涌现,彻底改变了环肽设计的研究范式。本文聚焦头尾相连环肽的计算设计,系统梳理上述方法的演进脉络、设计流程与关键案例,以期为该领域的进一步发展提供参考。
二、领域背景与技术挑战
2.1 环肽设计的核心难题
头尾相连环肽的设计面临三重根本性挑战。
第一,构象空间复杂:环化带来的几何约束使得骨架采样空间急剧收窄,传统物理建模方法难以有效探索。
第二,训练数据匮乏:与蛋白质结构数据库中的数十万条目相比,实验解析的环肽结构数量极少,严重制约了监督学习方法的训练规模。
第三,序列-结构关系非线性:短环肽的折叠行为对序列变化极为敏感,同一骨架下不同序列可能导致截然不同的构象偏好。
2.2 从传统方法到深度学习的范式转变
早期环肽设计主要依赖 Rosetta 等基于物理能量函数的计算方法,通过随机骨架采样与序列优化相结合进行设计。这类方法虽然在生成稳定环肽骨架方面取得了一定成功,但在蛋白结合环肽设计中表现有限——设计分子的亲和力通常不高,且实验结构与设计模型偏差较大。深度学习的引入改变了这一局面,通过将结构预测网络改造为生成模型,研究者开始以数据驱动的方式直接探索环肽的化学空间。后续发展进一步向原子级统一建模与跨模态生成演进,标志着该领域正从“专一任务、分步设计”向“统一框架、端到端生成”转型。
三、环肽设计方法的演进脉络
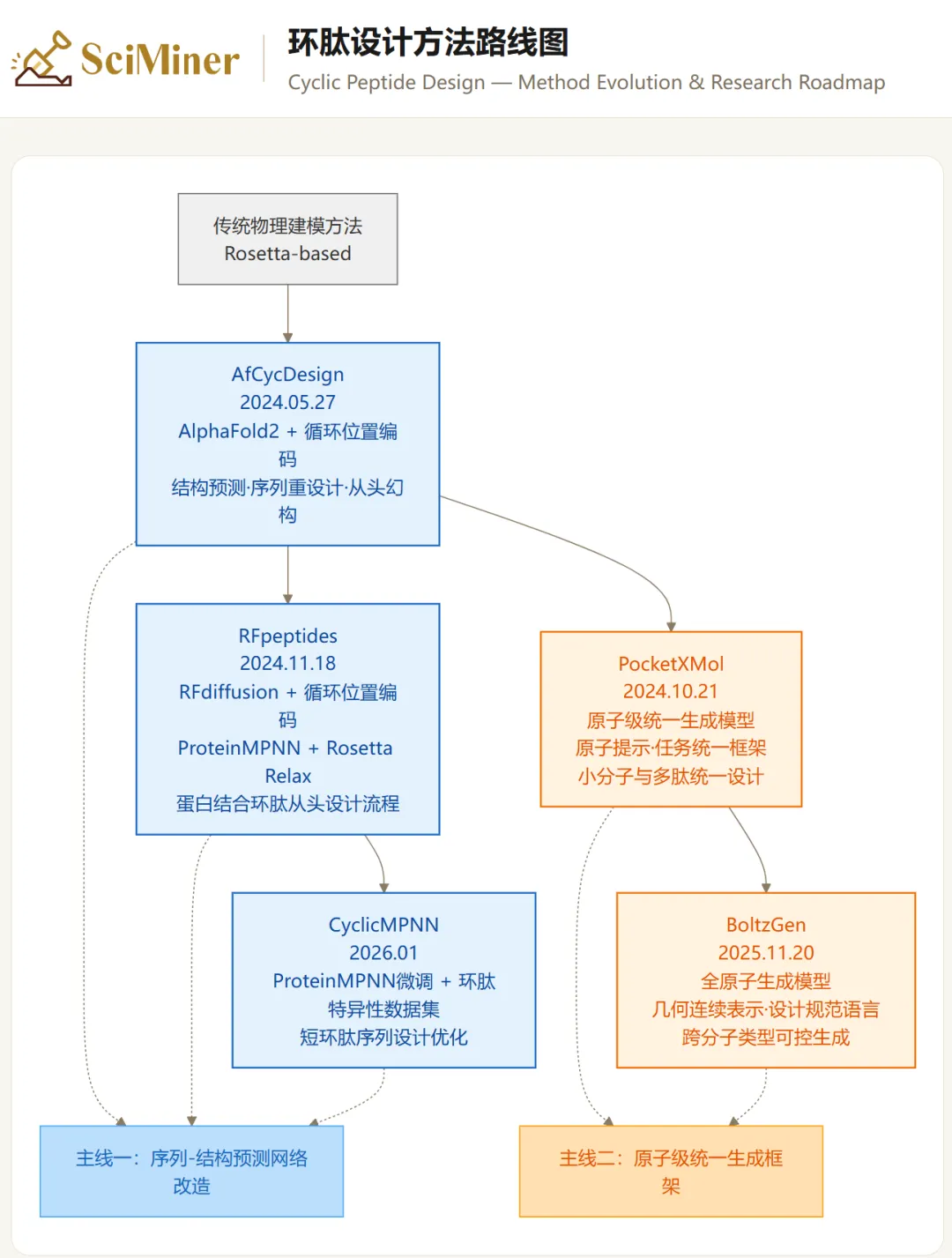
上述五种方法并非孤立出现,而是沿着两条技术主线形成了一条清晰的演进路径(图1)。
主线一:基于序列-结构预测网络的改造。
AfCycDesign开创性地将AlphaFold2改造为环肽专用预测与生成工具,通过在相对位置编码中引入“循环偏置”(cyclic offset)来处理头尾环化的拓扑约束。随后,RFpeptides将这一思想进一步扩展,整合RFdiffusion的扩散生成能力与ProteinMPNN的序列优化,构建了首套完整的蛋白结合环肽从头设计流程。在此基础上,CyclicMPNN针对短环肽序列设计的特殊需求,通过环肽特异性数据集对ProteinMPNN进行微调,在保持高计算效率的同时显著提升了序列-骨架的结构吻合度。这条主线体现了从结构预测能力改造,到生成式骨架设计,再到序列优化精细化的逐步深入。
主线二:原子级统一生成框架的构建。
BoltzGen率先提出了全原子生成模型的统一设计理念,以几何连续表示替代离散残基标签,通过单一模型同时完成结构预测与结合体设计,并引入灵活的设计规范语言实现跨分子类型的可控生成。PocketXMol则将这一理念推向了更本质的层面,以“原子提示”(atomic prompt)作为任务规范,将小分子、多肽等不同分子类型统一为同一种原子级表示,在无需任务特定微调的前提下实现了13项基准任务中的11项最先进性能。这条主线体现了从多模态设计到真正统一框架的跃升。
四、代表性设计方法详解
4.1 AfCycDesign:环肽专用结构预测与生成模型
AfCycDesign由Rettie等人于2025年5月发表于Nature Communications,是首个将AlphaFold2深度改造用于环肽结构预测与设计的框架。
核心技术:AfCycDesign的核心创新在于对AlphaFold2相对位置编码的“循环化”改造。在AlphaFold2中,相对位置编码用于刻画序列中残基i与j之间的线性距离;AfCycDesign引入“循环偏置”(cyclic offset)机制——当残基索引j越过序列中点时,编码从正向切换为负向,从而使模型“感知”到N端与C端的邻近关系。这一简洁而优雅的改造使模型无需重新训练即可处理头尾环化的拓扑约束。
设计流程:AfCycDesign支持三种模式。(1)结构预测:给定环肽序列,预测其三维构象;(2)序列重设计:在给定骨架约束下,反向设计最优氨基酸序列;(3)从头幻构(de novo hallucination):在无任何先验骨架的前提下,通过梯度优化生成全新的环肽结构与序列。三种模式共用同一个经过循环偏置改造的AlphaFold2网络。
关键成果:AfCycDesign生成了超过10,000个结构多样的环肽设计,预测折叠置信度高。实验验证层面,8个从头设计序列的X射线晶体结构与其设计模型高度吻合(主链RMSD < 1.0 Å),证明了原子级精度。研究者进一步以幻构所得肽为起始骨架,设计靶向MDM2和Keap1的结合剂,达到了纳摩尔级的IC50值。
4.2 RFpeptides:蛋白结合大环肽的从头设计流程
RFpeptides由David Baker团队(Gaurav Bhardwaj、Frank DiMaio等)于2024年11月以预印本发布,2025年6月正式发表于Nature Chemical Biology。这是首个专门用于蛋白结合大环肽从头设计的完整深度学习流程。
核心技术:RFpeptides整合了三项关键技术模块。(1)循环位置编码:在RoseTTAFold2(RF2)结构预测网络和RFdiffusion扩散模型中引入与AfCycDesign原理一致的循环相对位置编码,使网络能够稳定预测已知天然环肽结构并生成多样化的大环骨架。(2)扩散骨架生成:RFdiffusion从噪声出发,在目标蛋白口袋的空间约束下逐步去噪,生成与该口袋精确匹配的环肽骨架。(3)序列优化:由ProteinMPNN生成骨架对应的氨基酸序列,再经Rosetta Relax进一步优化结合界面和整体结构质量。
设计流程:首先,选择目标蛋白上的结合口袋并定义热点残基;其次,RFdiffusion生成与该口袋形状匹配的环肽骨架(通常生成1-2万个);再次,ProteinMPNN为每个骨架设计多个序列(通常4个);随后,通过深度学习置信度指标和物理基础指标(如接触分子表面、形状互补性等)进行多轮筛选;最后,选择最优设计进行实验验证。整个流程中,针对每个靶点仅测试不超过20个设计分子,相比传统高通量筛选的数十亿次测试,效率提升极为显著。
4.3 CyclicMPNN:面向环肽骨架的序列设计优化
CyclicMPNN由Hosseinzadeh等人于2026年1月发布在bioRxiv,是专门针对短环肽序列设计问题对ProteinMPNN进行微调的优化工具。
核心技术:ProteinMPNN是当前最常用的固定骨架序列设计模型,但其训练数据以球蛋白为主,短环肽的结构特征在训练分布中严重不足。CyclicMPNN通过在环肽富集数据集上对ProteinMPNN进行微调(fine-tuning)来解决这一问题。训练数据混合了来自PDB的实验解析环肽结构和计算机生成的环肽骨架——后者先经ProteinMPNN设计序列,再通过结构预测评估,仅保留预测结构与目标骨架RMSD较低的“高置信度”样本。该数据集经过聚类去冗余后,用于200个epoch的微调,选取困惑度最低的checkpoint。模型架构本身未作改变,性能提升完全来自训练分布的适配。
关键结果:在6-10残基的环肽骨架测试中,CyclicMPNN将中位主链RMSD从ProteinMPNN的1.55 Å降低至1.13 Å。在motif约束设计任务中(将Nrf2来源的“EETG”motif嵌入8残基环肽骨架),CyclicMPNN成功通过了稳定性阈值的设计数量翻倍(12 vs 6)。此外,PNear能量漏斗分析显示CyclicMPNN设计具有更明显的折叠倾向。
CyclicMPNN的定位是序列设计优化工具而非完整设计流程,它可以与AfCycDesign或RFpeptides生成的环肽骨架无缝对接,为骨架提供更稳定、更可靠的序列方案。
4.4 PocketXMol:原子级统一生成模型
PocketXMol由清华大学马剑竹团队等合作研发,于2026年2月发表于Cell,标志着环肽设计领域的一次范式跃升——从“任务特定模型”走向“原子级统一框架”。
核心技术:PocketXMol提出了三大创新。(1)原子级统一表示:将小分子、多肽、片段等所有输入对象抽象为原子类型、三维坐标和化学键关系的基本集合,从根本上打破分子类型壁垒。(2)原子提示(atomic prompt):以原子级约束作为任务规范,模型的生成行为由条件输入控制,而非依赖任务特定网络结构。(3)通用去噪器:所有生成任务——无论小分子设计、多肽生成、片段连接还是结构优化——均通过同一扩散去噪核心完成,实现任务间的知识共享与迁移。
设计流程:PocketXMol的工作流程极具灵活性。给定一个蛋白口袋后,模型既可以生成匹配的小分子,也可以生成结合多肽;给定一个分子片段,模型可以完成结构扩展;给定功能或约束标签,模型可以生成满足条件的候选分子。对环肽设计而言,PocketXMol支持从backbone构建到序列设计与侧链打包的完整流程,但这些步骤不再由多个独立模型分步完成,而是在同一原子级表示下统一实现。
关键结果:PocketXMol在13项计算基准中的11项上达到了最先进性能,超越了55个基线模型。在PD-L1结合肽设计中,其成功率远超随机文库筛选,结合亲和力达纳摩尔级。PocketXMol首次证明:原子级统一模型可以同时胜任小分子和多肽的设计任务,且无需任何任务特定微调。
4.5 BoltzGen:全原子跨模态结合体设计
BoltzGen由MIT团队(Hannes Stark等)联合多家机构于2025年11月发布在bioRxiv,是首个将结构预测与结合体设计统一于单一全原子生成模型中的框架。
核心技术:BoltzGen的核心创新体现在两个层面。(1)几何连续表示:以连续几何向量替代传统离散残基标签,在单一体系中实现蛋白折叠与结合体设计的联合训练。模型主体采用PairFormer架构,通过三角注意力高效建模原子间的空间关系,并结合几何残基编码在连续空间中同时推断残基类型与原子坐标。(2)设计规范语言:提供了一种灵活的YAML格式设计规范,允许用户通过声明式语句指定共价键约束、结构约束、结合位点、环化方式(包括头尾环化)等设计条件。
设计流程:BoltzGen采用端到端的生成范式。用户通过YAML配置文件定义设计目标(如“在KRAS的特定位点设计一个环肽”),模型从噪声出发,在目标蛋白口袋的几何约束下逐步去噪,同时生成环肽的骨架构象、序列和侧链取向。训练数据采用多模态联合训练策略,涵盖了蛋白结构、结合复合物、肽类分子等多种来源,使模型在每一次训练迭代中随机承担折叠预测、结合体设计或结构补全任务。
关键结果:BoltzGen在涉及26个靶点、跨越纳米抗体到环肽的8项湿实验设计活动中进行了全面验证。在9个与训练集相似度极低的新颖靶点上,15种纳米抗体和蛋白结合体设计测试中,66%的靶点获得了纳摩尔级亲和力。这首次证明了单一模型体系可在多模态生物分子设计中实现折叠与结合性能的同步最优。目前,BoltzGen已开源模型权重、数据和代码。
五、设计案例解析
5.1 高亲和力结合剂设计:RFpeptides的标杆案例
RFpeptides在四种治疗相关靶点上的系统验证,为从头环肽设计树立了重要基准。
靶向MCL1:MCL1是抗凋亡蛋白,在多种癌症中过表达。RFpeptides生成了9,965个多样化环肽骨架,经筛选后合成14种设计。其中3种表现出结合活性,最佳设计MCB_D2的Kd为2 μM,其晶体结构与设计模型的主链RMSD仅为0.7 Å。
靶向GABARAP:GABARAP是自噬相关蛋白,其结合口袋缺乏α-螺旋特征,是检验设计方法结构适应性的理想靶点。研究者定义了6个热点残基,设计了约8万个模型,最终筛选13个代表性设计用于实验。结果极为惊艳:GAB_D8和GAB_D23分别以6 nM和36 nM的亲和力结合靶点,其中GAB_D8为目前已知亲和力最高的大环GABARAP结合物。
靶向RbtA(无实验结构) :RbtA是鲍曼不动杆菌的膜蛋白,设计时无可用的X射线晶体结构,仅依靠AF2/RF2的预测结构。即便在此挑战下,RFpeptides仍成功获得了Kd < 10 nM的高亲和力结合物,展示了其对新靶点出色的泛化能力。
5.2 统一框架的跨类型设计:PocketXMol的双重验证
PocketXMol在caspase-9抑制剂设计与PD-L1结合肽设计中进行了双线实验验证,充分展示了原子级统一框架的实用价值。在caspase-9抑制剂设计中,PocketXMol生成的小分子抑制剂效力与市售泛caspase抑制剂相当。在PD-L1结合肽设计中,PocketXMol设计的结合肽成功率显著高于随机文库筛选,结合亲和力达纳摩尔级,并可在体内肺肿瘤成像中特异性结合PD-L1阳性细胞。这两个案例的意义在于:同一模型、同一表示、无任何任务特定微调,即可在不同分子类型上同时取得成功,验证了原子级统一范式的可行性。
5.3 特定靶点应用:AfCycDesign与BoltzGen的代表性工作
AfCycDesign的MDM2/Keap1结合剂设计:AfCycDesign利用幻构生成的环肽集合作为起始骨架,对MDM2(肿瘤抑制因子p53的负调控因子)和Keap1(氧化应激通路关键蛋白)设计了高亲和力结合剂,IC50达到纳摩尔级别。这证明了AfCycDesign幻构生成的环肽骨架不仅结构精准,而且具备成为功能性结合剂的潜力。
BoltzGen的KRAS与阿片肽设计:BoltzGen提供了针对KRAS蛋白特定位点的环肽设计YAML配置示例,展示了设计规范语言在实际靶点上的直接应用。此外,BoltzGen也被用于设计靶向μ-阿片受体的肽类分子,从beta-内啡肽结构出发生成新型结合肽。
六、方法比较
方法 | 核心创新 | 设计能力 | 实验验证 |
AfCycDesign | AlphaFold2+循环位置编码 | 结构预测·序列重设计·从头幻构 | 8个X射线晶体结构(RMSD<1.0 Å),MDM2/Keap1纳摩尔结合剂 |
RFpeptides | RFdiffusion+循环位置编码+ProteinMPNN集成 | 蛋白结合环肽从头设计完整流程 | 4个靶点(MCL1/MDM2/GABARAP/RbtA),纳米-微摩尔级亲和力 |
CyclicMPNN | ProteinMPNN在环肽数据集上的微调 | 短环肽序列设计优化(6-14残基) | 计算验证(RMSD降低约0.4 Å) |
PocketXMol | 原子级统一表示+原子提示 | 小分子/多肽统一设计(无需微调) | Caspase-9抑制剂(媲美市售药物)+PD-L1结合肽(纳摩尔级) |
BoltzGen | 几何连续表示+设计规范语言 | 全原子跨模态结合体设计(纳米抗体·环肽等) | 8项设计活动·26个靶点·66%纳摩尔成功率 |
七、挑战与展望
7.1 尽管上述方法取得了显著进展,计算设计仍面临多重挑战
环化拓扑的多样性:天然环肽除头尾环化外,还存在侧链-侧链、头-侧链、多环及打结环肽等多种拓扑形式,当前方法对复杂环化模式的建模能力仍有限。
非天然氨基酸:天然环肽中广泛存在的D-氨基酸、N-甲基化氨基酸及翻译后修饰,在现有深度学习框架中缺乏充分表示。
构象柔性:环肽在溶液中可能存在多种构象状态,而现有方法多聚焦于单一最低能量构象的生成,对构象系综的建模仍是难题。
细胞渗透性与口服生物利用度:当前设计目标主要聚焦于结合亲和力,但治疗性环肽的细胞穿透能力和口服可用性同样关键,这些性质与结构特征的关系尚待深入理解。
7.2 展望未来,几个方向值得关注
多模态联合优化:将亲和力、稳定性、细胞渗透性和代谢稳定性纳入统一的优化框架,实现治疗性环肽的多目标协同设计。
构象系综建模:借鉴Boltzmann生成器等热力学采样方法,从单一构象设计走向构象系综的生成与控制。
实验-计算闭环迭代:建立自动化设计-合成-表征-反馈的闭环平台,以实验数据持续迭代优化模型。
天然产物启发式设计:天然环肽中蕴藏着丰富的结构motif和功能模式,将其编码为模型先验可能产生更高效的结合剂。
八、结语
从AfCycDesign的循环位置编码到PocketXMol的原子级统一框架,头尾相连环肽的计算设计在短短两年间完成了从“专用工具”到“通用平台”的范式跃迁。当前领域正处于两个关键趋势的交汇点:一方面,RFpeptides与CyclicMPNN代表了“深度专业化”路径,通过针对性改造成熟模型来解决特定设计环节;另一方面,BoltzGen与PocketXMol则引领着“统一化”潮流,以原子级表示和统一生成核心打破分子类型与任务边界。这两种趋势并非互斥,而是共同塑造了环肽设计领域的未来图景——一个既拥有专业工具的精准高效、又具备统一平台的灵活通用的计算设计生态系统。随着模型能力的持续提升与实验验证闭环的建立,从头设计具有治疗价值的环肽药物将不再遥不可及。
参考文献
[1] Rettie SA, Campbell KV, Bera AK, et al. Cyclic peptide structure prediction and design using AlphaFold2. Nature Communications, 2025, 16: 4730.
[2] Bhardwaj G, DiMaio F, Baker D, et al. Accurate de novo design of high-affinity protein-binding macrocycles using deep learning. Nature Chemical Biology, 2025.
[3] Powers AC, Janthana Y, Hosseinzadeh P. CyclicMPNN: Stable cyclic peptide sequence generation. bioRxiv, 2026.
[4] Ma J, Peng X, et al. Unified modeling of 3D molecular generation via atomic interactions with PocketXMol. Cell, 2026.
[5] Stark H, Faltings F, Choi MG, et al. BoltzGen: Toward universal binder design. bioRxiv, 2025.
以上所有工具均已在SciMiner平台部署,欢迎大家免费试用,并关注平台后续的评测。
 夜雨聆风
夜雨聆风