2026年4月16日,斯坦福大学Alex Gao团队在《Science》发表最新研究,揭示了一种前所未见的DNA合成机制—细菌防御系统DRT3中的一个逆转录酶亚基,在完全没有核酸模板的情况下,仅凭蛋白质自身的活性位点氨基酸残基,就能精准合成交替的poly(AC)重复DNA。
背景:核酸聚合酶的两个世界
生命中的DNA合成,历来遵循一条铁律:要么有模板,要么没有序列特异性。
所有已知的核酸聚合酶大致分为两类。一类是"模板依赖型",忠实地按照已有的核酸序列进行复制,比如DNA聚合酶、RNA聚合酶、逆转录酶;另一类是"模板非依赖型",它们合成的产物要么是单调的均聚物(比如poly(A)),要么是近乎随机的短序列,缺乏精确的序列规律。
唯一的例外是真核生物中的核苷酸转移酶RDE-3,它能在RNA 3'端添加交替的poly(UG)序列。但在这之外,是否还存在其他能够精准合成序列特异性核酸的非模板依赖机制?这个问题一直悬而未决。
这篇来自斯坦福大学的新研究,给出了一个令人惊喜的答案。而这个答案,藏在细菌与噬菌体亿万年军备竞赛的最前线。
主角登场:DRT3,一套"双引擎"防御系统
近年来,细菌中被称为防御相关逆转录酶(Defense-associated Reverse Transcriptases,DRTs)的免疫系统受到广泛关注。这类系统不靠切断外来DNA来防御病毒,而是反其道而行之—主动合成DNA来实现抗噬菌体免疫。
在已知的DRT家族成员中,DRT3有着独一无二的组成:它同时包含两个来自不同进化支系的逆转录酶:Drt3a(第2类UG逆转录酶)和Drt3b(第1类UG逆转录酶),以及一条非编码RNA(ncRNA)。这种"双引擎"的架构在所有DRT系统中绝无仅有。
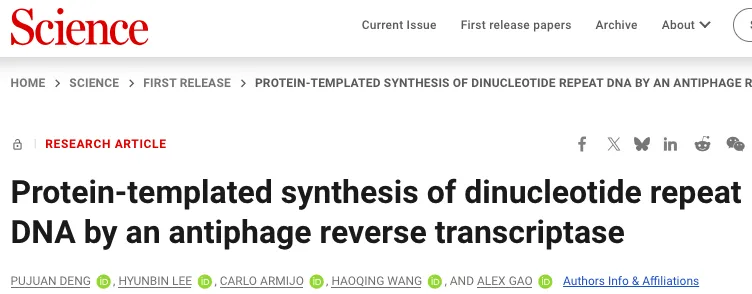
研究团队克隆了两个DRT3系统:来自大肠杆菌GF3-3的EcDRT3和来自大肠杆菌ECOR12的Ec2DRT3(二者氨基酸序列同一性32%),并验证了它们在异源大肠杆菌K-12中均能对T1、T4、T5噬菌体提供强效防御,且防御活性同时依赖两个RT活性位点和ncRNA。
DRT3合成什么? 答案令人意外:细胞测序实验揭示,DRT3在不依赖噬菌体感染的情况下,就能持续合成poly(GT/AC)交替二核苷酸重复的双链DNA。
结构揭秘:一个精密的六聚体机器
为了理解DRT3如何运作,研究团队利用冷冻电镜(cryo-EM)在2.6 Å的高分辨率下解析了EcDRT3复合体的两种构象:静息态(不含dNTP)和延伸态(含dNTP)。
结构显示,EcDRT3形成了一个具有D3对称性的大型六聚体复合物,包含各6个拷贝的Drt3a、Drt3b和ncRNA。其基本单元是一个1:1:1的Drt3a–Drt3b–ncRNA原聚体,三个原聚体形成一个三聚体,两个三聚体再"尾对尾"二聚化,构成最终的六聚体。
在复合物外侧,可以清晰观察到DNA产物双链的存在。这正是DRT3源源不断合成的poly(GT/AC) dsDNA产物。
这一六聚体的组织方式与另一DRT成员AbiK相似(均为"三聚体的二聚化"),但与DRT9的"二聚体的三聚化"构型不同,展示了UG逆转录酶家族在结构上的多样性。
第一引擎 Drt3a:类端粒酶的RNA模板合成
Drt3a负责合成poly(GT)单链DNA,走的是一条经典的RNA模板依赖路线。
ncRNA包含四个茎环结构(SL1–SL4),其保守的A¹⁰⁸CACAC¹¹³基序被精确定位在Drt3a的活性位点中,作为模板来指导poly(GT)合成。冷冻电镜结构清晰分辨出产物–模板双链的形成:静息态中活性位点有5个核苷酸产物(TGTGT),延伸态则解析出6个核苷酸。
Drt3a的拇指域上有一段独特的β-hairpin延伸(残基323-338),紧邻模板基序C113的3'端,研究者推测其功能类似于端粒酶的"拇指环",在每轮二核苷酸添加后帮助解离产物–模板双链,从而允许下一轮合成开始循环。
这与端粒酶的机制高度呼应:端粒酶同样以RNA为模板,周而复始地合成串联重复序列。事实上,Drt3a在结构上与端粒酶、II型内含子逆转录酶及DRT2、DRT9等第2类UG逆转录酶均高度相似。
第二引擎 Drt3b:史无前例的"蛋白质模板"合成
如果说Drt3a的机制已经足够精彩,那么Drt3b的发现则真正改写了核酸聚合酶的认知边界。
Drt3b负责合成poly(AC)单链DNA,而这一切,发生在完全没有核酸模板的情况下。
活性位点结构分析发现,Drt3b的模板结合通道被自身的C端片段(残基645-650)和一个Drt3b特有的延伸内部环(残基112-169)共同封堵,使得任何外来核酸模板都无法进入。此外,Drt3b的N端保守残基Glu26也占据了正常模板链所在的位置。
那么,没有模板,序列特异性从何而来?
答案在于一种全新的蛋白质模板机制:Drt3b活性位点内的nascent cDNA链呈现出一种异常的骨架扭结构型,将三个碱基(dC15-dA16-dC17)压缩进通常只容纳两个碱基的空间。这种扭曲几何构型触发了一张蛋白质–DNA碱基互作网络,以蛋白质侧链取代核酸模板的结构功能:
- Glu26
是核心"门卫":其侧链伸入核苷酸结合口袋,模仿一个模板碱基的功能,通过两个氢键与dA18的N6氨基特异性结合,从而精准区分dATP和dGTP、dTTP; - Arg253
则作为"副模板":通过阳离子–π相互作用偏好嘌呤,并与前一个dC17的Watson-Crick边形成三个氢键,协助区分dCTP和dTTP; 此外还有多个残基(Arg408、Thr335/Thr338、Arg168/Tyr289、Tyr170等)对上游4个碱基(dC13-dA16)形成碱基特异性或构型稳定性接触,共同构成一张覆盖6个末端碱基的蛋白质"信息编码网络"。
突变验证证实了这套机制的精密性:Glu26突变为Ala(E26A)导致合成严重截短,突变为Gln(E26Q)则在引入dGTP后发生dA位点的错误掺入,表明Glu26是dATP选择的关键门控残基。两种突变体均完全丧失抗噬菌体防御能力。
值得注意的是,Drt3b与同属第1类UG逆转录酶的AbiK在整体结构和酪氨酸引物机制上高度相似,但AbiK只能合成随机序列的DNA。正是Drt3b中这些精细的活性位点适应性改造,赋予了它独一无二的序列特异性聚合能力,彰显了UG逆转录酶家族在功能多样性上的惊人可塑性。
至于引物的来源,研究发现Drt3b C末端的Tyr650(在不同同源物中偶尔为Ser)通过羟基与DNA形成共价加合物,充当引发合成的起始位点。Tyr650的突变彻底废除了DNA合成和抗噬菌体功能。酪氨酸引物机制在多个DRT系统(AbiK、Abi-P2、AbiA、DRT9)中普遍存在,提示这是第1类UG逆转录酶的一个共同特征。
两条链,缺一不可
DRT3的抗噬菌体防御,依赖于两条链的协同合成。实验证明,破坏任意一个RT的活性位点,防御活性即完全丧失。尽管另一个RT仍能在体外继续合成其对应的单链DNA。这说明,双链dsDNA产物,而非单链中间体,才是执行免疫功能的关键分子实体。
至于poly(GT/AC) dsDNA如何实现抗噬菌体,目前尚不完全清楚。论文推测,这种高度重复的序列可能有助于形成多链通过互补退火组成的高级网络结构,或倾向采取非B型DNA构象(如滑链结构),从而作为"分子海绵",滴定吸附噬菌体来源的DNA结合蛋白,干扰其复制,类似于此前对DRT9 poly(A) DNA功能的推测。
触发开关:噬菌体T1蛋白ST61
研究团队通过适应性进化筛选到5株能够逃逸EcDRT3防御的T1噬菌体突变体,测序发现它们全部携带同一个未表征基因ST61的失活突变。进一步实验表明,将ST61与EcDRT3共表达会对细菌产生持续毒性,而破坏DRT3系统中任一组分(Drt3a、Drt3b或ncRNA)均能消除这种毒性。这表明,ST61是触发DRT3介导防御所必需的噬菌体编码蛋白,是激活这套免疫机器的"扳机"。
意义:重新认识核酸聚合酶的边界
这项研究至少在三个层面具有重要意义:
一、发现了全新的聚合酶机制。 目前已知的蛋白质模板碱基加入仅限于极短的产物,如CCA添加酶在tRNA 3'端添加CCA三核苷酸,或DNA跨损伤聚合酶Rev1仅模板化单个胞嘧啶。Drt3b则能持续合成长链、序列特异性的DNA,将蛋白质模板聚合酶的产物长度推到了一个全新的量级,展示了生命中生物信息传递的一种前所未见的模式。
二、完善了DRT家族的功能图谱。 第1类UG逆转录酶(如AbiK、AbiP2)此前被认为只能合成随机序列;第2类UG逆转录酶(如DRT2、DRT9)则利用ncRNA模板合成重复序列。DRT3将这两种能力融合在同一个系统中:Drt3a(第2类)以ncRNA为模板,Drt3b(第1类)以蛋白质为模板,两条互补链协同产生dsDNA,在DRT家族中独树一帜。
三、拓展了对抗噬菌体免疫多样性的认识。 细菌免疫系统不断刷新我们对生命创造力的认知。从CRISPR的精准切割,到DRT2的从头基因合成,再到DRT9的poly(A)滴定,如今又有DRT3以蛋白质充当聚合酶模板,噬菌体与细菌之间的这场无尽军备竞赛,依然在不断催生出令人叹为观止的分子创新。
 夜雨聆风
夜雨聆风