干细胞注射疗法面临两大“致命伤”:注射后高达90% 的细胞因机械应力和缺乏锚定而流失,且难以在靶点定植分化。Sung Min Han等人发表于 《Cell Biomaterials》 的研究,从海洋贻贝中汲取灵感,利用工程化贻贝基质蛋白(PTMP-RGD)与透明质酸形成复合凝聚体(CoPTMP-RGD),构建了一种可注射的仿生细胞外基质(ECM)。该平台实现了>98% 的干细胞包裹效率,并在体内将细胞滞留率提升2倍以上(从22.7%到超50%),同时显著促进新生血管形成。
研究流程:贻贝蛋白序列挖掘与AI结构预测 → PTMP-RGD重组表达与纯化 → 与HA形成复合凝聚体 → 理化表征(剪切变稀/血液相容性)→ 体外细胞功能验证(粘附/增殖/干性/分化)→ 体内滞留与血管化评估(小鼠皮下注射)
一、为什么这是突破?——“仿生ECM”凝聚体,让干细胞“住得舒服”
传统水凝胶载体注射后细胞流失严重,且缺乏生物活性信号。本研究首次将贻贝来源的胶原结合蛋白(PTMP)与RGD整合素识别序列融合,并通过静电复合凝聚与透明质酸自组装成可注射载体。该平台不仅模拟了天然ECM的物理支撑和化学信号,还利用vWF-A结构域主动结合胶原,实现“锚定-保护-促血管”三位一体功能。
二、实验逻辑+关键数据:环环相扣的“设计-验证”链条
实验逻辑: 从海洋蛋白中“借”来胶原结合能力 → 引入RGD获得细胞粘附信号 → 与HA复合获得可注射性 → 体外验证细胞相容性 → 体内验证滞留与血管化。
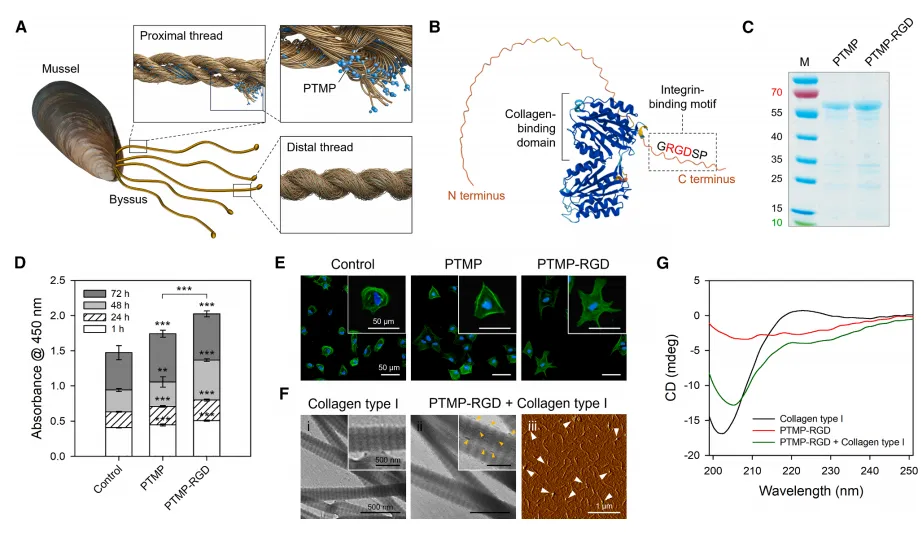
蛋白工程与AI设计:将贻贝PTMP的vWF-A结构域与RGD序列融合,AlphaFold预测其与胶原的结合模式,实验证实PTMP-RGD显著促进MSC粘附和铺展(细胞面积增加2.5倍)。→ 数据意义:AI指导的蛋白设计成功赋予材料胶原结合和整合素激活双重功能。
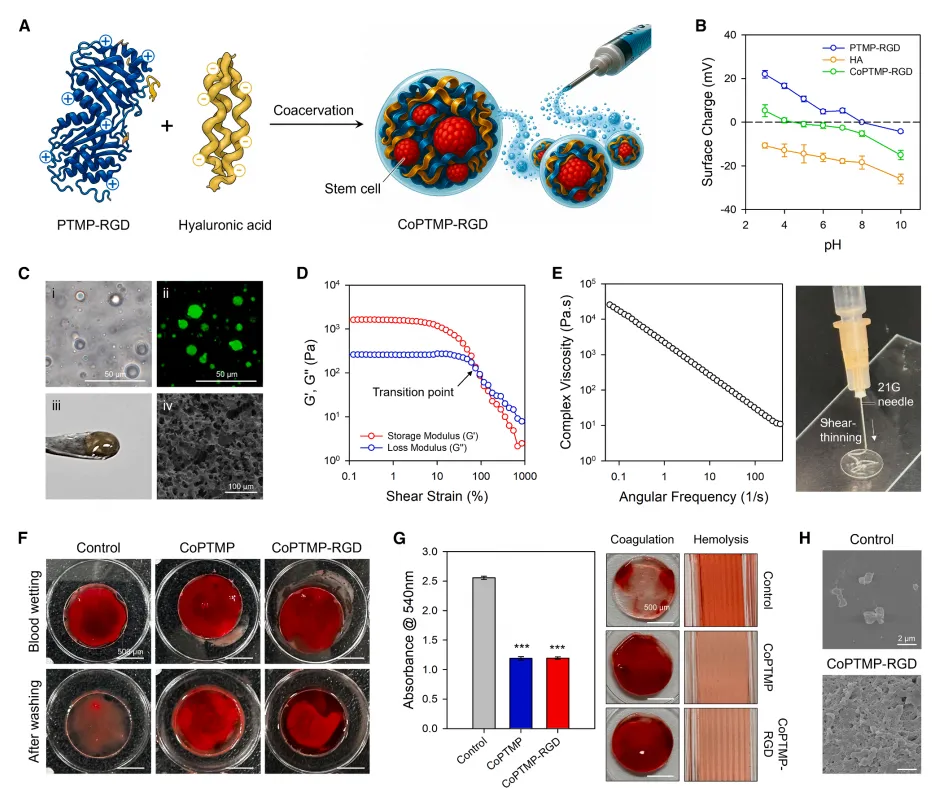
凝聚体制备与流变学:PTMP-RGD与HA在pH 5.0、质量比6:4时形成复合凝聚体,表现出剪切变稀行为(高剪切下粘度下降100倍),可通过21G针头注射。→ 数据意义:证明该载体具备优异的可注射性,适合微创手术。
细胞包裹与功能维持:CoPTMP-RGD实现>98% 的MSC包裹效率(密度高达10⁷ cells/mL),包裹后细胞存活率>95%,OCT4/SOX2干性标志物表达维持至少3天,且成骨/成软骨/成脂三系分化能力完整。→ 数据意义:凝聚体不仅“装得进”,还能“养得好”,不损伤干细胞特性。
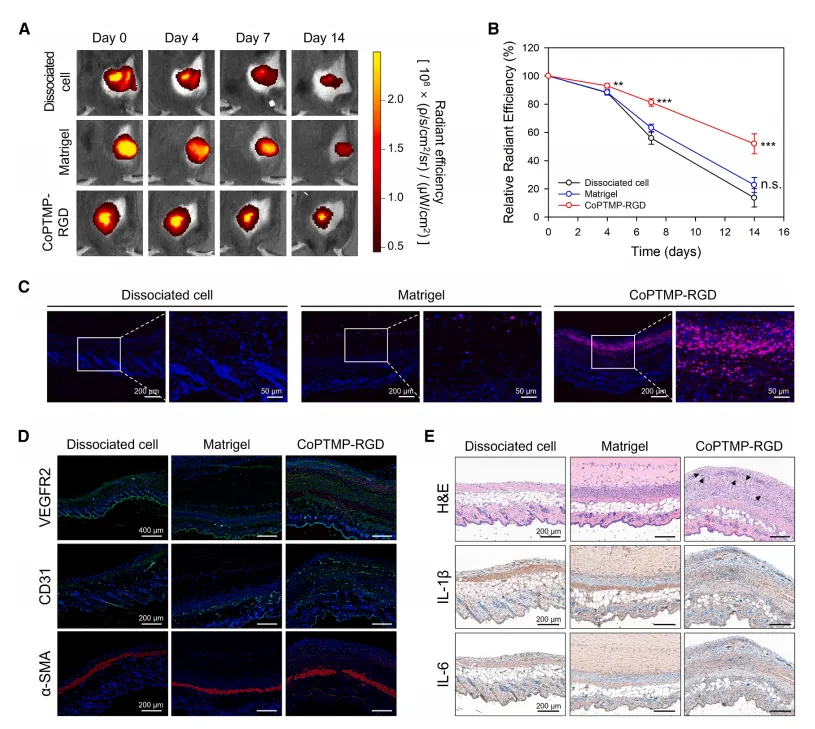
体内滞留与血管化:小鼠皮下注射后,CoPTMP-RGD组在14天时细胞滞留率超50%,而对照组仅22.7%。免疫荧光显示VEGFR2、CD31和α-SMA信号显著增强,表明新生血管成熟且稳定。→ 数据意义:首次在体内验证了该类凝聚体平台可显著提升干细胞定植和促血管能力。
三、结果验证或讨论:从“材料”到“组织”的深度解读
仿生设计,双信号协同:PTMP-RGD融合蛋白同时携带“锚定胶原”(vWF-A)和“粘附细胞”(RGD)两个功能域。这模拟了天然ECM中整合素配体与胶原的结合模式,实现了材料-细胞-宿主组织的三方对话,远优于单一功能材料。
凝聚体化学,温和包裹:复合凝聚通过静电作用在水相中自发形成,无需有机溶剂、高温或紫外交联,对干细胞极其温和。低界面张力(~1-10 μN/m)使细胞在包裹过程中几乎不受剪切损伤。
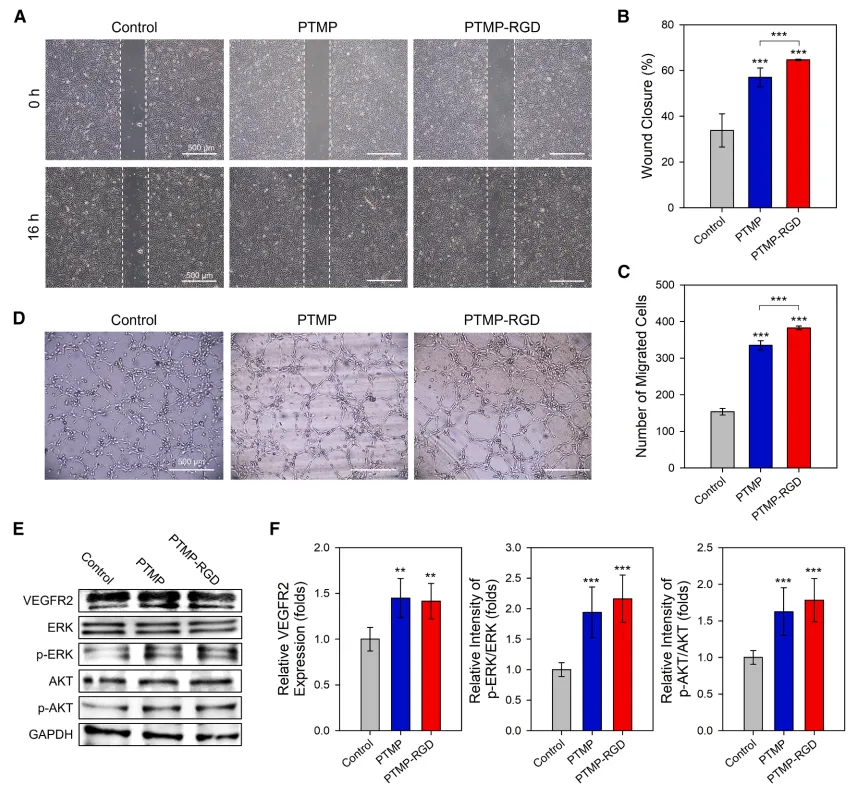
血管化生态位,主动诱导:体内实验显示,CoPTMP-RGD不仅“留住”了细胞,还诱导了宿主来源的血管新生(CD31⁺内皮细胞和α-SMA⁺周细胞共定位)。这得益于PTMP-RGD激活了VEGFR2-AKT-ERK信号轴,主动创造了一个促血管的再生微环境。
酶控降解,时空匹配:CoPTMP-RGD在透明质酸酶作用下约70%在1个月内降解,与组织再生的时间窗口匹配。降解过程中缓慢释放的MSC可进一步参与修复,实现了“载体-细胞”的动态接力。
四、为什么这么做?——方法学优势
AI驱动的蛋白设计:利用AlphaFold3预测PTMP-RGD的三维结构和胶原结合界面,大幅减少了试错成本,实现了“计算指导实验”的精准工程。
模块化融合蛋白策略:将胶原结合域(vWF-A)和细胞粘附域(RGD)整合到同一个重组蛋白中,确保了两种功能的化学计量比1:1,避免物理混合带来的批次差异。
静电复合凝聚一步成型:无需复杂的化学交联或光聚合,仅通过调节pH和混合比即可在5分钟内自组装成可注射载体,工艺极简、可放大。
多维度体内验证:结合IVIS活体成像、组织切片免疫荧光(CD31/α-SMA/VEGFR2)和H&E染色,从细胞数量、血管结构、炎症反应三个维度全面评估载体性能。
五、技术局限
动物模型局限:仅使用C57BL/6小鼠皮下注射模型,尚未在疾病模型(如心肌梗死、骨缺损)中验证治疗 efficacy,也未评估长期安全性(>3个月)。
降解产物代谢不清:虽然HA和PTMP-RGD理论上可生物降解,但其降解片段在体内的分布、代谢和潜在免疫原性未被系统研究。
机制深度有限:虽证实了FAK-AKT-ERK通路的激活,但未使用基因敲除或特异性抑制剂进行因果验证,RGD-整合素的具体亚型(如αVβ3 vs α5β1)未鉴定。
规模化生产挑战:重组PTMP-RGD在大肠杆菌中表达,但产量和纯化成本未详细报道。凝聚体的批间一致性和长期储存稳定性也需进一步验证。
六、意义与展望
本研究首次将海洋贻贝蛋白工程与复合凝聚体化学相结合,为干细胞递送提供了一个“即插即用”的仿生平台。其意义在于:
理论层面:证明了通过融合蛋白设计,可将天然ECM的“结构支撑、细胞粘附、生长因子结合”等多重功能重构于一个简单的凝聚体系统中。
技术层面:建立了“AI结构预测 → 重组表达 → 静电自组装 → 体内验证”的完整技术链条,可推广到其他组织工程材料的开发。
转化层面:CoPTMP-RGD具备优异的可注射性、血液相容性和细胞保护能力,有望用于心肌梗死、糖尿病足溃疡、骨关节炎等需要局部细胞治疗的疾病。
展望未来:1)在多种疾病模型中验证治疗 efficacy;2)探索负载其他细胞类型(如iPSC、CAR-T)的可行性;3)结合3D生物打印,构建复杂组织;4)利用AI优化蛋白序列,进一步提高胶原亲和力和细胞响应性。
文献来源:Han, S.M., Baek, M.J., & Jo, Y.K. Marine-inspired proteinaceous coacervates as an injectable extracellular matrix mimicry for enhanced stem cell delivery. Cell Biomaterials. 2026;2:100423. doi:10.1016/j.cellbio.2026.100423
相关阅读:
相分离+影响干细胞:FXR1凝聚体调控mRNA的定位与翻译,影响核孔功能与细胞命运转换
2025 JBC 细胞里的“新大陆”:从发现相分离到设计凝聚物——可编程、可调控、可应用的合成凝聚物世界

 夜雨聆风
夜雨聆风