 点击蓝字,关注我们
点击蓝字,关注我们

01
科研速递
🔬 文献速递:深度学习新模型准确预测ESCC免疫治疗完全缓解
对于食管鳞状细胞癌患者,在接受新辅助免疫联合化疗后,达到病理完全缓解是理想的治疗目标。然而,临床上如何提前、准确地识别出这部分能够实现pCR的患者,仍是一大挑战。
近日,一项发表于 《Journal for Immunotherapy of Cancer》(IF:10.3)的前沿研究,提出了一个基于 CT影像的深度学习模型 —— Vision-Mamba。该模型在预测pCR方面展现出较高的准确性,为临床制定个体化治疗方案提供了新的、无创的决策工具。
对这个前沿的人工智能+肿瘤免疫方向感兴趣的读者,千万不要错过这篇文献的深度解读!赶紧跟随我们的脚步,一起学习其创新的研究思路与先进方法吧!


1中文标题:体素级影像组学和深度学习预测食管鳞状细胞癌新辅助免疫治疗联合化疗后的病理完全缓解
发表时间:2025年5月
发表期刊:J Immunother Cancer
影响因子:IF=10.6
02
研究亮点
🧠 研究背景:精准预测pCR,让部分ESCC患者免于不必要的手术
在食管鳞状细胞癌的治疗中,新辅助免疫联合化疗能使约 40%~50% 的患者达到病理完全缓解,但随之而来的术后并发症率也高达40%左右。若能在治疗前精准预测哪些患者能达到pCR,这部分患者则有可能避免创伤性手术,转而采用 “观察等待” 的器官保留策略,从而极大提升生活质量。
然而,传统的放射组学方法在提取特征时会丢失肿瘤空间异质性的关键信息;而纯粹的深度学习模型又容易在小样本数据中过拟合,影响泛化能力。因此,本研究旨在开发并验证一种基于术前CT图像的创新深度学习模型,以准确预测ESCC患者接受nICT后的pCR状态,为临床治疗决策提供可靠的无创工具。
03
研究方法
🧪 研究方法:多中心回顾性研究构建高解释性AI预测模型
1. 📊 患者入组与数据划分
患者来源:本研究为一项多中心回顾性研究,共纳入741名接受新辅助免疫联合化疗后行根治性食管切除术的ESCC患者。
数据集划分:数据来自三个独立机构,按如下方式划分以确保模型泛化能力:
训练集(469例)与内部验证集(118例):来自同一机构
外部验证集1(120例)与外部验证集2(34例):分别来自另外两个机构
2. 💉 治疗方案与病理评估标准
治疗方案:所有患者接受至少一个周期的nICT(免疫治疗与铂类化疗同步)。
手术时机:nICT结束后 4-8周 内行食管切除术。
病理评估:由专业病理学家根据美国病理学家学会(CAP)的TRG分级评估标本。pCR定义为原发肿瘤部位无存活肿瘤细胞(TRG 0级)。
3. 🖥️ 影像处理与特征提取
CT影像标准化:所有增强胸部CT影像经标准化与归一化处理。
肿瘤区域分割:由两名经验丰富的放射科医生手动勾画肿瘤区域,并使用 3D Slicer 软件精细调整。
特征提取:从勾画区域提取 90个体素级放射组学特征图,涵盖强度与纹理特征。
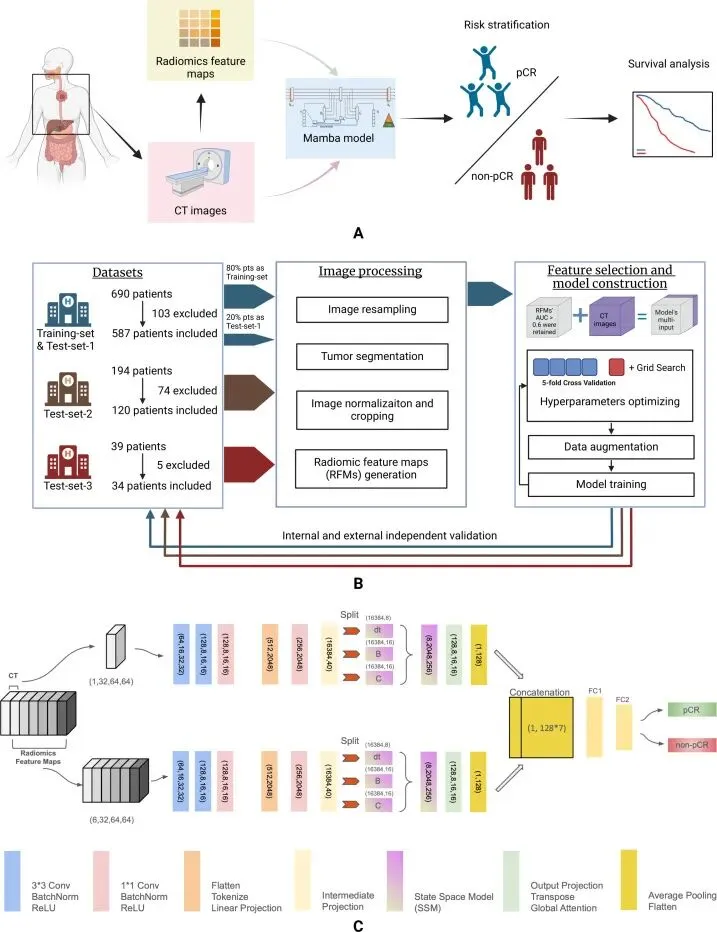
4. 🤖 创新模型构建(Vision-Mamba)
本研究提出创新的 Vision-Mamba深度学习架构:
双路输入:模型采用双通路设计,独立处理原始CT图像与放射组学特征图。
序列建模:引入双向状态空间模型高效处理长序列数据,再通过全局注意力与平均池化层整合特征。
预测输出:整合后的特征输入全连接层,输出pCR概率预测。
5. ⚖️ 模型比较与可解释性验证
性能比较:与传统放射组学方法及主流深度学习模型(如3D-ResNet、Vision Transformer)进行对比,评估指标包括准确率、AUC、敏感性、特异性。
可解释性分析:采用 SHAP分析揭示模型决策的关键影像特征,增强模型透明度与临床可信度。
04
研究结果
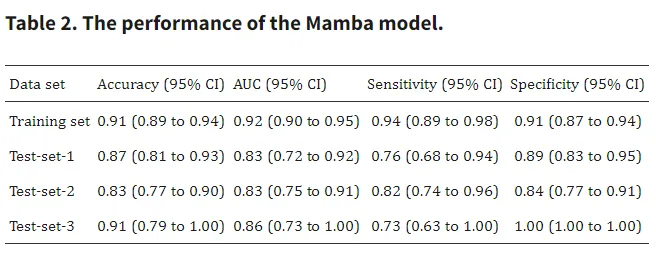
Vision-Mamba模型在训练与验证过程中均表现出优异的预测性能:
训练集:准确率0.83-0.91,AUC值0.83-0.92,敏感性0.73-0.94,特异性0.84-1.0。
验证集:性能指标与训练集高度匹配,表明模型未出现过拟合。
外部验证集:模型在独立的外部数据集上同样表现出稳健的性能与良好的泛化能力,证明了其跨中心应用的可靠性。
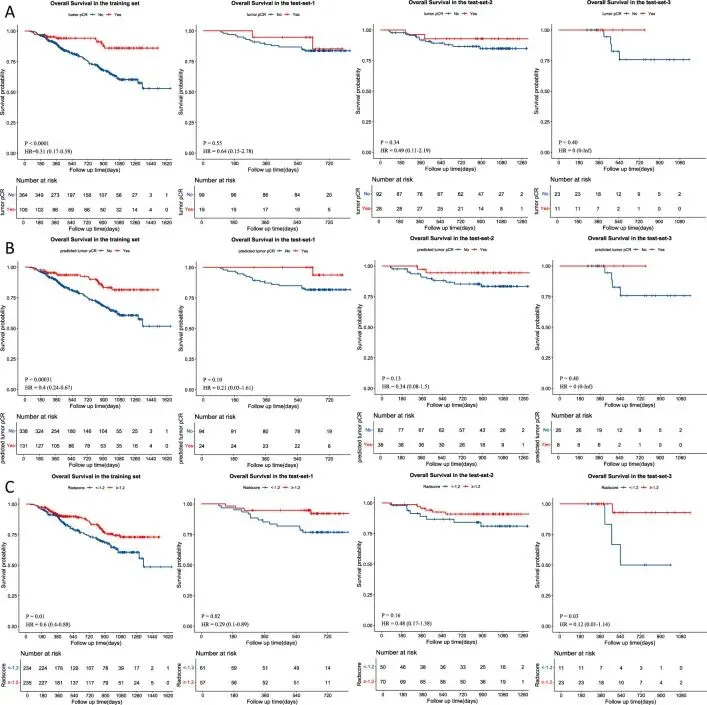
Vision-Mamba模型展现出强大的预后分层能力:
风险区分显著:模型能够基于预测的风险评分(界值为-1.2),将患者有效区分为高风险组与低风险组,两组间的生存差异具有高度统计学显著性,其分层能力优于传统方法。
生存预测准确:根据模型评分进行预后分析发现,风险评分低于中位数的患者,其总生存期显著优于评分高于中位数的患者,这为临床个体化治疗决策提供了重要依据。
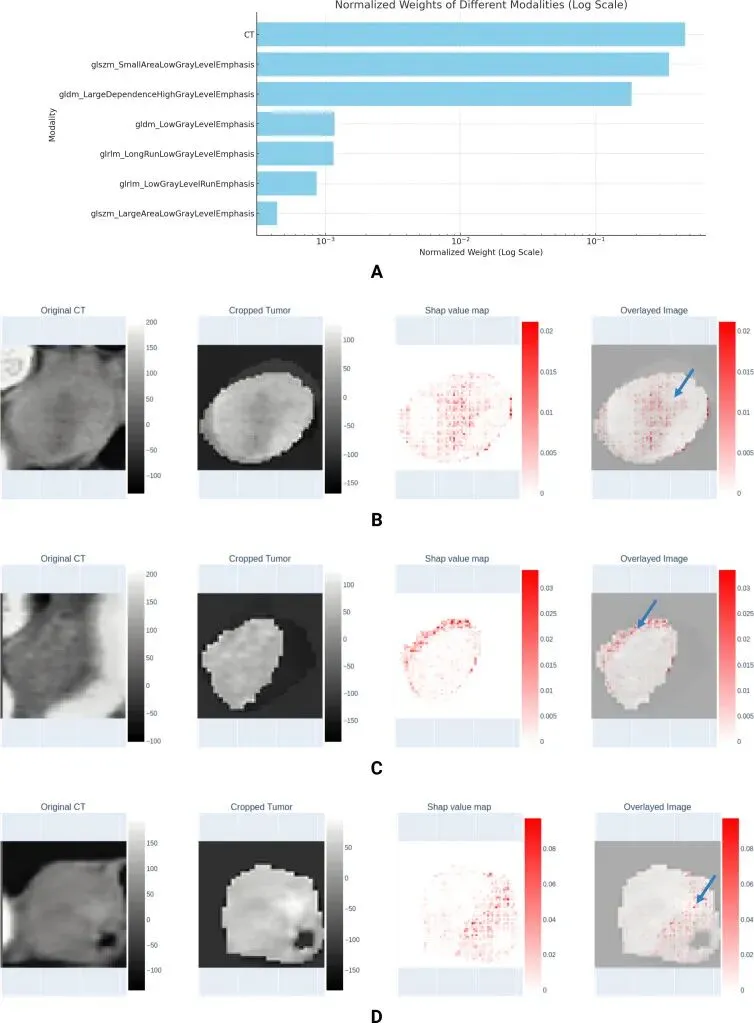
通过 SHAP可解释性分析,研究揭示了Vision-Mamba模型做出预测所依据的关键影像特征:
特征重要性排序:原始CT图像本身对模型预测的贡献最大。其次,两个特定的放射组学特征也至关重要:
glszm_SmallAreaLowGrayLevelEmphasis(反映小面积低灰度区域聚集)gldm_LargeDependenceHighGrayLevelEmphasis(反映高灰度区域的大依赖性)。关键解剖区域:SHAP值图直观显示,肿瘤内部的坏死区域(贡献 34.97%)与 肿瘤边缘的增强区域(贡献 18.54%)是模型预测最关键的两个解剖区域,其他显著增强区域也贡献显著。
这从影像学角度解释了模型“看到”了什么,极大地提升了其临床可信度与接受度。
05
文章小结
💡 文献亮点及经验借鉴
1. 技术创新亮点
体素级放射组学:摒弃传统特征压缩方法,在体素层面提取放射组学特征,完整保留了肿瘤的空间异质性信息,克服了既往方法的根本局限。
Vision-Mamba 架构:创新性地引入双向状态空间模型,能够高效处理医学图像中的长序列数据,提升了模型对复杂影像模式的捕捉能力。
方法学严谨性:研究通过多中心外部验证确保了模型的普适性与稳健性,并利用 SHAP 可视化技术为模型决策提供了直观解释(如发现肿瘤坏死区与预后的强关联),增强了临床可信度。
2. 临床意义与未来展望
该研究证实了 Vision-Mamba 模型在预测食管癌新辅助免疫治疗疗效方面具有显著潜力。虽然仍需更多前瞻性临床研究验证,但它为制定个体化治疗策略(如筛选可避免手术的pCR患者)提供了切实可行的新思路。
未来,随着技术持续优化与多中心大数据的积累,AI 辅助临床决策有望成为肿瘤诊疗中的常规工具,帮助医生更精准地评估治疗反应、优化患者全程管理,最终实现从“一刀切”到“一人一策”的诊疗模式跨越。
【欢迎随时联系我们,一起把握发文先机!】
END

往期推荐
12.5/Q2,广西医科大:使用 FAERS 数据库系统分析舒更葡糖相关的药物不良反应信号
9.7/Q1,机器学习与FAERS 数据库挖掘相结合:机器学习指导药物不良反应与体外靶点药理学的关联
FAERS数据新警示:奥希替尼肌毒性风险被低估,远不止于心肌病
 夜雨聆风
夜雨聆风