

















单细胞+空转+实验验证,国自然前期基础首选!
文章信息
标题:The CEBPB+ glioblastoma subcluster specifically drives the formation of M2 tumor-associated macrophages to promote malignancy growth
期刊:Theranostics
影响因子:12.4
中科院分区:1区
发表时间:2024年7月2日(Published: 2024-7-2)


背景解读
No.1

研究疾病为胶质瘤,表型为M2巨噬细胞。通过单细胞联合空间转录组分析,识别了M2巨噬显著相关的特异性恶性亚群,后续锁定关键转录因子CEBPB,通过体内外实验验证其对M2极化的调控,再通过细胞通讯探索下游SPP1信号通路。
核心亮点:全公共数据+国自然热点巨噬细胞,高端套路模板!

No.2
研究结果详解

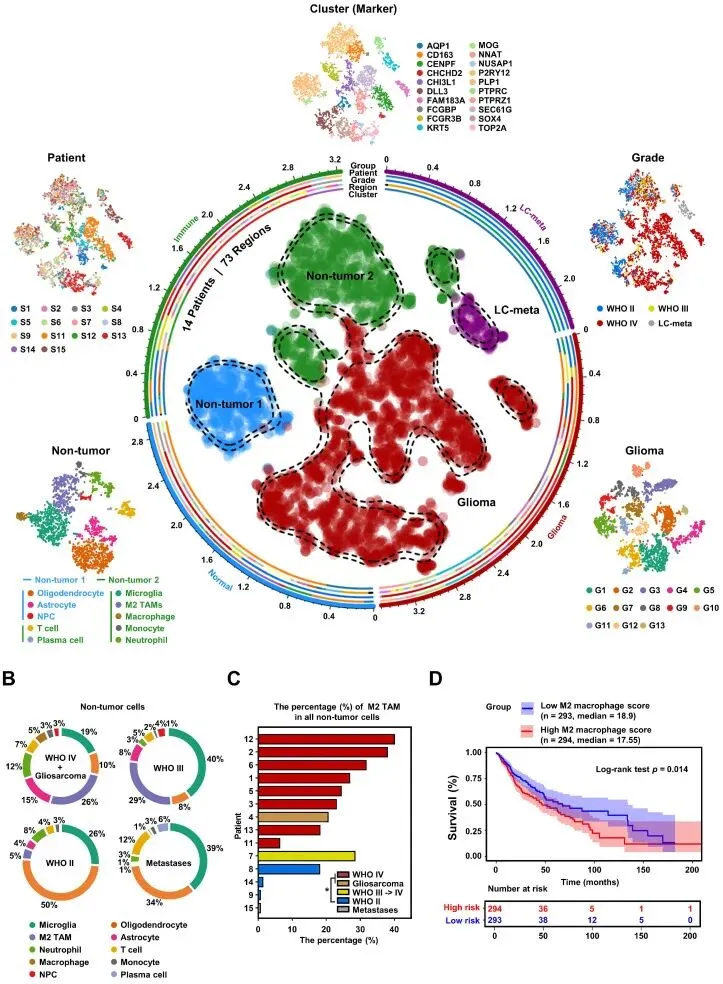
一、M2型巨噬细胞富集与胶质瘤恶性进展的相关性
展示胶质瘤单细胞图谱,饼图显示不同患者的非肿瘤细胞分布。14名患者中M2型TAM在非肿瘤细胞中占一定比例。TCGA GBMLGG队列数据显示,M2型巨噬细胞浸润评分与胶质瘤恶性进展显著相关。
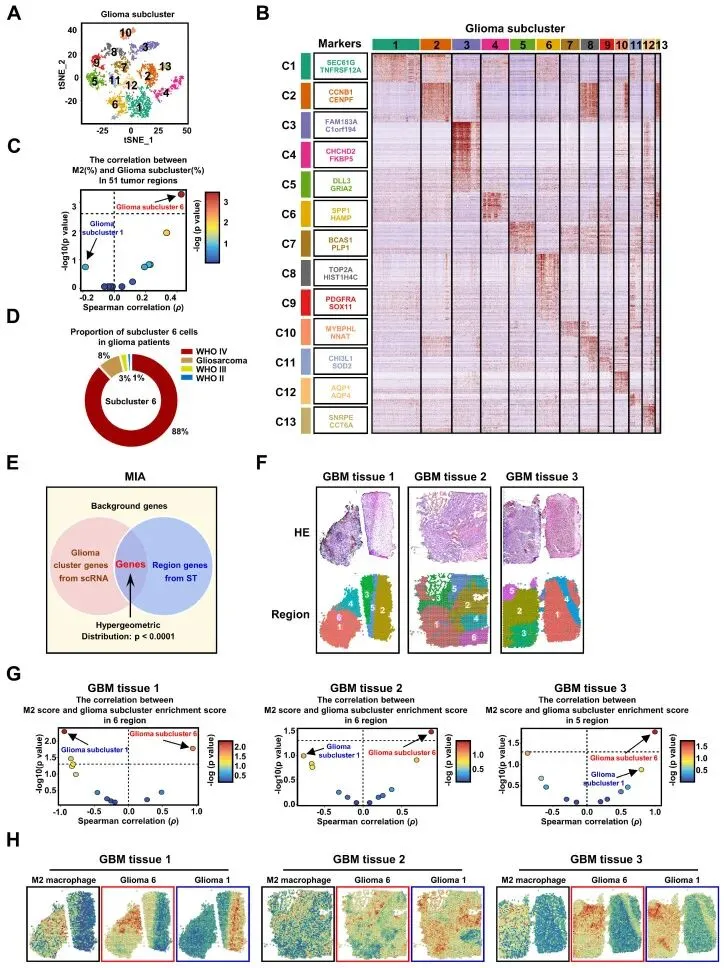
二、GBM亚簇6与M2型TAM分布高度相关
分析所有胶质瘤细胞得到13个细胞簇,展示标记基因表达模式。在51个肿瘤区域内,计算各胶质瘤亚簇与M2型TAM的Spearman相关性。空间转录组分析证实,M2评分与胶质瘤亚簇富集评分呈正相关。
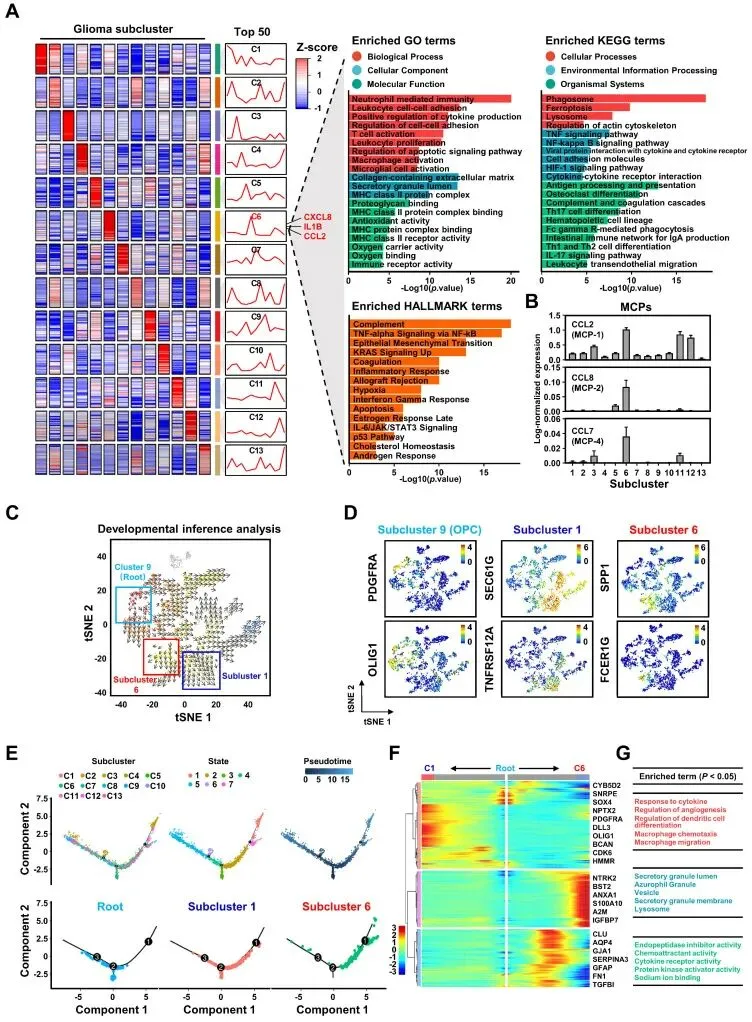
三、GBM亚簇6的生物功能学分析
对各簇前50个标记基因进行GO、KEGG及通路富集分析。发育推断分析展示细胞状态动态变化,拟时序分析展示从根到簇1和簇6的轨迹。簇6基因模块富集于特定功能通路。
四、揭示CEBPB是GBM簇6的特异性转录因子
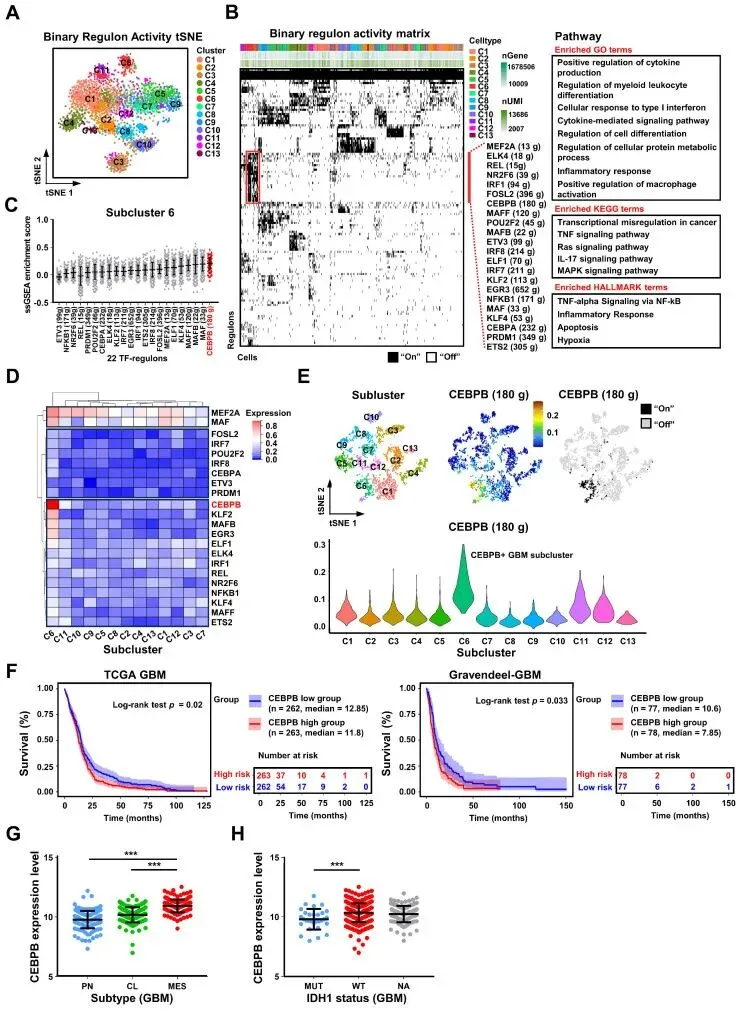
基于二元调控子活性的t-SNE分析,展示不同胶质瘤簇中的主调控转录因子。簇6中22个转录因子调控组的ssGSEA富集评分显示,CEBPB是关键转录因子。TCGA和Gravendeel队列中CEBPB高表达与生存期缩短相关。
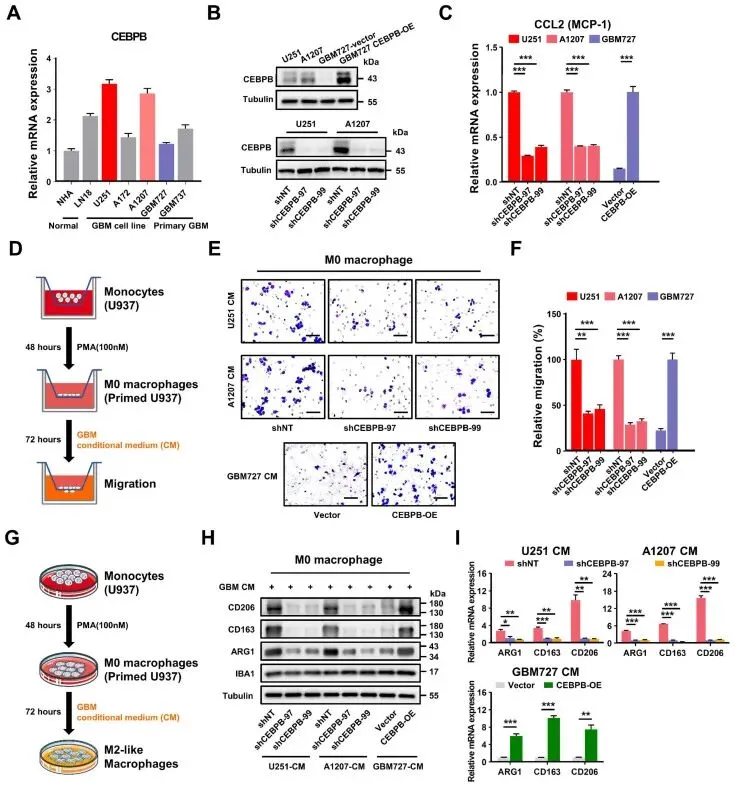
五、CEBPB体外招募TAM并诱导M2极化
qPCR和WB验证CEBPB在GBM细胞中高表达。敲低CEBPB后CCL2表达下降。体外迁移实验显示,敲低CEBPB的GBM条件培养基吸引巨噬细胞数量显著减少。WB和qPCR证实,CEBPB高表达的GBM条件培养基促进M2标志物(CD206、CD163)上调。
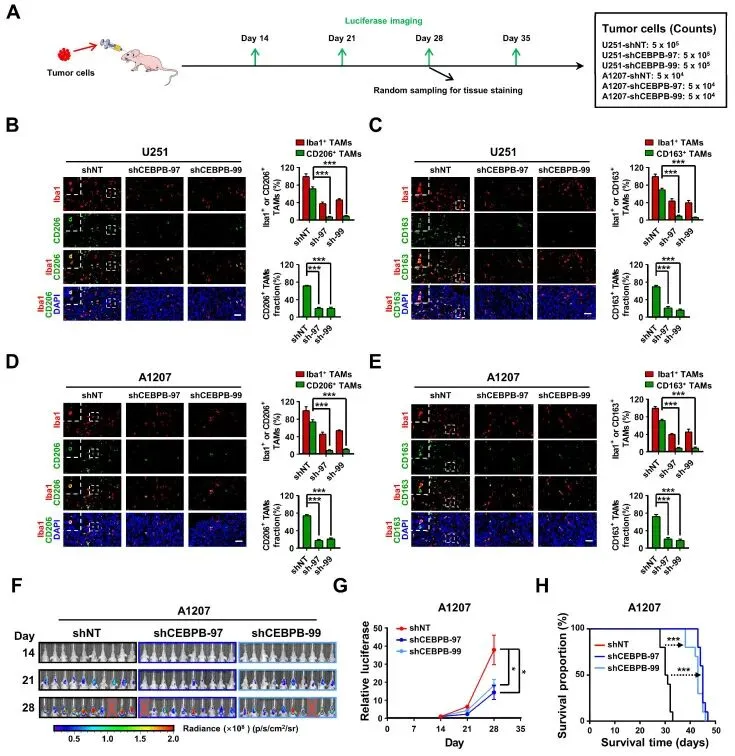
六、CEBPB体内促使TAM向M2极化促进肿瘤生长
免疫荧光显示,敲低CEBPB的异种移植瘤中M2标志物(CD206、CD163)表达下降。体内肿瘤生长实验显示,敲低CEBPB显著抑制肿瘤生长。
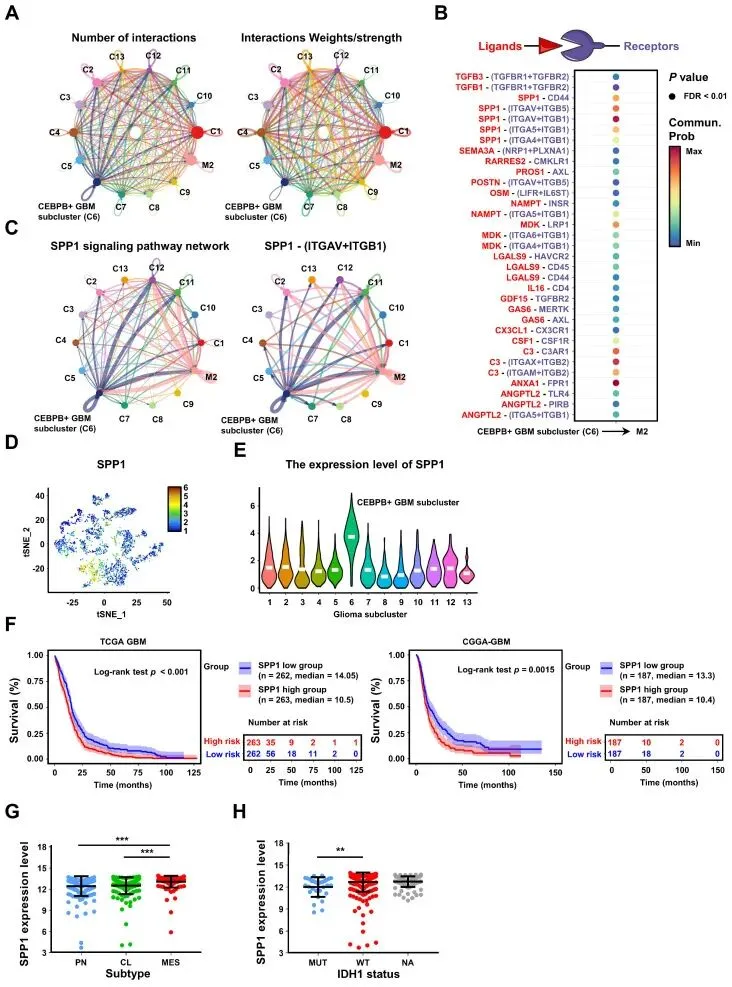
七、CEBPB通过SPP1-整合素αvβ1-Akt通路诱导M2极化
细胞通讯分析显示CEBPB+ GBM亚群与M2型TAMs之间存在SPP1配体-受体相互作用。SPP1在GBM簇6中高表达,高表达与生存期缩短相关。

研究框架
No.3
单细胞图谱 → 13个恶性亚簇 → 与M2评分相关性分析 → 锁定亚簇6 → 空间转录组验证 → 功能富集分析 → 拟时序分析 → 转录因子筛选 → 锁定CEBPB → 体外功能(迁移+M2极化) → 体内验证(免疫荧光+肿瘤生长) → 通讯分析 → 下游SPP1通路

No.4
核心可借鉴之处
全公共数据:Bulk + 单细胞 + 空间转录组,数据量大、工作量足
国自然热点:M2巨噬细胞极化,表型热门且机制清晰
干湿结合完美:生信发现→体外验证→体内验证,逻辑闭环
转录因子切入:从CEBPB调控入手,机制深度够
通讯分析收尾:SPP1信号通路,衔接上下游
适合模仿的选题方向
No.5
肺癌:M2 TAM + 恶性亚群 + 转录因子 + 免疫耐药
肝癌:TAM极化 + 空间定位 + 靶向治疗
乳腺癌:M2巨噬 + 转移亚群 + 趋化因子通路
胃癌:TAM招募 + EMT + TGF-β信号
胰腺癌:M2极化 + 基质互作 + 化疗耐药
No.6
小结
这篇文章是高端生信的经典模板:单细胞发现→空转验证→转录因子锁定→体外体内功能→通讯机制。
全公共数据+国自然热点,12+名副其实,非常适合作为国自然前期基础!


 夜雨聆风
夜雨聆风