
当人工智能不断深入生命科学与医学研究,医学正在从以观察和验证为主,走向以建模、预测和闭环优化为特征的新阶段。本期合集聚焦上海交通大学附属新华医院/上海大学转化医学研究院苏佳灿教授团队提出AI虚拟生命三重奏。AI虚拟类器官(AIVOs) 从类器官出发,提出面向组织层级的数字孪生框架,试图将实体类器官扩展为可计算、可更新、可交互的虚拟系统;AI虚拟细胞外囊泡(AIVEVs) 将这一思路延伸至细胞间通信层级,希望把细胞外囊泡的生成、载货和通信过程纳入可解释、可预测的数字模型;Virtual Medicine 则从更宏观的视角,系统勾勒出人工智能赋能诊断、治疗、健康管理与临床决策的整体图景。三篇文章层层递进,呈现出一条从虚拟组织模型、到虚拟通信载体、再到虚拟医疗生态的清晰脉络。
AI虚拟类器官:推动类器官研究迈向可计算时代

从湿实验到硅基计算:什么是 AIVOs
类器官为发育生物学、疾病建模和药物筛选提供了重要的体外研究平台,但其发展仍受到批次差异、纵向读数稀疏和难以规模化等问题的制约。基于此,AIVOs 被提出为一种存在于计算空间中的类器官尺度数字孪生体,也被称为 silicon organoids。它以虚拟细胞为基本单元,通过融合多模态和纵向测量数据,并结合受生物物理先验约束的虚拟仪器与混合机制模块,对类器官的组成、状态变化和扰动响应进行计算化重建。
这意味着,AIVOs 并不是现实类器官的简单数字拷贝,也不是静态数据库,而是一个能够持续更新、进行虚拟实验并与实体系统形成反馈闭环的数字孪生系统。真实类器官和患者相关的组学、成像与功能数据可以不断校准模型,模型则反过来指导后续实验设计和干预选择,从而推动类器官研究从实验驱动走向数据—模型—预测协同驱动。
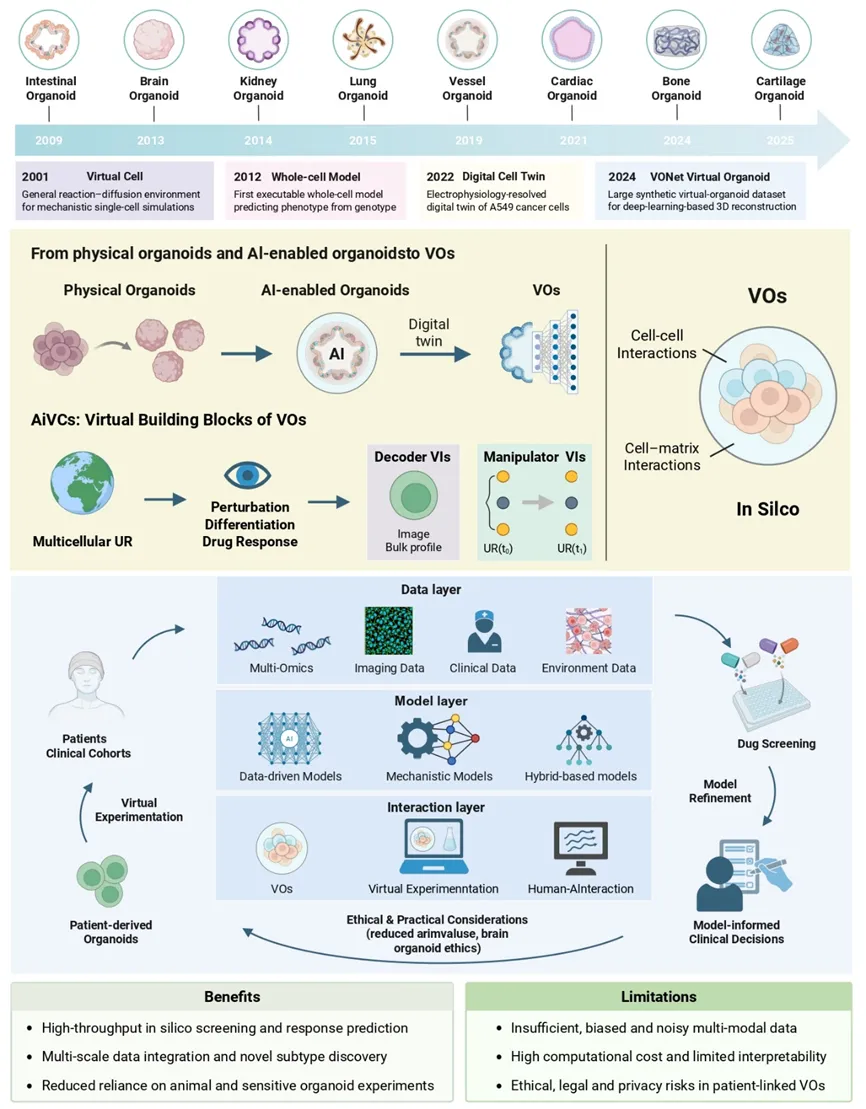
图1:虚拟类器官:演变、构建与生物医学应用
2.构建逻辑:数据-模型-交互的三位一体
构建一个逼真的虚拟类器官,绝非简单的图像渲染。作者提出了一套严密的架构,即“数据-模型-交互”闭环:AIVOs 的核心并非单纯的图像重建,而是一套由数据层、模型层和交互层组成的整体架构。数据层负责整合多组学、单细胞与空间组学、高内涵显微成像、活细胞成像以及患者临床与微环境信息;模型层结合数据驱动方法与机制模型,对细胞行为、细胞—基质互作以及营养、药物和力学环境进行跨尺度建模;交互层则连接虚拟类器官与实体类器官,使模型更新、虚拟扰动和实验反馈能够形成闭环。
文章特别强调,AIVOs 的价值不只是做预测,更在于通过持续的数据输入和模型修正,实现对类器官状态的动态表征,并为药物筛选、疾病分型、耐药分析和临床决策支持提供计算基础。
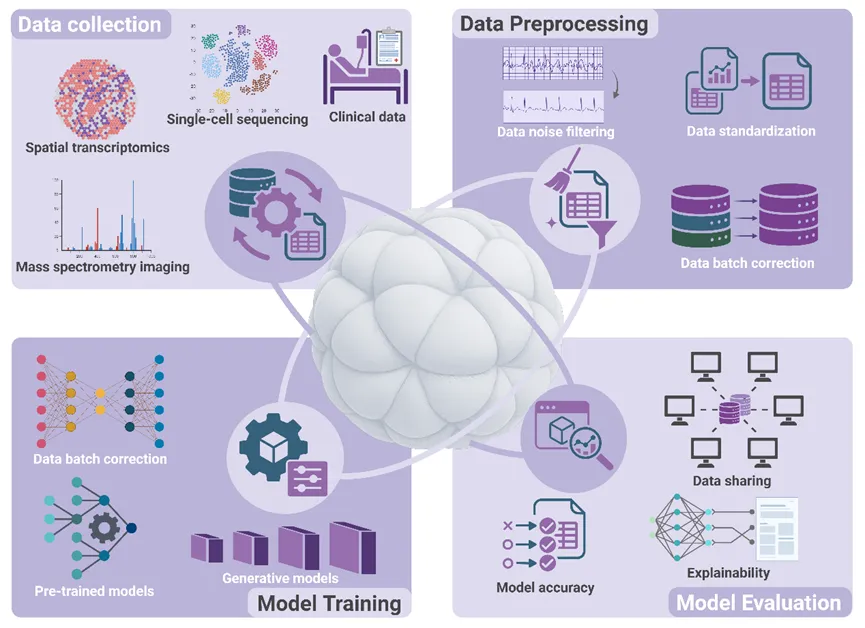
图2:虚拟类器官的构建架构
AI虚拟细胞外囊泡:把细胞通信带入数字建模

1.为什么要做AIVEVs,什么是AIVEVs
如果说 AIVOs 关注的是组织和类器官层面的数字孪生,那么 AIVEVs 则将这一思路进一步推进到细胞间通信层级。细胞外囊泡是细胞释放的纳米级膜性结构,携带蛋白、核酸和脂质等多种生物活性分子,在细胞通信、疾病诊断和药物递送中具有重要意义。与此同时,EVs 研究也长期面临来源异质性强、载货分选机制复杂、实验成本较高以及关键过程难以动态追踪等问题。
基于这一背景,文章提出了 AIVEVs,即 AI 虚拟细胞外囊泡。其核心目标是将 EVs 的生物发生、载货分选和细胞间通信过程纳入数字模型,通过整合多组学数据和生物学机制,对潜在治疗性 EVs、细胞通信行为以及疾病相关诊断标志物进行预测和分析。文章同时指出,AIVEVs 并不是为了替代真实实验,而是希望形成从 in silico prediction 到实验验证的闭环流程,从而提高研究效率并推动临床转化。
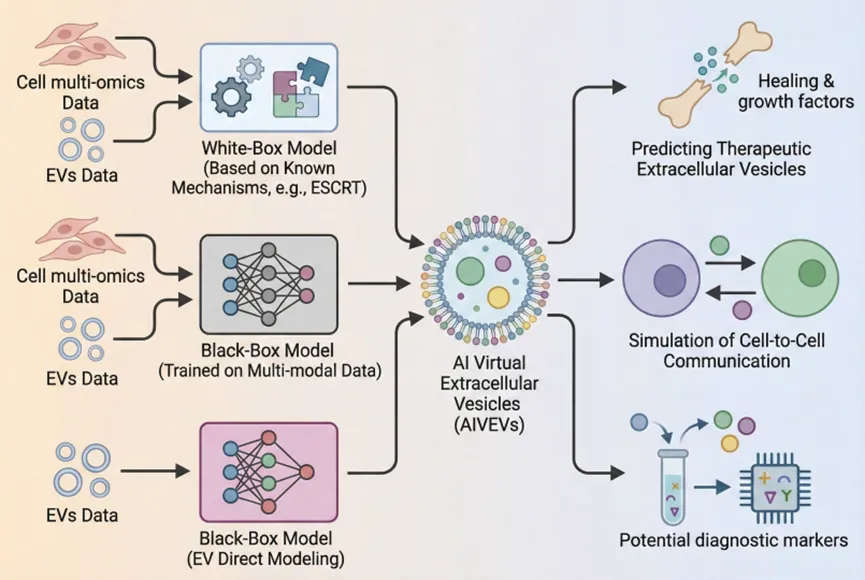
图3:AIVEVs 的生成与应用
2.AIVEVs 怎么做:白盒、黑盒与闭环验证
在建模路径上,AIVEVs 提出了知识驱动的白盒模型与数据驱动的黑盒模型并行的双轨范式。白盒模型以已知机制为基础,例如 ESCRT 相关过程和分子互作网络,更强调机制约束和可解释性;黑盒模型则直接利用细胞与 EVs 的多组学数据进行学习,更适合处理高维复杂数据中的潜在规律。两类模型共同指向对 EVs 生物发生、载货分选和通信行为的模拟。
文章进一步强调,AIVEVs 的发展方向并不是在白盒与黑盒之间二选一,而是走向知识与数据融合的混合建模框架,在提高预测能力的同时保留必要的可解释性,并通过实验反馈不断修正模型。
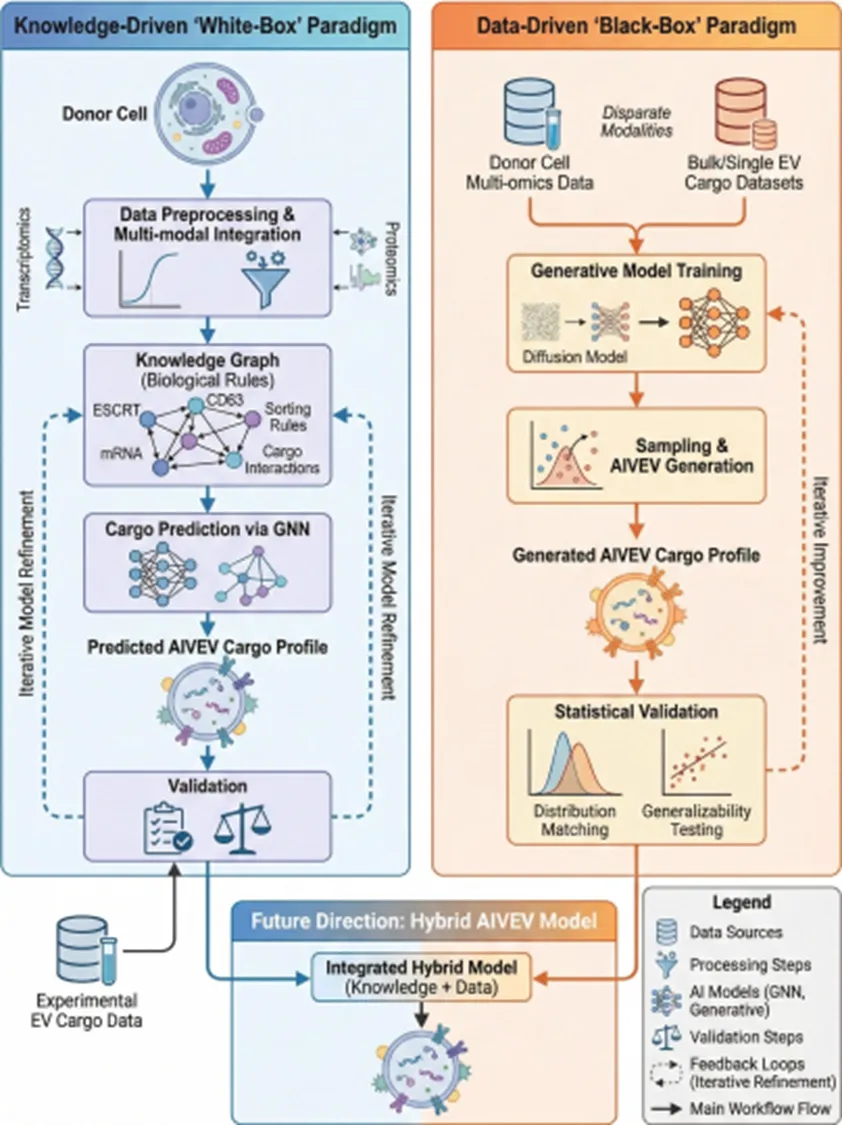
图4:知识驱动与数据驱动的双轨并行
Virtual Medicine:从单点 AI 应用走向医疗全流程重构

1.什么是Virtual Medicine?
与 AIVOs 和 AIVEVs 聚焦具体生命系统不同,Virtual Medicine 从更宏观的层面提出了一个新概念:它被定义为一种由 AI 赋能、突破物理限制的综合性医疗实践生态。文章指出,医学的发展已从经验医学、循证医学走到精准医学,而在数据碎片化、医疗资源不均和多组学整合复杂度不断增加的背景下,虚拟医学正在成为新的发展方向。
Virtual Medicine 并不是单指某一种模型或工具,而是系统总结了医疗 AI 在电子病历分析、医学影像、多模态诊断、药物发现、精准肿瘤学、智能外科、临床决策支持、健康管理和公共卫生中的应用,同时特别强调了大语言模型和多模态 AI 在虚拟医疗交互、临床推理和文书处理中的潜力。
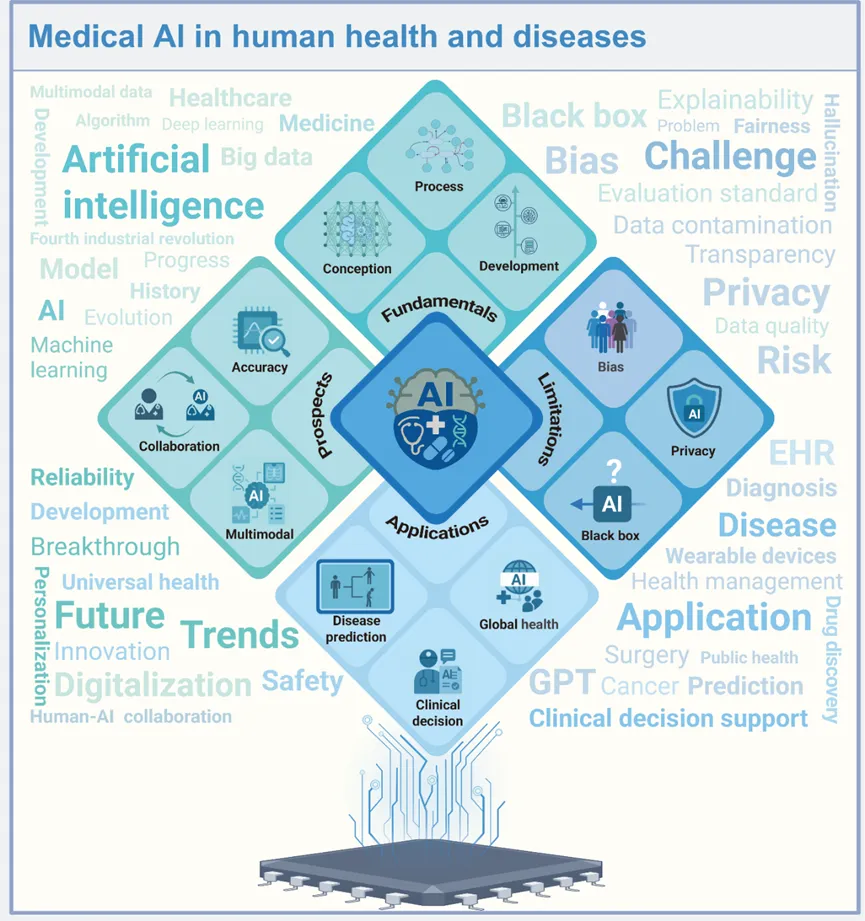
图5:医疗AI在人类健康与疾病中的全景图
2.Virtual Medicine应用图景
文章指出,Virtual Medicine 覆盖的是医疗全流程,而不是单一场景。它既包括基于 EHR 的疾病预测、医学影像辅助诊断和多模态诊断,也包括 AI 赋能的药物发现、临床治疗、智能外科、健康管理、公共卫生监测和资源受限环境下的医疗服务。换言之,Virtual Medicine 更像是一个上位概念,用来整合不同层面的医疗 AI 能力,并推动诊断、治疗和健康管理向更加智能、精准和可及的方向发展。
同时,文章也没有回避现实挑战。模型透明性不足、数据偏倚、公平性、患者隐私和标准化评价体系,仍是虚拟医学真正走向可信应用必须面对的问题。
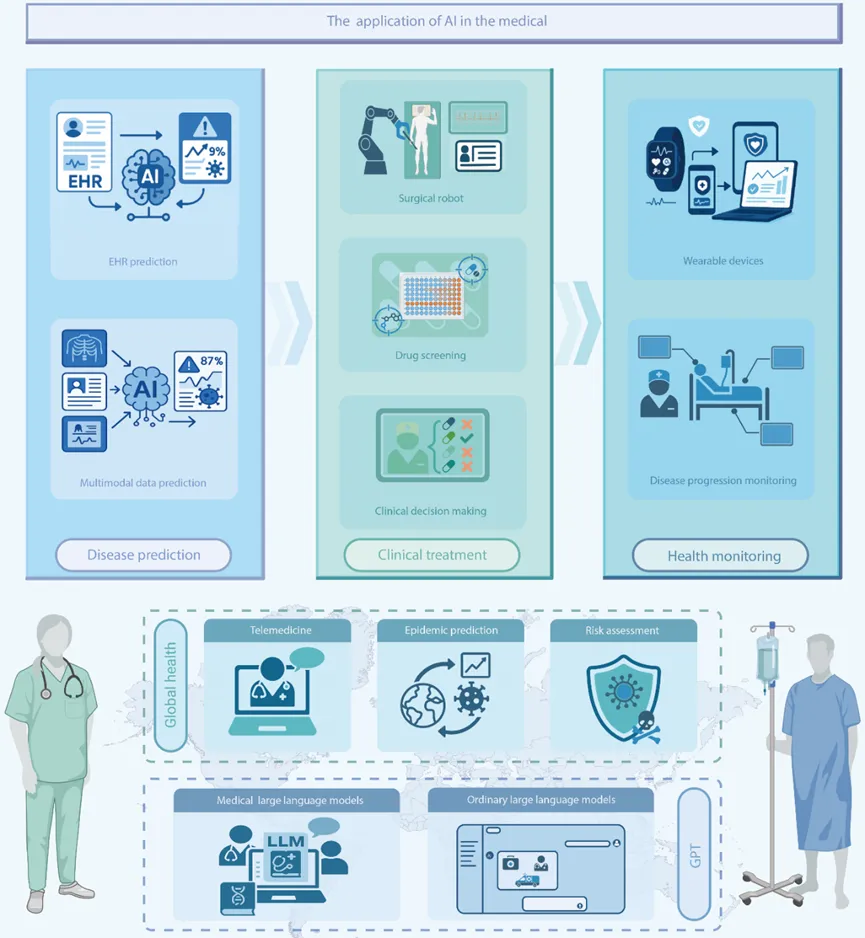
图6:Virtual Medicine在不同场景下的应用
总结与展望
从 AIVOs 到 AIVEVs,再到 Virtual Medicine,这三篇工作共同指向一种正在形成的新范式:让多模态数据、生命机制、实验系统与人工智能模型深度耦合,使医学研究从经验驱动逐步走向模型驱动,从单点验证逐步走向持续迭代。虚拟类器官为复杂组织建模提供了中观载体,虚拟囊泡为细胞通信与精准递送提供了新的计算入口,而虚拟医学则进一步把这种能力扩展到临床全流程。随着高质量数据积累、模型可解释性提升和验证体系不断完善,未来医学将更可计算、更可预测,也更接近真正意义上的精准化与智能化。
文章链接:
https://doi.org/10.1016/j.bioactmat.2025.12.030
https://doi.org/10.1016/j.bioactmat.2025.12.050
https://doi.org/10.1016/j.mmr.2026.100012
 夜雨聆风
夜雨聆风