文档内容
专练 36 新型化学电源
授课提示:对应学生用书71页
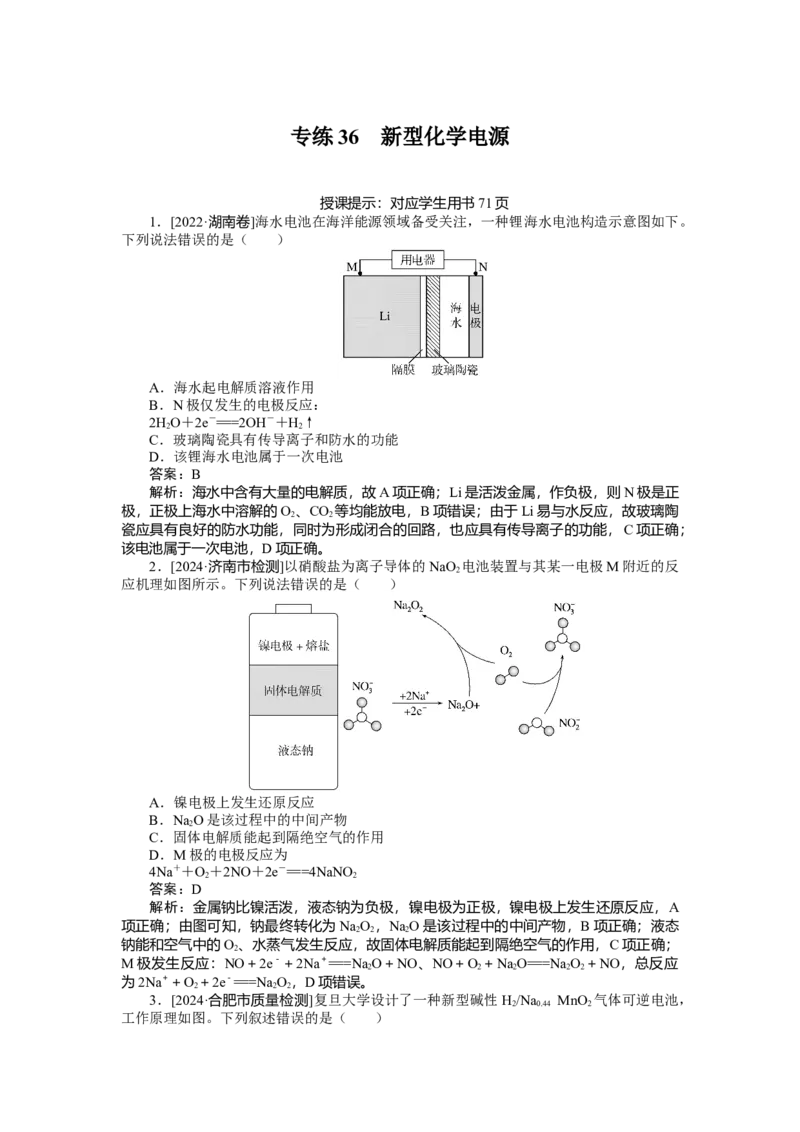
1.[2022·湖南卷]海水电池在海洋能源领域备受关注,一种锂海水电池构造示意图如下。
下列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
2HO+2e-===2OH-+H↑
2 2
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂海水电池属于一次电池
答案:B
解析:海水中含有大量的电解质,故A项正确;Li是活泼金属,作负极,则N极是正
极,正极上海水中溶解的O 、CO 等均能放电,B项错误;由于Li易与水反应,故玻璃陶
2 2
瓷应具有良好的防水功能,同时为形成闭合的回路,也应具有传导离子的功能,C项正确;
该电池属于一次电池,D项正确。
2.[2024·济南市检测]以硝酸盐为离子导体的NaO 电池装置与其某一电极M附近的反
2
应机理如图所示。下列说法错误的是( )
A.镍电极上发生还原反应
B.NaO是该过程中的中间产物
2
C.固体电解质能起到隔绝空气的作用
D.M极的电极反应为
4Na++O+2NO+2e-===4NaNO
2 2
答案:D
解析:金属钠比镍活泼,液态钠为负极,镍电极为正极,镍电极上发生还原反应,A
项正确;由图可知,钠最终转化为NaO ,NaO是该过程中的中间产物,B项正确;液态
2 2 2
钠能和空气中的O 、水蒸气发生反应,故固体电解质能起到隔绝空气的作用,C项正确;
2
M极发生反应:NO+2e-+2Na+===Na O+NO、NO+O +NaO===Na O +NO,总反应
2 2 2 2 2
为2Na++O+2e-===Na O,D项错误。
2 2 2
3.[2024·合肥市质量检测]复旦大学设计了一种新型碱性H/Na MnO 气体可逆电池,
2 0.44 2
工作原理如图。下列叙述错误的是( )A.放电时N为电池正极
B.放电时负极反应:H-2e-+2OH-===2H O
2 2
C.充电时Na+由N极向M极移动
D.充电时阳极反应:Na MnO +(x+y)Na+-(x+y)e-===Na MnO
0.44-x 2 0.44+y 2
答案:D
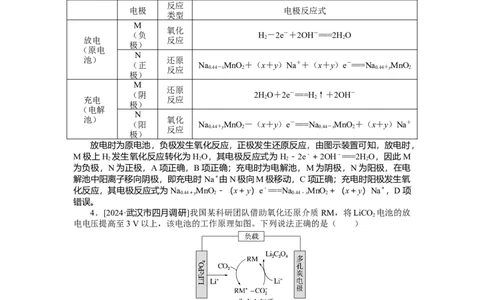
解析:电池分析
反应
电极 电极反应式
类型
M
氧化
(负 H-2e-+2OH-===2H O
放电 反应 2 2
极)
(原电
N
池) 还原
(正 Na MnO +(x+y)Na++(x+y)e-===Na MnO
反应 0.44-x 2 0.44+y 2
极)
M
还原
(阴 2HO+2e-===H ↑+2OH-
充电 反应 2 2
极)
(电解
N
池) 氧化
(阳 Na MnO -(x+y)e-===Na MnO +(x+y)Na+
反应 0.44+y 2 0.44-x 2
极)
放电时为原电池,负极发生氧化反应,正极发生还原反应,由图示装置可知,放电时,
M极上H 发生氧化反应转化为HO,其电极反应式为H -2e-+2OH-===2H O,因此M
2 2 2 2
为负极,N为正极,A项正确,B项正确;充电时为电解池,M为阴极,N为阳极,在电
解池中阳离子移向阴极,即充电时Na+由N极向M极移动,C项正确;充电时阳极发生氧
化反应,其电极反应式为Na MnO -(x+y)e-===Na MnO +(x+y)Na+,D项
0.44+y 2 0.44-x 2
错误。
4.[2024·武汉市四月调研]我国某科研团队借助氧化还原介质RM,将LiCO 电池的放
2
电电压提高至3 V以上,该电池的工作原理如图。下列说法正确的是( )
A.LiFePO 电极的电势比多孔炭电极的高
4
B.负极反应:
LiFePO -xe-===Li FePO +xLi+
4 1-x 4
C.RM和RM+-CO均为该电池反应的催化剂
D.LiFePO 电极每减重7 g,就有22 g CO 被固定
4 2
答案:B
解析:由图中Li+移动方向可知,LiFePO 电极为负极,则LiFePO 电极的电势比多孔
4 4
炭电极的低,A项错误;由图中的物质转化关系可知负极反应为 LiFePO -xe-===Li
4 1-
FePO +xLi+,B项正确;RM是该电池反应的催化剂,RM+-CO为中间产物,C项错误;
x 4
由CO +RM―→RM+-CO、2RM+-CO+2Li++2e-===2RM+LiC O 知,2 mol Li+参与
2 2 2 4
反应,固定2 mol CO ,则负极减重7 g,有44 g CO 被固定,D项错误。
2 25.[2024·广州市综合测试]一种简单钒液流电池的结构及工作原理示意图如图所示,下
列说法不正确的是( )
A.放电时,H+从N极区向M极区移动
B.充电时,电极M是阳极
C.每消耗1 mol VO,有2 mol H+通过质子交换膜
D.充电时的总反应:VO2++HO+V3+===VO+2H++V2+
2
答案:C
解析:根据放电时M极上VO转化为VO2+,发生还原反应,知M极为正极,N电极
上V2+转化为V3+,发生氧化反应,则N极为负极,放电时H+从负极N极区向正极M极
区移动,A项正确;放电时M极为正极,则充电时M极为阳极,B项正确;根据正极反应:
VO+e-+2H+===VO2++HO知,每消耗1 mol VO,转移1 mol电子,有1 mol H+通过质
2
子交换膜,C项错误;充电和放电互为逆过程,放电时的总反应为 VO+2H++V2+===VO2
++V3++HO,则充电时的总反应为VO2++V3++HO===VO+2H++V2+,D项正确。
2 2
6.MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料
为H ,电解质为熔融的KCO 。已知该电池的总反应为2H +O===2H O,下列有关该电
2 2 3 2 2 2
池的说法正确的是( )
A.该电池的正极反应式为
4OH-+4e-===O ↑+2HO
2 2
B.该电池的负极反应式为H-2e-===2H+
2
C.放电时OH-向负极移动
D.当生成1 mol H O时,转移2 mol电子
2
答案:D
解析:该燃料电池的燃料为 H ,电解质为熔融的 KCO ,总反应为 2H +
2 2 3 2
O===2H O,负极反应式为2H +2CO-4e-===2H O+2CO ,正极反应式为O +2CO +4e
2 2 2 2 2 2 2
-===2CO,故A、B均错误;电解质中移动的阴离子为 CO,不是OH-,故C错误;根据
负极反应式知,生成1 mol H O时转移2 mol电子,故D正确。
2
7.我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。
图中贮液器可储存电解质溶液,提高电池的容量。
下列叙述不正确的是( )
A.放电时,a电极反应为IBr-+2e-===2I-+Br-
2
B.放电时,溶液中离子的数目增大
C.充电时,b电极每增重0.65 g,溶液中有0.02 mol I-被氧化
D.充电时,a电极接外电源负极
答案:D
解析:本题涉及原电池正负极的判断、电极反应式的书写等知识,通过工作原理示意图的分析,考查学生接受、吸收、整合化学信息的能力。新型高能电池的原理应用体现了
科学探究与创新意识的学科核心素养。
由工作原理示意图中Zn2+迁移的方向可判断放电时a为正极,b为负极。放电时,a极
得到电子,发生还原反应,使溶液中离子数目增大,A、B项正确;充电时,a极接外接电
源的正极,D项错误;充电时,b极为阴极,电极反应式为Zn2++2e-===Zn,每增重0.65
g,转移0.02 mol电子,a极为阳极,电极反应式为2I-+Br--2e-===I Br-,转移0.02 mol
2
电子,有0.02 mol I-被氧化,C项正确。
8.[2024·江苏扬州中学月考]如图是一种电解质溶液可以循环流动的新型电池。下列说
法正确的是( )
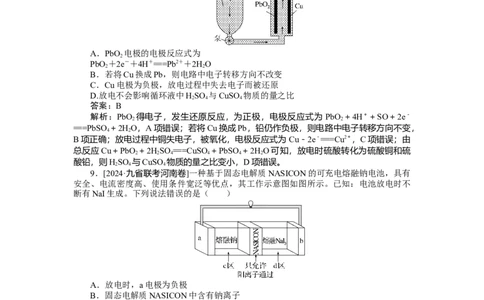
A.PbO 电极的电极反应式为
2
PbO +2e-+4H+===Pb2++2HO
2 2
B.若将Cu换成Pb,则电路中电子转移方向不改变
C.Cu电极为负极,放电过程中失去电子而被还原
D.放电不会影响循环液中HSO 与CuSO 物质的量之比
2 4 4
答案:B
解析:PbO 得电子,发生还原反应,为正极,电极反应式为 PbO +4H++SO+2e-
2 2
===PbSO +2HO,A项错误;若将Cu换成Pb,铅仍作负极,则电路中电子转移方向不变,
4 2
B项正确;放电过程中铜失电子,被氧化,电极反应式为 Cu-2e-===Cu2+,C项错误;由
总反应Cu+PbO +2HSO ===CuSO +PbSO +2HO可知,放电时硫酸转化为硫酸铜和硫
2 2 4 4 4 2
酸铅,则HSO 与CuSO 物质的量之比变小,D项错误。
2 4 4
9.[2024·九省联考河南卷]一种基于固态电解质NASICON的可充电熔融钠电池,具有
安全、电流密度高、使用条件宽泛等优点,其工作示意图如图所示。已知:电池放电时不
断有NaI生成。下列说法错误的是( )
A.放电时,a电极为负极
B.固态电解质NASICON中含有钠离子
C.充电时,阳极的电极反应式为3I--2e-===I
D.放电时,转移1 mol电子时,c区和d区的质量差改变23 g
答案:D
解析:题干情境中指出“电池放电时不断有NaI生成”,再分析电池工作原理图情境:10.[2024·河北石家庄二中月考]科学家发明了一种Al-PbO 电池,电解质溶液中溶质
2
为KSO 、HSO 、KOH,通过x和y两种离子交换膜将电解质溶液隔开,形成 M、R、N
2 4 2 4
三个电解质溶液区域(a>b),结构示意图如图所示。下列说法正确的是( )
A.K+通过x膜移向M区
B.R区域的电解质浓度逐渐减小
C.放电时,Al电极发生的反应为
Al-3e-+4OH-===[Al(OH)]-
4
D.消耗1.8 g Al时N区电解质溶液质量减少18.0 g
答案:C
解析:由图可知,原电池工作时,Al电极为负极,被氧化生成[Al(OH) ]-,PbO 电
4 2
极为正极,发生还原反应,电解质溶液中溶质M为KOH,R为KSO ,N为HSO 。M区
2 4 2 4
为负极区,阳离子流向正极区,故K+通过x膜移向R区,A项错误;钾离子通过x膜向R
区移动,SO通过y膜向R区移动,R区域的电解质浓度逐渐增大,B项错误;原电池工作
时,Al作负极,负极反应为Al-3e-+4OH-===[Al(OH)]-,C项正确;消耗1.8 g Al时
4
电路中转移的电子物质的量为×3=0.2 mol,则N区有0.1 mol SO经过y进入R区,根据负
极反应式 PbO +SO+2e-+4H+===PbSO +2HO,消耗0.1 mol SO,同时流出 0.1 mol
2 4 2
SO,故相当于N区消耗了0.2 mol H SO 同时生成了0.2 mol H O,N区电解质溶液质量减
2 4 2
少了0.2 mol×98 g·mol-1-0.2 mol×18 g·mol-1=16.0 g,D项错误。
11.[2023·全国乙卷]室温钠硫电池被认为是一种成本低、比能量高的能源存储系统。
一种室温钠硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂
有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S +e-―→S,S
8
+e-―→S,2Na++S+2(1-)e-―→NaS
2 x下列叙述错误的是( )
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S+2e-―→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
答案:A
解析:由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。
充电时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至
钠电极,A错误;放电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉
在b电极上得电子与a电极释放出的Na+结合得到NaS,电子在外电路的流向为a→b,B
2 x
正确;将题给的一系列方程式依次标号为①②③,由×①+×②+③可以得到放电时正极的
反应式为2Na++S +2e-―→NaS,C正确;炭化纤维素纸中含有大量的炭,炭具有良好
8 2 x
的导电性,可以增强硫电极的导电性能,D正确;故答案选A。