文档内容
专练 43 弱电解质的电离平衡
授课提示:对应学生用书85页
一、选择题
1.[2024·广东深圳模拟]下列说法正确的是( )
A.醋酸溶液的浓度增大,醋酸的电离程度随之增大
B.0.1 mol·L-1的CHCOOH溶液,升高温度,CHCOOH的电离程度增大
3 3
C.常温下,在0.1 mol·L-1的醋酸溶液中,水电离出的H+浓度为10-13 mol·L-1
D.盐酸中的c(H+)比醋酸溶液中的c(H+)大
答案:B
解析:醋酸溶液的浓度越小,醋酸的电离程度越大,A项错误;弱电解质的电离为吸
热过程,所以0.1 mol·L-1的CHCOOH溶液,升高温度,电离平衡正向移动,CHCOOH
3 3
的电离程度增大,B项正确;醋酸为弱电解质,在水溶液中部分电离,所以在 0.1 mol·L-1
的醋酸溶液中,H+溶液小于10-1 mol·L-1,则常温下,由水电离出的H+浓度应大于10-13
mol·L-1,C项错误;盐酸和醋酸溶液的浓度未知,不能比较盐酸、醋酸溶液中的c(H+)大
小,D项错误。
2.[2024·浙江十校联盟月考]下列说法正确的是( )
A.为确定某酸HA是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则HA是弱
2 2
酸;若pH<7,则HA是强酸
2
B.常温下,pH=3的醋酸溶液中加入少量醋酸钠固体,溶液pH增大,醋酸的电离程
度增大
C.25 ℃时,将0.1 mol·L-1的HA溶液加水稀释至pH=3.0,所得溶液中的c(OH-)=
1×10-11 mol·L-1
D.用同浓度的NaOH溶液分别与等体积等pH的盐酸和醋酸溶液恰好完全反应,盐酸
消耗的NaOH溶液体积多
答案:C
解析:若NaHA溶液的pH<7,HA也可能是弱酸,如亚硫酸氢钠溶液呈酸性,但亚
2
硫酸是弱酸,A项错误;常温下,pH=3的醋酸溶液中加入少量醋酸钠固体,醋酸根离子
浓度增大,抑制醋酸电离,溶液pH增大,醋酸的电离程度减小,B项错误;25 ℃时,将
0.1 mol·L-1的HA溶液加水稀释至pH=3.0,所得溶液中氢离子浓度是0.001 mol·L-1,则溶
液中c(OH-)= mol·L-1=1×10-11 mol·L-1,C项正确;醋酸是弱酸,要得到等体积等pH
的盐酸和醋酸溶液,所使用醋酸的物质的量大于 HCl的物质的量,则用同浓度的NaOH溶
液分别与等体积等pH的盐酸和酸酸溶液恰好完全反应,醋酸溶液消耗的 NaOH溶液体积
多,D项错误。
3.[2024·哈尔滨师大青冈实验中学月考]下列无法证明某酸HA是弱酸的实验方案是(
)
A.室温下,测得0.1 mol·L-1HA溶液的pH>1,证明HA是弱酸
B.碳酸钠溶液中滴入0.1 mol·L-1的HA溶液,产生大量无色气体
C.室温下测得某HA溶液的pH=a,用蒸馏水稀释100倍测得溶液pH=b,且b-a<
2
D.室温下,用pH试纸测得0.1 mol·L-1 NaA溶液的pH>7答案:B
解析:室温下测得0.1 mol·L-1 HA溶液的pH>1,证明HA在溶液中部分电离出氢离子,
则说明HA是弱酸,A不选;碳酸钠溶液中滴入0.1 mol·L-1的HA溶液,产生大量无色气
体,说明HA的酸性大于碳酸,但无法证明HA为强酸还是弱酸,B选;室温下测得某HA
溶液的pH=a,用蒸馏水稀释100倍测得溶液PH=b,且b-a<2,说明稀释过程中HA又
电离出氢离子,则证明HA为弱酸,C不选;室温下,用PH试纸测得0.1 mol·L-1 NaA溶
液的pH>7,说明NaA为强碱弱酸盐,则证明HA为弱酸,D不选。
4.25 ℃时,下列说法正确的是 ( )
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D.100 mL pH= 10.00的NaCO 溶液中水电离出的H+的物质的量为1.0×10-5 mol
2 3
答案:D
解析:NaHA溶液呈酸性,可能是HA-的电离程度大于其水解程度,不能据此得出
HA为强酸的结论,A错误;可溶性正盐BA溶液呈中性,不能推测BA为强酸强碱盐,因
2
为也可能是B+和A-的水解程度相同,即BA也可能是弱酸弱碱盐,B错误;弱酸的浓度
越小,其电离程度越大,因此0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度α >α ,C
1 2
错误;溶液中水电离出的氢离子浓度一定等于水电离出的氢氧根离子浓度,pH=10.00的
NaCO 溶液中水电离出的OH-的物质的量浓度为1.0×10-4 mol·L-1,则水电离出的H+的
2 3
物质的量浓度也是1.0×10-4 mol·L-1,则100 mL pH=10.00的NaCO 溶液中水电离出H+
2 3
的物质的量为1.0×10-4 mol·L-1×100×10-3 L=1.0×10-5 mol,D正确。
5.[2024·石家庄市质量检测]已知:
HClO 苯酚 HCO
2 3
K =4.5×10-7
K=4.0×10-8 K=1.0×10-10 a1
a a K =4.7×10-11
a2
下列实验中,因通入CO 的量不同而产物不同的是( )
2
A.向苯酚钠溶液中通入CO
2
B.向NaClO溶液中通入CO
2
C.向NaCO 溶液中通入CO
2 3 2
D.向Ba(OH) 溶液中通入CO
2 2
答案:D
解析:由题给各物质的电离平衡常数可知,苯酚的酸性弱于碳酸,强于碳酸氢根离子,
故向苯酚钠溶液中通入CO 气体,只能生成苯酚和碳酸氢钠,A项产物与通入CO 的量无
2 2
关;由题给各物质的电离平衡常数可知,次氯酸的酸性比碳酸弱,比碳酸氢根离子强,故
向次氯酸钠溶液中通入CO 气体,只能生成次氯酸和碳酸氢钠,B项产物与通入CO 的量
2 2
无关;向碳酸钠溶液中通入CO 气体,只能生成碳酸氢钠,C项产物与通入CO 的量无关;
2 2
向氢氧化钡溶液中通入少量二氧化碳,生成碳酸钡白色沉淀[Ba(OH) +CO===BaCO ↓+
2 2 3
HO],通入过量二氧化碳,生成碳酸氢钡[Ba(OH) +2CO===Ba(HCO )],D项因通入CO
2 2 2 3 2 2
的量不同而产物不同。
6.[2024·浙江嘉兴高三月考]下列说法不正确的是( )
A.MCl 在水溶液中的电离方程式为:MCl ===M2++2Cl-, M(OH) 可能是弱电解质
2 2 2
B.足量的锌分别与等体积的盐酸(pH=1)和醋酸(0.1 mol·L-1)反应,在相同条件下产
生的氢气体积相同
C.NaHSO 溶液显酸性的原因是HSO的电离强于水解
3
D.pH相同的氨水和氢氧化钠加水稀释相同倍数后,c(NH)=c(Na+)答案:D
解析:MCl 属于盐,在水中完全电离,但M(OH) 可能是强碱,也可能是弱碱,A正
2 2
确;等体积的盐酸(pH=1)和醋酸(0.1 mol·L-1)中H+的物质的量相同,因此加入过量的
Zn,产生氢气的量相同,相同条件下,体积相同,B正确;HSO在水中既有电离也有水解,
NaHSO 溶液显酸性,说明HSO的电离程度大于水解,C正确;NH ·H O为弱碱,NaOH
3 3 2
为强碱,相同pH时,c(NH ·H O)>c(NaOH),加水稀释促进NH ·H O的电离,即稀释相同
3 2 3 2
倍数后,c(NH)>c(Na+),D错误。
7.[2024·哈尔滨师大青冈实验中学月考]常温下,向10 mL b mol·L-1的CHCOOH溶
3
液中滴加等体积的0.01 mol·L-1的NaOH溶液,充分反应后溶液中c(CHCOO-)=c(Na+),
3
下列说法不正确的是( )
A.b>0.01
B.混合后溶液呈中性
C.CHCOOH的电离常数K=
3 a
D.向CHCOOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
3
答案:D
解析:因为CHCOOH为弱酸,NaOH为强碱,反应生成CHCOONa,根据电荷守恒
3 3
可得c(Na+)+c(H+)=c(CHCOO-)+c(OH-),因为c(Na+)=c(CHCOO-),可得c(H+)=
3 3
c(OH-),则混合后溶液呈中性。又因为CHCOONa水解呈碱性,所以CHCOOH应过量,
3 3
使溶液呈中性,所以b>0.01,A、 B正确;反应后溶液呈中性,c(H+)=10-7 mol·L-1,
c(CHCOO-)=c(Na+)=1/2×0.01 mol·L-1=0.005 mol·L-1,c(CHCOOH)=1/2×(b-0.01)
3 3
mol·L-1,所以CHCOOH的电离常数K=,C正确;向CHCOOH溶液中滴加NaOH溶液
3 a 3
的过程中,水的电离程度先增大,CHCOOH完全反应后,再滴加NaOH溶液,水的电离
3
程度减小,D错误。
8.苯甲酸钠(COONa,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑
菌能力显著高于A-。已知25 ℃时,HA的K =6.25×10-5,HCO 的K =4.17×10-7,
a 2 3 a1
K =4.90×10-11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO 气体。
a2 2
下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)( )
A.相比于未充CO 的饮料,碳酸饮料的抑菌能力较低
2
B.提高CO 充气压力,饮料中c(A-)不变
2
C.当pH为5.0时,饮料中=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO)+c(CO)+c(OH-)-c(HA)
答案:C
解析:充CO 的饮料,碳酸电离显酸性,促进A-水解,苯甲酸浓度较大,抑菌能力较
2
高,故A项错误;提高CO 充气压力,溶液中氢离子浓度增大,温度不变,K 不变,因此
2 a
饮料中c(A-)减小,故B项错误;当pH为5.0时,c(H+)=10-5 mol·L-1,根据HA的K
a
=,则有===0.16,故C项正确;根据电荷守恒有:c(H+)+c(Na+)=c(HCO)+2c(CO)+
c(OH-)+c(A-),根据物料守恒有:c(Na+)=c(HA)+c(A-),因此离子浓度关系为:c(H+)
=c(HCO)+2c(CO)+c(OH-)-c(HA),故D项错误。
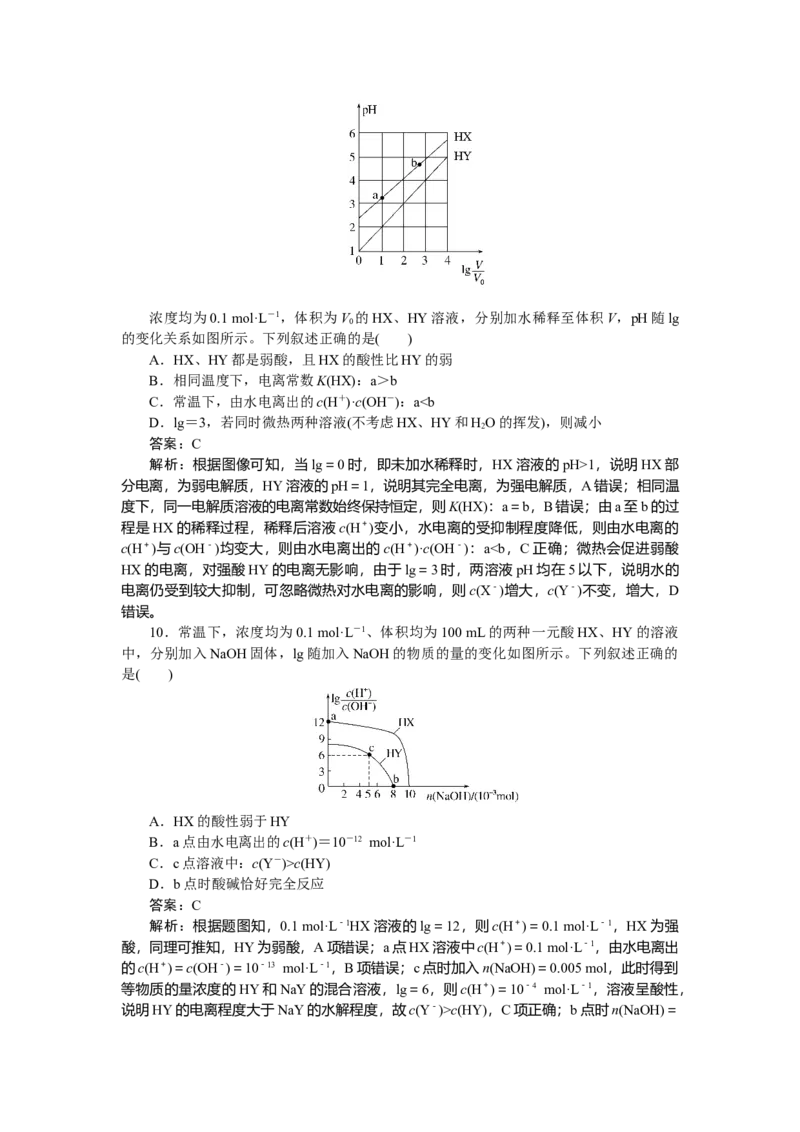
9.浓度均为0.1 mol·L-1,体积为V 的HX、HY溶液,分别加水稀释至体积V,pH随lg
0
的变化关系如图所示。下列叙述正确的是( )
A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.相同温度下,电离常数K(HX):a>b
C.常温下,由水电离出的c(H+)·c(OH-):a1,说明HX部
分电离,为弱电解质,HY溶液的pH=1,说明其完全电离,为强电解质,A错误;相同温
度下,同一电解质溶液的电离常数始终保持恒定,则K(HX):a=b,B错误;由a至b的过
程是HX的稀释过程,稀释后溶液c(H+)变小,水电离的受抑制程度降低,则由水电离的
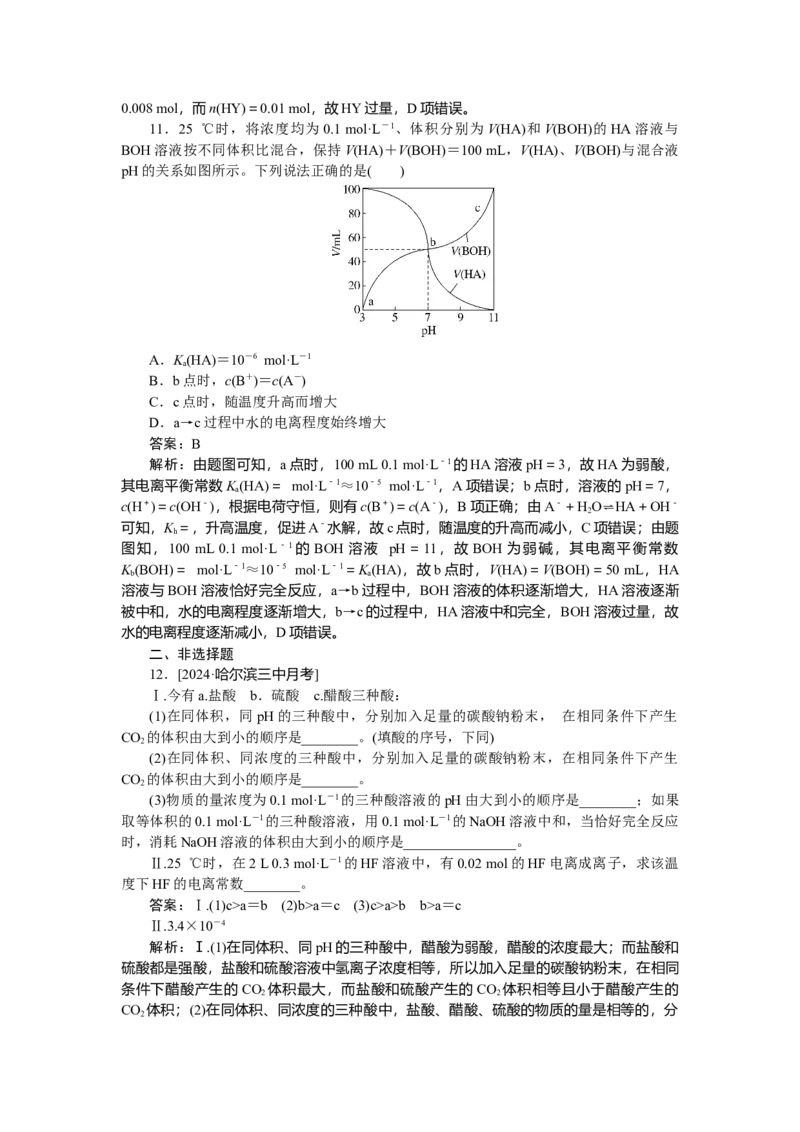
c(H+)与c(OH-)均变大,则由水电离出的c(H+)·c(OH-):ac(HY)
D.b点时酸碱恰好完全反应
答案:C
解析:根据题图知,0.1 mol·L-1HX溶液的lg=12,则c(H+)=0.1 mol·L-1,HX为强
酸,同理可推知,HY为弱酸,A项错误;a点HX溶液中c(H+)=0.1 mol·L-1,由水电离出
的c(H+)=c(OH-)=10-13 mol·L-1,B项错误;c点时加入n(NaOH)=0.005 mol,此时得到
等物质的量浓度的HY和NaY的混合溶液,lg=6,则c(H+)=10-4 mol·L-1,溶液呈酸性,
说明HY的电离程度大于NaY的水解程度,故c(Y-)>c(HY),C项正确;b点时n(NaOH)=0.008 mol,而n(HY)=0.01 mol,故HY过量,D项错误。
11.25 ℃时,将浓度均为0.1 mol·L-1、体积分别为V(HA)和V(BOH)的HA溶液与
BOH溶液按不同体积比混合,保持V(HA)+V(BOH)=100 mL,V(HA)、V(BOH)与混合液
pH的关系如图所示。下列说法正确的是( )
A.K(HA)=10-6 mol·L-1
a
B.b点时,c(B+)=c(A-)
C.c点时,随温度升高而增大
D.a→c过程中水的电离程度始终增大
答案:B
解析:由题图可知,a点时,100 mL 0.1 mol·L-1的HA溶液pH=3,故HA为弱酸,
其电离平衡常数K(HA)= mol·L-1≈10-5 mol·L-1,A项错误;b点时,溶液的pH=7,
a
c(H+)=c(OH-),根据电荷守恒,则有c(B+)=c(A-),B项正确;由A-+H
2
O⇌HA+OH-
可知,K =,升高温度,促进A-水解,故c点时,随温度的升高而减小,C项错误;由题
h
图知,100 mL 0.1 mol·L-1的 BOH 溶液 pH=11,故 BOH 为弱碱,其电离平衡常数
K (BOH)= mol·L-1≈10-5 mol·L-1=K(HA),故b点时,V(HA)=V(BOH)=50 mL,HA
b a
溶液与BOH溶液恰好完全反应,a→b过程中,BOH溶液的体积逐渐增大,HA溶液逐渐
被中和,水的电离程度逐渐增大,b→c的过程中,HA溶液中和完全,BOH溶液过量,故
水的电离程度逐渐减小,D项错误。
二、非选择题
12.[2024·哈尔滨三中月考]
Ⅰ.今有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)在同体积,同pH的三种酸中,分别加入足量的碳酸钠粉末, 在相同条件下产生
CO 的体积由大到小的顺序是________。(填酸的序号,下同)
2
(2)在同体积、同浓度的三种酸中,分别加入足量的碳酸钠粉末,在相同条件下产生
CO 的体积由大到小的顺序是________。
2
(3)物质的量浓度为0.1 mol·L-1的三种酸溶液的pH由大到小的顺序是________;如果
取等体积的0.1 mol·L-1的三种酸溶液,用0.1 mol·L-1的NaOH溶液中和,当恰好完全反应
时,消耗NaOH溶液的体积由大到小的顺序是________________。
Ⅱ.25 ℃时,在2 L 0.3 mol·L-1的HF溶液中,有0.02 mol的HF电离成离子,求该温
度下HF的电离常数________。
答案:Ⅰ.(1)c>a=b (2)b>a=c (3)c>a>b b>a=c
Ⅱ.3.4×10-4
解析:Ⅰ.(1)在同体积、同pH的三种酸中,醋酸为弱酸,醋酸的浓度最大;而盐酸和
硫酸都是强酸,盐酸和硫酸溶液中氢离子浓度相等,所以加入足量的碳酸钠粉末,在相同
条件下醋酸产生的CO 体积最大,而盐酸和硫酸产生的CO 体积相等且小于醋酸产生的
2 2
CO 体积;(2)在同体积、同浓度的三种酸中,盐酸、醋酸、硫酸的物质的量是相等的,分
2别加入足量的碳酸钠粉末,在相同条件下盐酸和醋酸产生CO 的体积一样,但是硫酸是二
2
元酸,加入足量的碳酸钠,在相同条件下产生 CO 的体积是盐酸、醋酸的2倍,所以产生
2
CO 的体积由大到小的顺序是:b>a=c;(3)硫酸是二元强酸,0.1 mol·L-1的硫酸中氢离子
2
浓度是0.2 mol·L-1,盐酸是一元强酸,0.1 mol·L-1的盐酸中氢离子浓度是0.1 mol·L-1,醋
酸是一元弱酸,0.1 mol·L-1的醋酸中氢离子浓度小于0.1 mol·L-1;氢离子浓度越大,则pH
越小,所以三种酸溶液的pH由大到小的顺序是:c>a>b; 等体积的0.1 mol·L-1的三种酸溶
液,硫酸是二元酸,氢离子的量最大,消耗的氢氧化钠最多,醋酸和盐酸都是一元酸,溶
质的物质的量一样,消耗氢氧化钠一样多,所以用0.1 mol·L-1的NaOH溶液分别中和三种
酸,消耗NaOH溶液的体积由大到小的顺序是:b>a=c。
Ⅱ.起始HF的物质的量是2 L×0.3 mol·L-1=0.6 mol;由题意列出下式:
各粒子浓度分别为:c(HF)=0.58/2=0.29 mol·L-1,c(H+)=0.02/2=0.01 mol·L-1,c(F
-)=0.02/2=0.01 mol·L-1,故HF的电离平衡常数为K =c(H+)×c(F-)/c(HF)=(0.01)2/0.29
a
=3.4×10-4。