文档内容
一、选择题
1. 空气的成分中,约占总体积 78% 的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
【答案】A
【解析】
试题分析:空气的成分中,约占总体积 78% 的气体是氮气,故答案选择A
考点:空气成分
2.下列现象中,一定发生化学反应的是( )
A.石蜡熔化 B.酒精挥发 C.木条燃烧 D.水结成冰
【答案】C
考点:物质的变化
3.下列物质中,由分子构成的是( )
A.硫酸铜 B.金刚石 C.水 D.氢氧化钠
【答案】C
【解析】
试题分析:A选项硫酸铜是由粒子构成的;B选项金刚石是由原子构成的;C选项水是由分子构成的;D
选项氢氧化钠是由离子构成的;故答案选择C
考点:物质的构成
4.下列实验操作中,正确的是( )
A.加热试管中的液体 B.用橡胶塞住试管 C.向试管中滴加液体 D.向试管中倾倒液体【答案】B
【解析】
试题分析:A选项试管中的液体加热时,液体的体积不能超过其体积的三分之一;B选项橡胶塞旋转塞入
试管中,是正确的操作;C选项向试管中滴加液体时,胶头滴管要悬空垂直滴加;D选项向试管中倾
倒液体时,瓶塞要倒放与试验台;故答案选择B
考点:基本操作
5.下列说法中, 错误的是( )
A.氢气、石油都是储量丰富的清洁能源 B.滥用化肥、农药会造成水体污染
C.油脂、糖类都是人体所需的营养物质 D.用灼烧法可区分羊毛和合成纤维
【答案】A
【解析】
试题分析:A选项是错误的叙述,氢气是清洁能源,而石油不属于清洁能源;B选项滥用化肥、农药会造
成水体污染,是正确的叙述;C选项油脂、糖类都是人体所需的营养物质,是正确的叙述;D选项用
灼烧法可区分羊毛和合成纤维,是正确的叙述,通过闻气体的气味就可达到目的;故答案选择A
考点:化学与生活、农业
6.某物质在空气中燃烧的化学方程式为 下列说法正确的是( )
A.X 的化学式是C H B.该反应属于置换
2 4
C.O 中氧元素的化合价为-2 D.CO 中碳、氧元素的质量比为 1:2
2 2
【答案】A
考点:质量守恒定律的应用、反应类型、化合价的计算
7.下列对有关事实的解释,错误的是( )
A.酒精需要密封保存 —— 酒精分子在不停运动
B.冰水共存物属于纯净物—— 冰和水都由分子构成
C.过氧化氢分解属于化学变化—— 过氧化氢分子本身发生变化
D.稀盐酸和硫都能使石蕊溶液变红 —— 两种溶液中都存在酸根离子
【答案】D考点:化学推理
8.下列说法中,正确的是( )
A.浓盐酸、硫酸都易挥发 B.CH、C HOH 都能作燃料
4 2 5
C.Al(OH) 、NaOH都能治疗胃酸过多症 D.CO、SO 都是有毒气体
3 2 2
【答案】B
【解析】
试题分析:A选项是错误的叙述,因为硫酸没有挥发性;B选项CH、C HOH 都能作燃料,是正确的叙述;
4 2 5
C选项是错误的叙述,因为氢氧化钠具有强腐蚀性,不能治疗胃酸过多;D选项是错误的叙述,二氧
化碳没有毒性,只是不支持呼吸;故答案选择B
考点:化学总结
9.下列说法中, 错误的是( )
A.加热蒸发食盐水时未用玻璃棒搅拌,会导致局部过液滴飞溅
B.未打磨的铝片放入稀盐酸中,能立即观察到剧烈反应产生大量气泡
C.将 CO 通入澄清石灰水中,未见混浊可能是 CO 中混有 HCl 气体
2 2
D.将红热的木炭缓慢地插入盛有O 的集气瓶中,能够充分利用O,有利于实验现象的观察
2 2
【答案】B
【解析】
试题分析:A.加热蒸发食盐水时未用玻璃棒搅拌,会导致局部过液滴飞溅,是正确的叙述;B选项是错
误的叙述,因为金属铝表面为氧化铝,氧化铝与盐酸反应时不产生气体;C选项将 CO 通入澄清石灰
2
水中,未见混浊可能是 CO 中混有 HCl 气体,是正确的叙述;D选项将红热的木炭缓慢地插入盛有O
2 2
的集气瓶中,能够充分利用O,有利于实验现象的观察,是正确的叙述;故答案选择B
2
考点:化学基础知识
10.下列实验能达到相应目的是( )
A.分离Zn和Cu的固体混合物 :加适量的Cu(NO ) 溶液,过滤
3 2
B.除去CaCl 溶液中少量的HCl :加过量Ca(OH) 固体,过滤
2 2C.验证BaSO 中含有BaCO :取样,加适量稀盐酸有气泡产生
4 3
D.制备Cu(OH) :将CuSO 溶液和适量Ba(OH) 溶液混合,过滤
2 4 2
【答案】C
考点:实验方案评价
二、非选择题(每空 1分,共 40 分)
11. 回答下列问题。
(1)氧元素的符号是 ;(2)3个氢原子可表示为 ;(3)生理盐水中溶剂的化学式为 。
【答案】(1)O;(2)3H;(3)HO。
2
【解析】
试题分析:(1)氧元素的符号是O;(2)3个氢原子可表示为3H;;(3)生理盐水中溶剂的化学式为
HO。
2
考点:化学符号的书写
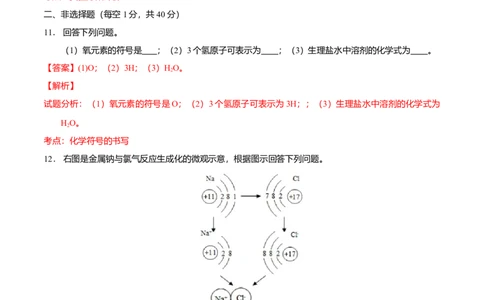
12. 右图是金属钠与氯气反应生成化的微观示意,根据图示回答下列问题。
(1)钠原子的最外层电数为 ;
(2)构成氯化钠的粒子是 ;
(3)由原子核外电层数与元素所在周期表中的相同可知,氯元素在周期表中应排第 周期。
【答案】(1)1;(2)钠离子和氯离子;(3)三。考点:原子的结构、构成物质的微粒
13.回答下列与水有关的问题。
(1)利用 的吸附性去除水中异味;
(2)生活中可通过 方法降低水的硬度;
(3)在电解水实验中, 极产生的气泡能够燃烧。
【答案】(1)活性炭;(2)煮沸;(3)负。
【解析】
试题分析:(1)利用活性炭的吸附性去除水中异味;(2)生活中可通过煮沸方法降低水的硬度;(3)
在电解水实验中,负极产生的气泡能够燃烧
考点:水知识
14. 结合下图所示实验,回答有关问题。
(1)实验一的目是 ;
(2)实验二的结论 :铁生锈是与 共同作用的结果;
(3)实验三,在 B试管加入 (写出一种情况),即可证明温度和固体颗粒大小都是影响冰糖
溶解快慢的因素。
【答案】(1)探究燃烧条件;(2)氧气和水;(3)10mL冷水5g粉末状冰糖。
【解析】
试题分析:1)实验一的目是探究燃烧条件;(2)实验二的结论 :铁生锈是与氧气和水共同作用的结果;
(3)根据探究因素可知实验三,在 B试管加入10mL冷水5g粉末状冰糖。
考点:对比试验
15.回答下列与含碳物质有关的问题。
(1)天然存在的最硬物质是 ;(2)能将CO 和CO 鉴别开的溶液是 ;
2
(3)KCO、NaCO、NaHCO 都能与 (填具体物质)反应,生成CO。
2 3 2 3 3 2
【答案】(1)金刚石;(2)澄清石灰水 ;(3)稀盐酸或稀硫酸。
【解析】
试题分析:(1)天然存在的最硬物质是金刚石;(2)能将CO 和CO 鉴别开的溶液是澄清石灰水;
2
(3)KCO、NaCO、NaHCO 都能与稀盐酸或稀硫酸反应,生成CO。
2 3 2 3 3 2
考点:碳和碳的化合物
16.根据下表数,回答问题。
(1)20℃时KNO 的溶解度是 g;
3
(2)60℃时,200g KNO 溶液中含溶质100g,将该溶液降温至20℃,可析出KNO g;
3 3
(3)NaCl溶液中含有少量KNO,提纯NaCl,采用的方法是 (选填“蒸发结晶”或降温结晶”)。
3
【答案】(1)31.6;(2)68.4g;(3)降温结晶。
考点:溶解度表、结晶方法
17.回答下列与金属有关的问题。
(1)铝合金和纯铝,硬度较大的是 ;
(2)工业上,把赤铁矿冶炼成的主要反应原理是3CO+Fe O 2Fe+3CO ,其中 发生了还原
2 3 2
反应;
(3)比较Mn、Pd (钯)、Cu 三种金属的活动性顺序
①将Mn 片、Pd 片分别加入到稀盐酸中,Mn 片表面有气泡产生,Pd 片没有变化。根据上述实验
现象,得出的结论是 ;
②要确切得出这三种金属的活动性顺序,还需将Pd 片加入到 溶液中,观察现象。
【答案】(1)铝合金;(2)Fe O;(3)①Mn活动性大于Pd;②硫酸铜(或氯化铜、硝酸铜)。
2 3考点:金属的性质、金属活动性顺序的应用
18.回答下列与配制溶液有关的问题。
(1)配置50g 质量分数为10%的NaCl溶液,需NaCl固体 g;
(2)用上述溶液配制50g质量分数为5%的NaCl溶液,量取水时仰视读数则所配溶液中质的量分数
5% (选填“大于”、小于或等于”);
(3)以上两个实验中,均用到的仪器有烧杯、滴管、量筒和 。
【答案】(1)5;(2)小于;(3)玻璃棒。
【解析】
试题分析:(1)配置50g 质量分数为10%的NaCl溶液,需NaCl固体为50g×10%=5g;2)用上述溶液配
制50g质量分数为5%的NaCl溶液,量取水时仰视读数,会造成读数偏小,量取的体积偏大,则所配
溶液中质的量分数偏小;(3)用到的仪器有烧杯、滴管、量筒和玻璃棒。
考点:溶液的配制、误差分析
19.以下是实验室制取气体的常用仪器,回答列问题。
(1)标号为e的仪器名称是 ;
(2)用2KMnO KMnO + MnO + O ↑制取O,并用向上排空气法收集。
4 2 4 2 2 2
①若制取3.2g O,理论上至少需要KMnO g;
2 4
②检验O 收集满的方法是 ;
2
(3)用大理石和稀盐酸反应制取CO,并用排水法收集;
2
①该反应的化学方程式为 ;
②组装制取置时,需选择上图中的a、b、h、i、k、l、m和 。
【答案】(1)试管;(2)31.6;②将带火星木条放在集气瓶口,若木条复燃,则收集满了;(3)①CaCO +2HCl==CaCl +H O+CO↑;②c。
3 2 2 2
考点:实验室制取气体的原理、装置的选择
20.氧化铁是一种重要的工原料,利用废屑(其中杂质不溶于水且与酸发生反应)制备氧化铁的流程如下:
(1)操作Ⅰ、Ⅱ的名称是 ;
(2)向废铁屑中加入的稀硫酸需过量,其目是 ;
(3)高温条件下,FeCO 与通入的O 发生反应的化学方程式是 。
3 2
【答案】(1)过滤;(2)将废铁屑中铁完全反应;(3)4FeCO+O 2Fe O+4CO。
3 2 2 3 2
【解析】
试题分析:(1)因为经过操作Ⅰ、Ⅱ出现固液分离,故的名称是过滤;(2)向废铁屑中加入的稀硫酸需过
量,其目的是将废铁屑中铁完全反应;(3)高温条件下,FeCO 与通入的O 发生反应的化学方程式
3 2
是4FeCO+O 2Fe O+4CO。
3 2 2 3 2
考点:工艺流程
21.下图所示,是为了验证稀硫酸化学性质做的 三个实验,回答下列问题。(1)A实验最终能观察到的现象是 ;
(2)B实验能体现出稀硫酸具有的化学性质是 ;
(3)C实验中发生反应的化学方程式为 ;
(4)将上述实验后所得溶液在烧杯中混合,观察到底部有沉淀层无色溶液,此时利用烧杯中的沉淀
再选择适当试剂即可证明C实验中所加BaCl 溶液过量,实验的操作及现象是 。
2
【答案】(1)溶液呈蓝色;(2)能与活泼金属或金属氧化物反应;(3)HSO +BaCl ==BaSO ↓+2HCl;
2 4 2 4
(4)向无色溶液中加入足量稀硫酸,始终有白色固体剩余
考点:酸的化学性质
22.结合下列所示实验,回答有关问题。
(1)有氨味的气体是 ;
(2)经检验,无色溶液C中含有NaCl,则可推测出 X溶液为 溶液;
(3)进一步测定可知,无色溶液 C的 pH >7,向其中加入适量的NaSO 溶液,无现象,写出色溶液
2 4
C中所含溶质的有可能情况 。
【答案】(1)氨气;(2)氯化钡;(3)氢氧化钠、氯化钠或氢氧化钠、氯化钠、硫酸钠。考点:物质的推断