文档内容
吉林省长春市2018年中考化学真题试题
一、选择题(共10分)考生注意:每小题只有一个选项符合题意;请用 2B铅笔将答题卡上
的相应序号涂黑.
1.(1分)(2018•长春)空气成分中,体积分数最大的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
2.(1分)(2018•长春)下列过程中,一定发生化学变化的是( )
A.水结成冰 B.石蜡融化 C.酒精挥发 D.木炭燃烧
3.(1分)(2018•长春)下列物质中,由离子构成的是( )
A.氧气 B.金刚石 C.氯化钠 D.蒸馏水
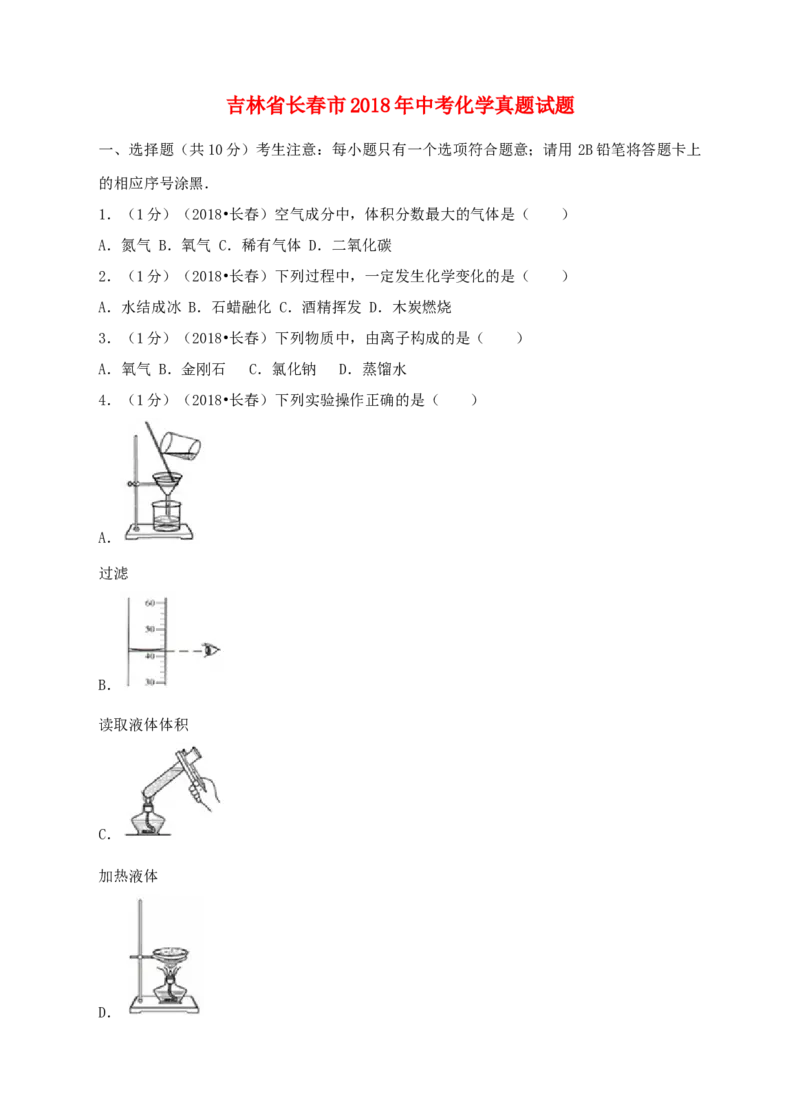
4.(1分)(2018•长春)下列实验操作正确的是( )
A.
过滤
B.
读取液体体积
C.
加热液体
D.蒸发
5.(1分)(2018•长春)下列对有关事实的解释中,错误的是( )
A.花香四溢﹣﹣分子在不断运动
B.HO和HO 的化学性质不同﹣﹣分子构成不同
2 2 2
C.气体可压缩储于钢瓶中﹣﹣分子数目变少
D.水蒸发属于物理变化﹣﹣分子种类没有改变
6.(1分)(2018•长春)有关甲烷(CH)的说法中,正确的是( )
4
A.甲烷分子由碳原子和氢原子构成
B.相对分子质量是16g
C.碳元素和氢元素的质量比是1:4
D.碳元素比氢元素的质量分数小
7.(1分)(2018•长春)化学与生活密切相关,下列说法中,错误的是( )
A.通过燃烧实验可以区分羊毛和合成纤维
B.开发使用新能源汽车可以节能减排
C.食品包装中填充氮气可以延长保质期
D.食用水果、蔬菜可以补充大量蛋白质
8 . ( 1 分 ) ( 2018• 长 春 ) 侯 氏 制 碱 法 的 生 产 过 程 涉 及 如 下 反 应 :
NH+CO+NaCl+X═NaHCO↓+NHCl,2NaHCO NaCO+CO↑+HO.下列说法错误的是(
3 2 3 4 3 2 3 2 2
)
A.X的化学式为HO
2
B.NaHCO 受热易分解
3
C.CO 和NaCO 中碳元素的化合价不同
2 2 3
D.NaHCO 分解产生的CO 可以回收再利用
3 2
9.(1分)(2018•长春)下列说法中,正确的是( )
A.含有氧元素的物质一定是氧化物
B.生成盐和水的反应一定是中和反应
C.与盐酸反应生成气体的物质一定是金属
D.含有铵根离子的氮肥与熟石灰混合研磨一定生成氨气
10.(1分)(2018•长春)下列实验中,能够达到实验目的是( )A.制备Cu(OH) 固体:用CuO与适量NaOH溶液混合
2
B.鉴别稀HSO 和稀盐酸:取样,分别滴加Ba(NO) 溶液
2 4 3 2
C.除去CO中的少量CO 气体:将气体通过灼热的CuO粉末
2
D.分离MnO 和KCl固体混合物:加入足量的水溶解,过滤
2
二、非选择题(共40分)
11.(3分)(2018•长春)回答下列问题。
(1)氧元素的符号为 ;
(2)两个氢离子可用符号表示为 ;
(3)水的化学式为 。
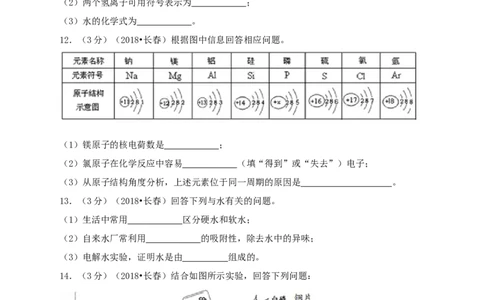
12.(3分)(2018•长春)根据图中信息回答相应问题。
(1)镁原子的核电荷数是 ;
(2)氯原子在化学反应中容易 (填“得到”或“失去”)电子;
(3)从原子结构角度分析,上述元素位于同一周期的原因是 。
13.(3分)(2018•长春)回答下列与水有关的问题。
(1)生活中常用 区分硬水和软水;
(2)自来水厂常利用 的吸附性,除去水中的异味;
(3)电解水实验,证明水是由 组成的。
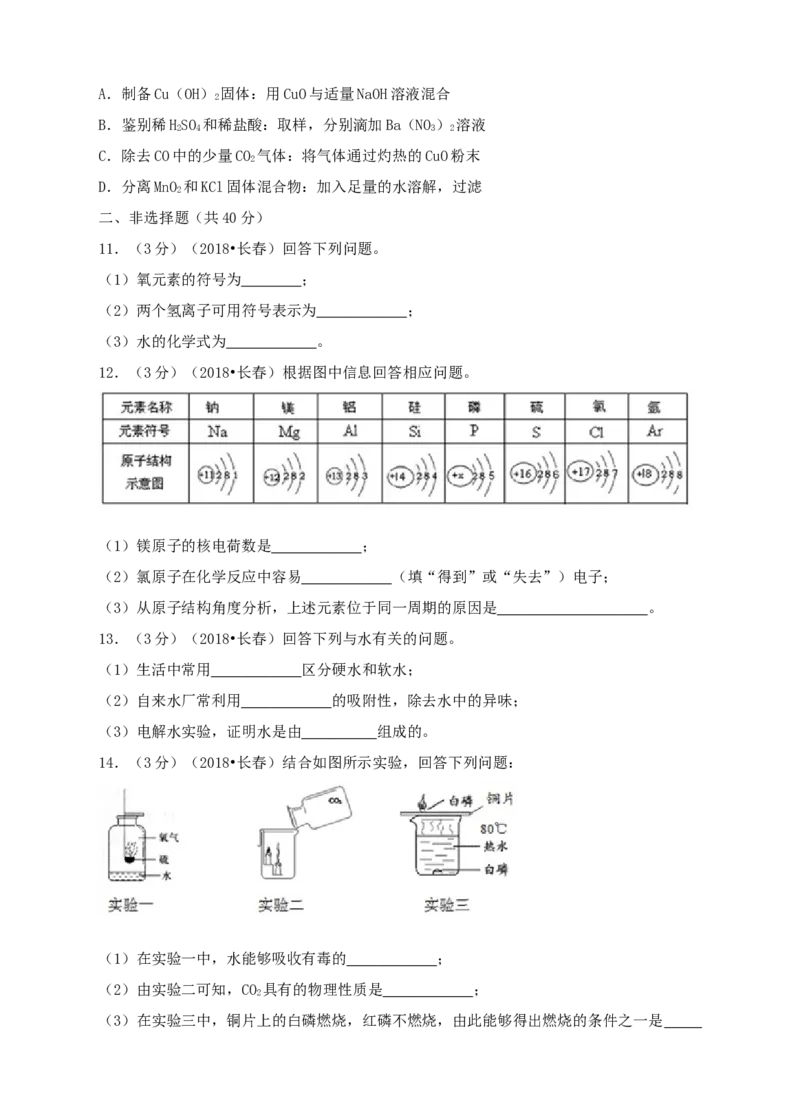
14.(3分)(2018•长春)结合如图所示实验,回答下列问题:
(1)在实验一中,水能够吸收有毒的 ;
(2)由实验二可知,CO 具有的物理性质是 ;
2
(3)在实验三中,铜片上的白磷燃烧,红磷不燃烧,由此能够得出燃烧的条件之一是。
15.(3分)(2018•长春)回答下列与含碳物质有关的问题。
(1)普通干电池采用石墨作为电极材料,是利用其优良的 性;
(2)高炉炼铁的主要反应为3CO+FeO 2Fe+3CO,该反应利用了CO化学性质中
2 3 2
的 性;
(3)碳酸钠、碳酸钙都含有CO2﹣,都能与盐酸反应生成盐、水和 。
3
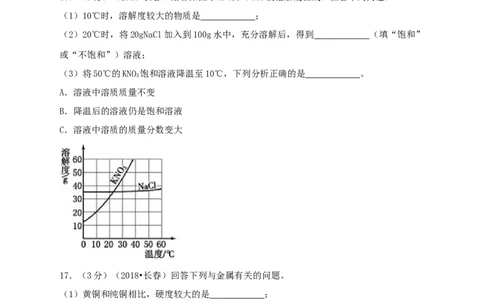
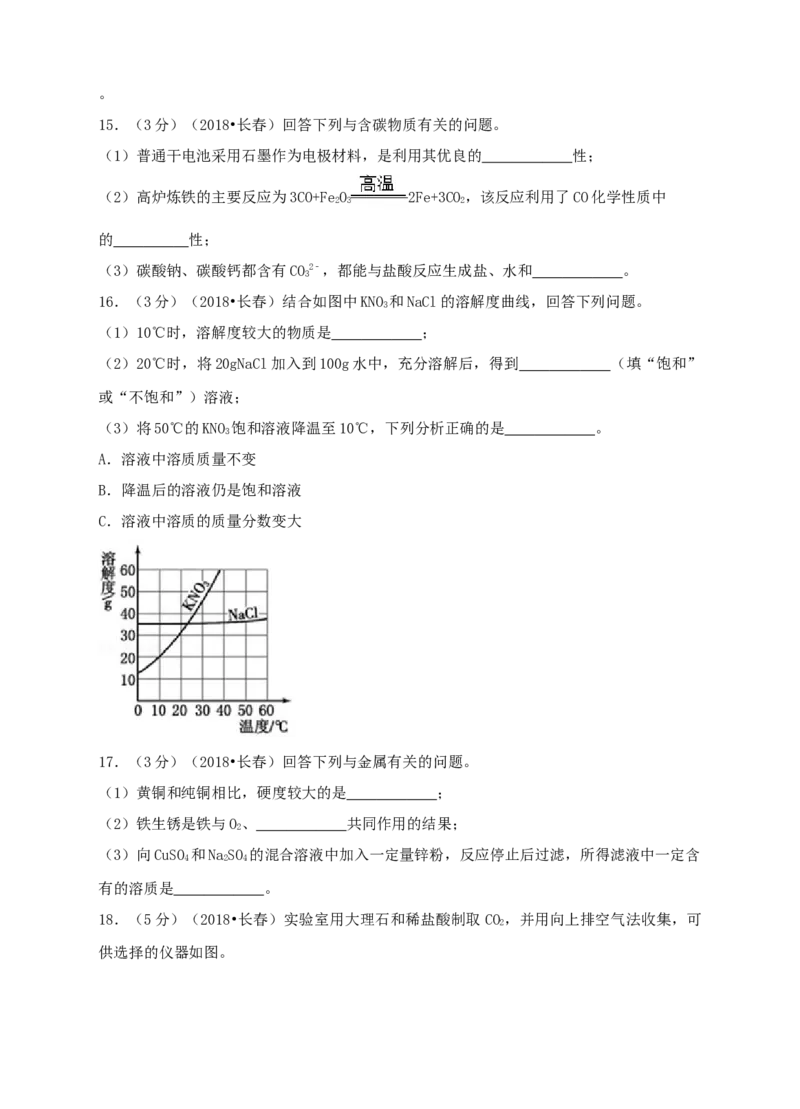
16.(3分)(2018•长春)结合如图中KNO 和NaCl的溶解度曲线,回答下列问题。
3
(1)10℃时,溶解度较大的物质是 ;
(2)20℃时,将20gNaCl加入到100g水中,充分溶解后,得到 (填“饱和”
或“不饱和”)溶液;
(3)将50℃的KNO 饱和溶液降温至10℃,下列分析正确的是 。
3
A.溶液中溶质质量不变
B.降温后的溶液仍是饱和溶液
C.溶液中溶质的质量分数变大
17.(3分)(2018•长春)回答下列与金属有关的问题。
(1)黄铜和纯铜相比,硬度较大的是 ;
(2)铁生锈是铁与O、 共同作用的结果;
2
(3)向CuSO 和NaSO 的混合溶液中加入一定量锌粉,反应停止后过滤,所得滤液中一定含
4 2 4
有的溶质是 。
18.(5分)(2018•长春)实验室用大理石和稀盐酸制取CO ,并用向上排空气法收集,可
2
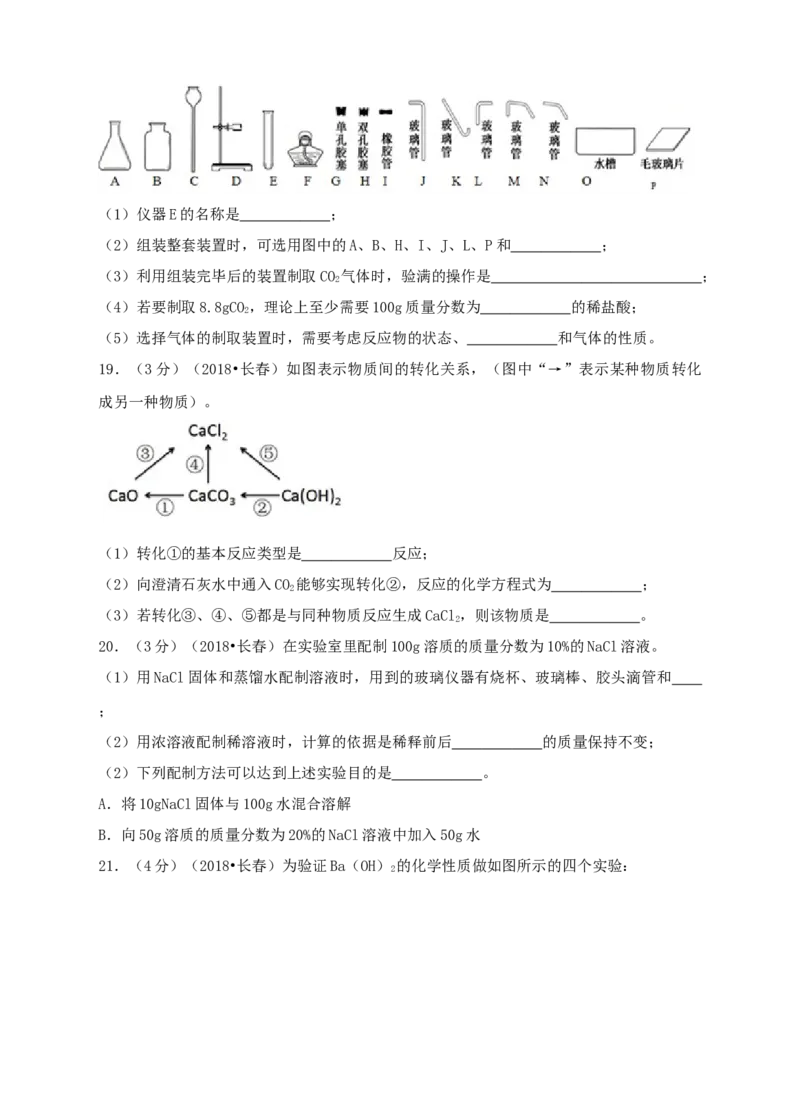
供选择的仪器如图。(1)仪器E的名称是 ;
(2)组装整套装置时,可选用图中的A、B、H、I、J、L、P和 ;
(3)利用组装完毕后的装置制取CO 气体时,验满的操作是 ;
2
(4)若要制取8.8gCO,理论上至少需要100g质量分数为 的稀盐酸;
2
(5)选择气体的制取装置时,需要考虑反应物的状态、 和气体的性质。
19.(3分)(2018•长春)如图表示物质间的转化关系,(图中“→”表示某种物质转化
成另一种物质)。
(1)转化①的基本反应类型是 反应;
(2)向澄清石灰水中通入CO 能够实现转化②,反应的化学方程式为 ;
2
(3)若转化③、④、⑤都是与同种物质反应生成CaCl,则该物质是 。
2
20.(3分)(2018•长春)在实验室里配制100g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
;
(2)用浓溶液配制稀溶液时,计算的依据是稀释前后 的质量保持不变;
(2)下列配制方法可以达到上述实验目的是 。
A.将10gNaCl固体与100g水混合溶解
B.向50g溶质的质量分数为20%的NaCl溶液中加入50g水
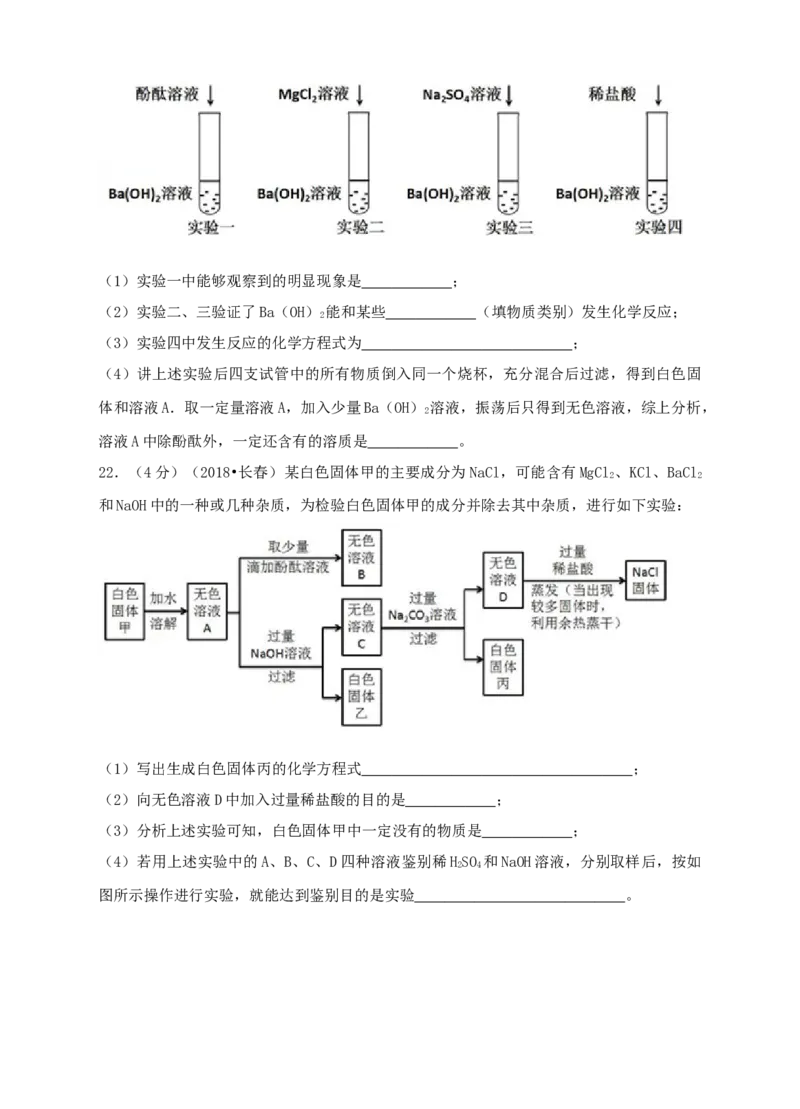
21.(4分)(2018•长春)为验证Ba(OH) 的化学性质做如图所示的四个实验:
2(1)实验一中能够观察到的明显现象是 ;
(2)实验二、三验证了Ba(OH) 能和某些 (填物质类别)发生化学反应;
2
(3)实验四中发生反应的化学方程式为 ;
(4)讲上述实验后四支试管中的所有物质倒入同一个烧杯,充分混合后过滤,得到白色固
体和溶液A.取一定量溶液A,加入少量Ba(OH) 溶液,振荡后只得到无色溶液,综上分析,
2
溶液A中除酚酞外,一定还含有的溶质是 。
22.(4分)(2018•长春)某白色固体甲的主要成分为NaCl,可能含有MgCl 、KCl、BaCl
2 2
和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
(1)写出生成白色固体丙的化学方程式 ;
(2)向无色溶液D中加入过量稀盐酸的目的是 ;
(3)分析上述实验可知,白色固体甲中一定没有的物质是 ;
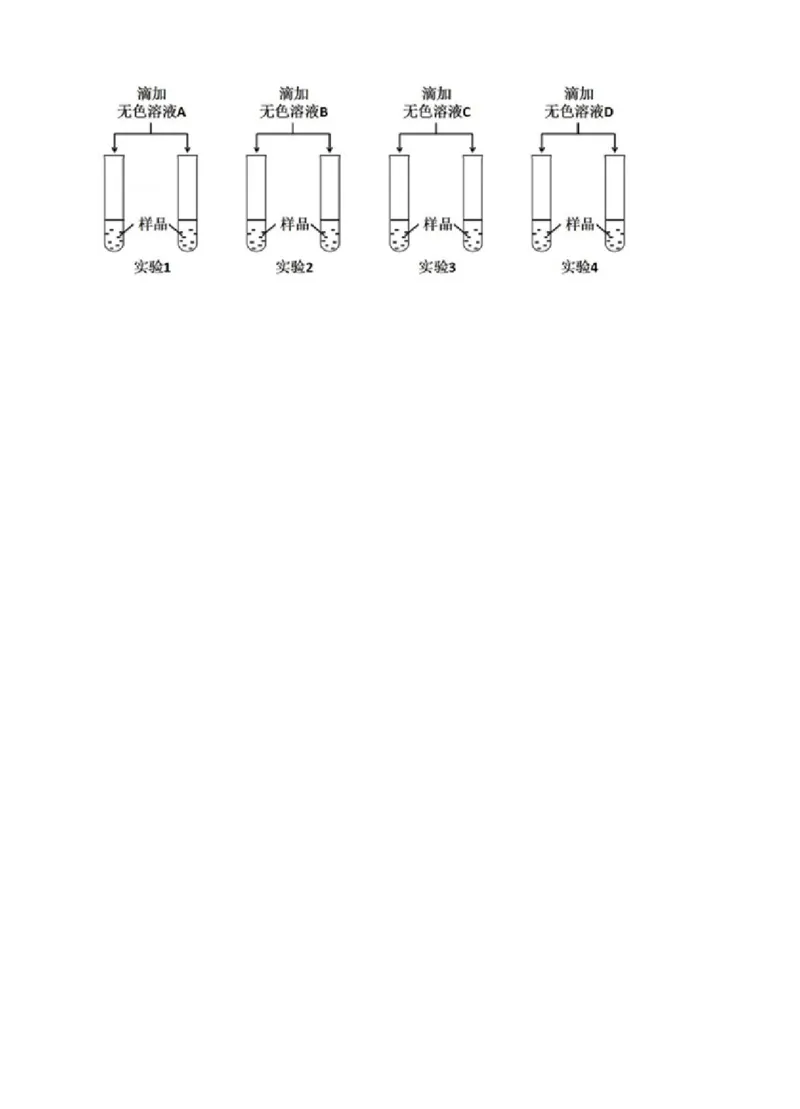
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀HSO 和NaOH溶液,分别取样后,按如
2 4
图所示操作进行实验,就能达到鉴别目的是实验 。