文档内容
2 0 2 4 年 上 教 师 资 格 笔 试 · 化 学 学 科 知 识 与 教 学 能 力
理 论 精 讲 - 化 学 基 本 概 念 4
讲师:沈蕾
更多干货关注 粉笔教师教育 粉笔教师离子反应P25
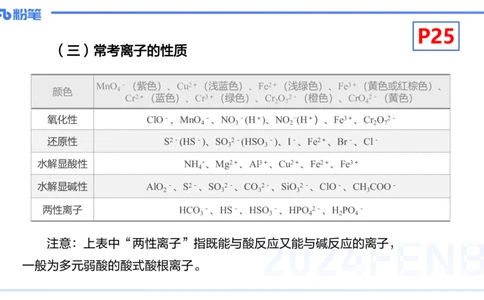
(三)常考离子的性质
MnO -(紫色)、Cu2+(浅蓝色)、Fe2+(浅绿色)、Fe3+(黄色或红棕色)、
颜色 4
Cr2+(蓝色)、Cr3+(绿色)、Cr O 2-(橙色)、CrO 2-(黄色)
2 7 4
氧化性 ClO-、MnO -、NO -(H+)、NO −(H+)、Fe3+、Cr O 2-
4 3 2 2 7
还原性 S2-(HS-)、SO 2-(HSO -)、I-、Fe2+、Br-、Cl-
3 3
水解显酸性 NH +、Mg2+、Al3+、Cu2+、Fe2+、Fe3+
4
水解显碱性 AlO -、S2-、SO 2-、CO 2-、SiO 2-、ClO-、CH COO-
2 3 3 3 3
两性离子 HCO -、HS-、HSO -、HPO 2-、H PO -
3 3 4 2 4
注意:上表中“两性离子”指既能与酸反应又能与碱反应的离子,
一般为多元弱酸的酸式酸根离子。P26
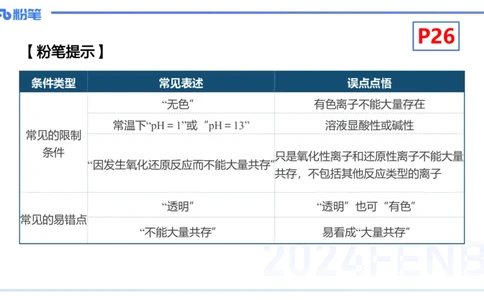
【粉笔提示】
条件类型 常见表述 误点点悟
“无色” 有色离子不能大量存在
常温下“pH=1”或“pH=13” 溶液显酸性或碱性
常见的限制
条件
只是氧化性离子和还原性离子不能大量
“因发生氧化还原反应而不能大量共存”
共存,不包括其他反应类型的离子
“透明” “透明”也可“有色”
常见的易错点
“不能大量共存” 易看成“大量共存”P26
条件类型 常见表述 误点点悟
“与 Al 反应放出 H ” 溶液既可能显酸性也可能显碱性
2
“由水电离出的c(H+)=1×10-12 mol·L-1” 溶液既可能显酸性也可能显碱性
常见的隐
含条件
“通入足量的NH ” 与NH ·H O反应的离子不能大量存在
3 3 2
NO - 、NO - 在酸性条件下具有强氧化性
2 3
(1)“一定大量共存”
常见题干
(2)“可能大量共存” 审清关键字
要求
(3)“不能大量共存”P29
5. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )。
A. 1.0mol/L 的 KNO 溶液:H+、Fe2+、Cl–、SO 2–
3 4
B. 使紫色石蕊呈红色的溶液:NH +、Ba2+、AlO –、Cl–
4 2
C. pH=12 的溶液:K+、Na+、CH COO–、Br–
3
D. 与铝反应产生大量氢气的溶液:Na+、K+、HCO -、NO -
3 3P29
6. 在指定溶液中一定能大量共存的离子是( )。
A. pH=1 的溶液中:K+、Na+、SO 2-、HCO -
4 3
B. 澄清透明的溶液中:Fe3+、Na+、Cl-、SO 2-
4
C. 能与铝反应生成氢气的溶液中:Mg2+、Na+、Cl-、NO -
3
D. pH=13 的溶液中:CH COO-、NH +、Cl-、Na+
3 4四、实验:酸碱中和滴定
(一)实验原理
1.定义
用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的浓度的
实验方法。
2.滴定原理
在中和反应中虽然表面上没有明显现象,但溶液的 pH 会发生很大
的变化,在滴定过程中指示剂会因 pH 突变而发生颜色的变化。通过溶
液的颜色变化可以判断出终点,从而测出消耗的酸(或碱)溶液的体
积,然后根据化学方程式中酸碱物质的量之比求出未知溶液的浓度。 P26P27
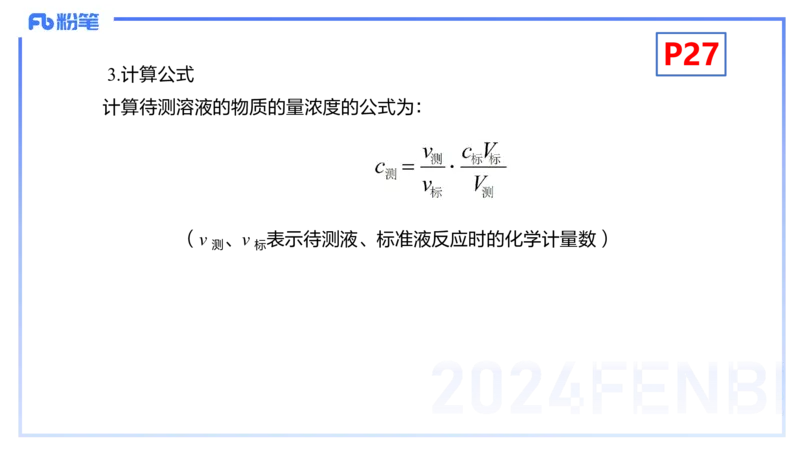
3.计算公式
计算待测溶液的物质的量浓度的公式为:
(v 、v 表示待测液、标准液反应时的化学计量数)
测 标P27
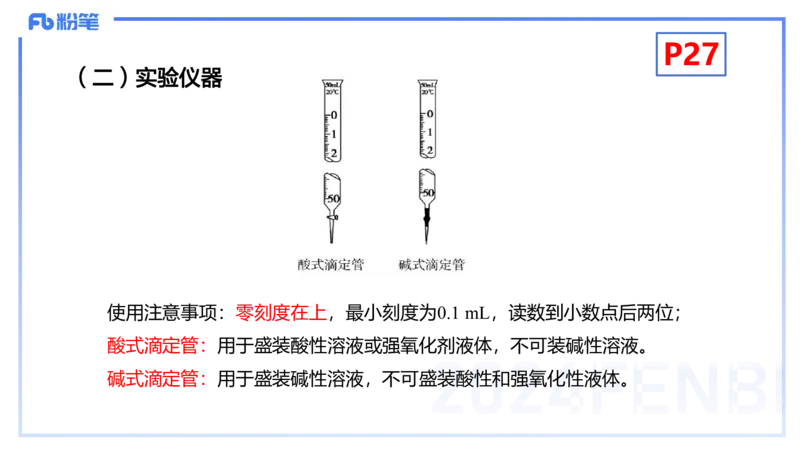
(二)实验仪器
使用注意事项:零刻度在上,最小刻度为0.1 mL,读数到小数点后两位;
酸式滴定管:用于盛装酸性溶液或强氧化剂液体,不可装碱性溶液。
碱式滴定管:用于盛装碱性溶液,不可盛装酸性和强氧化性液体。P27
(三)实验试剂
标准液、待测液、指示剂。
(四)中和滴定操作(以标准 HCl 溶液,滴定 NaOH 溶液为例)
1.洗涤
锥形瓶:用蒸馏水洗涤,不能用待测溶液润洗。P28
滴定管:将检验后不漏液的酸式、碱式滴定管先用蒸馏水洗涤,
再用所盛溶液各润洗 2 ~ 3 遍。
洗涤的原则是少量多次,洗涤的方法是从滴定管上口加入 3 ~
5mL 所要盛装的酸或碱溶液,倾斜着转动滴定管,使液体润湿全部滴
定管内壁,然后,一手控制活塞将液体从滴定管下部放入预置的烧杯
中。
洗净的标准是管内壁不挂水珠。P28
2.取液
标准液:向酸式滴定管中注入标准盐酸至“0”刻度以上,调节液
面至“0”或“0”以下,使尖嘴部分充满溶液且不留有气泡,记下刻
度。
待测液:将待测 NaOH 溶液加入碱式滴定管中,调节液面使尖嘴部
分充满溶液且不留气泡,准确放出一定体积的溶液至锥形瓶中,加入
2 ~ 3 滴甲基橙。P28
3.滴定
在锥形瓶下垫一张白纸,滴定过程中用左手控制活塞,右手不断振
荡锥形瓶,眼睛注视锥形瓶中溶液的颜色变化,直至加入一滴盐酸后,
溶液由黄色变为橙色,且振荡后30s 内不变色, 即达到滴定终点,停
止滴定。
4.读数
平视滴定管中凹液面最低点,读取溶液体积。
5.计算
重复滴定2~3次,取几次结果的平均值。
以上五个步骤可以提炼为“洗—取—滴—读—算”5 个关键字。P28
(五)中和滴定的误差分析
中和滴定是一个要求较高的定量实验,每一处不当或错误操作都
会带来误差。
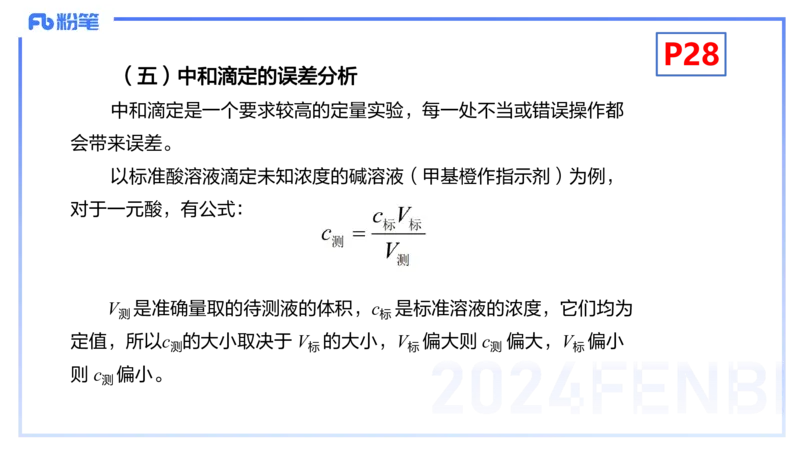
以标准酸溶液滴定未知浓度的碱溶液(甲基橙作指示剂)为例,
对于一元酸,有公式:
V 是准确量取的待测液的体积,c 是标准溶液的浓度,它们均为
测 标
定值,所以c 的大小取决于 V 的大小,V 偏大则 c 偏大,V 偏小
测 标 标 测 标
则 c 偏小。
测P28
常见的因操作不当而引起的误差有:
步骤 操作 V c
A B
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 变小 偏低
洗涤
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
碱式滴定管放出碱液前有气泡,放
取液 变小 偏低
出液体后气泡消失P29
步骤 操作 V c
A B
酸 式滴定管滴定前有气泡,滴定终点时
变大 偏高
气泡消失
振荡锥形瓶时部分液体溅出 变小 偏低
滴定
部分酸液滴出锥形瓶外 变大 偏高
滴入酸液过快,停止滴定后反加一滴氢氧化
变大 偏高
钠溶液无变化
滴定前读数正确,滴定后俯视读数
变小 偏低
(或前仰后俯)
滴定前读数正确,滴定后仰视读数
读数
变大 偏高
(或前俯后仰)
两次滴定所消耗酸液的体积相差太大 无法判断氧化还原反应P30
一、氧化还原反应的概念、本质与特征
(一)概念
根据反应中有无电子转移或元素化合价是否发生变化,可以把化
学反应划分为氧化还原反应和非氧化还原反应。
(二)本质
电子转移(电子得失或偏移)。
(三)特征
反应前后元素化合价发生变化(氧化还原反应的最佳判据)。P31
(四)氧化反应与还原反应关系图P31
【粉笔提示】
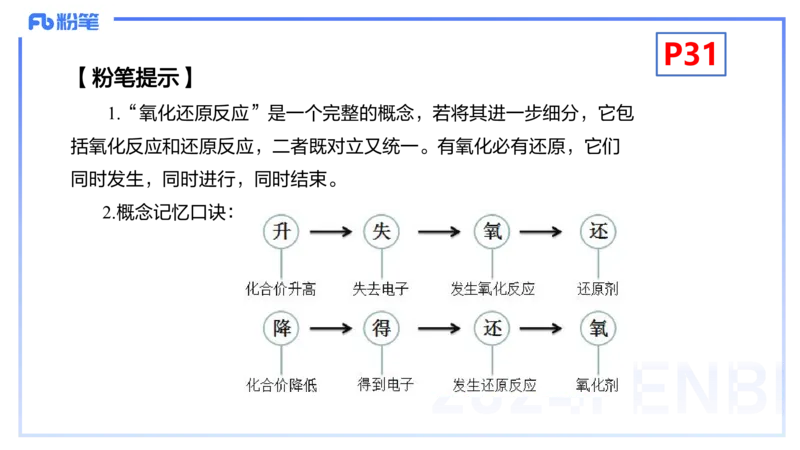
1.“氧化还原反应”是一个完整的概念,若将其进一步细分,它包
括氧化反应和还原反应,二者既对立又统一。有氧化必有还原,它们
同时发生,同时进行,同时结束。
2.概念记忆口诀:P31
二、氧化还原反应与四种基本反应类型
【粉笔提示】
1.化合反应可能是氧化还原反应,有单质参加的化合反应一般是氧化还原反应。
2.分解反应可能是氧化还原反应,有单质生成的分解反应一般是氧化还原反应。
3.置换反应都是氧化还原反应,复分解反应都不是氧化还原反应。
4.同素异形体之间的转化是化学变化,但不视为氧化还原反应。P32
三、中学化学中常见的氧化剂和还原剂
常见的氧化剂
第一类 活泼的非金属单质 例:F 、Cl 、Br 、O 、O 等
2 2 2 2 3
第二类 高价态的金属阳离子 例:Fe3+、Cu2+等
第三类 变价元素的高价含氧化合物 例:KMnO 、K Cr O 、浓H SO 、HNO 等
4 2 2 7 2 4 3
其他 HClO、漂白粉、MnO 、Na O 、H O 、银氨溶液、新制Cu(OH) 悬浊液等
2 2 2 2 2 2P91
常见的还原剂
第一类 活泼的金属单质 例:K、Na、Mg、Al、Fe、Zn等
第二类 某些非金属单质 例:H 、C、Si、S等
2
例:CO、Fe(OH) 、SO 、H S、HBr、HI、
2 2 2
第三类 变价元素的低价态化合物
NH 、H C O (草酸)、N H (肼)等
3 2 2 4 2 4
其他 S2-(HS-)、SO 2-(HSO -)、I-、Fe2+、Br-、Cl-等
3 3P32
【粉笔提示】
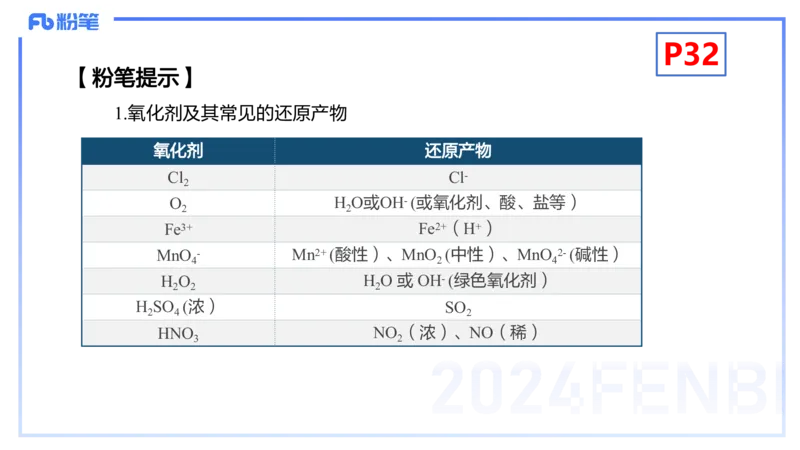
1.氧化剂及其常见的还原产物
氧化剂 还原产物
Cl Cl-
2
O H O或OH- (或氧化剂、酸、盐等)
2 2
Fe3+ Fe2+(H+)
MnO - Mn2+ (酸性)、MnO (中性)、MnO 2- (碱性)
4 2 4
H O H O 或 OH- (绿色氧化剂)
2 2 2
H SO (浓) SO
2 4 2
HNO NO (浓)、NO(稀)
3 2P33
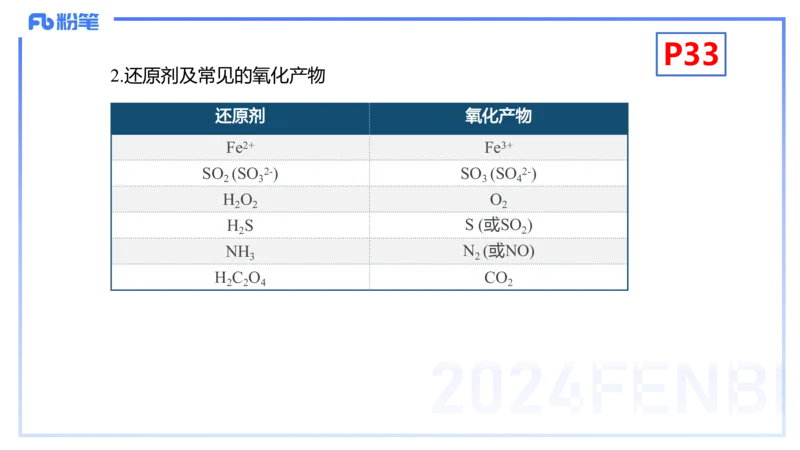
2.还原剂及常见的氧化产物
还原剂 氧化产物
Fe2+ Fe3+
SO (SO 2-) SO (SO 2-)
2 3 3 4
H O O
2 2 2
H S S (或SO )
2 2
NH N (或NO)
3 2
H C O CO
2 2 4 2P33
四、氧化还原反应的计算依据
1.氧化剂得到的电子总数=还原剂失去的电子总数(电子得失守恒)。
2.对于离子反应,反应前后电荷平衡(电荷守恒)。
3.各元素原子个数相等(质量守恒)。P33
【粉笔提示】
知识误区点拨:
1.含有最高价态元素的化合物不一定具有强氧化性,元素价态越高,
不一定氧化性越强。
例如:H PO 中+5价的P无氧化性;
3 4
氧化性 HClO