文档内容
2013 年四川省绵阳市中考化学试卷(教师版)
一、选择题(每小题3分,共63分.每小题只有一个选项是最符合题目要求的)
1.(3分)生活中的下列现象,不包含化学变化是( )
A.牛奶在空气中久置后产生酸味
B.家庭装修、装饰材料散发出难闻气味
C.铁制水龙头渗漏引起白色洗面盆滴水处发黄
D.旅游城市标志青铜奔马(马踏飞燕)变绿
【微点】化学变化和物理变化的判别.
【思路】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化
学变化与物理变化的本质区别是有无新物质生成,据此抓住化学变化和物理变化的区别
结合事实进行分析判断即可。
【解析】解:A、牛奶在空气中久置后产生酸味过程中有对人体有害的新物质生成,属
于化学变化。
B、装饰材料散发出难闻气味过程中只是状态发生改变,没有新物质生成,属于物理变
化。
C、白色洗面盆滴水处发黄过程中有新物质生成,属于化学变化。
D、青铜奔马变绿过程中有新物质铜绿等生成,属于化学变化。
故选:B。
【点拨】本题难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是
指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成
属于化学变化。
2.(3分)我们每一个人都应传播“低碳”理念,倡导“低碳”生活.下列做法不属于
“低碳”生活的是( )
A.节日燃放烟花爆竹
B.多骑自行车,少乘汽车
C.用电子贺卡代替纸质生日贺卡
D.秸秆粉碎还田而不焚烧
【微点】自然界中的碳循环.
【思路】“低碳生活”指的是生活作息时所耗用的能量要尽量减少,特别是减少二氧化
第 1 页 / 共 14 页碳的排放量,减缓生态恶化;可以从节电、节能和回收等环节来改变生活细节,据此进
行分析判断即可.
【解析】解:A、节日燃放烟花爆竹,增加了空气污染物、二氧化碳的排放,故选项不
符合“低碳生活”理念。
B、多骑自行车,少乘汽车,能减少交通工具的使用,从而减少二氧化碳的排放,故选
项符合“低碳生活”理念。
C、用电子贺卡代替纸质生日贺卡,能减少能源的消耗、二氧化碳的排放,故选项符合
“低碳生活”理念。
D、秸秆粉碎还田而不焚烧,既能给土壤增加肥料,又减少二氧化碳的排放,故选项符
合“低碳生活”理念。
故选:A。
【点拨】低碳生活理念已成为人们的共识,节能减排的措施和观念是化学考查的热点,
要用低碳生活理念指导自己的活动,把节能减排的措施运用到生产、生活中去.
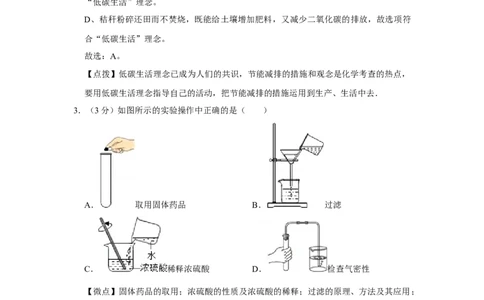
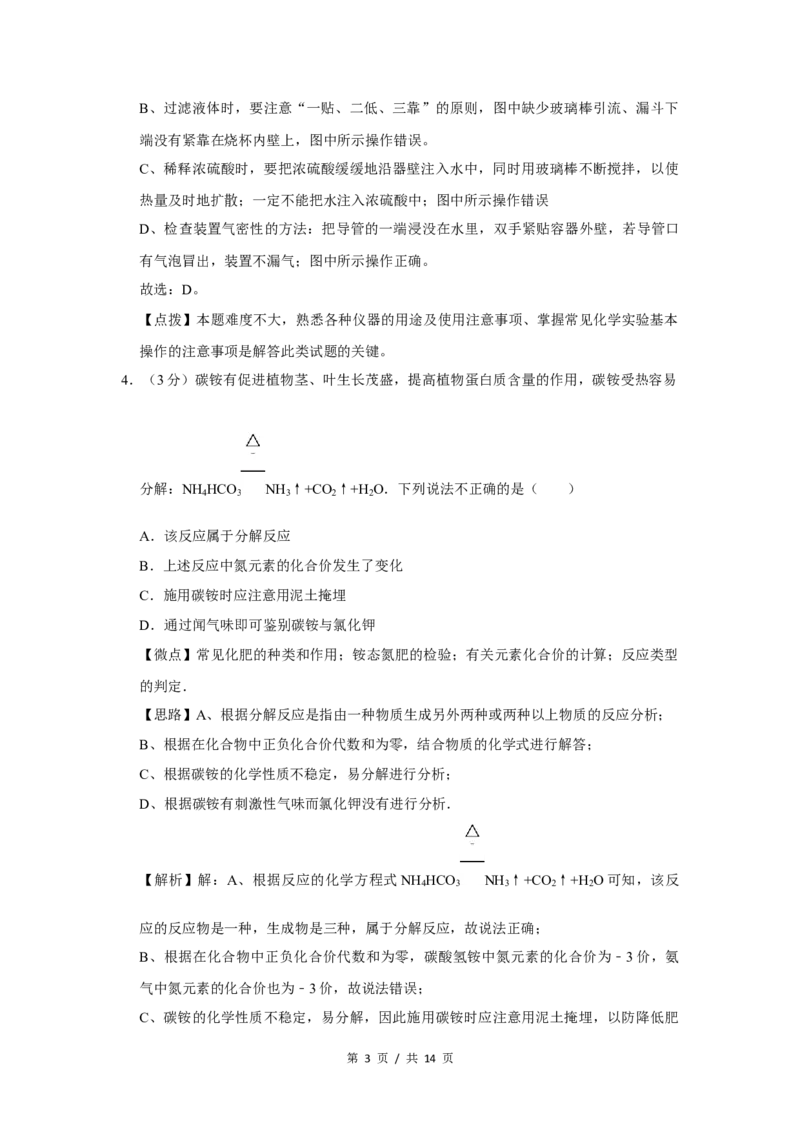
3.(3分)如图所示的实验操作中正确的是( )
A. 取用固体药品 B. 过滤
C. 稀释浓硫酸 D. 检查气密性
【微点】固体药品的取用;浓硫酸的性质及浓硫酸的稀释;过滤的原理、方法及其应用;
检查装置的气密性.
【思路】A、根据向试管中装块状固体药品的方法进行分析判断。
B、过滤液体时,要注意“一贴、二低、三靠”的原则。
C、根据浓硫酸的稀释方法进行分析判断。
D、根据检查装置气密性的方法进行分析判断。
【解析】解:A、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在
试管口,再慢慢将试管竖立起来,图中所示操作错误。
第 2 页 / 共 14 页B、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下
端没有紧靠在烧杯内壁上,图中所示操作错误。
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使
热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口
有气泡冒出,装置不漏气;图中所示操作正确。
故选:D。
【点拨】本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本
操作的注意事项是解答此类试题的关键。
4.(3分)碳铵有促进植物茎、叶生长茂盛,提高植物蛋白质含量的作用,碳铵受热容易
分解:NH HCO NH ↑+CO ↑+H O.下列说法不正确的是( )
4 3 3 2 2
A.该反应属于分解反应
B.上述反应中氮元素的化合价发生了变化
C.施用碳铵时应注意用泥土掩埋
D.通过闻气味即可鉴别碳铵与氯化钾
【微点】常见化肥的种类和作用;铵态氮肥的检验;有关元素化合价的计算;反应类型
的判定.
【思路】A、根据分解反应是指由一种物质生成另外两种或两种以上物质的反应分析;
B、根据在化合物中正负化合价代数和为零,结合物质的化学式进行解答;
C、根据碳铵的化学性质不稳定,易分解进行分析;
D、根据碳铵有刺激性气味而氯化钾没有进行分析.
【解析】解:A、根据反应的化学方程式NH HCO NH ↑+CO ↑+H O可知,该反
4 3 3 2 2
应的反应物是一种,生成物是三种,属于分解反应,故说法正确;
B、根据在化合物中正负化合价代数和为零,碳酸氢铵中氮元素的化合价为﹣3价,氨
气中氮元素的化合价也为﹣3价,故说法错误;
C、碳铵的化学性质不稳定,易分解,因此施用碳铵时应注意用泥土掩埋,以防降低肥
第 3 页 / 共 14 页效,故说法正确;
D、碳铵有刺激性气味而氯化钾没有,因此可通过闻气味的方法鉴别碳铵与氯化钾,故
说法正确;
故选:B。
【点拨】本题难度不大,但综合性较强,掌握反应类型的判断、化合价的计算以及物质
的性质和鉴别即可解答.
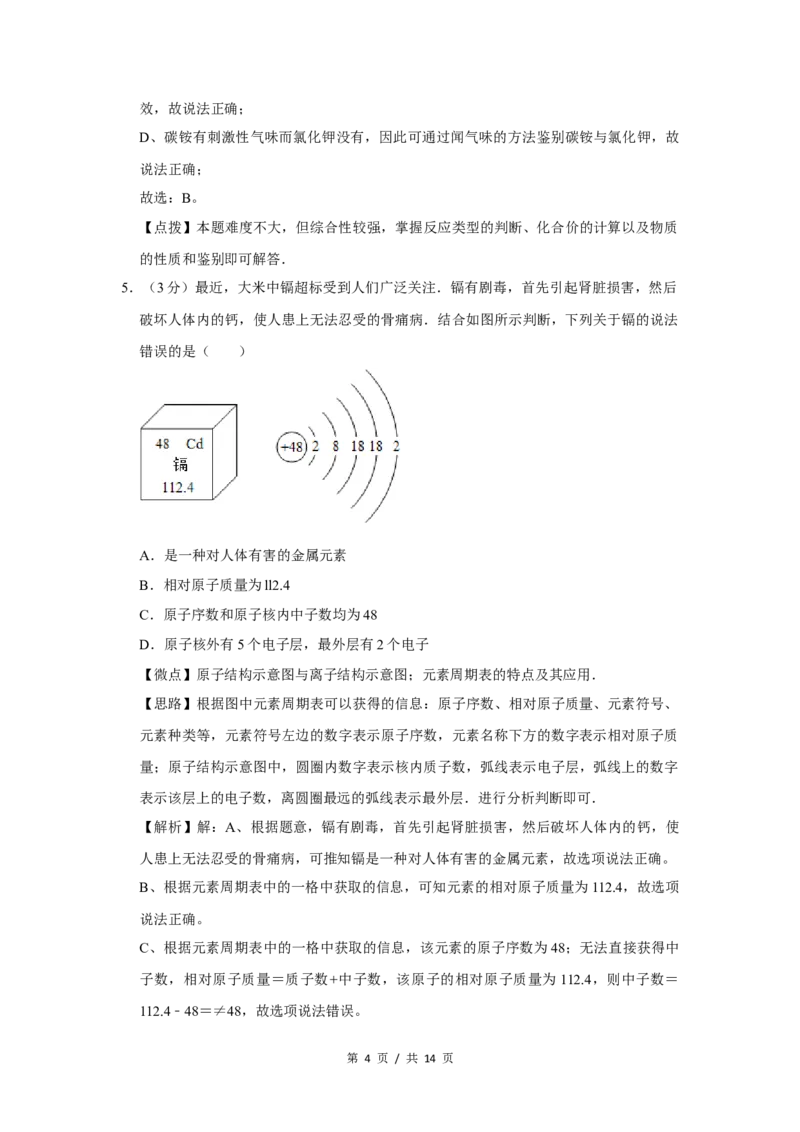
5.(3分)最近,大米中镉超标受到人们广泛关注.镉有剧毒,首先引起肾脏损害,然后
破坏人体内的钙,使人患上无法忍受的骨痛病.结合如图所示判断,下列关于镉的说法
错误的是( )
A.是一种对人体有害的金属元素
B.相对原子质量为ll2.4
C.原子序数和原子核内中子数均为48
D.原子核外有5个电子层,最外层有2个电子
【微点】原子结构示意图与离子结构示意图;元素周期表的特点及其应用.
【思路】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、
元素种类等,元素符号左边的数字表示原子序数,元素名称下方的数字表示相对原子质
量;原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字
表示该层上的电子数,离圆圈最远的弧线表示最外层.进行分析判断即可.
【解析】解:A、根据题意,镉有剧毒,首先引起肾脏损害,然后破坏人体内的钙,使
人患上无法忍受的骨痛病,可推知镉是一种对人体有害的金属元素,故选项说法正确。
B、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为112.4,故选项
说法正确。
C、根据元素周期表中的一格中获取的信息,该元素的原子序数为48;无法直接获得中
子数,相对原子质量=质子数+中子数,该原子的相对原子质量为112.4,则中子数=
112.4﹣48=≠48,故选项说法错误。
第 4 页 / 共 14 页D、由镉的原子结构示意图,原子核外有5个电子层,最外层有2个电子,故选项说法
正确。
故选:C。
【点拨】本题难度不大,灵活运用元素周期表中元素的信息,了解原子结构示意图的意
义是正确解答本题的关键.
6.(3分)下列着火情况下,相应灭火措施及其理由均正确的是( )
选 着火情况 灭火措施 理由
项
A 不慎将酒精灯内酒精洒 用湿抹布扑盖 隔绝空气,降低可燃物着
在实验桌上燃烧起来 火点
B 在寝室吸烟引起被褥燃 迅速打开门窗并泼水 通风透气,降低可燃物温
烧 度
C 歌厅因电线老化短路起 首先使用泡沫灭火器 降低可燃物温度并隔绝空
火 灭火, 气
然后断开电源
D 林区发生火灾 砍倒附近树木 移走可燃物
开辟隔离带
A.A B.B C.C D.D
【微点】灭火的原理和方法.
【思路】根据灭火原理: 清除或隔离可燃物, 隔绝氧气或空气, 使温度降到可
燃物的着火点以下,据此结①合生活中常用的灭火方②法进行分析解答. ③
【解析】解:A、酒精灯内酒精洒在实验桌上燃烧起来,用湿抹布扑盖,隔绝空气,使
温度降到着火点以下;可燃物的着火点一般是不变的,不能降低可燃物的着火点,故选
项说法错误。
B、在寝室吸烟引起被褥燃烧,不能立即打开门窗,否则空气流通,火势更旺,故选项
说法错误。
C、歌厅因电线老化短路起火,为防止触电,首先应切断电源,再使用泡沫灭火器灭火,
故选项说法错误。
D、林区发生火灾,砍倒附近树木开辟隔离带,是利用了移除可燃物的原理,故选项说
法正确。
故选:D。
【点拨】本题难度不大,掌握灭火原理(清除或隔离可燃物,隔绝氧气或空气,使温度
降到可燃物的着火点以下)并能灵活运用是正确解答本题的关键.
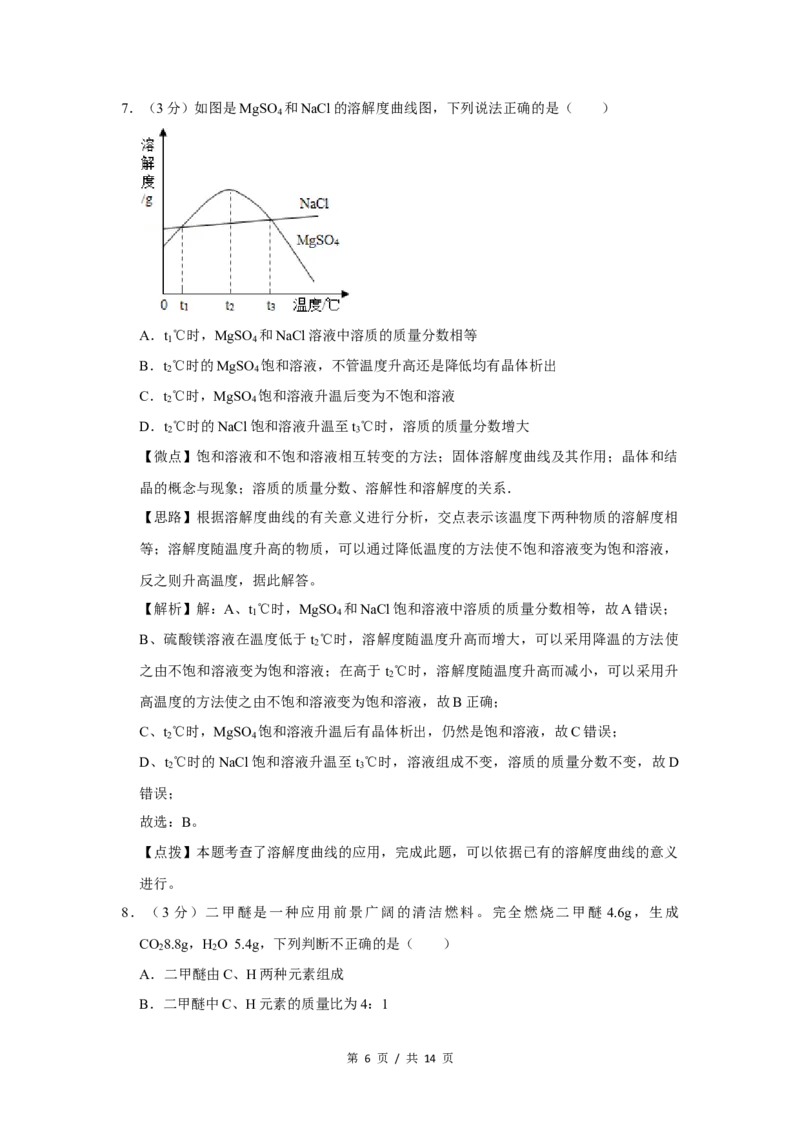
第 5 页 / 共 14 页7.(3分)如图是MgSO 和NaCl的溶解度曲线图,下列说法正确的是( )
4
A.t ℃时,MgSO 和NaCl溶液中溶质的质量分数相等
1 4
B.t ℃时的MgSO 饱和溶液,不管温度升高还是降低均有晶体析出
2 4
C.t ℃时,MgSO 饱和溶液升温后变为不饱和溶液
2 4
D.t ℃时的NaCl饱和溶液升温至t ℃时,溶质的质量分数增大
2 3
【微点】饱和溶液和不饱和溶液相互转变的方法;固体溶解度曲线及其作用;晶体和结
晶的概念与现象;溶质的质量分数、溶解性和溶解度的关系.
【思路】根据溶解度曲线的有关意义进行分析,交点表示该温度下两种物质的溶解度相
等;溶解度随温度升高的物质,可以通过降低温度的方法使不饱和溶液变为饱和溶液,
反之则升高温度,据此解答。
【解析】解:A、t ℃时,MgSO 和NaCl饱和溶液中溶质的质量分数相等,故A错误;
1 4
B、硫酸镁溶液在温度低于t ℃时,溶解度随温度升高而增大,可以采用降温的方法使
2
之由不饱和溶液变为饱和溶液;在高于t ℃时,溶解度随温度升高而减小,可以采用升
2
高温度的方法使之由不饱和溶液变为饱和溶液,故B正确;
C、t ℃时,MgSO 饱和溶液升温后有晶体析出,仍然是饱和溶液,故C错误;
2 4
D、t ℃时的NaCl饱和溶液升温至t ℃时,溶液组成不变,溶质的质量分数不变,故D
2 3
错误;
故选:B。
【点拨】本题考查了溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线的意义
进行。
8.(3 分)二甲醚是一种应用前景广阔的清洁燃料。完全燃烧二甲醚 4.6g,生成
CO 8.8g,H O 5.4g,下列判断不正确的是( )
2 2
A.二甲醚由C、H两种元素组成
B.二甲醚中C、H元素的质量比为4:1
第 6 页 / 共 14 页C.二甲醚中H的质量分数为l3%
D.4.6g二甲醚完全燃烧消耗O 9.6g
2
【微点】质量守恒定律及其应用.
【思路】根据质量守恒定律,反应前后,元素种类、质量不变,结合题意、化合物中各
元素质量比=各原子的相对原子质量×原子个数之比进行分析判断。
【解析】解:由题意,完全燃烧二甲醚4.6g,生成CO 8.8g,H O 5.4g,8.8gCO 中含碳
2 2 2
元素的质量为 8.8g 100%=2.4g,H O5.4g 中含氢元素的质量为 5.4g
2
100%=0.6g。
A、由质量守恒定律,反应前后,元素种类、质量不变,二甲醚中C、H元素的质量之
和为2.4g+0.6g=3g<4.6g,则二甲醚中一定含有氧元素,故选项说法错误。
B、由质量守恒定律,反应前后,元素种类、质量不变,二甲醚中 C、H元素的质量分
别为2.4g、0.6g,则二甲醚中C、H元素的质量比为2.4g:0.6g=4:1,故选项说法正确。
C、二甲醚中H的质量分数为 100%≈13%,故选项说法正确。
D、由质量守恒定律,4.6g二甲醚完全燃烧消耗O 的质量为8.8g+5.4g﹣4.6g=9.6g,故
2
选项说法正确。
故选:A。
【点拨】本题难度不大,理解质量守恒定律(反应前后,元素种类、质量不变)并能灵
活运用是正确解答本题的关键。
9.(3分)将ag铁和碳的混合物在氧气中充分灼烧,冷却,称量,发现剩余固体的质量仍
为ag,该混合物中碳的质量分数为( )
A.30.0% B.22.2% C.27.6% D.10.3%
【微点】根据化学反应方程式的计算.
【思路】根据题意可知,铁和碳的混合物在氧气中充分灼烧,铁与氧气反应生成了四氧
化三铁,固体质量增加了,碳与氧气反应生成了二氧化碳,固体的质量减少了.由剩余
固体的质量不变可知,参加反应的氧气的质量等于混合物中碳的质量,该混合物中碳的
第 7 页 / 共 14 页质量分数即为四氧化三铁中氧元素的质量分数.
【解析】解:由题意可知,铁和碳的混合物在氧气中充分灼烧,铁与氧气反应生成了四
氧化三铁,固体质量增加了,碳与氧气反应生成了二氧化碳,固体的质量减少了。由剩
余固体的质量不变可知,参加反应的氧气的质量等于混合物中碳的质量,该混合物中碳
的质量分数即为四氧化三铁中氧元素的质量分数。
四氧化三铁中氧元素的质量分数是: 27.6%
由以上计算可知,A、B、D错误,C正确。
故选:C。
【点拨】本道题比较难,解题的关键是根据物质的变化,找出碳与氧气的质量关系,即
可计算出碳的质量分数.
二、填空与解答题
10.(18分)(1)豆浆是价廉物美的饮品,豆浆中含有丰富的植物蛋白。
从平衡膳食考虑,我们在喝豆浆时无需搭配 C (填下列选项的序号字母)。
①A.核桃或花生以增加油脂 B.蔬菜或水果以增加维生素
C.牛奶或鸡蛋以增加蛋白质 D.馒头或面包以增加糖类
家庭常用豆浆机制作强浆,豆浆机的内胆为不锈钢,手柄为酚醛塑料。导线外套为氯
②丁橡胶,则豆浆机用到的材料包括 金属材料 、 有机合成材料 两类。
(2)高炉炼铁的原理是在高温下,利用炉内反应生成的 CO把铁从铁矿石中 还原
出来。炉内生成C0的化学反应方程式为 C+ 0 CO 、 CO +C 2CO 。
2 2 2
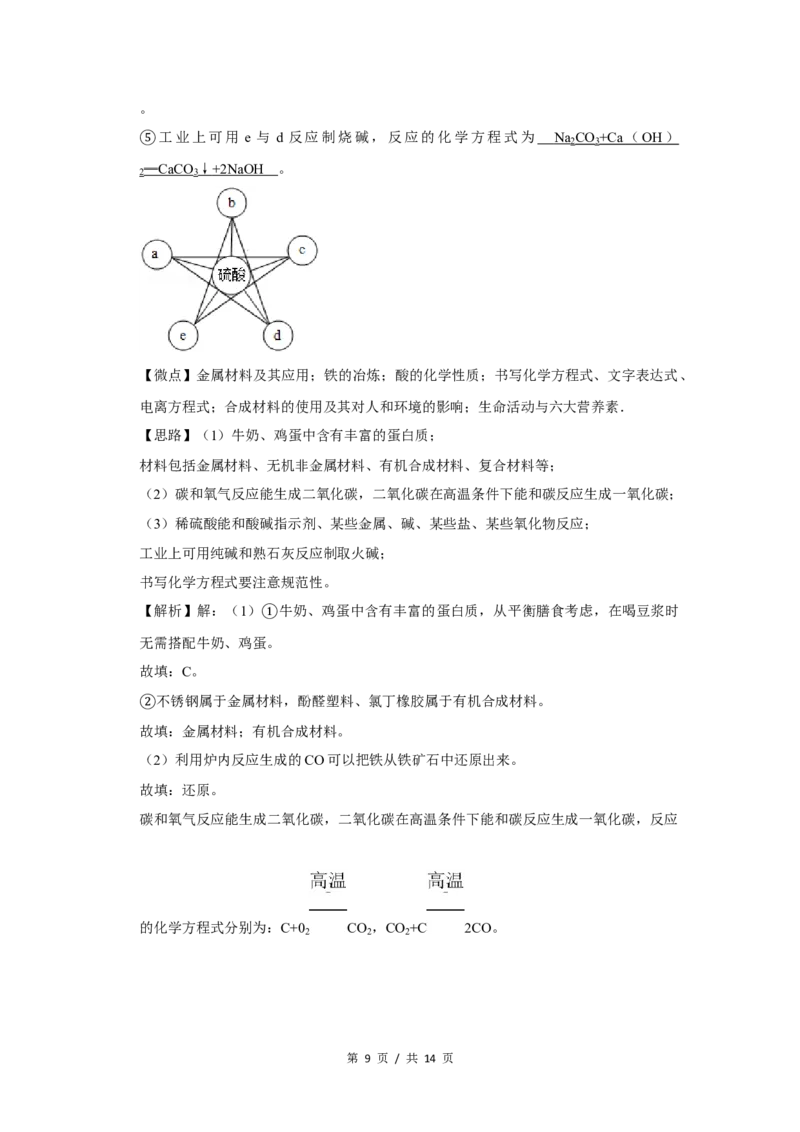
(3)咎博同学用“思维导图”来归纳总结硫酸的化学性质,如图表示硫酸能与 a~e五
类物质反应,请你回答下列问题:
a为石蕊溶液,反应的现象是 石蕊溶液由紫色变为红色 。
①b 是活泼金属,以地壳中含量最多的金属元素为例,写出反应的化学方程式:
②2Al+3H SO ═ A l ( SO ) +3H ↑
2 4 2 4 3 2
c是金属氧化物,所属反应类型是 复分解反应 ;d是哪一类化合物? 碱 。
③e是盐,写出有气体生成的化学反应方程式: H
2
SO
4
+Na
2
CO
3
═ N a
2
SO
4
+H
2
0+CO
2
↑
④
第 8 页 / 共 14 页。
工业上可用 e 与 d 反应制烧碱,反应的化学方程式为 N a CO +Ca ( OH )
2 3
⑤ ═ CaCO ↓ +2NaOH 。
2 3
【微点】金属材料及其应用;铁的冶炼;酸的化学性质;书写化学方程式、文字表达式、
电离方程式;合成材料的使用及其对人和环境的影响;生命活动与六大营养素.
【思路】(1)牛奶、鸡蛋中含有丰富的蛋白质;
材料包括金属材料、无机非金属材料、有机合成材料、复合材料等;
(2)碳和氧气反应能生成二氧化碳,二氧化碳在高温条件下能和碳反应生成一氧化碳;
(3)稀硫酸能和酸碱指示剂、某些金属、碱、某些盐、某些氧化物反应;
工业上可用纯碱和熟石灰反应制取火碱;
书写化学方程式要注意规范性。
【解析】解:(1) 牛奶、鸡蛋中含有丰富的蛋白质,从平衡膳食考虑,在喝豆浆时
无需搭配牛奶、鸡蛋①。
故填:C。
不锈钢属于金属材料,酚醛塑料、氯丁橡胶属于有机合成材料。
②故填:金属材料;有机合成材料。
(2)利用炉内反应生成的CO可以把铁从铁矿石中还原出来。
故填:还原。
碳和氧气反应能生成二氧化碳,二氧化碳在高温条件下能和碳反应生成一氧化碳,反应
的化学方程式分别为:C+0 CO ,CO +C 2CO。
2 2 2
第 9 页 / 共 14 页故填:C+0 CO ; CO +C 2CO。
2 2 2
(3) 稀硫酸能使石蕊试液变红色。
故填:①石蕊溶液由紫色变为红色。
地壳中含量最多的金属元素是铝元素,铝和稀硫酸反应能生成硫酸铝和氢气,反应的
②化学方程式为:2Al+3H SO ═Al (SO ) +3H ↑。
2 4 2 4 3 2
故填:2Al+3H SO ═Al (SO ) +3H ↑。
2 4 2 4 3 2
金属氧化物能和稀硫酸交换成分,生成盐和水,属于复分解反应。
③故填:复分解反应。
因为e是盐,所以d是碱。
故填:碱。
碳酸钠属于盐,能和稀硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:
④H SO +Na CO ═Na SO +H O+CO ↑。
2 4 2 3 2 4 2 2
故填:H SO +Na CO ═Na SO +H O+CO ↑。
2 4 2 3 2 4 2 2
工业上可用纯碱和熟石灰反应制取火碱,纯碱是碳酸钠的俗称,熟石灰是氢氧化钙的
⑤俗 称 , 碳 酸 钠 和 氢 氧 化 钙 反 应 的 化 学 方 程 式 为 : Na CO +Ca ( OH )
2 3
═CaCO ↓+2NaOH。
2 3
故填:Na CO +Ca(OH) ═CaCO ↓+2NaOH。
2 3 2 3
【点拨】本题主要考查化学方程式的书写,书写化学方程式时要注意四步,一是反应物
和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否
有“↑”或“↓”。
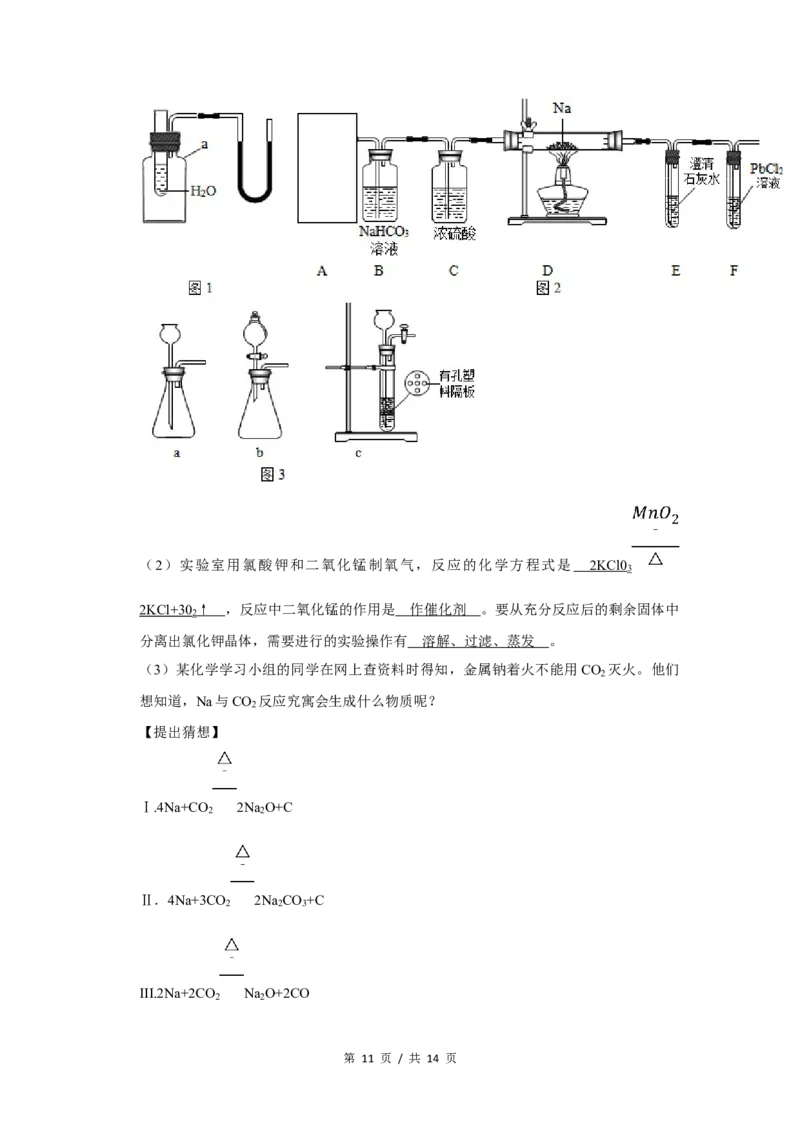
11.(8分)(1)用如图1所示装置进行实验,探究物质溶解是吸热还是放热,仪器a的
名称是 广口瓶 。若出现导管中红墨水液面左管降低右管升高,则试管中加入的物质
可以是 BC (填序号)。
A.NH NO 固体;B.浓硫酸;C.NaOH固体;D.CaCO 固体。
4 3 3
第 10 页 / 共 14 页(2)实验室用氯酸钾和二氧化锰制氧气,反应的化学方程式是 2KCl 0
3
2KCl+30 ↑ ,反应中二氧化锰的作用是 作催化剂 。要从充分反应后的剩余固体中
2
分离出氯化钾晶体,需要进行的实验操作有 溶解、过滤、蒸发 。
(3)某化学学习小组的同学在网上查资料时得知,金属钠着火不能用CO 灭火。他们
2
想知道,Na与CO 反应究寓会生成什么物质呢?
2
【提出猜想】
Ⅰ.4Na+CO 2Na O+C
2 2
Ⅱ.4Na+3CO 2Na CO +C
2 2 3
III.2Na+2CO Na O+2CO
2 2
第 11 页 / 共 14 页溶液检验:PdCl +CO+H O═Pd(黑色)↓+2HCl+CO
2 2 2
【实验操究】该小组成员设计了如图2所示实验:
【分析讨论】
装 置 A 用 盐 酸 与 石 灰 石 反 应 制 备 CO , 反 应 的 化 学 方 程 式 为
2
①CaCO +2HCl ═ CaCl +H 0+CO ↑ 。为使制备CO 的反应能随开随用,随关随停,所
3 2 2 2 2
选装置应是图3中的 c 。
装置 B 的作用是除去二氧化碳气体中混有的 HCl 气体,反应的化学方程式是
②HCl+NaHCO ═ NaCl+H 0+CO ↑ ;装置C的作用是 除去二氧化碳气体中的水蒸气
3 2 2
。
经检查整套装置气密性良好,装好药品使A中产生CO ,必须待装置E中出现 澄清
2
③石灰水变浑浊 现象时再点燃酒精灯,其目的是 排出反应装置中的空气,防止钠与氧
气反应 。
【实验结论】
实验观察到的现象是:装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,
则猜想 Ⅲ 是正确的。
【微点】实验探究物质的性质或变化规律;混合物的分离方法;气体的净化(除杂);
实验室制取氧气的反应原理;催化剂的特点与催化作用;二氧化碳的实验室制法;溶解
时的吸热或放热现象;书写化学方程式、文字表达式、电离方程式.
【思路】(1)根据常见仪器的名称回答;导管中红墨水液面左管降低右管升高,则试
管中加入的物质溶于水时放热;
(2)根据化学方程式书写的步骤写出氯酸钾和二氧化锰混合制取氧气的化学方程式即
可;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过
滤、蒸发;
(3)【分析讨论】根据化学方程式的书写方法和各装置的作用进行分析;
【实验结论】根据题中信息结合实验现象进行分析。
【解析】解:(1)仪器a的名称是广口瓶;导管中红墨水液面左管降低右管升高,则
试管中加入的物质溶于水时放热,NH NO 固体溶于水时吸热;浓硫酸溶于水时放热;
4 3
NaOH固体溶于水时放热;CaCO 固体不溶于水;
3
(2)实验室用氯酸钾和二氧化锰制氧气,反应的化学方程式是 2KCl0
3
第 12 页 / 共 14 页2KCl+30 ↑;反应中二氧化锰的作用是做催化剂;要从充分反应后的剩余固体中分离出
2
氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
(3)【分析讨论】
盐酸与石灰石反应的化学方程式为CaCO +2HCl═CaCl +H O+CO ↑;为使制备CO
3 2 2 2 2
①的反应能随开随用,随关随停,所选装置应是图3中的c。
碳酸氢钠和氯化氢反应生成氯化钠、水和二氧化碳,反应的化学方程式是
②HCl+NaHCO ═NaCl+H O+CO ↑;浓硫酸具有吸水性,能除去二氧化碳气体中的水蒸
3 2 2
气;
为防止钠与氧气反应,因此应先排出反应装置中的空气,当装置E中澄清石灰水变浑
③浊时,说明空气已排除完毕;
【实验结论】
根据题中信息可知,若装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,
则猜想Ⅲ正确;
故答案为:(1)广口瓶; BC;
(2)2KCl0 2KCl+30 ↑;作催化剂;溶解、过滤、蒸发;
3 2
(3)【分析讨论】
CaCO +2HCl═CaCl +H O+CO ↑;c;
3 2 2 2
①HCl+NaHCO
3
═NaCl+H
2
O+CO
2
↑;除去二氧化碳气体中的水蒸气;
②澄清石灰水变浑浊;排出反应装置中的空气,防止钠与氧气反应;
③【实验结论】根据实验观察到的现象是:装置D中的硬质玻璃管内残留白色固体,装置
F中产生黑色沉淀,说明猜想Ⅲ是正确的;
故答案为:Ⅲ。
【点拨】确理解实验装置的作用,为明确实验操作和实验目的基础和前提,难度较大。
12.(7分)四川泡菜深受人们喜爱。
(1)家庭用含NaCl 94%的袋装食用盐配制泡菜水,要求泡菜水中 NaCl的质量分数为
18.8%,则1000g水中需加袋装食用盐 25 0 g。
(2)要测定某泡菜水中NaCl的含量,取70mL澄清的泡菜水(密度为1.1g/cm3),加
入足量的AgNO 溶液,充分反应后滤出沉淀,洗净烘干后称得其质量为28.7g。假设泡
3
菜水中的其他物质均不与AgNO 溶液反应,求这种泡菜水中NaCl的质量分数。
3
第 13 页 / 共 14 页(计算结果保留l位小数,无计算过程不给分)
【微点】有关溶质质量分数的简单计算;根据化学反应方程式的计算.
【思路】(1)根据溶质质量分数的公式进行计算;
(2)根据氯化钠与硝酸银反应的方程式,由氯化银的质量可求出氯化钠的质量,再根
据溶质质量分数的公式进行计算。
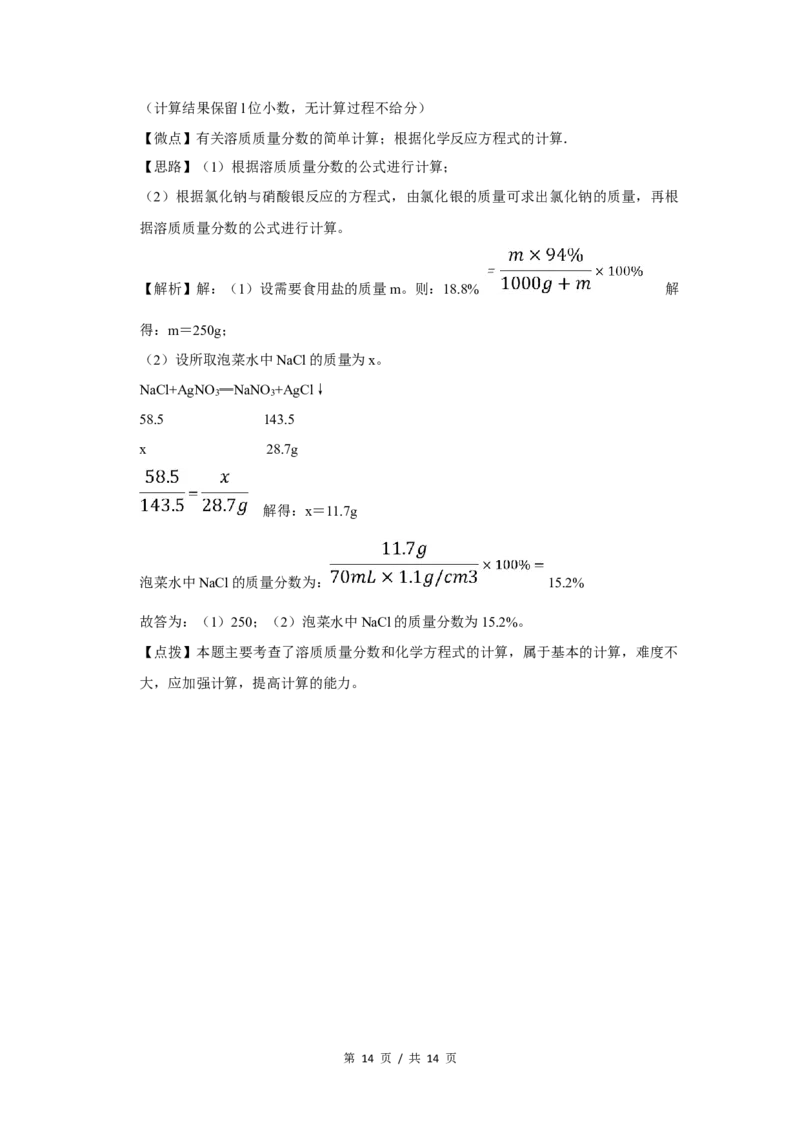
【解析】解:(1)设需要食用盐的质量m。则:18.8% 解
得:m=250g;
(2)设所取泡菜水中NaCl的质量为x。
NaCl+AgNO ═NaNO +AgCl↓
3 3
58.5 143.5
x 28.7g
解得:x=11.7g
泡菜水中NaCl的质量分数为: 15.2%
故答为:(1)250;(2)泡菜水中NaCl的质量分数为15.2%。
【点拨】本题主要考查了溶质质量分数和化学方程式的计算,属于基本的计算,难度不
大,应加强计算,提高计算的能力。
第 14 页 / 共 14 页