文档内容
2015年四川省绵阳市中考化学试卷
一、选择题(本大题包括21个小题,共63分。每小题只有一个选项是最符合题意的)
1.(3分)下列生活中常见的变化中,均属于化学变化的一组是( )
A.滴水成冰、钢铁生锈 B.石蜡熔化、水分蒸发
C.粮食酿酒、烟花燃放 D.汽油挥发、云消雾散
2.(3分)氧气的化学性质比较活泼,能与多种物质反应.下列对有关反应的描述正确的
是( )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色的三氧化二铁
B.硫在氧气里燃烧,发出蓝紫色火焰,生成无色无味的气体
C.铁、硫、酒精在氧气中的燃烧都是化合反应
D.物质与氧气发生的反应属于氧化反应
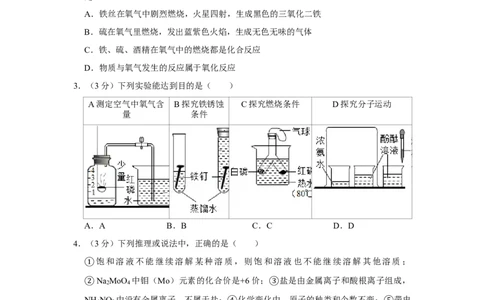
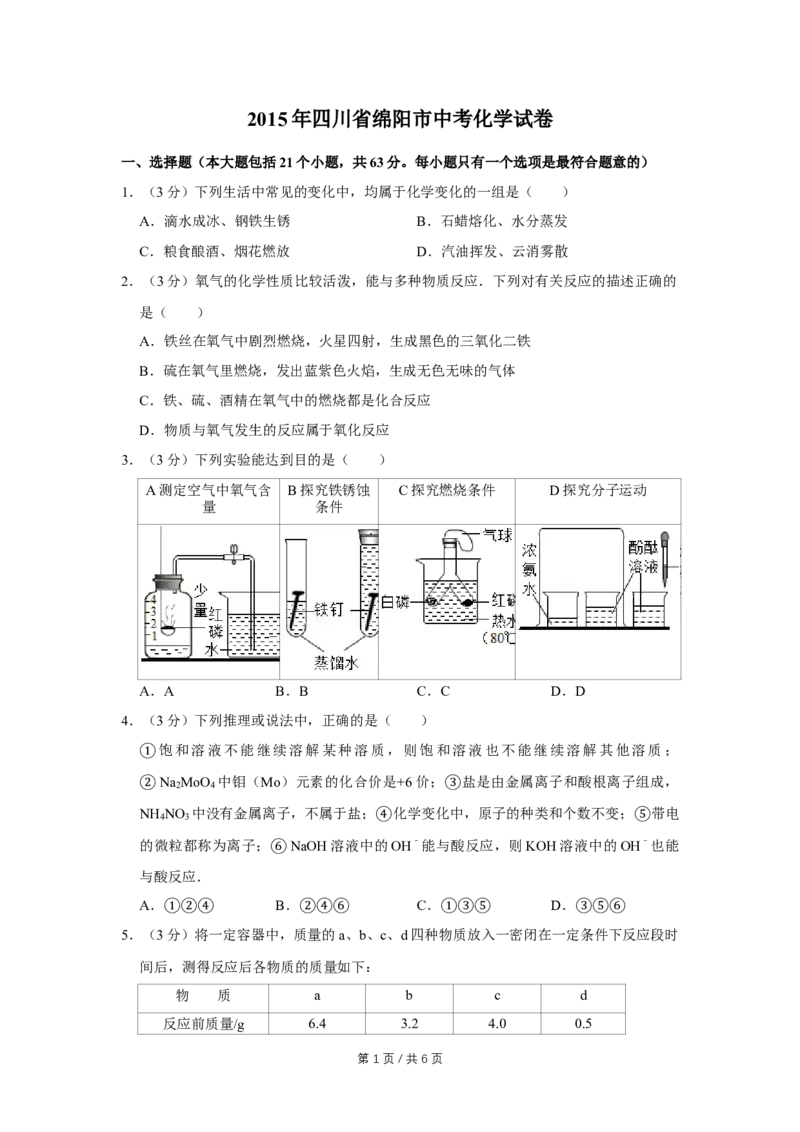
3.(3分)下列实验能达到目的是( )
A测定空气中氧气含 B探究铁锈蚀 C探究燃烧条件 D探究分子运动
量 条件
A.A B.B C.C D.D
4.(3分)下列推理或说法中,正确的是( )
饱和溶液不能继续溶解某种溶质,则饱和溶液也不能继续溶解其他溶质;
①Na MoO 中钼(Mo)元素的化合价是+6价; 盐是由金属离子和酸根离子组成,
2 4
②NH NO 中没有金属离子,不属于盐; 化学变化③中,原子的种类和个数不变; 带电
4 3
的微粒都称为离子; NaOH溶液中的④OH﹣能与酸反应,则KOH溶液中的OH⑤﹣也能
与酸反应. ⑥
A. B. C. D.
5.(3①分)②将④一定容器中,质②量④的⑥a、b、c、d四种物①质③放⑤入一密闭在一定③条⑤件下⑥反应段时
间后,测得反应后各物质的质量如下:
物 质 a b c d
反应前质量/g 6.4 3.2 4.0 0.5
第 1 页 / 共 6 页反应后质量/g 待测 2.56 7.2 0.5
下列说法错误的是( )
A.a和b是反应物,d可能是催化剂
B.反应后a的质量为2.56g
C.c物中元素的种类,一定等于a、b、两种物质中元素的种类
D.若a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为1:2
6.(3分)氢化钙(CaH )固体是一种储氢材料,是登山运动员常用的能源提供剂.已知:
2
氢化钙通常用氢气与钙加热制得.
①氢化钙要密封保存,遇水反应生成氢氧化钙和氢气.
②下列判断中正确的是( )
A.氢化钙的化学性质稳定
B. 中发生化合反应, 中发生复分解反应
C.①氢化钙作为能源提供剂②是因为与水反应能生成氢气
D.氢化钙可用于干燥潮湿的二氧化碳、氯化氢等气体
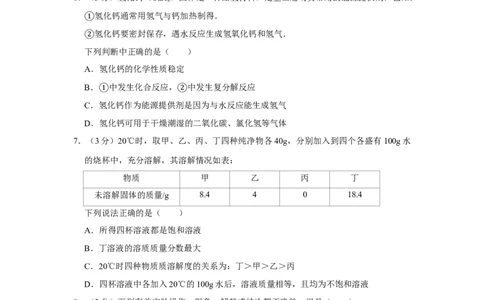
7.(3分)20℃时,取甲、乙、丙、丁四种纯净物各40g,分别加入到四个各盛有100g水
的烧杯中,充分溶解,其溶解情况如表:
物质 甲 乙 丙 丁
未溶解固体的质量/g 8.4 4 0 18.4
下列说法正确的是( )
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20℃时四种物质质溶解度的关系为:丁>甲>乙>丙
D.四杯溶液中各加入20℃的100g水后,溶液质量相等,且均为不饱和溶液
8.(3分)下列有关实验操作、现象、解释或结论都正确的一组是( )
选项 实验操作 现象 解释或结论
A 将水加入浓硫酸中配置成稀硫酸, 有气泡产生 Mg是活泼金属
将镁条置于其中
B 验纯后,将纯净氢气直接在空气中 产生淡蓝色火焰 氢气可以在空气中安
点燃 静的燃烧
C 向一未知无色溶液中,加入适量的 有无色气体产生 该无色未知溶液中一
稀盐酸溶液 定有CO 2﹣
3
D 将ag的铁钉投入到硫酸铜溶液 铁钉上覆盖一层红色 金属活动顺序为:Fe
第 2 页 / 共 6 页中,反应一段时间后,取出、洗 的物质 >Cu,且析出铜的质
净、烘干、称量为bg 量为(b﹣a)g
A.A B.B C.C D.D
9.(3分)取一定质量的石灰石(所含杂质不溶于水,不与酸反应,高温也不分解),高
温煅烧一段时间后得到78g固体,该固体与400g浓度为14.6%的稀盐酸恰好完全反应后,
过滤得到20g滤渣,则原石灰石中碳酸钙的质量分数为( )
A.74.4% B.80.0% C.83.8% D.92.6%
二、填空与解答题(共6小题,共97分)
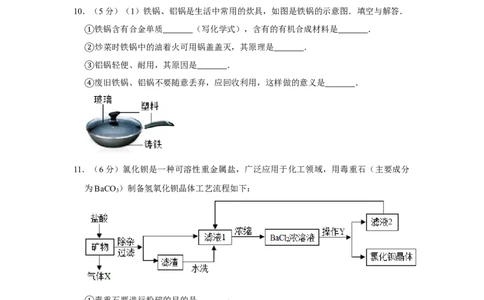
10.(5分)(1)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图.填空与解答.
铁锅含有合金单质 (写化学式),含有的有机合成材料是 .
①炒菜时铁锅中的油着火可用锅盖盖灭,其原理是 .
②铝锅轻便、耐用,其原因是 .
③废旧铁锅、铝锅不要随意丢弃,应回收利用,这样做的意义是 .
④
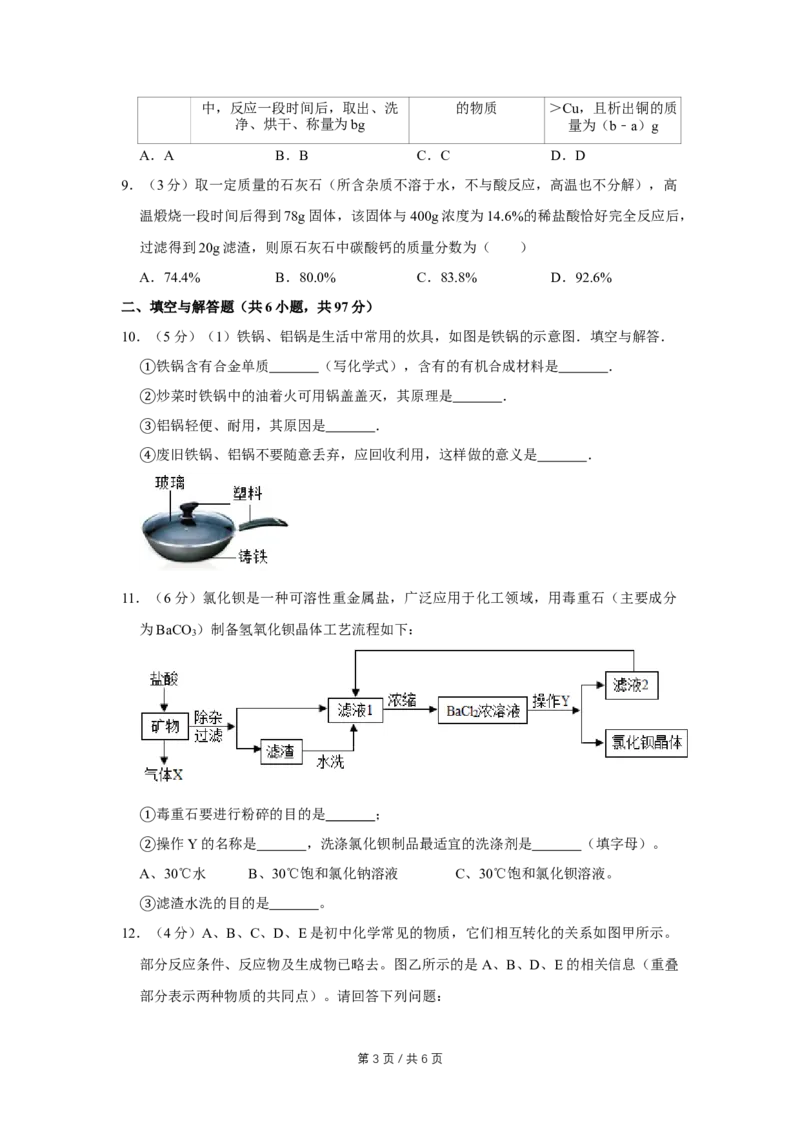
11.(6分)氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分
为BaCO )制备氢氧化钡晶体工艺流程如下:
3
毒重石要进行粉碎的目的是 ;
①操作Y的名称是 ,洗涤氯化钡制品最适宜的洗涤剂是 (填字母)。
②A、30℃水 B、30℃饱和氯化钠溶液 C、30℃饱和氯化钡溶液。
滤渣水洗的目的是 。
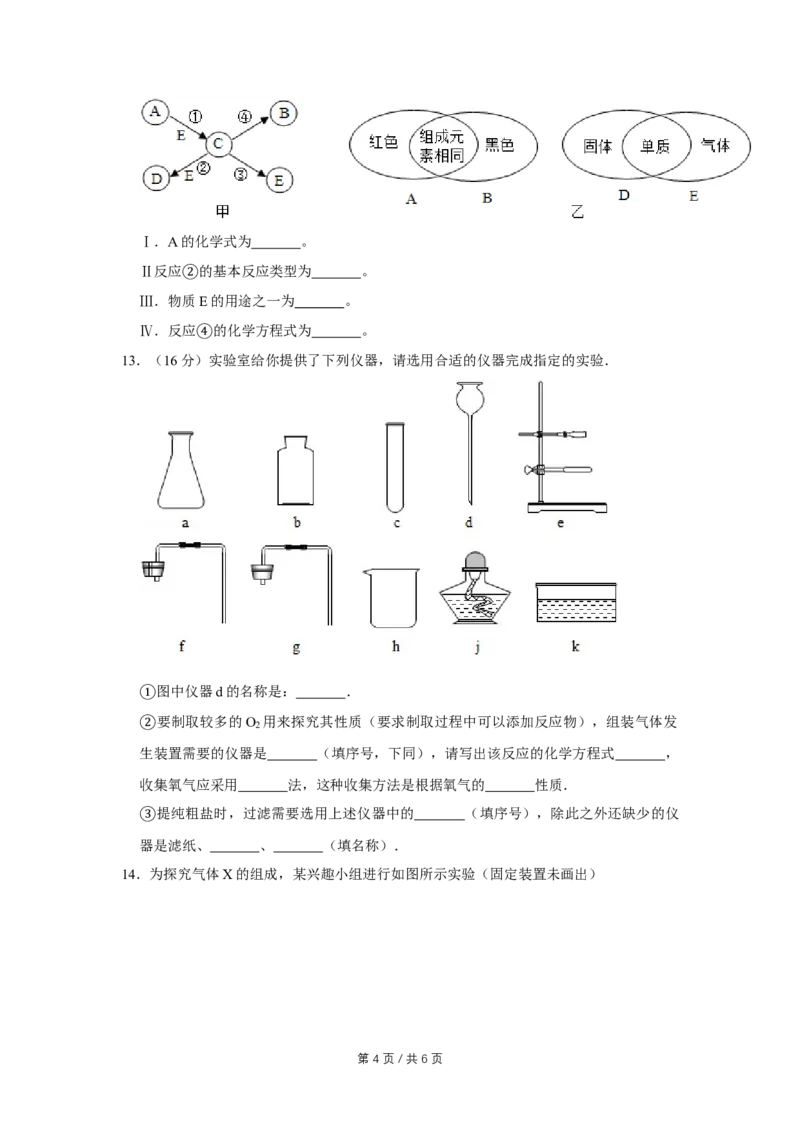
12.③(4分)A、B、C、D、E是初中化学常见的物质,它们相互转化的关系如图甲所示。
部分反应条件、反应物及生成物已略去。图乙所示的是A、B、D、E的相关信息(重叠
部分表示两种物质的共同点)。请回答下列问题:
第 3 页 / 共 6 页Ⅰ.A的化学式为 。
Ⅱ反应 的基本反应类型为 。
Ⅲ.物②质E的用途之一为 。
Ⅳ.反应 的化学方程式为 。
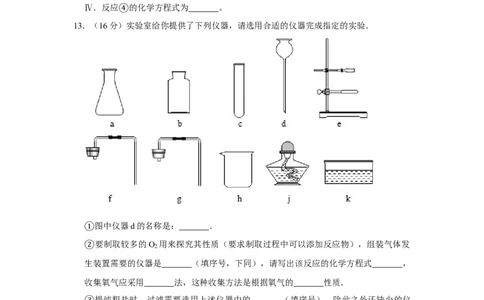
13.(16分)④实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验.
图中仪器d的名称是: .
①要制取较多的O
2
用来探究其性质(要求制取过程中可以添加反应物),组装气体发
②生装置需要的仪器是 (填序号,下同),请写出该反应的化学方程式 ,
收集氧气应采用 法,这种收集方法是根据氧气的 性质.
提纯粗盐时,过滤需要选用上述仪器中的 (填序号),除此之外还缺少的仪
③器是滤纸、 、 (填名称).
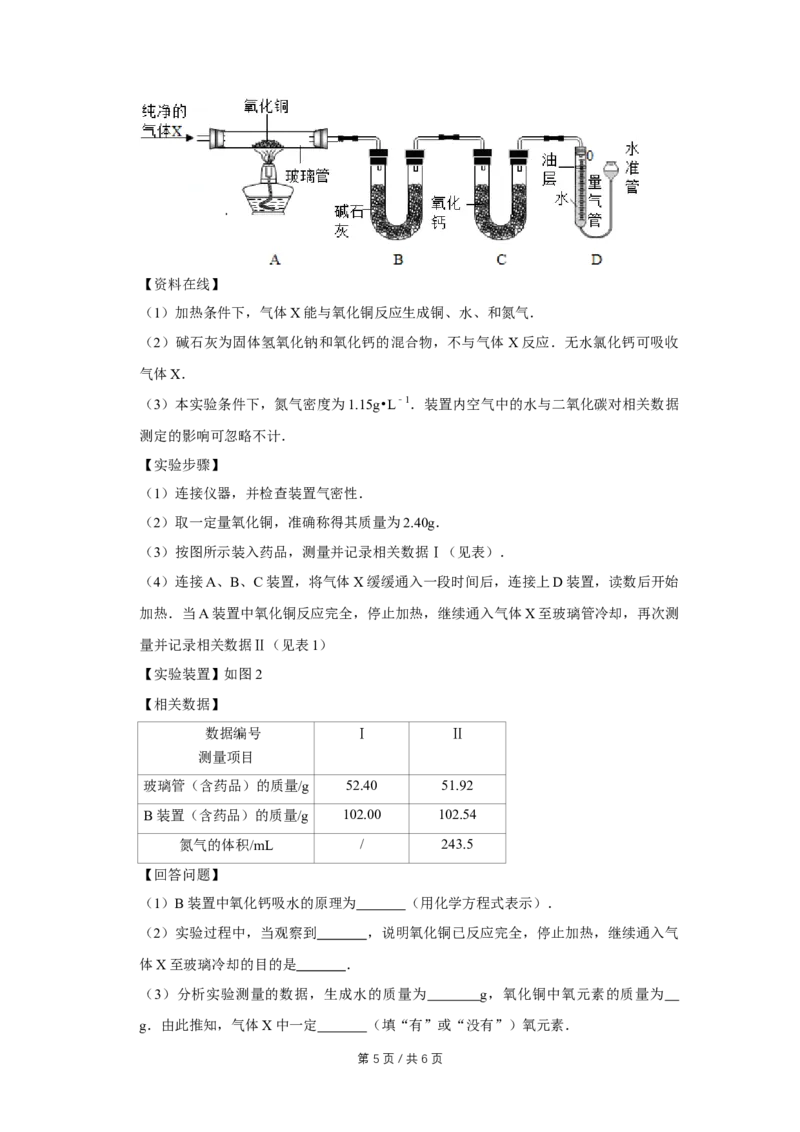
14.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出)
第 4 页 / 共 6 页【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水、和氮气.
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体 X反应.无水氯化钙可吸收
气体X.
(3)本实验条件下,氮气密度为1.15g•L﹣1.装置内空气中的水与二氧化碳对相关数据
测定的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)取一定量氧化铜,准确称得其质量为2.40g.
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始
加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测
量并记录相关数据Ⅱ(见表1)
【实验装置】如图2
【相关数据】
数据编号 Ⅰ Ⅱ
测量项目
玻璃管(含药品)的质量/g 52.40 51.92
B装置(含药品)的质量/g 102.00 102.54
氮气的体积/mL / 243.5
【回答问题】
(1)B装置中氧化钙吸水的原理为 (用化学方程式表示).
(2)实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气
体X至玻璃冷却的目的是 .
(3)分析实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为
g.由此推知,气体X中一定 (填“有”或“没有”)氧元素.
第 5 页 / 共 6 页(4)通过计算推导出气体X的化学式为 .气体X还原氧化铜的化学方程式为:
.
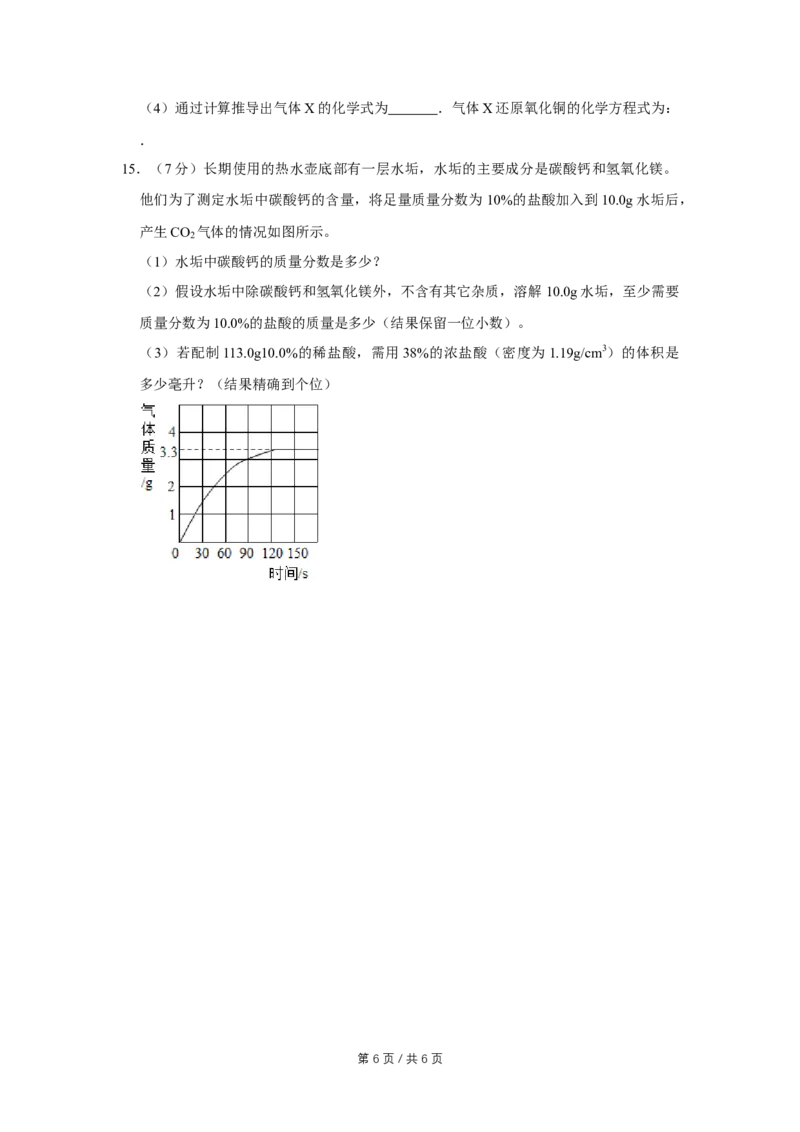
15.(7分)长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。
他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10.0g水垢后,
产生CO 气体的情况如图所示。
2
(1)水垢中碳酸钙的质量分数是多少?
(2)假设水垢中除碳酸钙和氢氧化镁外,不含有其它杂质,溶解10.0g水垢,至少需要
质量分数为10.0%的盐酸的质量是多少(结果保留一位小数)。
(3)若配制113.0g10.0%的稀盐酸,需用38%的浓盐酸(密度为1.19g/cm3)的体积是
多少毫升?(结果精确到个位)
第 6 页 / 共 6 页