文档内容
南海中学2025-2026学年上学期高三期中考试
化学试卷
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,
只有一项符合题目要求)
1.下列说法中正确的有( )
①金属晶体的导电性、导热性均与自由电子有关
②水结成冰密度减小与水分子之间能形成氢键有关
③HF、HCl、HBr、HI的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤H S、H Se、H Te的热稳定性依次减弱,熔沸点依次升高
2 2 2
⑥硬度由大到小:金刚石>碳化硅>晶体硅
A. ②③④⑥ B. ①②③⑥ C. ①②④⑤ D.
①②⑤⑥
【答案】D
【解析】①给金属晶体加电压时,晶体中的自由电子定向移动形成电流,自由电子的移动能传递
热能,因此金属晶体的导电性、导热性均与自由电子有关,①正确;②冰和水的密度不同主要是
由于水分子间存在氢键,氢键在液态水中使一个水分子与4个水分子相连,而当水凝固时,水分子
排列得很规则,氢键会拉伸水分子,使得水分子之间距离增大,体积也就增大,密度减小,②正
确;③F、Cl、Br、I的非金属性依次减弱,则其离子的还原性逐渐增强,且元素的非金属性越强,
其简单氢化物的热稳定性越强,则HF、HCl、HBr、HI的还原性逐渐增强,热稳定性依次减弱,
③错误;。④分子晶体熔、沸点的高低取决于分子间作用力的强弱,与共价键强弱无关,④错误;
⑤S、Se、Te非金属性依次减弱,故H S、H Se、H Te的热稳定性依次减弱,但是H S、H Se、
2 2 2 2 2
H Te的相对分子质量依次增大,其熔沸点依次升高,⑤正确;。⑥三种晶体为共价晶体,共价键
2
的键长越短,共价键越强,硬度越大,键长:C—C<C—Si<Si—Si,则硬度:金刚石>碳化硅>
晶体硅,⑥正确。故选D。
2.下列说法错误的是( )
A. 相同温度下,I 在CCl 中的溶解度大于其在水中的 B. KCl和SiO 晶体熔化时,克
2 4 2
服粒子间作用力的类型相同
C. ❑ 40Ca32S晶体中电子总数与中子总数相等 D. PCl 分子中各原子最外层都
3
满足8电子结构
【答案】B
【解析】I 是非极性分子,CCl 也是非极性分子,两者相似相溶,水为极性分子,因此碘在水中
2 4的溶解度较小,A项正确;KCl晶体熔化时破坏离子键,而SiO 熔化时破坏共价键,B项错误;
2
❑ 40Ca32S电子总数为20+16=36,而中子数为(40-20)+(32-16)=36,C项正确;PCl 为共价
3
化合物,电子式为: ,可知各原子最外层均满足8电子的结构,D项正确。选B。
3.分子中含有手性碳原子的物质具有光学活性。有机化合物 有光学活
性。则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
A. 与乙酸发生酯化反应 B. 与NaOH水溶液共热
C. 与银氨溶液作用 D. 在催化剂存在下与氢气作用
【答案】C
【解析】 与乙酸发生酯化反应后,—CHOH转化为—CHOOCCH ,
2 2 3
生 成 的 有 机 物 不 含 有 手 性 碳 原 子 , 没 有 光 学 活 性 , 故 A 不 符 合 题 意 ;
与 NaOH 水溶液共热发生水解反应后,—CHOOCCH 转化为—
2 3
CHOH,生成的有机物不含有手性碳原子,没有光学活性,故 B 不符合题意;
2
与银氨溶液作用发生银镜反应后,—CHO转化为—COOH,分子中
仍含有手性碳原子,仍有光学活性,故C符合题意; 在催化剂存在下
与氢气作用发生加成反应后,—CHO转化为—CHOH,生成的有机物不含有手性碳原子,没有光
2
学活性,故D不符合题意;故选C。
4.某有机物蒸气完全燃烧需三倍于其体积的氧气,产生二倍于其体积的二氧化碳(体积均在相同状
况下测定),该有机物可能是( )
A. C HOH
3 7
B. CHCHO
3
C. CHCOCH
3 3
D. C H
2 4【答案】D
【解析】设有机物分子式为CHO,燃烧的通式为CHO+(x+ - )O xCO + HO,由题意
x y z x y z 2 2 2
得,x+ - =3,x=2,则y-2z=4。由x=2知A、C项不合题意;把y=4,z=1代入y-2z=4
知,B项不合题意。
5.化学处处呈现美,宏观世界的美由微观结构决定。下列有关物质组成和结构表达正确的是(
)
A. Fe原子结构示意图: B. 反-2-丁烯的球棍模型为:
C. 丙烯分子的结构简式为:CH CHCH D. 石英的分子式为:SiO
2 3 2
【答案】A
【解析】Fe为26号元素,故原子结构示意图为 ,故A正确; 是
顺-2-丁烯的分子的球棍模型, 是反-2-丁烯的分子的球棍模型,故B错误;丙烯分子的
结构简式为:CHCH=CH ,故C错误;二氧化硅不存在分子,石英的化学式为SiO ,故D错误。
3 2 2
选A。
6.下列实验装置图正确的是( )A. 答案A B. 答案B C. 答案C D. 答案D
【答案】C
【解析】制备的乙炔含有H S,HS能使溴水褪色,产生干扰,需先通过硫酸铜溶液洗气,A错误;
2 2
液溴易挥发,会与AgNO 溶液反应产生淡黄色沉淀,有干扰,应该先通过CCl 溶液除去液溴,B错
3 4
误;乙醇与乙酸在浓硫酸作用下发生酯化反应,得到乙酸乙酯,有防止倒吸装置,饱和碳酸钠的
作用是吸收乙醇,除去乙酸,降低乙酸乙酯的溶解度使之析出,C正确;温度计水银球的位置应在
支管口处,D错误。故选C。
7.干冰(固态二氧化碳)在﹣78℃ 时可直接升华为气体,其晶胞结构如下图所示。下列说法不正确
的是( )
A. 1 mol CO 分子中含有2 molπ键 B. 每个晶胞中含有4个CO 分子
2 2
C. 每个CO 分子周围有8个紧邻CO 分子 D. 干冰升华时需克服分子间作用力
2 2
【答案】C
【解析】一个二氧化碳分子中有两个π键,故1 mol CO 分子中含有2 molπ键,A正确;根据
21 1
晶胞结构可知,该晶胞中有8个分子在顶点,6个分子在面心,故分子总数为8× +6× =4,B
8 2
正确;根据晶胞结构可知,在该晶体中每个每个CO 分子周围有12个紧邻CO 分子,C错误;干
2 2
冰分子间的作用力为分子间作用力,故其升华时需要克服的作用力为分子间作用力,D正确。故选
C。
8.中华民族有着灿烂的文化积淀。在下列古代发明和工艺中不涉及化学变化的是( )
A. 孔明灯 B. 用树皮、棉、麻造纸 C. 烧制彩陶 D. 淘黄金
【答案】D
【解析】孔明灯是利用物质燃烧产生的热能将灯放入高空,发生了化学变化,A项不符合题意。造
纸的过程中既有物理变化,又有化学变化,B项不符合题意。陶瓷烧制过程中有机物逐渐被除去,
无机氧化物之间进行反应生成硅酸盐类物质,涉及化学变化,C项不符合题意。金的化学性质稳定,
在自然界中以游离态形式存在,打捞起河里或湖里的淤泥后,用淘盘将淤泥洗去,可以得到金,
没有发生化学变化,D项符合题意。
9.短周期主族元素X、Y、Z、W、Q、R的原子序数依次增大,其中只有Z和W是金属元素。X
原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z的原子半径是短周期
主族元素中最大的,Q与Y同族。下列说法一定正确的是( )
A. 简单离子半径的大小顺序:W>Q>R>Y
B. X、Z、Q最高价氧化物对应水化物均可与W的最高价氧化物对应水化物反应
C. X的氢化物沸点低于Y的氢化物沸点
D. ZY 可用于呼吸面具或潜水艇中作为氧气的来源
2 2
【答案】D
【解析】X原子的最外层电子数是其内层电子数的2倍,核外有6个电子,X为C;Y是地壳中含
量最高的元素,Y为O;Q与Y同族,则Q为S;R原子序数大于S,且为短周期,为Cl;Z的原
子半径是短周期主族元素中最大的,Z为Na;W为金属,为Mg或Al,X、Y、Z、W、Q、R分别
为C、O、Na、Mg或Al、S、Cl。Y、W、Q、R分别为O、Mg或Al、S、Cl,具有相同核外电子
排布的简单离子,序数越大,半径越小,则半径的大小顺序:S2->Cl->O2-> Mg2+或Al3+,A说法
错误;Z的氧化物为氧化钠,若W为Mg时,氢氧化钠与氢氧化镁不反应,B说法错误;X的氢化
物为烃类,沸点不一定低于水的沸点,C说法错误;ZY 为NaO ,能与水或二氧化碳反应产生氧
2 2 2 2
气,可用于呼吸面具或潜水艇中作为氧气的来源,D说法正确。
10.下列分子中含有“手性碳原子”的是( )
A. CBr F B. CHCHCHOH C. CHCHCH D.
2 2 3 2 2 3 2 3
CHCH(NO )COOH
3 2【答案】D
【解析】在有机物分子中,当一个碳原子连有4个不同的原子或原子团时,这种碳原子被称为“手
性碳原子”,题目所给4个选项中,只有CHCH(NO )COOH中从左数第二个碳原子连接了4个不
3 2
同的原子或原子团,故D项正确。
11.下列化学用语正确的是( )
A. NCl 的VSEPR模型: B. NaCl溶液的中水合钠离子:
3
C. H 中共价键的电子云图: D. 基态硒的简化电子排布式:[Ar]4s24p4
2
【答案】A
5-3×1
【解析】NCl 的价电子对数为3+ =4,VSEPR模型为四面体,A正确;NaCl溶液的中水合
3 2
钠离子为 ,B错误;H 中共价键类型为s-s σ键,其电子云图为 ,C错误;基态硒的
2
简化电子排布式为[Ar]3d104s24p4,D错误。故选A。
12.某款香水中的香氛主要由以下三种化合物构成,下列说法正确的是( )
月桂烯 柠檬醛 香叶醇
A. 月桂烯分子中所有原子可能共平面 B. 柠檬醛和香叶醇是同分异构体
C. 香叶醇能发生加成反应、氧化反应、酯化反应 D. 三种有机物的一氯代物均有
7种(不考虑立体异构)
【答案】C
【解析】月桂烯分子含有4个—CH,分子中所有原子不可能共平面,A项错误;柠檬醛的分子式为
3
C H O,香叶醇的分子式为C H O,分子式不同,两者不是同分异构体,B项错误;香叶醇分子中含
10 16 10 18
有碳碳双键,能发生加成反应,含有—OH,能发生氧化反应和酯化反应,C项正确;月桂烯、香叶醇的
一氯代物有7种,柠檬醛的一氯代物有6种,D项错误。
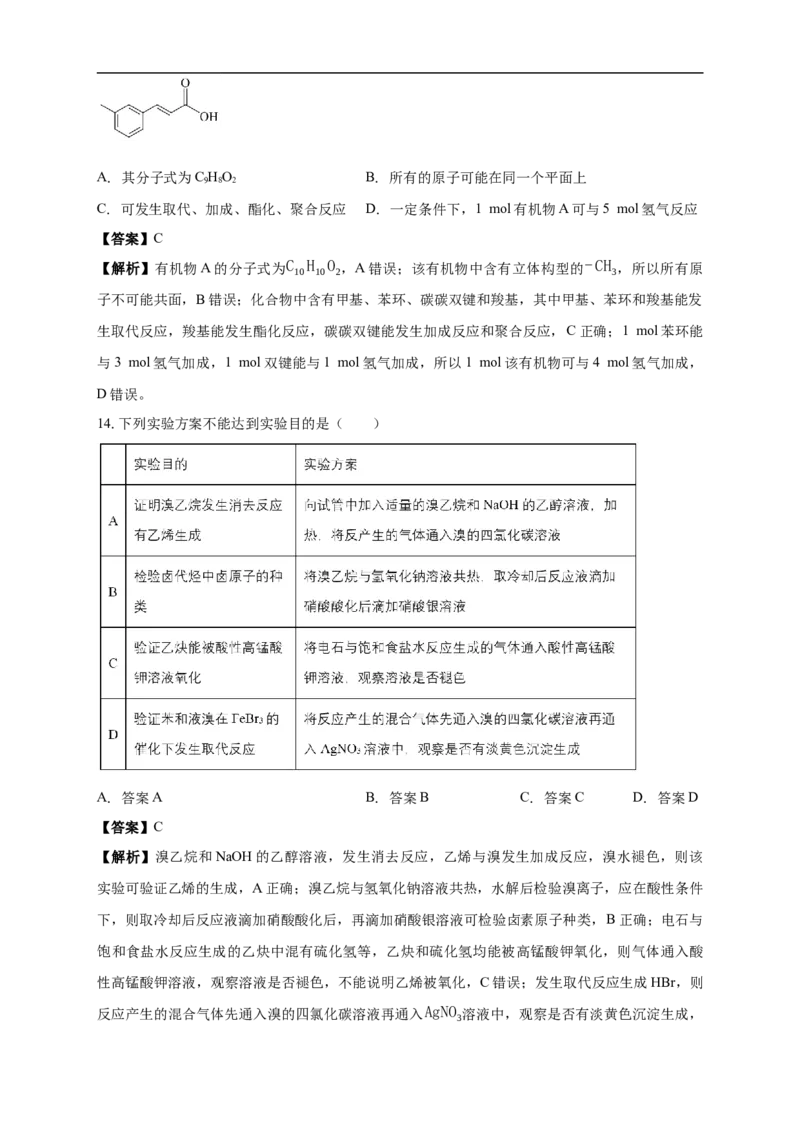
13.已知有机物A的结构如图所示,有关有机物A的性质描述正确的是( )A. 其分子式为C HO B. 所有的原子可能在同一个平面上
9 8 2
C. 可发生取代、加成、酯化、聚合反应 D. 一定条件下,1 mol有机物A可与5 mol氢气反应
【答案】C
【解析】有机物A的分子式为C H O ,A错误;该有机物中含有立体构型的-CH ,所以所有原
10 10 2 3
子不可能共面,B错误;化合物中含有甲基、苯环、碳碳双键和羧基,其中甲基、苯环和羧基能发
生取代反应,羧基能发生酯化反应,碳碳双键能发生加成反应和聚合反应,C正确;1 mol苯环能
与3 mol氢气加成,1 mol双键能与1 mol氢气加成,所以1 mol该有机物可与4 mol氢气加成,
D错误。
14.下列实验方案不能达到实验目的是( )
A. 答案A B. 答案B C. 答案C D. 答案D
【答案】C
【解析】溴乙烷和NaOH的乙醇溶液,发生消去反应,乙烯与溴发生加成反应,溴水褪色,则该
实验可验证乙烯的生成,A正确;溴乙烷与氢氧化钠溶液共热,水解后检验溴离子,应在酸性条件
下,则取冷却后反应液滴加硝酸酸化后,再滴加硝酸银溶液可检验卤素原子种类,B正确;电石与
饱和食盐水反应生成的乙炔中混有硫化氢等,乙炔和硫化氢均能被高锰酸钾氧化,则气体通入酸
性高锰酸钾溶液,观察溶液是否褪色,不能说明乙烯被氧化,C错误;发生取代反应生成HBr,则
反应产生的混合气体先通入溴的四氯化碳溶液再通入AgNO 溶液中,观察是否有淡黄色沉淀生成,
3可说明发生取代反应,D正确。
15.以X为原料制备缓释布洛芬的合成路线如下:
下列说法不正确的是( )
A. X不存在顺反异构
B. 试剂a为CHCHOH
3 2
C. N→缓释布洛芬为加聚反应
D. 布洛芬的结构简式为
【答案】B
【解析】 分子中碳碳双键右侧碳原子连有两个相同的氢原子,不存在顺反异构,故A
正确;由有机物的转化关系可知,一定条件下, 与 HOCH CHOH 反应生成
2 2
,则a为HOCH CHOH、M为 ,故B错误;N→缓释布
2 2
洛芬的反应为一定条件下, 发生加聚反应生成 ,故 C 正确;在浓硫酸作用下,M
与 共热发生酯化反应生成 N
, 则 布 洛 芬 的 结 构 简 式 为
,故D正确;故选B。
二、非选择题(本大题共4小题,共55分)
16.高纯超细氧化铝是重要的功能材料,利用废铝催化剂可以制备( α-Al₂O₃,既降低环境污染
又 可 提 高 铝 资 源 的 利 用 率 。 已 知 废 铝 催 化 剂 的 主 要 成 分 为 Al₂O₃( 含 少 量 杂 质
SiO₂、FeO、Fe₂O₃),其制备实验流程如图:
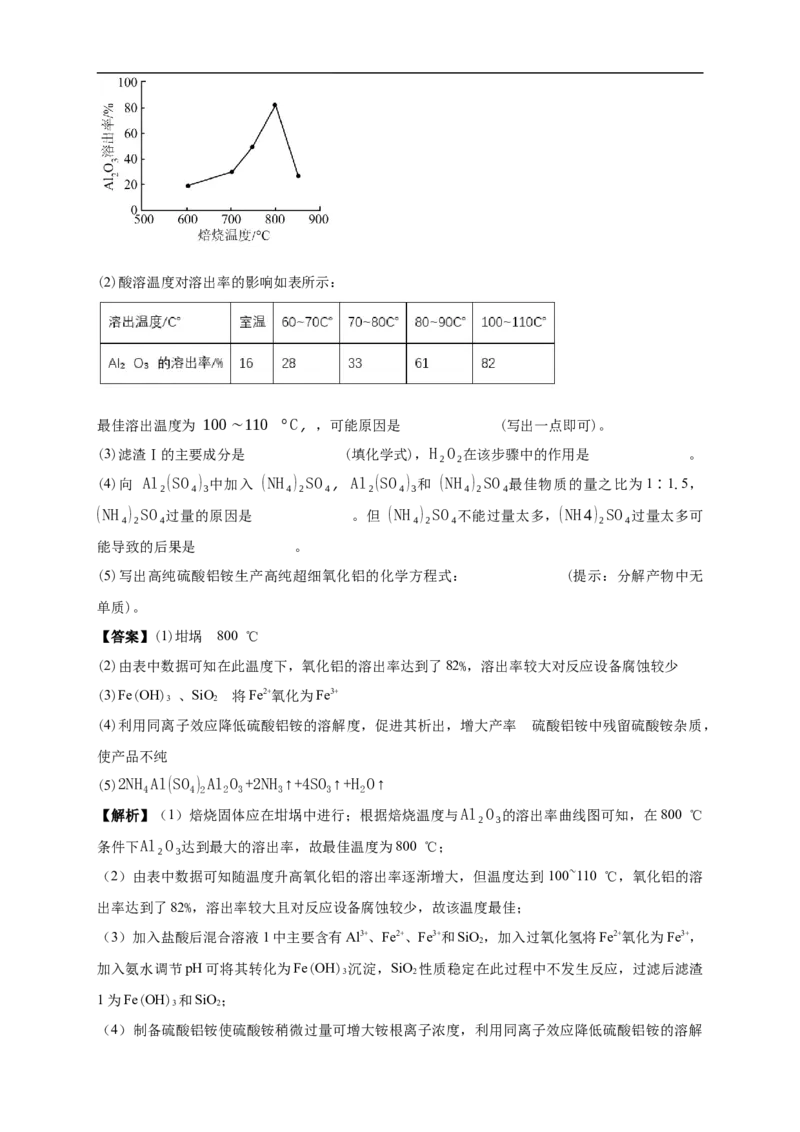
(1)焙烧应在 (填仪器名称) 中进行,焙烧温度与Al₂O₃的溶出率如图所示,焙烧的
最佳温度为 。(2)酸溶温度对溶出率的影响如表所示:
最佳溶出温度为 100∼110 °C,,可能原因是 (写出一点即可)。
(3)滤渣Ⅰ的主要成分是 (填化学式),H₂O₂在该步骤中的作用是 。
(4)向 Al₂(SO₄)₃中加入 (NH₄)₂SO₄,Al₂(SO₄)₃和 (NH₄)₂SO₄最佳物质的量之比为1∶1.5,
(NH₄)₂SO₄过量的原因是 。但 (NH₄)₂SO₄不能过量太多,(NH4)₂SO₄过量太多可
能导致的后果是 。
(5)写出高纯硫酸铝铵生产高纯超细氧化铝的化学方程式: (提示:分解产物中无
单质)。
【答案】(1)坩埚 800 ℃
(2)由表中数据可知在此温度下,氧化铝的溶出率达到了82%,溶出率较大对反应设备腐蚀较少
(3)Fe(OH) 、SiO 将Fe2+氧化为Fe3+
3 2
(4)利用同离子效应降低硫酸铝铵的溶解度,促进其析出,增大产率 硫酸铝铵中残留硫酸铵杂质,
使产品不纯
(5)2NH Al(SO ) Al O +2NH ↑+4SO ↑+H O↑
4 4 2 2 3 3 3 2
【解析】(1)焙烧固体应在坩埚中进行;根据焙烧温度与Al₂O₃的溶出率曲线图可知,在800 ℃
条件下Al₂O₃达到最大的溶出率,故最佳温度为800 ℃;
(2)由表中数据可知随温度升高氧化铝的溶出率逐渐增大,但温度达到 100~110 ℃,氧化铝的溶
出率达到了82%,溶出率较大且对反应设备腐蚀较少,故该温度最佳;
(3)加入盐酸后混合溶液1中主要含有Al3+、Fe2+、Fe3+和SiO,加入过氧化氢将Fe2+氧化为Fe3+,
2
加入氨水调节pH可将其转化为Fe(OH) 沉淀,SiO 性质稳定在此过程中不发生反应,过滤后滤渣
3 2
1为Fe(OH) 和SiO;
3 2
(4)制备硫酸铝铵使硫酸铵稍微过量可增大铵根离子浓度,利用同离子效应降低硫酸铝铵的溶解度,促进产品析出,增大产率,但是过量太多会使硫酸铝铵中残留硫酸铵杂质,使产品不纯;
(5)根据题中提示分解产物中无单质,推测高纯硫酸铝铵高温分解生产高纯超细氧化铝的化学方
程式为2NH Al(SO ) Al O +2NH ↑+4SO ↑+H O↑。
4 4 2 2 3 3 3 2
17.常温下将浓度为0.1 mol·L-1HF溶液加水稀释,下列各量如何变化?(填“变大”“变小”
或“不变”)
(1) ____________、 ____________、 ____________。
(2) ________、 ________。
【答案】(1)变大 变大 变大 (2)不变 不变
【解析】(1) = ,加水稀释HF的电离平衡正向移动,n(H+)增大,n(HF)减小,故 增
大;加水稀释c(F-)、c(H+)减小,c(OH-)增大,故 增大;加水稀释,n(F-)增大,n(HF)减
小,故 = ,增大。
(2) =K(HF),不变, = = ,不变。
a
18.完成下列填空:
(1)写出实验室制备乙烯的化学方程式: ,其中浓硫酸的用量
远远超过作为催化剂的正常用量,原因是 ,某次实验中,
给出了铁架台、铁圈、石棉网、铁夹、三芯酒精灯、圆底烧瓶、双孔橡皮塞和导管等实验用品,
还缺少的实验仪器是 。
(2)验证乙烯加成反应性质时,需对乙烯气体中的干扰物质进行处理,可选用的试剂是
(填写化学式);能确定乙烯通入溴水中发生了加成反应的事实是 。(选填编号)
a.溴水褪色 b.有油状物质生成
c.反应后水溶液酸性增强 d.反应后水溶液接近中性
浓硫酸
【答案】(1)C H OH → CH =CH ↑+H O 浓硫酸还具有吸水性,反应生成的水被浓硫酸吸收,
2 5 2 2 2
170℃
使反应向有利于生成乙烯的方向进行 温度计
(2)NaOH d
浓硫酸
【解析】(1)实验室用乙醇的消去制备乙烯,反应的化学方程式为:C H OH → CH =CH ↑+H O;
2 5 2 2 2
170℃
醇制取乙烯的同时还生成水,浓硫酸在反应中作催化剂和脱水剂,浓硫酸的用量远远超过作为催化剂的正常用量,原因是:浓硫酸还具有吸水性,反应生成的水被浓硫酸吸收,使反应向有利于
生成乙烯的方向进行;实验室制备乙烯需要严格控制温度在170℃,需要温度计精准测量反应温度;
(2)乙醇生成乙烯的反应中,浓硫酸作催化剂和脱水剂,浓硫酸还有强氧化性,与乙醇发生氧化还
原反应,因此产物中有可能存在SO ,会对乙烯的验证造成干扰,选择氢氧化钠溶液吸收SO 。a.
2 2
若乙烯与溴水发生取代反应也可使溴水褪色;b.若乙烯与溴水发生取代反应也有油状物质生成;
c.若反应后水溶液酸性增强,说明乙烯与溴水发生了取代反应;d.反应后水溶液接近中性,说明
反应后没有HBr生成,说明乙烯与溴水发生了加成反应,符合题意。
19.金属铝晶体的结构如图甲所示,其晶胞特征如图乙所示。若铝的原子半径为 1.42×10-10m,相
对原子质量为27。
(1)晶胞中铝原子周围等距离且最近的铝原子个数为________,一个晶胞中金属铝原子的数目为
________________。
(2)试求金属铝晶体中的晶胞长度,即图丙中AB的长度为________m,一个金属铝晶胞的体积为
________cm3。
(3)金属铝的密度为________。
【答案】(1)12 4 (2)4.02×10-10 6.48×10-23 (3)2.77 g·cm-3
【解析】(1)根据金属铝晶胞结构,一个铝原子周围距离最近且等距离的铝原子共12个;一个晶胞
中金属铝原子的数目为8× +6× =4。(2)金属铝晶胞棱长(a)和铝原子的半径(r)的关系为 a=
4r,故a=2 r,一个金属铝晶胞的体积为 V=a3=16 ×(1.42×10-10)3m3≈6.48×10-29m3。
(3)ρ= = ≈2.77 g·cm-3。