文档内容
微信公众号:文采学社
2 0 2 5 上 教 师 资 格 · 化 学 学 科 笔 试
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
主讲老师 张世雄
粉笔教师教育 粉笔教师目
录
content
微信公众号:文采学社
1 原子结构与性质
社
学
采
道
2 分文子结构与性质
渠
:
新
号
更
众
一
公
唯
信
微
3 晶体结构与性质微信公众号:文采学社
原子结构与性质
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
书上无
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
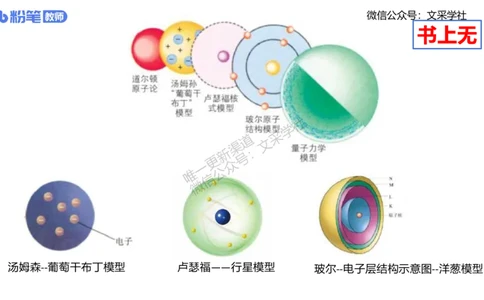
汤姆森--葡萄干布丁模型 卢瑟福——行星模型 玻尔--电子层结构示意图--洋葱模型微信公众号:文采学社
书上无
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
卢瑟福--α粒子轰击金箔实验微信公众号:文采学社
P84
一、原子结构
(一)原子的构成
1.原子构成
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
结论: 原子序数 = 核电荷数 = 质子数 = 核外电子数微信公众号:文采学社
P85
2.两组常见概念
(1)基态与激发态、原子光谱
①基态
处于最低能量的原子叫作基态原子。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P85
②激发态
当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激
发态原子。例如:电子可以从 1s 跃迁到 2s、2p……。
相反,电子从较高能量的激发态跃迁到较低能量的激发态乃至基
社
态时,将释放能量。光(辐射)是电子释放能量学的重要形式之一。
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P85
③原子光谱
不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱
仪摄取各种元素的电子的吸收光谱或发射光谱,总称原子光谱。
社
学
Li
采
道
文
渠
:
新
号
更
众
一
公
唯
信
He
微
Hg
发射光谱 吸收光谱微信公众号:文采学社
P85
(2)电子云和原子轨道
①电子云
电子云是电子在核外空间概率密度分布的形象化描绘,电子云图
中小黑点的疏密表示电子在原子核外空间某处出现概率的大小。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P85
②原子轨道
量子力学把电子在原子核外的一个空间运动状态称为一个原子轨
道。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
1s 原子轨道微信公众号:文采学社
P85
(二)四个量子数
1.主量子数(n)
主量子数表示电子出现最大概率区域离核的远近(电子层)和电子能
量的高低。
社
学
采
n 的取值为 1,2,3……n 等正整数,道目前只取至 7。
文
渠
:
新
号
更
n 值表示电子层数,对应的电子层 众 符号为 K,L,M,N,O,P,Q。
一
公
唯
信
n 值越大,轨道能量越高。微微信公众号:文采学社
P85
2.角量子数(l)
角量子数表示电子亚层和能级,也可以描述原子轨道(或电子云)
的形状。
l 的取值受制于 n 值,l 只能取 0 ~(n-1)的正整数,对于同一
社
学
采
个 n 值,可能有 n 个 l 值,即 0,1,2,3道 ······(n-1),即能级数等
文
渠
:
新
号
于能层序数。 更
众
一
公
唯
信
微微信公众号:文采学社
P86
l 取值 0 1 2
电子状态 s p d
原子轨道形状 球形 哑铃形/纺锤形 花瓣形
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P86
对多电子原子而言,n 相同时,一般情况是 l 值越大,能量越高。
但对于单电子原子,如氢原子,能量不受 l 的影响,只与 n 有关。
主量子数 1 2 3社 4
学
采
道
文
电子层 K L 渠 M N
:
新
号
更
众
一
角量子数 0 0,公1 0,1,2 0,1,2,3
唯
信
微
能及符号 1s 2s,2p 3s,3p,3d 4s,4p,4d,4f微信公众号:文采学社
P86
3. 磁量子数(m)
磁量子数表示原子轨道在空间的伸展方向。 m 的取值受制于 l 值,
m 只能取 0,±1;±2 ······ ±l,共有(2l+1)个取值。
例如:当 l=0 时,m=0,m 只有 1 个取值,表示 s 轨道在核外空
社
学
采
间只有 1 种分布方向,呈球形对称; 道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P86
当 l=1 时,m = 0,±1,m 有 3 个取值,表示 p 轨道有 3 种空
间取向,且相互垂直:沿 x 轴方向伸展的称 p 轨道;沿 y 轴方向伸展
x
的称 p 轨道;沿 z 轴方向伸展的称 p 轨道。
y z
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P86
当 l=2 时,m=0,±1,±2,m 有 5 个取值,表示 d 轨道有 5
种空间取向,对应5 条 d 轨道,分别为 d 、d 、d 、d 2 2 、d 2。
xy xz yz x −y z
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P86
小结:
1. s,p,d,f 各分层中的原子轨道数分别为 1,3,5,7,所以
各分层最多只能容纳 2, 6,10,14 个电子。又因为每个电子层中原
子轨道总数为 n2,所以各电子层中电子的最大容量为 2n2 个。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
书上无
【单选】主量子数n=4时,原子核外在该层的原子轨道数为( )。
A.4个 B.9个 C.16个 D.32个
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P86
小结:
2.磁量子数与电子能量无关。
n 与 l 相同、仅 m 值不同的轨道具有相同的能量,这种能量相同
的轨道称为简并轨道(或等价轨道)。
社
学
采
如 p 亚层有三条简并轨道 p ,p ,p道;
x y z 文
渠
:
新
号
d 亚层有五条简并轨道 d ,d更,d ,d 2 2 ,d 2。
众
xy 一xz yz x −y z
公
唯
信
这些简并轨道在外磁场作用下,由于取向不同,会产生能量上的
微
差异,这就是线状光谱在磁场作用下发生分裂的原因。微信公众号:文采学社
P86
4. 自旋量子数(m )
s
自旋量子数 m 用于表示电子自旋的运动方向。
s
自旋量子数共有两种取值,顺时针方向为 ,逆时针方向为 。
社
学
采
道
电子处于 或 状态时所具有
渠
的能量文相同。
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
书上无
【单选】原子序数为11的元素的最外层电子的四个量子数为( )。
1 1
A. n 1, l 0, m 0, m B. n 社 2, l 1, m 0, m
s 学 s
2 采 2
道
文
渠
:
新
号
更
1众 1
一
公
n 3, l 0, m 0, m 唯 n 4, l 0, m 0, m
C. 信 D.
s 微 s
2 2微信公众号:文采学社
书上无
【单选】在多电子原子中,各电子具有下列量子数,其中能量最高的
电子是( )。
1
社
A.2,1,-1,
学
2 采
道
文
渠
:
新
号
1 更
众
B.2,0,0, 一
- 公
唯
信
2
微
1
C.3,1,1, -
2
1
D.3,2,-1,
2微信公众号:文采学社
P87
(三)原子核外电子的排布规律
1.能量最低原理
电子在原子中所处的状态总是尽可能使整个体系的能量为最低,
这样的体系最稳定。因此电子总是优先占据可供占据的能量最低的轨
社
学
采
道,而后按照原子轨道近似能级图(又叫道构造原理图)依次进入能量
文
渠
:
新
号
更
较高的轨道,这就称为能量最低原理。
众
一
公
唯
信
微微信公众号:文采学社
P87
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
能量排布顺序:1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p微信公众号:文采学社
P87
2.洪特规则
电子排布在同一能级的不同轨道时,基态原子中的电子总是优先
单独占据一个轨道,并且自旋方向相同。
社
学
采
洪特规则特例:当等价原子轨道处于道全充满(p6,d10,f14),半
文
渠
:
新
号
充满(p3,d5,f7)和全空(p0,d0更,f0)时为稳定状态。
众
一
公
唯
信
微微信公众号:文采学社
P87
3.泡利原理
每个电子的运动状态都不同,同一条轨道最多只能容纳两个自旋
状态不同的电子。电子的两种自旋方向为顺时针方向和逆时针方向,
用“↑“和”↓”表示。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P87
(四)电子排布式与轨道表示式
1.电子排布式
在能级符号的右上角用数字表示该能级上排布的电子数目的式子。
(1)电子排布式的书写分为三步:
社
学
采
①按能量关系写出正确的轨道; 道
文
渠
:
新
号
更
②将电子从能量最低的 1s 亚层依 众 次往能量较高的亚层上排布,
一
公
唯
信
只有前面的亚层填满后,才能去微填充后面的亚层,将空轨道删去;
③按能层的顺序进行整理得出电子排布式。微信公众号:文采学社
P88
例1:写出 Fe的电子排布式。
26
第一步:1s 2s 2p 3s 3p 4s 3d;
第二步:1s2 2s2 2p6 3s2 3p6 4s2 3d6 ;
第三步:1s2 2s2 2p6 3s2 3p6 3d6 4s2。
社
学
采
Fe原子的电子排布式为:1s2 2s2 2p6道 3s2 3p6 3d6 4s2。
26 文
渠
:
新
号
更
众
一
公
唯
信
例2:写出 Fe2+的电子排布式。
微
26
Fe2+是在 Fe 原子的基础上失去2个电子形成的。
因此 Fe2+的电子排布式为:1s2 2s2 2p6 3s2 3p6 3d6。
26微信公众号:文采学社
P88
根据洪特规则特例:Cr、Cu 的电子排布式要做适当的调整。
Cr 原子的电子排布式为 1s2 2s2 2p6 3s2 3p6 3d54s1
Cu 原子的电子排布式为 1s2 2s2 2p6 3s2 3p6 3d104s1
社
学
采
道
文
渠
:
(2)电子排布式的简化写法 新
号
更
众
一
公
用前一周期的稀有气体原子唯加方括号的形式表示内层电子(又叫
信
微
原子实)。
例如:Fe 的简化电子排布式为[Ar]3d64s2微信公众号:文采学社
P88
2.轨道表示式
表示电子所处轨道及自旋状态的式子。用一个方框、圆圈或两条短线表
示一个给定量子数 n、l、m 的轨道,用箭头“↑“”↓”来区别自旋方向不同的电子。
可以反映粒子的电子层、电子亚层和自旋方向,但是无法体现伸展方向。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P89
二、元素周期表与元素周期律
(一)元素周期表的结构
电子层数相同的元素按原子序数递增的顺序从左到右排成横行,
最外层电子数相同的元素按电子层数递增的顺序从社上到下排成纵行而
学
采
道
得到的表叫元素周期表。 文
渠
:
新
号
更
众
元素周期表是元素周期律的一具体表现形式,反映了元素之间相互
公
唯
信
微
联系的规律。微信公众号:文采学社
P89
1.周期和族
周期:具有相同的
电子层数的元素按原子
序数递增的顺序排列成
社
学
采
的横行。 道
文
渠
:
新
号
族:最外层电子数 更
众
一
公
唯
信
相同的元素按电子层数
微
递增的顺序排成的纵行。微信公众号:文采学社
P89
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
书上无
【2019年上初中】2015 年 12 月 30 日,国际纯粹与应用化学联合会宣
布,元素周期表里加入第 113号、115 号、117 号和 118 号元素,下列表述
社
错误的是( )。
学
采
道
文
渠
:
A. 周期表的一个横行表示一个周期新
号
更
众
一
公
唯
信
B. 113 号、115 号、117 号元素都是主族元素
微
C. 如果再发现 119 号、120 号元素,它们将加入周期表的第七周期
D. 113 号、115 号、117 号、118 号元素都是人造元素微信公众号:文采学社
P90
2.元素、核素、同位素
元素:具有相同核电荷数(质子数)的一类原子的总称。 例如,12C、
13C、14C同属于碳元素。
核素:具有一定数目质子和一定数目中子的一种原子。每一种原子为一
社
学
种核素,如12C、13C、14C各为一种核素。
采
道
文
渠
:
新
同位素:具有相同质子数、不同中子数的同一元素的不同核素互为同位
号
更
众
一
公
唯
素。同位,指核素的质子数相同,信在元素周期表中占有相同的位置。
微
例如:12C、13C、14C,
16O、17O、18O,
35Cl、37Cl,
1H、2H、3H 分别互为同位素。微信公众号:文采学社
P90
同位素的化学性质相似,物理性质不同。
同位素之间的转化不属于化学变化。原子的裂变、聚变中虽有新
物质形成,但它们不属于中学化学变化研究的范畴。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P90
3.价电子层
周期表上元素的“外围电子排布”简称“价电子层”,这是由于这些
能级上的电子数可在化学反应中发生变化。
价电子层中的电子称为价电子。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
粉笔教师教育 粉笔教师