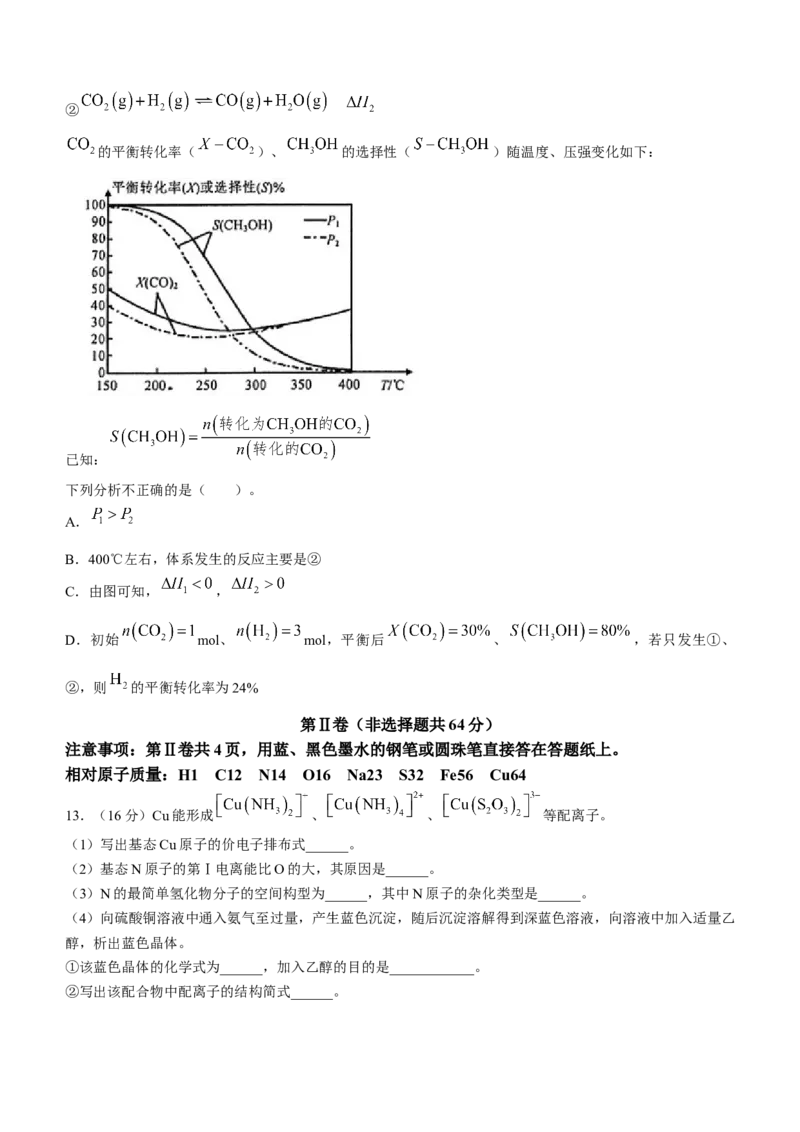
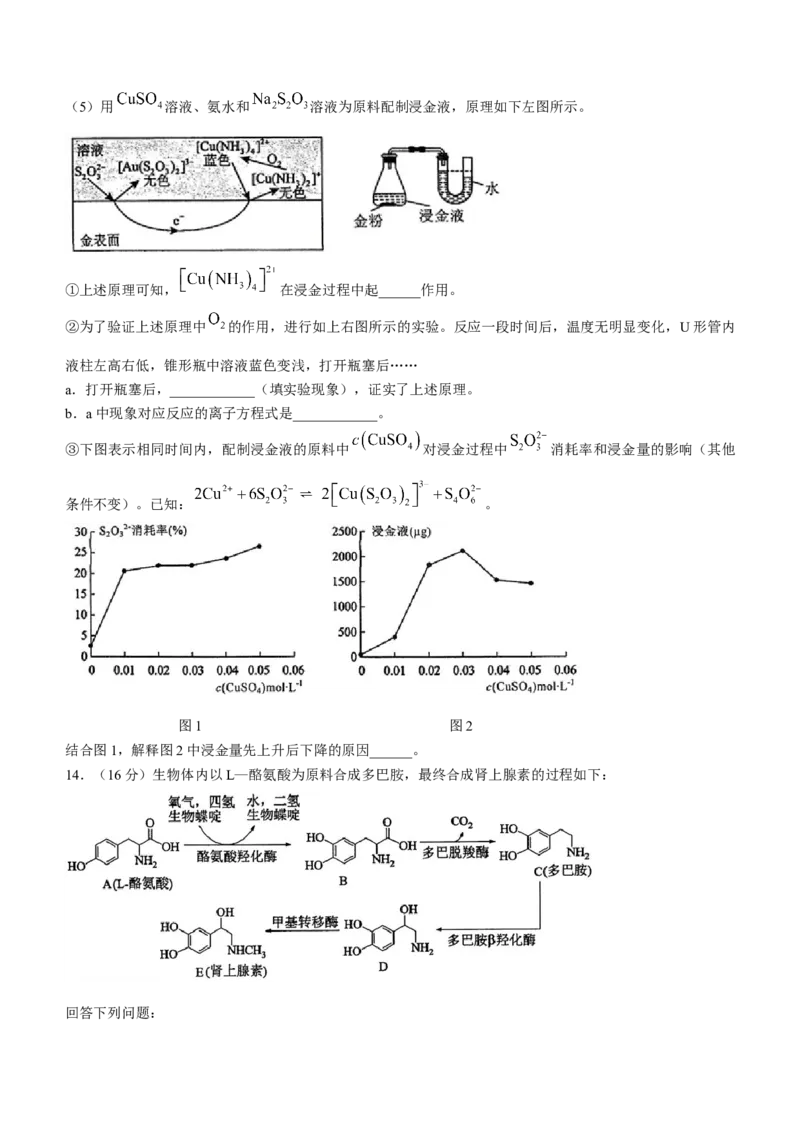
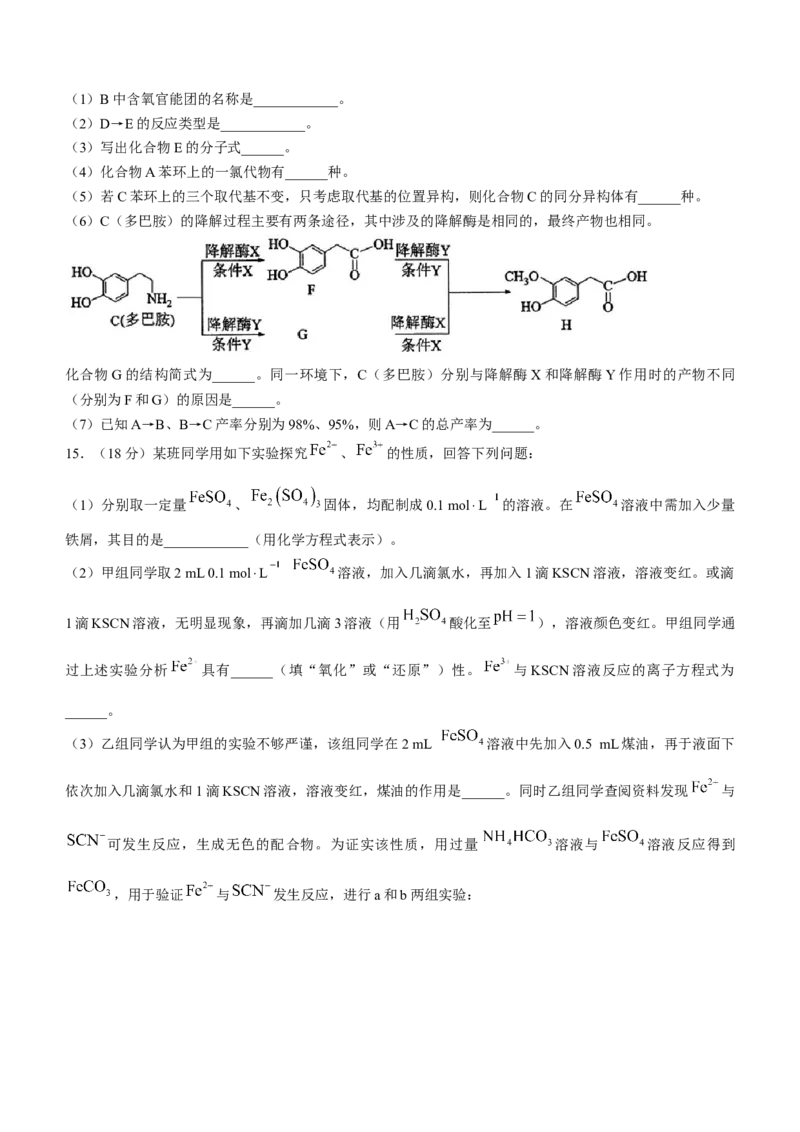
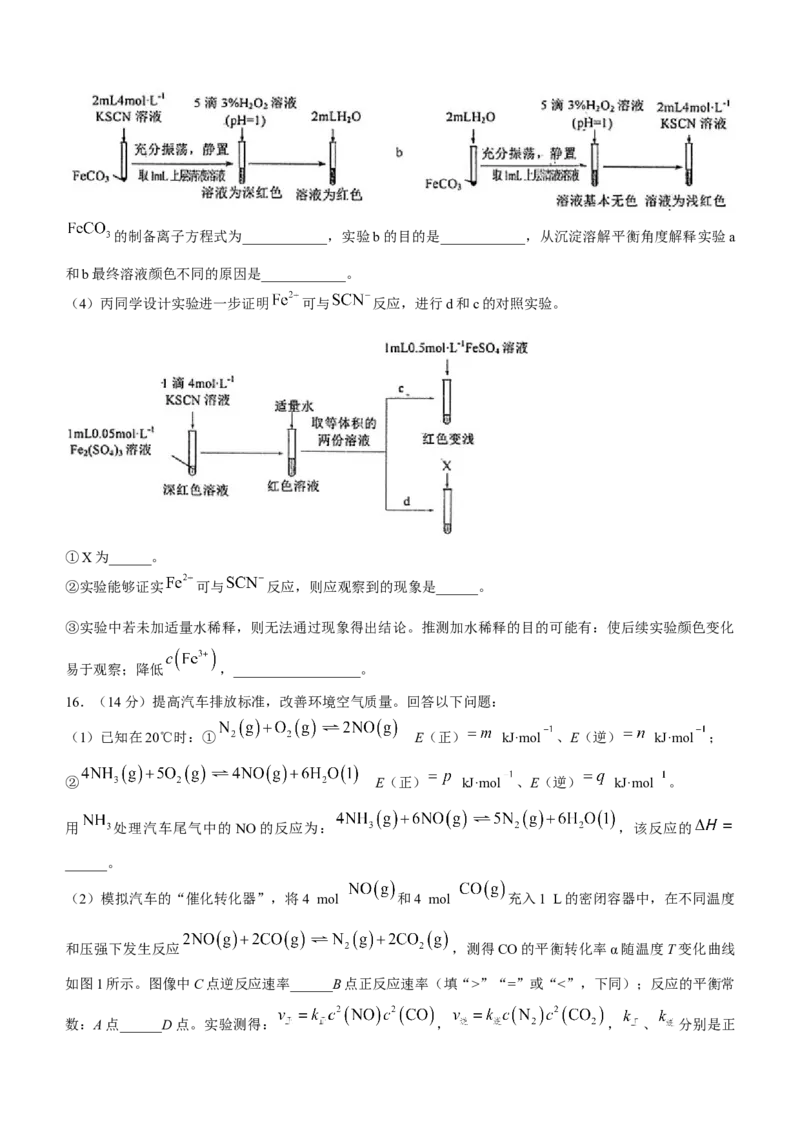
文档内容
和平区 2023—2024 学年度第一学期高三年级期末考试
化学学科考试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 100分。考试时间60分钟。答题
时,请将第Ⅰ卷每小题答案选出后,用2B铅笔涂在答题卡的相应位置上,若仅答在卷子上则不
给分。将第Ⅱ卷各题直接答在答题卡相应位置上。
相对原子质量:H1 C12 N14 O16 Fe56 Cr52 Zn65
第Ⅰ卷(选择题共36分)
选择题(本题包括12小题,每小题3分,共36分。每小题只有一个选项符合题意。)
1.中国古诗词中,不少名言佳句描写了劳动人民的生产与生活,其知识性与文艺性珠璧交辉,彰显了中华民
族的文化自信。下列关于古诗词的说法中不正确的是( )。
A.“故人具鸡黍,邀我至田家”中的“黍”的主要成分是淀粉
B.“无边落木萧萧下”中的“落木”的主要成分是纤维素
C.“壮志饥餐胡虏肉,笑谈渴饮匈奴血”中的“肉”和“血”都是脂肪
D.“愈风传乌鸡,秋卵方漫吃”中的“卵”主要指蛋白质
2.下列各项中不属于化学变化的是( )。
A.石油分馏 B.油脂硬化 C.煤的液化 D.橡胶硫化
3.下列物质不能通过相应单质一步化合而成的是( )。
A.HCl B.CuS C.NO D.
4.化学与生活密切相关,下列说法不正确的是( )。
A. 可用作焊接金属的保护气 B. 可用作食品膨松剂
C.高纯硅可用于制作光导纤维 D.漂粉精可用于游泳池的消毒
5.下列说法正确的是( )。
A.基态氧原子价电子排布图:
B.基态Cr原子电子排布式
C. 的空间结构:平面三角形
D.冰中的氢键示意图:
6.用已知浓度的NaOH溶液测定浓硫酸试剂中 含量的主要操作中,不需要用到的仪器为( )。A. B. C. D.
7.下列金属冶炼的反应原理,不恰当的是( )。
A.2NaCl(爆炸) B.
C. (葡萄糖) D.
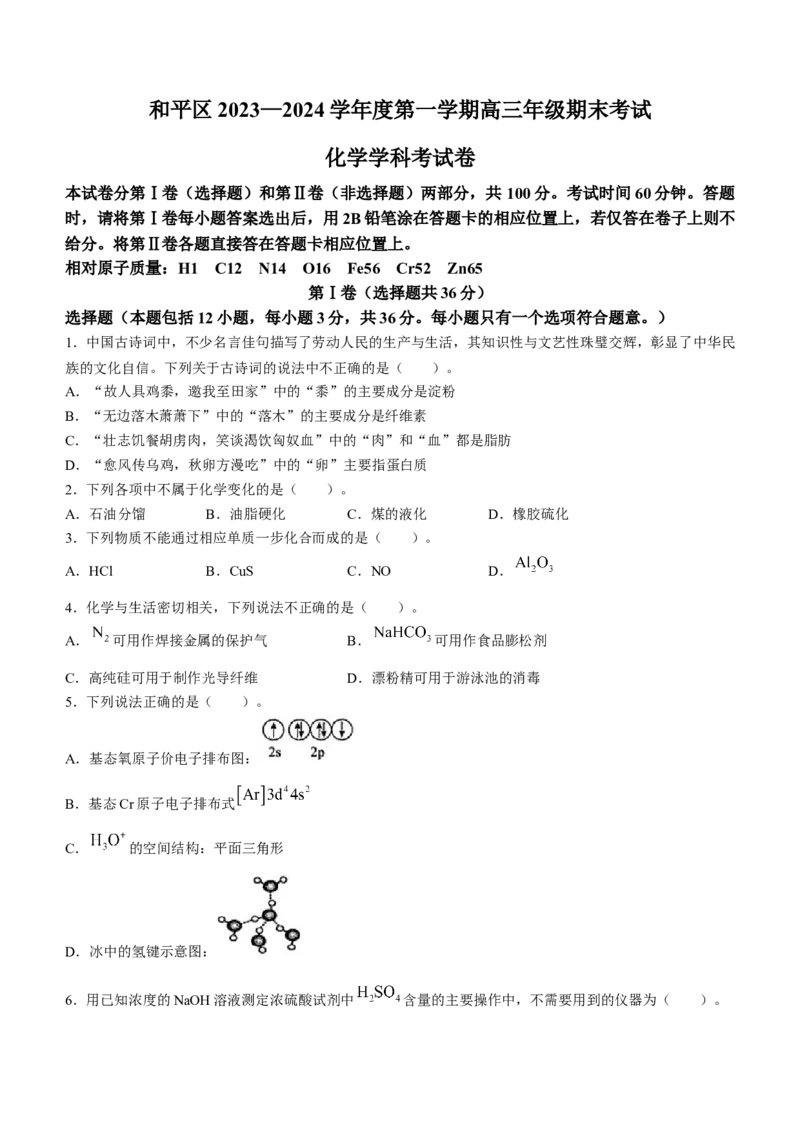
8.三百多年前,著名化学家波义耳使用铁盐和没食子酸(结构简式如图)制造了墨水。下列有关没食子酸的
说法不正确的是( )。
A.分子式为 B.可与浓溴水发生取代反应
C.所有原子有可能处于同一平面上 D.1 mol没食子酸最多可与4 mol 反应
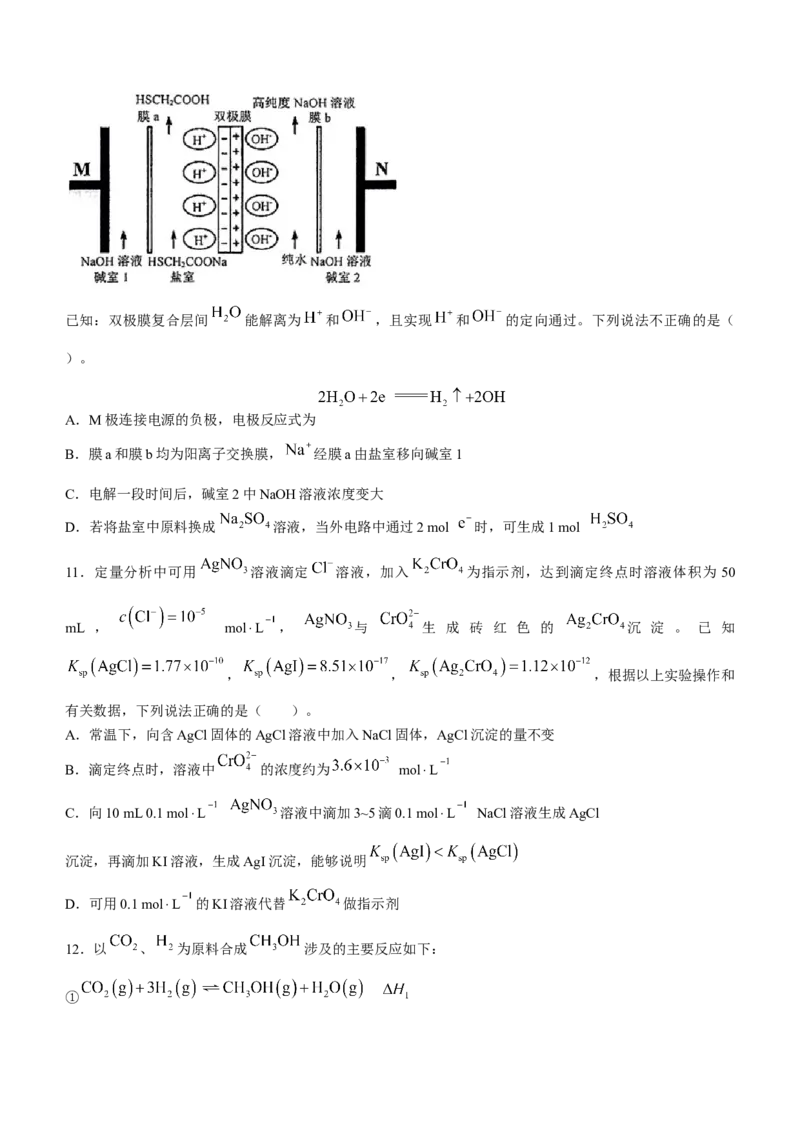
9.X、Y、Z、W是原子序数依次增大的短周期主族元素,Y、Z、W位于同一周期,基态W原子的核外电子
总数是其最高能级电子数的2倍,它们形成的某种阴离子的结构如图所示。下列说法不正确的是( )
A.由X、Y、W三种元素形成的酸都是二元酸
B.该阴离子与X⁺形成的化合物是两性物质
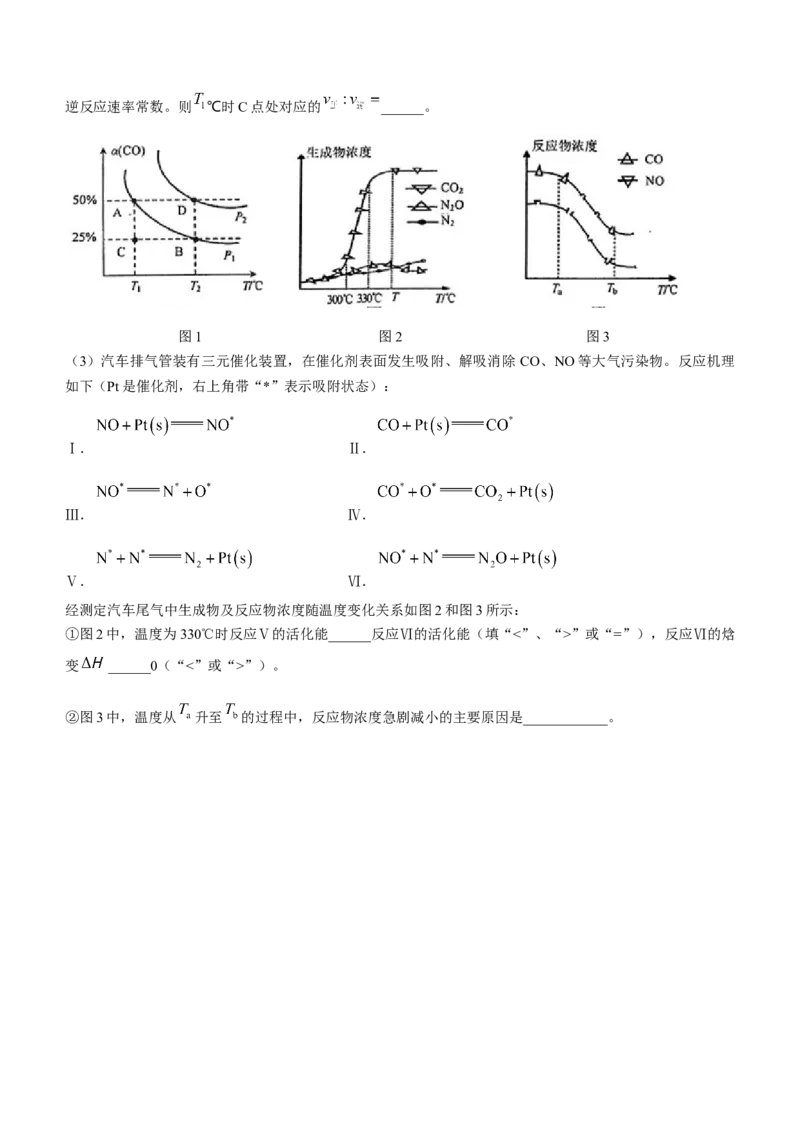
C.元素的第一电离能:Y”“=”或“<”,下同);反应的平衡常
数:A点______D点。实验测得: , , 、 分别是正逆反应速率常数。则 ℃时C点处对应的 ______。
图1 图2 图3
(3)汽车排气管装有三元催化装置,在催化剂表面发生吸附、解吸消除 CO、NO等大气污染物。反应机理
如下(Pt是催化剂,右上角带“*”表示吸附状态):
Ⅰ. Ⅱ.
Ⅲ. Ⅳ.
Ⅴ. Ⅵ.
经测定汽车尾气中生成物及反应物浓度随温度变化关系如图2和图3所示:
①图2中,温度为330℃时反应Ⅴ的活化能______反应Ⅵ的活化能(填“<”、“>”或“=”),反应Ⅵ的焓
变 ______0(“<”或“>”)。
②图3中,温度从 升至 的过程中,反应物浓度急剧减小的主要原因是____________。和平区 2023—2024 学年度第一学期高三年级期末考试
化学学科考试卷参考答案
选择题本卷共12小题,每题3分,共36分。
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 C A B C D A B D A C B D
第Ⅱ卷(非选择题共64分)
13.(共16分)
(1) (1分)
(2)N原子的2p能级处于较稳定的半充满状态(2分)
(3)三角锥形;(1分) (1分)
(4)① ;(1分) 降低 的溶解度(2分)
② (1分)
(5)①催化(1分)
②a.锥形瓶中溶液蓝色复原(2分)
b. (2分)
③当 mol⋅L 时,随着 的增大, 的浓度增
大,浸金速率增大;当 mol⋅L 时,游离的 消耗 ,使 浓度减小,浸金
速率减小(2分)
14.(共16分)
(1)羟基、羧基(2分) (2)取代反应(2分)
(3) (2分) (4)2(2分) (5)5(2分)
(6) (2分) 催化剂具有选择性(2分)
(7)93%(或93.1%)(2分)
15.(共18分)(1) (2分)
(2)还原;(1分) (2分)
(3)分层后可以隔离溶液与空气接触,排除氧气对实验的影响;(2分)
;(2分)
通过实验b排除了 溶解产生的 对实验的影响;(2分)
与 溶解电离产生的 结合,沉淀溶液平衡正向移动,溶液中的 (包括 与 生
成物)浓度增大,与酸性 反应产生的 增大, 与 生成物浓度增大,溶液红色加深(2
分)
(4)①1 mL 0.5 mol⋅L 溶液(1分)
②溶液红色更浅(2分)
③使 平衡逆向移动,增加 的量提高与 反应的可能性(2分)
16.(共14分)
(1) kJ⋅mol (2分)
(2)<;(2分) >;(2分) 40.5(2分)
(3)①>;(2分) <;(2分)
②升温,催化剂活性增强,速率逐渐加快,则反应物浓度急剧减小(2分)